Ситуационная задача 36
 Скачать 1.82 Mb. Скачать 1.82 Mb.
|
|
Кислота аскорбиновая имеет в своей структуре ендиольную группу. Она при воздействии кислорода находящегося в растворе и над поверхностью переходит в 2,3-дикетоаскорбиновую кислоту, лишенную С-витаминной активности. Для стабилизации применяют антиоксидант натрия сульфит безводный (2,0 на 1000 мл). Антиоксидант будет окисляться в первую очередь, при этом аскорбиновая кислота оснанется стабильной С целью снижения болезненности инъекций к раствору добавляют натрия гидрокарбонат в эквивалентном количестве. Осмотическая активность Эквивалент по натрия хлориду для аскорбиновой кислоты 0,18, для натрия гидрокарбоната 0,65 Чтобы раствор 100 мл был изотоническим в нем должно быть 0,9 г натрия хлорида 0,18*10+0,65*4,7=4,9 это больше чем 0,9 значит раствор гипертоничный. 2. Предложите методы стабилизации инъекционных растворов легко-окисляющихся веществ в промышленном производстве и их хранение. Укажите механизм стабилизации. Процесс окисления можно замедлить следующими способами:
В фармацевтической практике используют антиоксиданты 2 и 3 групп. Из соединений 3 группы наиболее часто используют соединения серы низкой валентности: натрия сульфит, натрия метабисульфит, тиомочевину, унтнол. Это прямые антиоксиданты, сильные восстановители. Применяют в качестве антиоксидантов и другие органические вещества, содержащие альдегидные, спиртовые, фенольные группы, например, парааминофенол, кислоту аскорбиновую и др. Антиоксиданты выявлены среди лекарственных веществ. В водных средах антирадикальную активность проявляют анальгин, амидопирин, резорцин, сальсолин, изониазид, салюзид и др. Замедляют процессы окисления комплексообразователи трилон Б и тетацин-натрий. Они связывают катионы металлов (железа, меди, хрома), которые катализируют процессы окисления на стадии распада гидропероксида. Скорость окислительно-восстановительной реакции зависит также от рН-раствора, т.е. наличия ионов гидроксила, которые оказывают на нее каталитическое действие. Поэтому для замедления процессов окисления вводят кислоту или буферные растворы. Для уменьшения концентрации кислорода в растворителе и над раствором воду для инъекций насыщают углекислотой, а процесс производства проводят в среде инертного газа. Таким образом, растворы легкоокисляющихся веществ стабилизируют: - введением стабилизаторов; - использованием комплексонов; - созданием оптимальных значений рН; - уменьшением содержания кислорода в растворителе и над раствором; - использованием светонепроницаемой тары для уменьшения инициирующего действия света. Запайка ампул Следующая операция - запайка ампул. Она очень ответственна, так как некачественная запайка влечет за собой брак продукции. Основные способы запайки: > оплавление кончиков капилляров; > оттяжка капилляров. При запайке оплавлением у непрерывно вращающейся ампулы нагревают кончик капилляра, и стекло само заплавляет отверстие капилляра. Работа автоматов основана на принципе движения ампул в гнездах вращающегося диска или транспортера, который проходит через газовые горелки. Они нагревают и запаивают капилляры ампул. Недостатки способа: наплыв стекла на конце капилляров, трещины и разгерметизащм ампул; необходимость соблюдения требований к размерам ампул; необходимость промывки капилляров ампул перед запайкой, В конструкции автомата предусматривается распылительная форсунка для душирования апирогенной водой. Оттяжка капилляров. При этом способе сначала разогревают капилляр непрерывно вращающейся ампулы, а затем отпаиваемую часть капилляра захватывают специальными щипцами и, оттягивая, отпаивают. В то же время отводят пламя горелки в сторону для пережёга стеклянной нити, образующейся в месте отпайки, и для оплавления запаянной части. Запайка с оттяжкой обеспечивает красивый внешний вид ампулы и высокое качество. Однако при запайке ампул с малым диаметром и тонкими стенками капилляр, при воздействии на него средств оттяжки,либо скручивается, либо разрушается. Этих недостатков лишен способ запайки с оттяжкой капилляра под действием струи сжатого воздуха. При этом отсутствует механический контакт с капилляром, имеется возможность пневмотранспортировки отходов, увеличивается производительность и упрощается конструкция запавчного узла. Этим способом можно качественно запаивать ампулы как большого, так и малого диаметра. В отдельных случаях, когда нельзя использовать термические способы запайки, ампулы укупоривают пластмассой. Для запайки ампул со взрывоопасными веществами используют нагрев с помощью электрического сопротивления. 3. Для количественного определения кислоты аскорбиновой применяют методы, основанные на ее кислотно-основных и окислительно-восстановительных свойствах: Кислотные свойства. Аскорбиновая кислота является гамма-лактоном, содержащим 2 спиртовых гидроксила в 5-м и 6-м положениях и 2 енольных гидроксила во 2-м и 3-м положении. Енольные гидроксилы обладают кислотными свойствами, дают кислую реакцию па лакмус, взаимодействуют и с NaOH. Кислотные свойства более выражены у гидроксила в 3-м положении: Стандартный раствор 0,1 М раствором натрия гидроксида 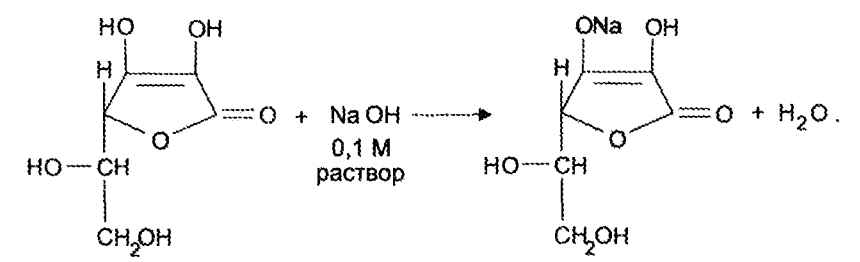 М (аскорбинов к-ты) 176,1 Фактор эквивалентности = 1 Эквивалент = 176,1 Восстановительные свойства. Выраженные восстановительные свойства кислоты аскорбиновой лежат в основе нескольких методик количественного определения данного лекарственного вещества (йодатометрия, йодометрия. йодхлорметрия). Окислители окисляют кислоту аскорбиновую до кислоты дикетоаскорбиновой. Иодатометрия. Кислоту аскорбиновую титруют в присутствии калия йодида, небольшого количества кислоты хлороводородной и крахмала 0,1 н. стандартным раствором калия йодата (стандартный раствор) до синего окрашивания: 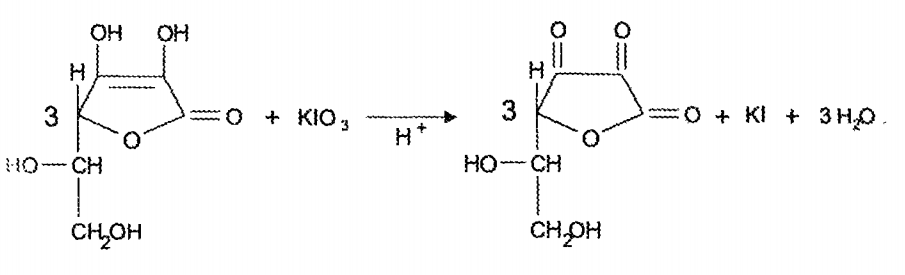 Избыточная капля титрованного раствора калия йодата реагирует с калия йодидом, выделяя йод, который указывает на конец титрования (желтое окрашивание); 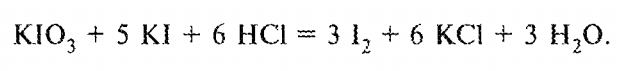 М (аскорбинов к-ты) 176,1 Фактор эквивалентности = 1/2 Эквивалент = 176,1*1/2=88,05 Йодометрия Стандартный раствор – 0,1 н. Раствор йода 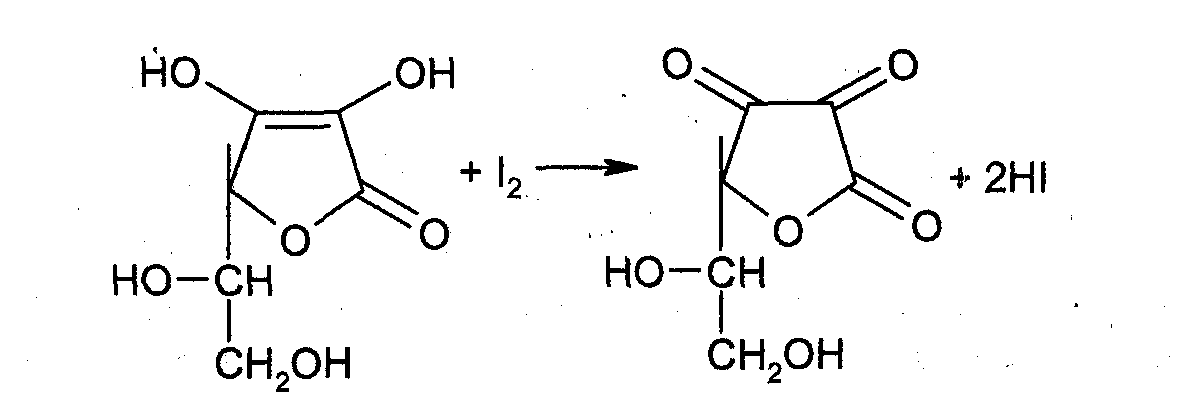 Индикатор крахмал, в конце раствор окрашивается в синий цвет или без индикатора до желтого окрашивания раствора. М (аскорбинов к-ты) 176,1 Фактор эквивалентности = 1/2 Эквивалент = 176,1*1/2=88,05 Йодхлорметрия 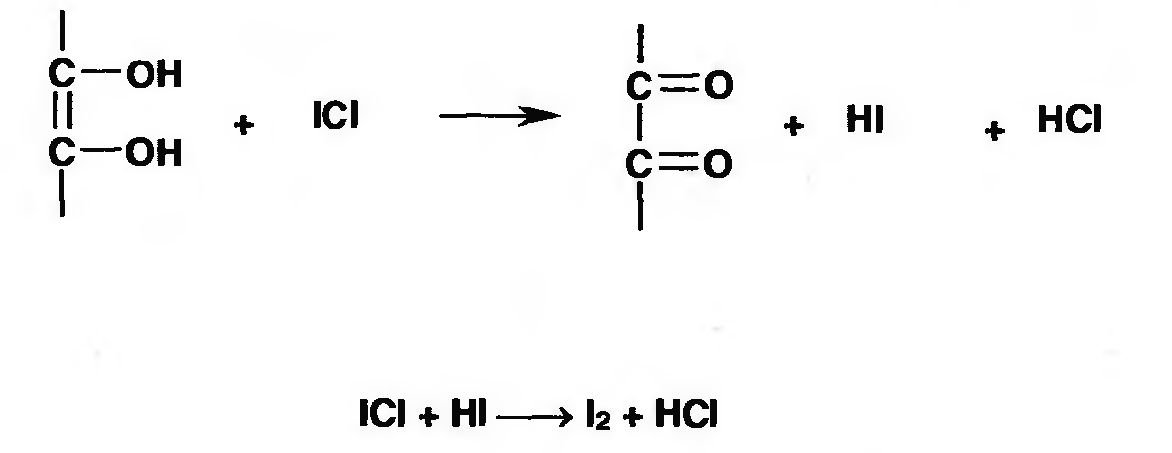 Титруют 0,1 М раствором йодмонохлорна (индикатор крахмал). Прибавления йодида не требуется, так как он образуется при взаимодействии кислоты аскорбиновой с титрантом. В эквивалентной точке выделяется йод, окрашивающий крахмал в синий цвет. М (аскорбинов к-ты) 176,1 Фактор эквивалентности = 1/2 Эквивалент = 176,1*1/2=88,05 4. К какому виду товарооборота относится отпуск товаров из аптеки институциональным потребителям? Институциальные потребители – это больницы, санатории, детские сады. Относится к оптовому товарообороту. В аптеках, где объем реализации входят продажи ЛПУ, основными факторами, лияющими на товарооборот являются: коечный фонд ЛПУ и его изменение, профиль ЛПУ, ассигнования выделенные ЛПУ на закупку ЛС и ИМН, размер средств ФОМС и добровольного страхования, наличие формуляров и их стоимость, дополнительные ассигнования. При расчете объема реализации организациям может быть применен метод динамических показателей (это учет товарооборота и инфляции в предыдущие годы), однако наиболее точным является ориентирвоание на предполагаемый размер ассигнований ЛПУ. Учет оптового товарооборота предусматривает определение стоимости отпуска ЛС аптекой ЛПУ и другим организациям. Оптовая реализация ЛС и ИМН аптекой ЛПУ и другим организациям осуществляется по розничным ценам согласно счетов или накладных требований, оформленных должным образом и подписанных руководителем, главным бухгалтером и скреплены печатью организации. Количество экземпляров накладных (требований), как правило, составляет 3-5, определяется исходя из принятого в аптеке первичного документооборота. Для обобщения данных выписанных счетов и накладных (требований) в аптеках ведется специальная форма реестра выписанных покупателям накладных (требований), по которой определяется общий оптовый товарооборот (кроме суммы льготных и бесплатных рецептов). В реестре отражается одной строкой отпуск конкретному покупателю товара согласно товарным группам (экстемпоральные и ГЛС, отпуск медикаментов в массе „ангро", перевязочные средства, другие товары). Следующим документом по учету оптовой реализации является оборотная ведомость по лицевым счетам покупателей и других расчетов. Оборотная ведомость по счетам покупателей (ЛПУ и другие организаций) позволяет провести взаиморасчеты аптеки со всеми покупателями. По данным взаиморасчетов предыдущего периода, суммы отпущенного товара и пересчета денег от ЛПУ и других организаций в отчетном периоде рассчитывается дебиторская (в пользу аптеки) или кредиторская (за аптекой) задолженность аптеки, фармацевтической фирмы. Оптовая реализация фармацевтических товаров аптеками и фармацевтическими фирмами может проводиться двумя способами: 1) первым событием происходит отпуск товаров (т.е. реализация с отсрочкой платежа); 2) первым событием происходит оплата (т.е. реализация по предоплате). В соответствии с этим и бухгалтерский учет реализации при этих двух способах отличается. При отстрочке платежа. Отгрузка товара отражается записью по дебету счета 62 «Расчеты с покупателями и заказчиками» и кредиту счета 46 "Реализация продукции (работ, услуг)" При предоплате. Полученная предоплата отражается записью по дебету счета 51 "Расчетные счета" и кредиту счета 62 "Расчеты с покупателями и заказчиками" 5. Дайте характеристику лекарственному растительному сырью - «Шиповника плоды».• Приведите латинские названия сырья, производящего растения, семейства. Fructus Rosae — плоды шиповника Собранные в период технической зрелости и высушенные плоды дикорастущих и культивируемых кустарников различных видов шиповника (розы) RosaL. из сем. розоцветных (Rosaceae).. В медицине используются представители: секц. RugosaeChrshan.: шиповник морщинистый (Rosarugosa.); секц. Cinnamomeae: шиповник майский (ш. коричный) — Rosamajalis, ш. иглистый (R. acicularis.), ш. даурский (R. davuricа.); секц. CaninaeDC: ш. собачий (R. canina), ш. щитконосный (R. corymbifera), ш. мелкоцветковый (R. micrantha), и некоторые другие виды. Химический состав. Плоды шиповника содержат кислоту аскорбиновую (от 0,2-1 % у низковитаминных видов н до 4-5 % у высоковитаминных); каротиноиды (бета-каротин и др.) до 10 мг%; токоферолы (витамин Е); флавоноиды (флавонолы — рутин, кемпферол; катехины; лейкоантоцианидины; антоцианы); гидролизуемые и конденсированные дубильные вещества, органические кислоты — лимонная и яблочная (2-4 %); жирное масло; пектиновые вещества (до 14 %); сахара (до 24 %); около 0,9 % свободных аминокислот (в основном аспарагиновой). Качественное и количественное определение содержания аскорбиновой кислоты в лекарственном растительном сырье связано с использованием 2,6-дихлориндофенолята натрия. Для количественного определения навеску сырья экстрагируют горячей водой и аликвоту экстракта титруют раствором реактива (синего цвета) до неисчезающей синеватой окраски (в ходе титрования аскорбиновая кислота окисляется, а реактив восстанавливается до бесцветной формы). Для качественного определения часть водного экстракта хроматографируют на пластинке «Силуфол», высушивают и обрабатывают указанным реактивом (нанеся одновременно раствор свидетеля – чистой аскорбиновой кислоты) – пятна аскорбиновой кислоты выглядят бесцветными на синем фоне. Количественное определение суммы органических кислот проводят алкалиметрически. 6. Охарактеризуйте методы получения вакцин. Половина из всех применяемых в настоящее время вакцин относится к живым вакцинам разного происхождения. Это вакцины как бактерийного происхождения, применяемые для профилактики сибирской язвы, чумы, туберкулеза и др., так и вирусного происхождения, применяемые для профилактики оспы, кори, гриппа, краснухи, полиомиелита и других заболеваний. Аттенуированные вакцины представляют собой препараты, полученные из естественных штаммов микроорганизмов с ослабленной для человека вирулентностью (аттенуированных). Аттенуацию (ослабление) проводят путем длительного воздействия антигенов на штамм химических (мутагены) и физических (температура, радиация) факторов или путем длительных пассажей на невосприимчивых животных или других биообъектах (эмбрионы птиц, культуры клеток). В качестве живых вакцин можно использовать дивергентные штаммы, то есть непатогенные для человека микробы имеющие общие протективные антигены с патогенными для человека возбудителями инфекционных болезней. Классическим примером дивергентных живых вакцин является вакцина против натуральной оспы человека, в которой используется непатогенный для человека вирус оспы коров. К дивергентным вакцинам также относися БЦЖ-вакцина, в которой используются родственные в антигенном отношении микобактерии бычьего типа. Рекомбинантные вакцины. В качестве примера можно привести получение рекомбинантной вакцины гепатита В. Как известно, вирус гепатита В не размножается in vitro , то есть в искусственных условиях. Для получения вакцины гепатита В выделенный ген этого вируса вставляют в дрожжевую клетку или в клетку E.coli. Затем уже промышленным способом эту культуру выращивают в ферментере на обогащенных питательных средах в аэробных условиях, получая значительные количества рекомбинантного белка, содержащего антиген вируса гепатита В. Введение такой вакцины приводит к образованию антител против гепатита В и создает иммунную защиту организма человека от этого тяжелого заболевания. Комбинированные вакцины. Как следует из названия, они комбинируются из отдельных вакцин, превращаясь при этом в поливакцины, которые способны иммунизировать сразу от нескольких инфекций. В качестве примера можно назвать поливакцину АКДС, содержащую дифтерийный и столбнячный анатоксины, а также коклюшные корпускулярные антигены. Эта вакцина, как известно, широко применяется в детской практике. Неживые (инактивированные) вакцины. Инактивированные вакцины в качестве действующего начала включают убитые химическим или физическим методом культуры патогенных бактерий или вирусов (цельноклеточные, цельновирионные вакцины) или же извлеченные из патогенных микробов (иногда вакцинных штаммов) комплексы, содержащие в своем составе протективные антигены (субклеточные, субвирионные вакцины). Для инактивации бактерий и вирусов применяют формальдегид, спирт, фенол или температурное воздействие, ультрафиолетовое облучение, ионизирующую радиацию. Для выделения из бактерий и вирусов антигенных комплексов (гликопротеинов, белков) применяют трихлоруксусную кислоту, фенол, ферменты, ультрацентрифугирование и т.д. Получают инактивированные вакцины путем выращивания на искусственных питательных средах патогенных бактерий или вирусов, которые затем подвергают инактивации или далее, проводят очистку и конструирование в виде жидкого или лиофильно высушенного препарата, в который обязательно добавляют консервант, иногда - адьюванты. Синтетические вакцины. Также антиген в молекулярной форме, особенно его детерминанты, можно получить химическим синтезом. Этим способом уже синтезированы детерминанты многих бактерий и вирусов, в том числе ВИЧ. Однако, химический синтез антигенов более трудоемок и имеет ограниченные возможности по сравнению с биосинтезом. СИТУАЦИОННАЯ ЗАДАЧА 40 1. В аптеку клинической больницы поступило требование из терапевтического отделения на изготовление инфузионного раствора. Возьми: Раствора глюкозы 20%.................................................100 мл Простерилизуй! Дай такие дозы числом............................................................................20 Обозначь. ...............................................................По 5 мл внутривенно.
Sterilisetur1 Da tales doses №20 Signa: Для внутривенного введения (реанимационное отделение) Раствор готовится в соответствии с прописью в приказе №214.
Растворы глюкозы при стерилизации, особенно во флаконах из щелочного стекла, подвергаются окислению и карамелизации. При этом наблюдается пожелтение, а иногда и побурение растворов. При выборе стабилизатора необходимо учитывать полифункциональный характер глюкозы. Она неустойчива в щелочной среде, под влиянием кислорода образуются оксикислоты: гликолевая, левулиновая, муравьиная и другие кислоты и оксиметилфурфурол. Для предотвращения этого процесса растворы глюкозы стабилизируют 0,1 М раствором кислоты хлороводородной до рН 3,0-4,1 Глюкоза неустойчива в кислой среде – образуется Д-глюконовая кислота и ее лактоны в результате их окисления, особенно в процессе стерилизации, образуется 5-оксиметилфурфурол, вызывая пожелтение раствора, что связано с дальнейшей карамелизацией. Таким образом, в качестве стабилизаторов в раствор глюкозы вводят по 1 литр 0,21 г натрия хлорида и 0,1 М раствора кислоты хлороводородной до рН 3,0-4,1. В аптечных условиях используют готовый стабилизатор Вейбеля, в состав которого входят: Натрия хлорид 5,2 Кислоты хлороводородной разведенной 4,4 мл Воды для инъекций до 1 литра Этот стабилизатор добавляют в количестве 5% от объема раствора и независимо от его концентрации. Раствор глюкозы готовится без стабилизаторы в детских лекарсвтенных формах. 2. Для обнаружения глюкозы студент предложил реакцию с раствором меди сульфата в щелочной среде, а для количественного определения - метод йодометрии. Дайте оценку выбору данных испытаний. |
