|
|
УЧЕБНИК Клиническая иммунология. Соколов Е.И. 1998. УЧЕБНИК Клиническая иммунология. Соколов Е.И. Содержание 1 сокращения, часто встречающиеся в тексте 2
ГЛАВА 3
МОРФОЛОГИЯ ИММУННОГО ОТВЕТА
3.1. ОРГАНЫ ИММУННОЙ СИСТЕМЫ
Несмотря на то что синтез антител может быть получен in vitro, когда анатомические связи между клетками иммунной системы нарушены, а нейроэндокринная регуляция отсутствует, для получения полноценного иммунного ответа необходим весь комплекс реакций, присущий целостному организму. Существует своеобразная иерархия органов иммунной системы, в которой можно выделить первичные и вторичные лимфоидные органы. К первым относятся тимус (вилочковая железа) и костный мозг (у птиц еще и фабрициева сумка), ко вторым — лимфатические узлы, селезенка, а также лимфоидная ткань, ассоциированная со слизистыми оболочками. Указанные органы связаны между собой и с остальными тканями организма с помощью кровеносной системы и лимфатических путей. По ним передвигаются рециркулирующие лимфоциты, за счет которых и осуществляется эта связь.
Костный мозг. В собственном смысле слова костный мозг не является лимфоидным органом. Тем не менее его значение для функционирования иммунной системы огромно. Именно в костном мозге из плюрипотентной стволовой клетки возникают все форменные элементы крови, в том числе и предшественники различных популяций лимфоцитов, а также макрофагальные клетки. Кроме того, есть данные, указывающие на то, что костный мозг является одним из основных мест синтеза антител. Так, у взрослой мыши в костном мозге сосредоточено до 80% всех клеток, секретирующих иммуноглобулины. Внутривенное введение клеток костного мозга может полностью восстановить иммунную систему у смертельно облученных животных. У млекопитающих костный мозг является эквивалентом фабрициевой сумки птиц — здесь созревают В-лимфоциты.
Тимус. Тимус представляет собой окруженный капсулой лимфоидный орган, который располагается за грудиной в переднем средостении. Это первый лимфоидный орган, возникающий в процессе эмбриогенеза у млекопитающих и птиц. Каждая доля тимуса (у млекопитающих их две) состоит из долек, частично отделенных одна от другой с помощью выростов капсулы, называемых перегородками, или трабекулами. Периферическую часть дольки занимает кора, а центральную часть — мозговое вещество. Важную роль в функционировании тимуса играет строма, состоящая главным образом из эпителиальных клеток. Эпителиальные клетки тимуса синтезируют ряд пептидных гормонов, из которых четыре изучены достаточно хорошо. К ним относятся тимулин, - и -тимозин и тимопоэтин. Активным центром последнего является пентапептид ТР-5. Указанные пептидные гормоны участвуют в многоэтапной дифференцировке лимфоцитов в тимусе.
Протимоциты привлекаются в тимус за счет хемотаксических факторов. По мере созревания на поверхности тимоцитов начинают экспрессироваться различные дифференцировочные антигены. Это могут быть маркеры, специфичные для тимоцитов коркового слоя (CD1) и характерные только для незрелых Т-клеток, постоянные маркеры Т-лимфоцитов (CD3, CD5), а также маркеры, специфичные для популяций хелперов/индукторов (CD4) и цитотоксических/ супрессорных лимфоцитов (CD8). В тимусе Т-лимфоциты приобретают способность распознавать антигены в контексте собственных антигенов МНС. Репертуар клонов Т-клеток формируется за счет механизмов клеточной селекции.
Существует два типа клональной селекции: положительная и отрицательная. Положительная селекция основана на распознавании антигена, ассоциированного с молекулами, являющимися продуктами собственных МНС. Отрицательной селекции подвергаются клетки, несущие аутореактивные Т-клеточные рецепторы. Стимуляция таких рецепторов антигенами МНС включает в клетках механизм программированной клеточной гибели (апоптоз), в результате чего происходит элиминация клонов аутореактивных Т-лимфоцитов. Механизм апоптотической гибели клеток уже упоминался при рассмотрении взаимодействия цитотоксической клетки-эффектора с клеткой-мишенью. Этот механизм играет важную роль в реализации разнообразных иммунных реакций, а также лежит в основе патогенеза многих заболеваний, поэтому рассмотрим несколько подробнее проблему апоптоза.
Апоптоз (программированная клеточная гибель, клеточное самоубийство) в отличие от некроза представляет собой физиологический механизм гибели клетки. Некроз, являющийся патологической формой гибели клетки, характеризуется острым нарушением клеточных структур, сопровождающимся быстрым набуханием клетки и лизисом. В противоположность этому апоптоз — контролируемая форма самопереваривания клетки. Этот механизм делает минимальным риск попадания клеточного содержимого в межклеточное пространство, в результате чего гибель клеток не сопровождаеься признаками реакции воспаления. При апоптозе включается механизм активации эндогенных протеаз с последующим разрушением цитоскелета и сжатием клетки. За счет активации эндонуклеаз деградирует ядерная ДНК. Последняя разрезается на отдельные фрагменты, которые вместе с частью цитоплазмы окружаются участком клеточной мембраны, образуя так называемые апоптотические тельца. Утилизация апоптотических телец осуществляется за счет фагоцитоза. Иногда, например при взаимодействии цитотоксического лимфоцита-эффектора с клеткой-мишенью, для индукции апоптоза необходимо связывание поверхностного Fas-белка (CD95), называемого также Fas-рецептором, с другим белком клеточной поверхности — Fas-лигандом. Последний относится к тому же семейству белков, что и TNF. Взаимодействие Fas-лиганда и Fas-рецептора запускает программу клеточной гибели. Эта программа может быть также запущена и через другие рецепторы, например TNF-рецептор I типа, рецепторы для глюкокортикоидов, циклофилины.
Патогенез многих заболеваний связан с нарушением механизма апоптотической гибели клеток. Заболевания, относящиеся к этой группе, можно разделить на заболевания, связанные с подавлением апоптоза, и заболевания, при которых, наоборот, имеет место усиление апоптотической гибели клеток. К первой группе относят злокачественные новообразования (множественная лимфома, карцинома с мутацией в области р53, гормонзависимые опухоли — рак грудной железы, рак предстательной железы, рак яичника), аутоиммунные заболевания (системная красная волчанка — СКВ и гломерулонефрит) и некоторые вирусные инфекции. Вторая группа включает СПИД, нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз и др.), синдромы миелодисплазии (апластическая анемия), ишемические нарушения (инфаркт миокарда, инсульт, другие синдромы, связанные с временным нарушением кровоснабжения), а также токсические повреждения печени (алкогольный цирроз).
Лимфатические узлы. Лимфатические узлы являются вторым (после кожи и слизистых оболочек) барьером на пути инфекции. Ткани организма дренируются лимфатическими сосудами, по которым лимфа поступает в ворота лимфатического узла. По афферентным сосудам лимфа поступает в краевой синус, диффундирует сквозь лимфоциты коркового вещества к макрофагам и синусам мозгового вещества. Затем по эфферентным сосудам лимфа поступает в грудной проток, а оттуда в кровь. Т- и В-лимфоциты расположены в лимфатическим узле неравномерно.
Покоящиеся В-лимфоциты образуют скопления в кортикальной области. Эти области называются первичными фолликулами. После антигенной стимуляции В-лимфоциты образуют вторичные фолликулы, в которых покоящиеся В-лимфоциты окружают зародышевый центр, содержащий крупные интенсивно пролиферирующие В-лимфобласты, ретикулярные макрофаги и специализированные дендритные клетки. Остальная часть кортикальной области также состоит преимущественно из В-клеток, хотя содержит и диффузно расположенные Т-лимфоциты.
Основная масса Т-лимфоцитов располагается в паракортикальной, или тимусзависимой, области лимфатического узла. При формировании иммунного ответа Т-лимфоциты этой области также превращаются в лимфобласты и активно пролиферируют. Однако при ответе на тимуснезависимый антиген (например, на пневмококковый полисахарид SIII) лимфоциты паракортикальной области не активируются, тогда как в фолликулах кортикальной зоны наблюдается интенсивная клеточная пролиферация с образованием зародышевых центров.
Селезенка. Лимфоидная ткань селезенки образует белую пульпу, окруженную заполненной эритроцитами красной пульпой. Участки красной пульпы содержат макрофаги и пронизаны венозными синусами. В-клетки занимают в селезенке краевую зону, а Т-лимфоциты — центральную.
Лимфоидная ткань, ассоциированная со слизистыми оболочками. Для обозначения этого вида лимфоидной ткани используется сокращение MALT (mucosal- associated lymphoid tissue). MALT представляет собой субэпителиальные скопления лимфоидной ткани, не ограниченной соединительнотканной капсулой. Лимфоидная ткань может располагаться диффузно, представляя собой скопления лимфоцитов, фагоцитов и плазматических клеток в легких или lamina propria стенки кишечника, или быть достаточно хорошо организованной с выраженными фолликулами. У человека это кольцо Вальдейера — Пирогова, состоящее из язычной, небной и глоточных миндалин, групповые лимфатические фолликулы (пейеровы бляшки) кишечника, а также аппендикс. MALT образует особую систему, в которой циркулируют клетки, синтезирующие IgA и IgE.
3.2. КЛЕТКИ, УЧАСТВУЮЩИЕ В ФОРМИРОВАНИИ ИММУННОГО ОТВЕТА
Макрофаги. Из всех клеток, участвующих в реализации иммунного ответа, макрофаг отличается наиболее выраженной полифункциональностью. К важнейшим функциям макрофагов следует отнести фагоцитоз, процессинг антигенов и представление процессированного антигена лимфоцитам, синтез цитокинов и компонентов системы комплемента, а также синтез многих лизосомных ферментов. Макрофаги образуются в костном мозге из промоноцитов и в форме моноцитов циркулируют в периферической крови. Попадая в различные ткани, они могут терять подвижность (становятся резидентными клетками), а их морфология может меняться (рис. 9). Тем не менее генетическая программа, ответственная за реализацию их функций, не претерпевает существенных изменений. Так, звездчатые ретикулоэндотелиоциты (купферовские клетки) печени, помещенные в искусственные условия, могут осуществлять презентацию антигенов Т-клеткам.
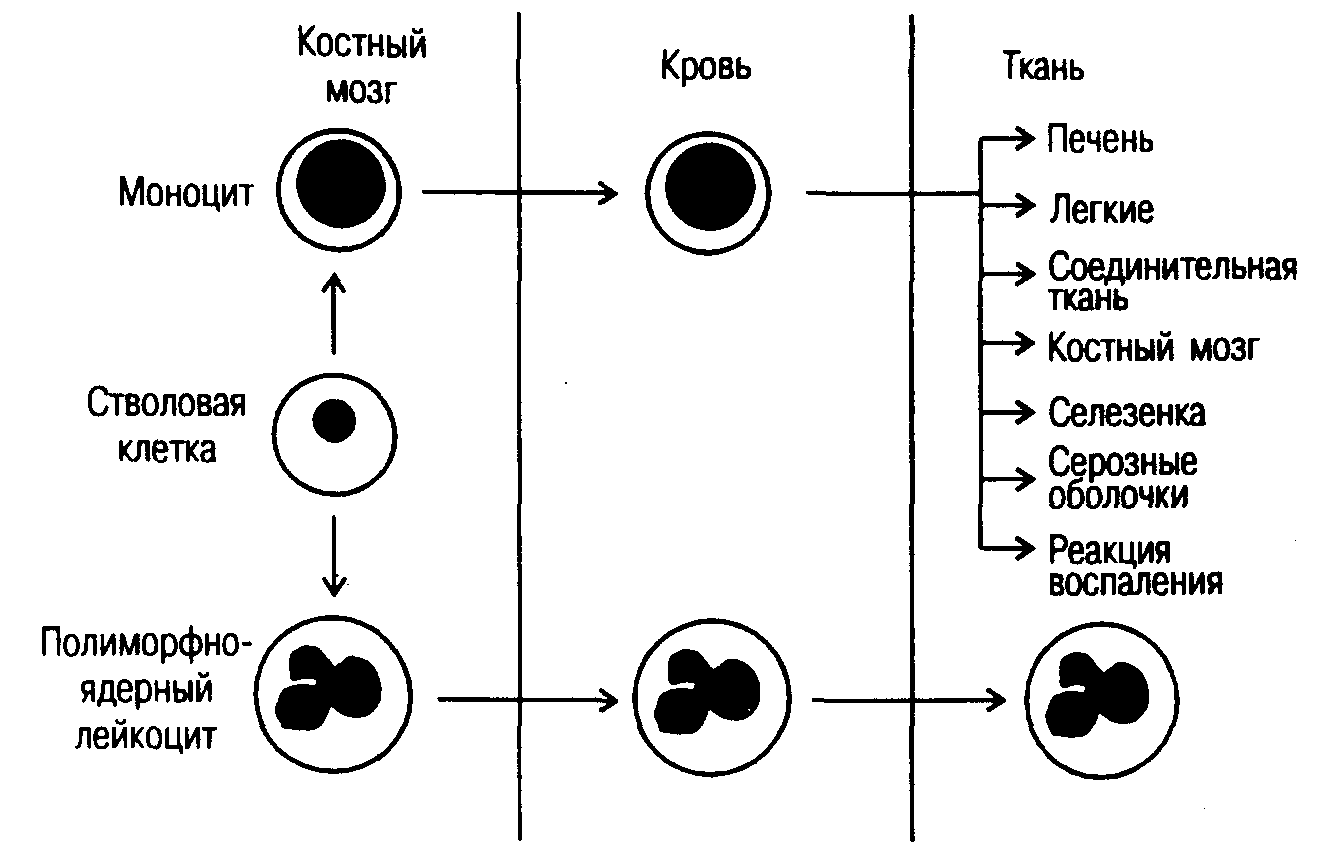
Рис. 9. Происхождение различных фагоцитирующих клеток.
Макрофаги обладают примитивным механизмом узнавания, основанным на взаимодействии углеводных остатков. С помощью этого механизма обеспечивается адгезия микроба на поверхности фагоцитирующей клетки. Частица, прикрепившаяся к поверхности макрофага, активирует актинмиозиновую сократительную систему, в результате чего образуются псевдоподии, с помощью которых плазматическая мембрана постепенно надвигается на объект фагоцитоза. В конечном итоге частица оказывается заключенной в вакуоль (в фагосому). Сразу же с фагосомой сливаются цитоплазматические гранулы, и их содержимое оказывается внутри фагосомы. В процессе фагоцитоза в макрофаге быстро активируется метаболизм глюкозы по гексозомонофосфатному пути и образуются свободные радикалы. Это вызывает резкое нарастание потребления кислорода («дыхательный взрыв»). События развиваются в следующей последовательности. Из моновалентного молекулярного кислорода образуется надперекисный анион (О2—), который спонтанно или под действием супероксиддисмутазы превращается в перекись водорода (Н2О2). В конечном итоге происходит вторичное образование гидроксильных радикалов (ОН) и синглетного (активного) кислорода ('О2).
Эта система зависимых от кислорода бактерицидных агентов дополняется кислороднезависимыми механизмами, которые включают катионные белки, повреждающие мембраны микроорганизмов, лизоцим, способный расщеплять мукопептиды клеточной стенки бактерий, лактоферрин, с помощью которого пролиферирующие бактерии лишаются железа, и набор протеолитических и гидролитических ферментов, переваривающих убитые микроорганизмы.
Лимфоциты. Долгое время считалось, что малый лимфоцит является высокодифференцированной клеткой, деление которой невозможно. Такое мнение сложилось среди гистологов и гематологов в связи с тем, что в лимфоцитах никогда не удавалось наблюдать фигуры митозов. Однако в конце 50-х — начале 60-х годов D. A. Hungerfbrd и Р. С. Novell показали, что при культивировании в присутствии экстракта из зерен красной фасоли Phaseolus vulgaris лимфоцитов периферической крови последние трансформируются в крупные бластные клетки, которые на 3-й и 4-й день культивирования можно видеть в состоянии митоза.
Примерно в это же время (60-е годы) пионерскими работами нескольких групп исследователей (R. A. Good, J. В. Miller, J. H. Humphrey и N. A. Mitchison) было установлено, что лимфоциты, несмотря на свое морфологическое единообразие, на самом деле состоят из двух разных клеточных популяций, имеющих совершенно различный онтогенез. Было показано, что продукция антител возможна только в результате кооперации двух популяций лимфоцитов — Т и В. Те и другие клетки образуются в костном мозге из стволовой кроветворной клетки, после чего предшественники Т-лимфоцитов попадают в тимус, где дифференцируются в зрелые Т-лимфоциты, а предшественники В-лимфоцитов созревают в других лимфоидных органах. Как отмечалось, у птиц таким органом является фабрициева сумка, у млекопитающих эквивалентом этого лимфоидного органа является костный мозг.
Сравнительная характеристика популяций Т- и В-лимфоцитов представлена в табл. 4.
Лимфоциты различаются между собой и по продолжительности жизни. Различают короткоживущие (5—6 дней) и долгоживущие (от нескольких месяцев до нескольких лет) лимфоциты. Клетки обеих этих категорий встречаются среди как Т-, так и В-лимфоцитов.
Популяция Т-лимфоцитов. Больше 50% лимфоцитов периферической крови и около 90% лимфоцитов грудного протока составляют Т-лимфоциты (среди последних более 70% — это долгоживущие лимфоциты). На мембране Т-лимфоцитов имеются характерные антигенные маркеры, отличающие эту популяцию от других лимфоидных клеток. Кроме того, Т-лимфоциты несут рецептор для эритроцитов барана (этот рецептор характерен только для Т-клеток человека). Благодаря данному рецептору Т-лимфоциты в смеси с эритроцитами барана образуют характерные фигуры розеток. Это свойство человеческих Т-лимфоцитов используется в лабораторной практике для их идентификации и подсчета (см. часть II, раздел 7.4). Важным свойством Т-лимфоцитов является их способность трансформироваться и пролиферировать в культуре под воздействием некоторых лектинов растительного происхождения. К ним относятся фитогемагглютинин (ФГА) и конканавалин А (Кон А).
Таблица 4. Сравнение свойств В- и Т-лимфоцигов
Свойство
|
В-лимфоциты
|
Т-лимфоциты
|
Морфология
|
Без особенностей
|
Без особенностей
|
Дифференцировка
|
Под влиянием фабрициевой сумки (у птиц); у млекопитающих — в костном мозге
|
Под влиянием тимуса
|
Поверхностные антигены
|
CD2 (рецептор для эритроцитов барана)
|
—
|
+
|
CD3
|
—
|
+
|
CD4
|
—
|
+
|
CD5
|
—
|
+
|
CD8
|
—
|
+
|
CD19
|
+
|
—
|
CD20
|
+
|
—
|
CD21
|
+
|
—
|
CD22
|
+
|
—
|
HLA
|
I класс (А, В, С)
|
+
|
+
|
II класс (DR. DQ, DP)
|
+
|
+ (на активированных Т-клетках)
|
Рецепторы
|
для антигена
|
+ (иммуноглобулиновый рецептор)
|
+ (неиммуноглобулино-вый рецептор)
|
для комплемента
|
+
|
—
|
Fc-рецептор
|
++
|
+
|
Пролиферативный ответ
|
ФГА
|
—
|
+
|
Кон А
|
—
|
+
|
СКЛ
|
—
|
+
|
МЛ (PWM)
|
+
|
+
|
ЛПС
|
+
|
—
|
Nocardia
|
+
|
—
|
Содержание в разных органах, %
|
Кровь
|
15—20
|
50—80
|
Лимфатические узлы
|
15
|
85
|
грудной проток
|
10
|
90
|
Костный мозг
|
10—15
|
<3
|
Тимус
|
<3
|
>97
|
Циркуляция
|
Слабая рециркуляция. Локализация в фолликулах вокруг зародышевых центров
|
Рециркуляция многих клеток. Локализация в тимусзависимых зонах
|
Продолжительность жизни
|
В большинстве — ко-роткоживущие, но есть и долгоживущие
|
Сосуществование коротко- и долгоживущих
|
Функция
|
Продукция антител
|
Секреция
|
Регуляция
|
ГЗТ
|
Не участвуют
|
Клетки-эффекторы и регуляторы
|
Отторжение трансплантата и опухоли
|
Продукция цитотокси-ческих и блокирующих антител
|
Цитотоксические клетки-эффекторы
|
Толерантность
|
Поздняя и транзисторная
|
Ранняя и стойкая
|
Популяция Т-лимфоцитов неоднородна, а состоит из нескольких субпопуляций, различающихся как по поверхностным антигенам, так и по функции. Это прежде всего Т-хелперы (индукторы), Т-супрессоры и ЦТЛ. Для первых характерен поверхностный маркер CD4, а для двух других — CD8.
Показано, что клетки с фенотипом CD4* также подразделяются на два функционально различных подтипа — Th1 и Th2. Th1-клетки участвуют в реализации реакции гиперчувствительности замедленного типа (ГЗТ) и способны, синтезировать ИЛ-2, ИФН и лимфотоксин, а Тh2-клетки продуцируют ИЛ-4, ИЛ-5, ИЛ-6 и ИЛ-10.
Популяция В-лимфоцитов. В-лимфоциты в отличие от Т-клеток обладают слабой способностью к рециркуляции. В связи с этим В-клетки практически отсутствуют в лимфе грудного протока, а в крови их количество составляет не более 30%. Среди В-лимфоцитов явно преобладают короткоживущие, хотя встречаются и долгоживущие клетки. Характерной особенностью В-лимфоцита является наличие на его поверхности иммуноглобулинового рецептора, а также рецептора к С'3. Эти свойства помогают в идентификации и подсчете количества В-лимфоцитов (см. часть II, раздел 7.4). Кроме того, на поверхности В-лимфоцитов имеются характерные антигенные маркеры, к которым получены моноклональные антитела (CD 19, CD20, CD22, а также CD21 — зрелые В-клетки и CD23 — плазматические клетки), используемые для идентификации В-лимфоцитов.
|
|
|
 Скачать 0.8 Mb.
Скачать 0.8 Mb.
