Справочный материал. Глава 25 – Органы дыхания. Справочный материал по Физиологии. Глава 25 Органы дыхания
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
|
Гипоксия Дыхание (внешнее дыхание в лёгких, транспорт газов в крови и тканевое дыхание) направлено на снабжение клеток, тканей, органов и организма кислородом. Недостаточное выполнение функции дыхания приводит к развитию кислородного голодания — гипоксии. Терминология. Гипоксия (кислородное голодание, кислородная недостаточность) — состояние, возникающее в результате недостаточного обеспечения организма кислородом и/или нарушения усвоения кислорода в ходе тканевого дыхания. Гипоксемия (уменьшение по сравнению с должным уровней напряжения и содержания кислорода в крови) нередко сочетается с гипоксией. Аноксия (отсутствие кислорода и прекращение процессов биологического окисления) и аноксемия (отсутствие кислорода в крови) в целостном живом организме не наблюдаются, эти состояния относятся к экспериментальным или специальным (перфузия отдельных органов) ситуациям. Классификация. Гипоксические состояния классифицируют с учётом их причин (этиологии), выраженности расстройств, скорости развития и длительности гипоксии. По этиологии выделяют несколько типов гипоксии (рис. 25–12), подразделяемых на экзогенные (нормо и гипобарическую гипоксию) и эндогенные. 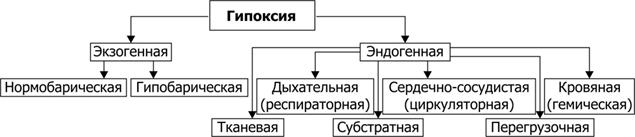 Рис. 25–12. Типы гипоксии по этиологии [17] Экзогенный тип гипоксии. Сюда относят нормо и гипобарическую гипоксию. Причина их развития: уменьшение Po2 вдыхаемого воздуха. Нормобарическая экзогенная гипоксия (барометрическое давление нормальное) развивается при ограничении поступления в организм кислорода с воздухом, что наблюдается при нахождении в небольшом и/или плохо вентилируемом пространстве (помещении, шахте, колодце, лифте), при нарушениях регенерации воздуха и/или подачи кислородной смеси для дыхания в летательных и глубинных аппаратах, автономных костюмах (космонавтов, лётчиков, водолазов, спасателей, пожарников), при нарушении методики проведения искусственной вентиляции лёгких. Гипобарическая экзогенная гипоксия (барометрическое давление понижено) развивается при снижении барометрического давления при подъёме на высоту (более 3000–3500 м, где Po2 воздуха снижено примерно до 100 мм рт.ст.) или в барокамере. В этих условиях возможно развитие либо горной, либо высотной, либо декомпрессионной болезни. Горная болезнь наблюдается при подъёме в горы, где организм подвергается воздействию не только пониженного содержания кислорода в воздухе и пониженного барометрического давления, но также более или менее выраженной физической нагрузки, охлаждения, повышенной инсоляции и других факторов средне и высокогорья. Высотная болезнь развивается у людей, поднятых на большую высоту в открытых летательных аппаратах, на креслах подъёмниках, а также при снижении давления в барокамере. В этих случаях на организм действуют в основном сниженные Po2 во вдыхаемом воздухе и барометрическое давление. Декомпрессионная болезнь наблюдается при резком снижении барометрического давления (например, в результате разгерметизации летательных аппаратов на высоте более 10 000–11 000 м). При этом формируется опасное для жизни состояние, отличающееся от горной и высотной болезни острым или даже молниеносным течением. Патогенез экзогенных гипоксий. Основные звенья развития экзогенной гипоксии (независимо от её причины): артериальная гипоксемия, гипокапния, респираторный алкалоз и артериальная гипотензия, сочетающаяся с уменьшенной перфузией (гипоперфузией) органов и тканей. Снижение напряжения кислорода в артериальной крови (Раo2 — артериальная гипоксемия) — начальное и главное звено механизма развития экзогенной гипоксии. Гипоксемия ведёт к нарушениям газообмена и метаболизма в тканях. Снижение напряжения в крови углекислого газа (Раco2 — гипокапния) возникает в результате компенсаторной гипервентиляции лёгких (развивается в связи с гипоксемией). Респираторный алкалоз является результатом гипокапнии. Снижение системного АД (артериальная гипотензия) обязательно сочетается с гипоперфузией тканей и в значительной мере является следствием гипокапнии. CO2 относится к числу основных факторов регуляции тонуса сосудов мозга. Значительное снижение Раco2 является сигналом к сужению просвета артериол мозга, сердца и уменьшения их кровоснабжения. Эти изменения служат причиной существенных расстройств жизнедеятельности организма, включая развитие обморока и коронарной недостаточности (проявляющейся стенокардией, а иногда — инфарктом миокарда). Параллельно с указанными отклонениями выявляются нарушения ионного баланса как в клетках, так и в биологических жидкостях: межклеточной, плазме крови (гипернатриемия, гипокалиемия и гипокальциемия), лимфе, ликворе. Эндогенные типы гипоксии (дыхательная, циркуляторная, гемическая, тканевая) являются результатом патологических процессов и болезней, приводящих к недостаточной вентиляции и перфузии лёгких, ухудшению транспорта к органам кислорода и субстратов обмена веществ и/или использования их тканями. Гипоксия может также развиться в результате резкого увеличения потребности организма в энергии в связи со значительно возросшими нагрузками (например, при значительном повышении физической нагрузки). При этом даже максимальная активация кислородтранспортных и энергопродуцирующих систем не способна ликвидировать энергодефицита (перегрузочная гипоксия). Дыхательная гипоксия. Причина дыхательной (респираторной) гипоксии — недостаточность газообмена в лёгких — дыхательная недостаточность. Развитие дыхательной недостаточности может быть обусловлено альвеолярной гиповентиляцией, сниженной перфузией кровью лёгких, нарушением диффузии кислорода через аэрогематический барьер, вентиляционно–перфузионным дисбалансом. Вне зависимости от происхождения дыхательной гипоксии, начальным патогенетическим звеном является артериальная гипоксемия. Альвеолярная гиповентиляция характеризуется тем, что объём вентиляции лёгких за единицу времени ниже потребности организма в газообмене за то же самое время. Такое состояние является результатом нарушения биомеханических свойств дыхательного аппарата и расстройства регуляции вентиляции лёгких. Снижение перфузии лёгких кровью вследствие уменьшения объёма циркулирующей крови (гиповолемии), недостаточности сократительной функции сердца, увеличения сопротивления току крови в сосудистом русле лёгких (лёгочная сосудистая гипертензия). Нарушение диффузии кислорода через аэрогематический барьер из-за утолщения и/или уплотнения компонентов альвеоло–капиллярной мембраны. Это ведёт к более или менее выраженному альвеоло–капиллярному разобщению газовой среды альвеол и крови капилляров, что наблюдается при отёке лёгких, диффузном фиброзе (разрастании соединительной ткани) интерстиция лёгких (например, при, при силикозе и асбестозе). Вентиляционно–перфузионный дисбаланс происходит при нарушении проходимости бронхов и/или бронхиол, снижении растяжимости альвеол, локальном снижении кровотока в лёгких. Такие изменения наблюдаются, например, при бронхоспазме и пневмосклерозе различного генеза, эмфиземе лёгких, эмболии или тромбозе ветвей их сосудистого русла. Это приводит к тому, что какие то регионы лёгких нормально вентилируются, но недостаточно перфузируются кровью, какие то напротив, хорошо кровоснабжаются, но недостаточно вентилируются. В связи с этим в крови, оттекающей от лёгких, выявляется гипоксемия. Изменения газового состава и рН крови при дыхательном типе гипоксии представлены на рис. 25–13. 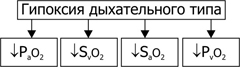 Рис. 25–13. Изменения газового состава и рН крови при гипоксии дыхательного типа [17] где Рао2 и Рvо2 (показатели напряжения кислорода в артериальной и венозной крови), Sao2 и Svo2 — показатели насыщения Hb в артериальной и венозной крови. Циркуляторная гипоксия. Причина развития сердечно сосудистой (циркуляторной, гемодинамической) гипоксии — недостаточность кровоснабжения тканей и органов, формирующейся на основе гиповолемии (уменьшение общего объёма крови в сосудистом русле и полостях сердца), сердечной недостаточности, снижения тонуса стенок сосудов, расстройств микроциркуляции, нарушений диффузии кислорода из капиллярной крови к клеткам. Гемический тип гипоксии. Причина развития кровяной (гемической) гипоксии: снижение эффективной кислородной ёмкости крови и, следовательно, транспортирующей кислород функции. Транспорт кислорода от лёгких к тканям почти полностью осуществляется при помощи Hb. Наибольшее количество кислорода, которое способен переносить Hb, равно 1,39 мл газообразного O2 на 1 г Hb. Реально транспортная способность Hb определяется количеством кислорода, связанного с Hb, и количеством кислорода, отданного тканям. При насыщении Hb кислородом в среднем на 96% кислородная ёмкость артериальной крови (VaO2) достигает примерно 20% (объёмных единиц). В венозной крови этот показатель приближается к 14% (объёмным единицам). Следовательно, артерио–венозная разница по кислороду составляет 6%. Гемический тип гипоксии характеризуется снижением способности Hb эритроцитов связывать кислород (в капиллярах лёгких), транспортировать O2 и отдавать оптимальное количество O2 в тканях. При гемической гипоксии реальная кислородная ёмкость крови может снижаться до 5–10% (объёмных). Тканевая гипоксия. Причины развития тканевой гипоксии: факторы, снижающие эффективность утилизации кислорода клетками тканей (обычно в результате ингибирования активности ферментов биологического окисления, значительного изменения физико химических параметров в тканях, торможения синтеза ферментов биологического окисления и повреждения мембран клеток) и/или сопряжения окисления и фосфорилирования. Субстратный тип гипоксии. Причины: дефицит в клетках субстратов биологического окисления. В клинической практике речь чаще всего идёт об глюкозе. При этом доставка к клеткам кислорода существенно не нарушена. Резистентность органов к гипоксии. При гипоксии нарушения функций органов и тканей выражены в разной мере. Наименьшей резистентностью к гипоксии обладает ткань нервной системы. Наибольшая устойчивость к гипоксии у костей, хрящей, сухожилий, связок. Даже в условиях тяжёлой гипоксии в них не обнаруживается значительных морфологических отклонений. В скелетной мускулатуре изменения структуры миофибрилл, а также их сократимости выявляются через 100–120 мин, а в миокарде — уже через 15–20 мин. В почках и печени морфологические отклонения и расстройства функций обнаруживаются обычно через 20–30 мин после начала гипоксии. Резистентность нервных клеток уменьшается в следующем порядке: периферические нервные узлы (так, в ганглиях вегетативной нервной системы морфологические изменения наступают через 50–60 мин) спинной мозг продолговатый мозг гиппокамп мозжечок кора больших полушарий. Прекращение оксигенации коры мозга вызывает значительные структурные и функциональные изменения в ней уже через 2–3 мин, в продолговатом мозге через 8–12 мин. Отсюда следует, что последствия гипоксии для организма в целом определяются степенью повреждения нейронов коры больших полушарий и временем их развития. Гиперкапния Гиперкапния — избыток углекислого газа в жидкостях тела. Если уровень альвеолярного PСО2 повышается от 60 до 75 мм рт.ст. дыхание становится глубоким и частым, а диспноэ (субъективное ощущение укорочения дыхания) более тяжёлым. Как только PCO2 возрастает от 80 до 100 мм рт.ст., возникает вялость и апатия, иногда полукоматозное состояние. Смерть может наступить при уровнях PСО2 от 120 до 150 мм рт.ст. Дыхательные адаптивные механизмы Приспособление (адаптация) системы дыхания к мышечной работе, к условиям необычной среды (пониженному и повышенному барометрическому давлению, гипоксии, загрязненной среде и т.д.), а также правильная диагностика и лечение дыхательных расстройств определяются глубиной понимания основных физиологических принципов дыхания и газообмена. Ряд респираторных заболеваний — результат неадекватной вентиляции, в то время как другие — результат затруднённой диффузии через аэрогематический барьер. Действие повышенного барометрического давления (гипербария). Давление при погружении в воду увеличивается на 1 атм на каждые 10 м глубины (соответственно увеличивается количество растворённых газов). Создание барокамер позволило изучить эффект и повышенного барометрического давления, и высоких давлений газов на тело человека без глубоководных погружений. Кислород. При PО2 около 3000 мм рт.ст. (около 4 атм) общее количество не связанного с Hb, а физически растворённого в крови кислорода составляет 9 мл/100 мл крови. МОЗГ особенно чувствителен к острому кислородному отравлению. После 30–минутной экспозиции в среде с давлением O2 в 4 атм возникают судорожные припадки с последующей комой. Токсическое влияние O2 на нервную систему вызвано действием т.н. активных форм кислорода (синглетного — 1O2, супероксидного радикала — O2–, пероксида водорода — Н2О2, гидроксильного радикала — OH–). В тканях с нормальным PО2 (40 мм рт.ст.) постоянно формируется небольшое количество активных форм кислорода. В тканях с повышенным PО2 (2 атм и выше) образуется много активных форм кислорода, подавляющих функцию ферментов, предназначенных для их удаления. Активные формы кислорода Супероксидный радикал O2– генерируют лейкоциты (особенно интенсивно при фагоцитозе), митохондрии в процессе окислительных реакций, разные ткани при метаболической трансформации катехоламинов, синтезе Пг и других соединений. Пероксид водорода H2О2 образуется при взаимодействии (дисмутации) радикалов O2– в цитозоле клеток и матриксе митохондрий. Этот процесс катализирует супероксид дисмутаза: O2– + O2– + 2H+ H2O2 + O2 O2– и H2O2 оказывают повреждающее действие и сами по себе, но под влиянием ионов железа, присутствующих как в цитоплазме, так и в биологических жидкостях, O2– и H2O2 могут трансформироваться под влиянием каталазы в весьма агрессивный и обладающий высоким патогенным эффектом гидроксильный радикал OH–: H2O2 + Fe2 + Fe3 + + OH + OH–; O2– + H2O2 O2 + OH + OH– Гидроксильные радикалы OH– активно вступают в реакции с органическими соединениями, главным образом липидами, а также нуклеиновыми кислотами и белками. В результате образуются другие активные радикалы и перекиси. При этом реакция может приобрести цепной лавинообразный характер. ЛЁГКИЕ. Дыхание в течение нескольких часов газовой смесью с высокой концентрацией O2 может привести к повреждению лёгких. Первые патологические изменения обнаруживаются в эндотелиальных клетках лёгочных капилляров. У здоровых добровольцев при дыхании чистым кислородом при нормальном атмосферном давлении через 24 ч возникают неприятные ощущения за грудиной, усугубляющиеся при глубоком дыхании. Кроме того, жизненная ёмкость лёгких у них снижается на 500–800 мл. Это обусловливает так называемый абсорбционный ателектаз, вызванный интенсивным переходом O2 в венозную кровь и быстрым спадением альвеол. Послеоперационный ателектаз часто встречается у больных, дышащих газовыми смесями с высоким содержанием O2. Особенно высокая вероятность спадения паренхимы лёгкого имеется в нижних его отделах, где паренхима лёгких расправлена в наименьшей степени. Азот. Во время водолазного погружения парциальное давление N2 возрастает, в результате этот плохо растворимый газ накапливается в тканях. Во время подъёма азот медленно удаляется из тканей. Если декомпрессия происходит слишком быстро, образуются пузырьки азота. Большое количество пузырьков сопровождается болями, особенно в области суставов (кессонная болезнь). В тяжёлых случаях могут возникать нарушения зрения, глухота и даже параличи. Для лечения декомпрессионной болезни пострадавшего помещают в специальную камеру с высоким давлением. Загрязнённая атмосфера. Рост числа автомобилей и промышленных предприятий делает загрязнённую атмосферу привычной средой обитания. К основным загрязнителям воздуха относятся различные окислы азота, серы, озон, угарный газ, углеводороды и пыль. Содержание загрязнений в воздухе значительно увеличивается при температурной инверсии, когда нагретый поверхностный воздух не может подниматься в верхние слои атмосферы (смог). Окислы азота вызывают воспаление верхних дыхательных путей и глаз. Окислы серы и озон также приводят к бронхитам, а в высоких концентрациях озон может вызывать отек лёгких. Угарный газ (CO) связывает Hb, а циклические углеводороды — потенциальные канцерогены. Эти вещества содержатся и в табачном дыме, причём в гораздо большей концентрации, чем в самой загрязнённой атмосфере. Экстремальные состояния Экстремальные состояния — общие тяжёлые состояния организма, развивающиеся под действием экстремальных факторов внешней или внутренней среды и характеризующиеся значительными расстройствами жизнедеятельности организма, чреватыми смертью. Экстремальные состояния проявляются, как правило, предельной активацией и последующим истощением механизмов адаптации, грубыми расстройствами функций органов и физиологических систем. Экстремальные состояния требуют неотложной врачебной помощи. К наиболее частым и клинически значимым неотложным состояниям относят коллапс, шок, кому и отравления. От экстремальных необходимо отличать терминальные состояния, которые представляют собой конечные этапы жизни организма, пограничное состояние между жизнью и смертью. К терминальным состояниям относят все стадии умирания — преагонию, агонию, клиническую смерть, биологическую смерь, а также начальный этап состояния после успешной реанимации. Периодические формы дыхания. Расстройства системы внешнего дыхания усугубляют течение экстремальных состояний в связи с потенцированием гипоксемии, гиперкапнии и гипоксии. На стадии недостаточности механизмов адаптации, как правило, развиваются так называемые периодические формы дыхания (Биота, ЧейнаСтокса, Куссмауля), а при тяжёлом течении — его полное прекращение — апноэ. Искусственная вентиляция лёгких (ИВЛ) проводится при ряде экстремальных состояний. |
