печёнка. Тема патофизиология печени
 Скачать 0.64 Mb. Скачать 0.64 Mb.
|
|
Тема № 7. ПАТОФИЗИОЛОГИЯ ПЕЧЕНИ. Этиология и патогенез печеночной недостаточности. Причины поражения печени: 1. Физические факторы – ионизирующее излучение, механическая травма; 2. Химические факторы (оказывающие гепатотоксическое действие) – экзогенные (алкоголь - острая или хроническая алкогольная интоксикация, лекарственные препараты - антибиотики, индометацин, парацетамол, яды) и эндогенные (про-дукты распада тканей при некрозе, ожогах, токсикоз беременных); 3. Инфекционные – вирусы, простейшие (лямблии), грибы, гельминты. 4. Алиментарные факторы – белковое голодание, жирная пища. 5. Аллергические реакции – на введение вакцин, сывороток, пищевых продуктов, лекарственных препаратов; 6. Эндокринные и обменные нарушения – сахарный диабет, ожирение; 7. Нарушение кровообращения в печени, длительный венозный застой – местное (тромбоз, эмболия, ишемия) и общее ((недостаточность кровообращения); 8. Генетические нарушения обмена веществ – врожденные пороки развития пече-ни, наследственные ферментопатии; 9. Опухоли и их метастазы Патогенез: (по книге) Модификация и/или деструкция плазмолеммы, других мембран и цитоскелета гепатоцитов, развитие иммунопатологических, воспалительных, свободнорадикальных процессов, активация гидролаз приводит к массированному разрушению клеток печени, выходу в интерстиций их содержимого, включая многочисленные гидролитические ферменты. Названные факторы дополнительно потенцируют воспалительные, иммунопатологические и свободнорадикальные реакции. Это, в свою очередь, делает процесс поражения печени тотальным и нарастающим по степени. Проявления печеночной недостаточности и механизмы их развития. Печёночная недостаточность характеризуется признаками расстройств обмена веществ и функций печени. • Расстройства обмена веществ. † Белки. ‡ Нарушение синтеза гепатоцитами альбуминов проявляется гипоальбуминемией и диспротеинемией. Гипоальбуминемия способствует развитию отёков и формированию асцита (в условиях повышения давления крови в сосудах воротной вены). ‡ Торможение синтеза белков системы гемостаза (проконвертина, проакцелерина, фибриногена, протромбина, факторов Кристмаса и Стюарта-Прауэр, антикоагулянтных белков C и S) приводит к гипокоагуляции белков крови, развитие геморрагического синдрома (кровоизлияний в ткани, кровотечений). ‡ Снижение эффективности реакций дезаминирования аминокислот приводит к увеличению содержания в крови и моче аминокислот. ‡ Подавление в гепатоцитах орнитинового цикла синтеза мочевины из токсичного для организма аммиака проявляется снижением повышением концентрации аммиака в крови. † Липиды. ‡ Нарушение синтеза в печёночных клетках ЛПНП и ЛПОНП (обладающих атерогенными эффектами), а также ЛПВП (оказывающих антиатерогенное действие) нередко сопровождается развитием липидной дистрофии печени (жирового гепатоза). ‡ Повышение в плазме крови уровня холестерина (обладающего проатерогенным свойством). † Углеводы. Для патологии печени характерны подавление гликогенеза, снижение эффективности гликогенолиза, нарушения образования глюкозы. Указанные расстройства проявляются низкой резистентностью организма к нагрузке глюкозой: гипогликемией натощак и гипергликемией вскоре после приёма пищи, особенно углеводной. † Витамины. При печёночной недостаточности развиваются гипо- и дисвитаминозы за счёт: ‡ нарушения высвобождения из продуктов питания и всасывания в кишечнике жирорастворимых витаминов A, D, E, K, ‡ снижения эффективности трансформации провитаминов в витамины (например, -каротина в витамин A), ‡ торможения образования коферментов из витаминов (например, тиаминпирофосфата из витамина B1, флавинмононуклеотида и динуклеотида из витамина B2, пиридоксаль–5–фосфата из витамина B6, коэнзима А из пантотеновой кислоты). † Минеральные вещества (железо, медь, хром). Например, при наследственной патологии — гемохроматозе в ткани печени накапливается железо, развиваются гепатомегалия и цирроз. • Нарушения функций печени. † Дезинтоксикационная функция. Характеризуется снижением эффективности процессов детоксикации в печени: ‡ эндогенных токсинов (образующихся и/или накапливающихся в кишечнике — фенолов, скатолов, аммиака, путресцина, кадаверинов и патогенных продуктов метаболизма — низкомолекулярных жирных кислот, сульфатированных аминокислот и др.). ‡ экзогенных ядовитых веществ (например, токсинов грибов и микробов; ядохимикатов; ЛС). † Антимикробная функция. При печёночной недостаточности страдают фагоцитоз клетками фон Купффера различных микроорганизмов, транспорт IgА в жёлчь, где они оказывают бактериостатическое и бактерицидное действие. Шунтовая печеночная кома: этиология, патогенез, проявления. Шунтовая кома («обходная»). Причина шунтовой (обходной) комы: интоксикация организма продуктами метаболизма, а также экзогенными веществами, в норме обезвреживающимися гепатоцитами. Это является результатом попадания их в общий кровоток, минуя печень, по портокавальным анастомозам. Последние развиваются в связи с портальной гипертензией. Наиболее часто данный вид комы прослеживается при таких заболеваниях печени как цирроз, приводящий к повышению артериального давления в системе воротной вены. Возникшая портальная гипертензия преобразует портокавальные анастомозы через геморроидальные, пищеводные и пупочную вены. По портокавальным анастомозам больший объем крови, оттекающий от ЖКТ, поступает в общий кровоток, минуя таким образом печень. Кровь будет больше концентрировать в себе не обезвреженные печенью продукты обмена из-за чего будет развиваться интоксикация метаболитами, не инактивировавшимися раннее. Одна из особенностей данного варианта развития печеночной комы состоит в отсутствии или слабой выраженности желтухи, поскольку шунтовая печеночная кома, особенно на начальных стадиях, не сопровождается значительными нарушениями желчеобразовательной и желчевыделительной функции печени. Другой особенностью шунтовой печеночной комы является большая зависимость ее возникновения от состояния кишечного пищеварения и состава потребляемой пищи. Пища, богатая белком, повышает вероятность развития комы из-за всасывания большого количества упомянутых выше продуктов белкового распада. 4. Печеночно-клеточная кома: этиология, патогенез, проявления. Паренхиматозная кома. Причина печёночно-клеточной (паренхиматозной) комы: интоксикация организма в связи с повреждением и гибелью значительной массы печени (например, при её травме, некрозе, удалении). В результате этого нарушаются все функции печени. Наибольшее патогенное значение при этом имеет утрата дезинтоксикационной функции. Печеночно-клеточная кома возникает при массивном некрозе паренхимы печени, когда происходит существенное расстройство всех ее функций. В основе развития комы лежат несколько патогенетических механизмов. Во-первых, это повышение в крови содержания веществ, оказывающих общетоксическое и, в особенности, церебротоксическое действие. Среда подобных веществ важнейшую роль играет свободный аммиак. Известно, что только гепатоциты имеют такой метаболический механизм как орнитиновый цикл, в ходе которого происходит трансформация постоянно образующегося в процессе белкового обмена NH3 в мочевину. Синтез мочевины в печени нарушается в случае повреждения не менее 80% всех печеночных клеток. Дополнительным источником накопления NH3 в организме является часть мочевины, экскретируемая слизистой оболочкой кишечника и расщепляющаяся в нем уреазами бактерий с образованием аммиака, который всасывается в кровь. Избыток аммиака оказывает прямое повреждающее действие на органы и ткани, ингибируя активность многих важнейших ферментов и, в частности, ферментов цикла Кребса. При этом часть аммиака связывается с α-кетоглютаровой кислотой с образованием глютаминовой кислоты. Возникающий в связи с этим дефицит α-кетоглютаровой кислоты значительно снижает интенсивность окислительных процессов, оказывает разобщающий эффект (уменьшает степень сопряженности окисления и фосфорилирования), что в итоге приводит к дефициту АТФ. Повышение концентрации аммиака в крови до 7-8 мг% (норма 0,01-0,03 мг%) несовместимо с жизнью. 5. Гемолитическая желтуха: этиология, патогенез, проявления. Надпеченочная (гемолитическая) желтуха, не связанная с поражением печени, возни- кает в связи с повышенным гемолизом эритроцитов и нарушением метаболизма били- рубина. Причины, вызывающие надпеченочную желтуху, различны. Имеется ряд на- следственно обусловленных энзимопатий и гемоглобинопатий, сопровождающихся гемолитической желтухой, например наследственная микросфероцитарная гемолити- ческая и серповидно-клеточная анемии. Выделяют также аутоиммунные, инфекцион- ные (при малярии, сепсисе), токсические (отравления мышьяком, свинцом, сероводо- родом, змеиным ядом) и другие приобретенные формы гемолитической анемии. При усиленном разрушении циркулирующих эритроцитов отмечается повышенная про- дукция непрямого билирубина. Печень способна метаболизировать и выделять в желчь количество билирубина, в 3-4 раза превышающее его нормальный физиологический уровень. При усиленном гемо- лизе эритроцитов печень не справляется ни с процессом конъюгации, ни с транспор- том образующегося в избытке билирубина, что может привести как минимум к 4- кратному увеличению его концентрации в крови. При этом варианте желтухи билиру- бин, казалось бы, должен быть только неконъюгированный, поскольку речь идет о на- коплении непрямого билирубина. Однако необходимо учитывать, что в печеночную клетку поступает избыточное количество билирубина, он конъюгируется, а транс- портная система выведения его из клетки может оказаться недостаточной, и тогда в крови, наряду с непрямым билирубином, увеличенное содержание которого будет обязательно преобладать, одновременно отмечается повышение и уровня прямого би- лирубина. Основными признаками этой желтухи являются повышение уровня билирубина преимущественно за счет неконъюгированной фракции, отсутствие билирубина в мо- че. Кроме того, при гемолитической желтухе в печени, желчевыводящих путях и ки- шечнике синтезируется избыточное количество глюкуронидов билирубина, уробили- ногена, стеркобилиногена (гиперхолия - увеличенная секреция желчи в кишечник), что приводит к увеличению количества уробилиногена и стеркобилиногена в моче и в фекалиях на фоне отсутствия клинических и лабораторных подтверждений заболеваний печени. Печень метаболизирует большее, чем в норме, количество пигмента, и по- этому билирубин усиленно выделяется через желчь и далее в кишечник. Накопления в крови желчных кислот и холестерина не происходит, так как отток желчи свободен. В некоторых случаях (цирроз, опухоли, инфекции) одновременно могут определяться как повышенный гемолиз эритроцитов, так и нарушения функций печени. Как прави- ло, при неосложненном ге- молизе уровень билирубина в сыворотке крови повышается лишь в 2-3 раза (40-60 мкмоль/л) и редко достигает 100 мкмоль/л. Неконъюгированная гипербилирубинемия возникает и вследствие нарушений конъюгации билирубина при снижении активности УДФ-глюкуронилтрансферазы. Почти у каждого новорожденного на 3-5-й день жизни отмечается незначительная, преходящая неконъюгированная гипербилирубинемия (до 50 мкмоль/л), связанная с еще незрелой в этот период глюкуронилтрансферазой. В течение нескольких дней жизни до 2 недель активность глюкуронилтрансферазы повышается и одновременно нормализуется уро- вень билирубина. 6. Механическая желтуха: этиология патогенез холемического и ахолического синдромов. Механическая желтуха. Для механической (подпечёночной, застойной, обтурационной) желтухи характерно развитие холемии и ахолии. † Причина: Стойкое нарушение выведения жёлчи по жёлчным капиллярам (что приводит к внутрипечёночному холестазу), по жёлчным протокам и из жёлчного пузыря. Две последние группы причин вначале приводят к внепечёночному (подпечёночному) холестазу, а при хроническом действии — и к внутрипечёночному. Наиболее частые факторы, приводящие к внутрипечёночному и внепечёночному холестазу. ‡ Закрывающие желчевыводящие пути изнутри (например, конкременты, опухоли, паразиты, гранулематозная ткань при билиарном циррозе). ‡ Сдавливающие жёлчные пути снаружи (например, новообразования головки поджелудочной железы или большого дуоденального сосочка; рубцовые изменения ткани вокруг желчевыводящих путей; увеличенные лимфоузлы). ‡ Нарушающие тонус и снижающие моторику стенок желчевыводящих путей (дискинезии). Указанные и другие факторы обусловливают повышение давления в жёлчных капиллярах, перерастяжение (вплоть до микроразрывов) и повышение проницаемости стенок желчеотводящих путей, диффузию компонентов жёлчи в кровь. При этом развивается билиарный гепатит 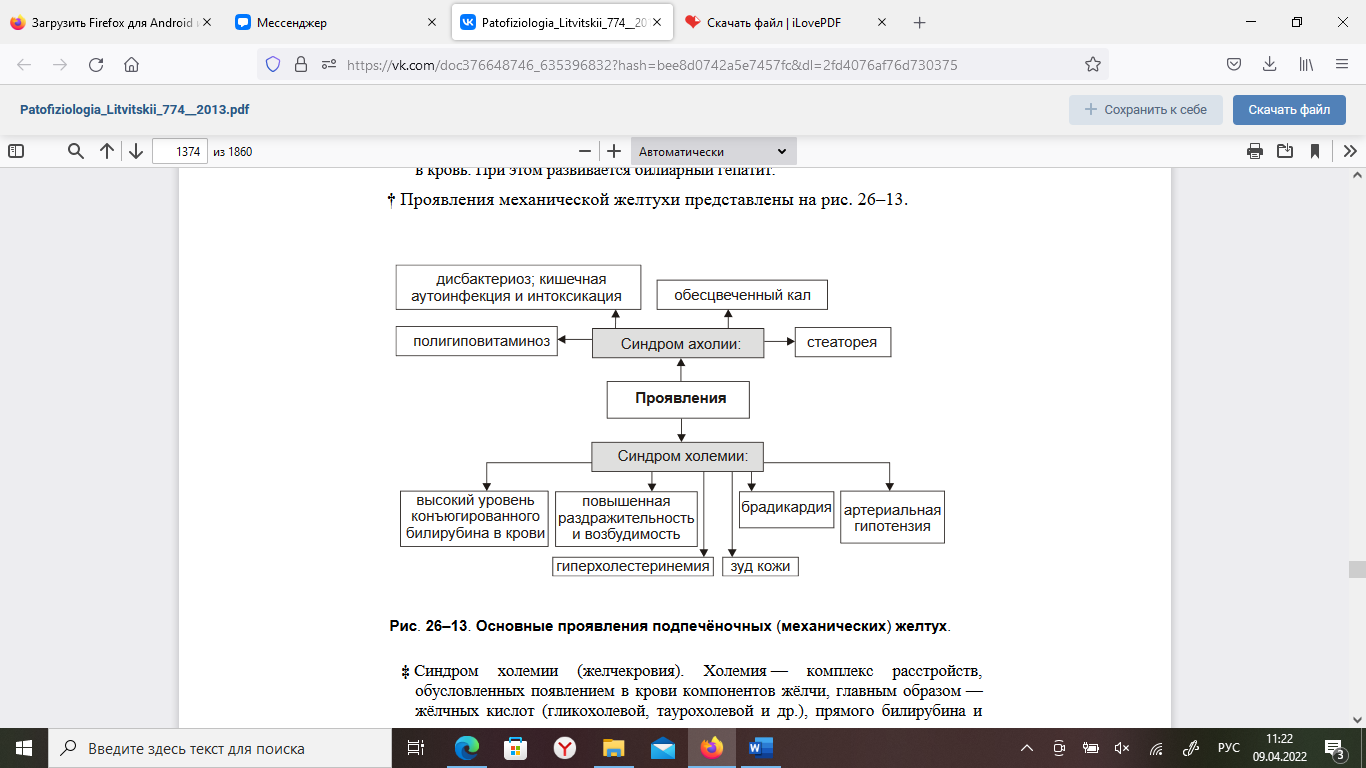 Синдром холемии (желчекровия). Холемия — комплекс расстройств, обусловленных появлением в крови компонентов жёлчи, главным образом — жёлчных кислот (гликохолевой, таурохолевой и др.), прямого билирубина и холестерина. Признаки холемии. § Высокая концентрация конъюгированного билирубина в крови (с развитием желтухи) и как следствие — в моче (в сочетании с жёлчными кислотами). Это придает моче тёмный цвет. § Гиперхолестеринемия. Избыток холестерина поглощается макрофагами и накапливается в виде ксантом (в коже кистей, предплечий, стоп) и/или ксантелазм (в коже вокруг глаз). § Зуд кожи вследствие раздражения жёлчными кислотами нервных окончаний Артериальная гипотензия вследствие снижения базального тонуса ГМК артериол, уменьшение адренореактивных свойств рецепторов сосудов и сердца, повышения тонуса бульбарных ядер блуждающего нерва под действием жирных кислот. § Брадикардия вследствие прямого тормозного влияния жёлчных кислот на клетки синусно-предсердного узла. § Повышенная раздражительность и возбудимость пациентов в результате снижения активности тормозных нейронов коры больших полушарий под действием компонентов жёлчи. § Депрессия, нарушение сна и бодрствования, повышенная утомляемость (развивается при хронической холемии). ‡ Синдром ахолии. Ахолия — состояние, характеризующееся значительным уменьшением или прекращением поступления жёлчи в кишечник, сочетающееся с нарушением полостного и мембранного пищеварения. Признаки ахолии. § Стеаторея — потеря организмом жиров с экскрементами в результате нарушения эмульгирования, переваривания и усвоения жира в кишечнике в связи с дефицитом жёлчи. § Дисбактериоз. § Кишечная аутоинфекция и интоксикация вследствие отсутствия бактерицидного и бактериостатического действия жёлчи. Это способствует активации процессов гниения и брожения в кишечнике и развитию метеоризма. § Полигиповитаминоз (в основном, за счёт дефицита жирорастворимых витаминов A, D, E, K). Дефицит указанных витаминов приводит к нарушению сумеречного зрения, деминерализации костей с развитием остеомаляции и переломов, снижение эффективности системы антиоксидантной защиты тканей, развитию геморрагического синдрома. § Обесцвеченный кал вследствие уменьшения или отсутствия жёлчи в кишечнике. ИЗ ЛЕКЦИИ Подпеченочная желтуха (механическая или обструктивная) развивается при возникновении препятствия току желчи по внепеченочным желчным протокам. Причинами возникновения являются: а) обтурация печеночного и общего желчного протоков камнем, паразитами, опухолью; б) сдавление желчных протоков опухолью близлежащих органов, кистами; в) сужение желчных протоков послеоперационными рубцами, спайками; г) дискинезия желчного пузыря в результате нарушения иннервации. При подпеченочной желтухе наблюдаются болевой синдром, тошнота, рвота, расстройства стула. Длительный холестаз сопровождается увеличением печени, что зависит от переполнения ее застойной желчью и увеличения массы печеночной ткани. В начале развития механической желтухи печеночные клетки еще продолжают вырабатывать желчь, но отток ее по обычным путям нарушен, и она изливается в лимфатические щели, попадая оттуда в кровь. В крови повышается в основном количество связанного билирубина. Выделение уробилина с мочой отсутствует, выделение стеркобилина с калом понижено или незначительно. В крови содержатся все составные части желчи, в том числе и желчные кислоты, приводящие к развитию холемии. Кроме того, для дан- ного вида желтухи характерна ахолия, причиной которой является стойкое нарушение выведения желчи по желчным капиллярам (что приводит к внутрипеченочному холе- стазу), протокам и из желчного пузыря. Синдром ахолии - состояние, характеризующееся значительным уменьшением или прекращением поступления желчи в кишечник, сочетающееся с нарушением полостного и мембранного пищеварения. При этом синдроме наблюдаются: а) стеаторея (потеря организмом жиров с калом в результате нарушения эмульгирования и усвоения жира в кишечнике из-за дефицита желчи); б) дисбактериоз; в) кишечная аутоинфекция и интоксикация вследствие выпадения бактерицидного действия желчи, что способствует активации процессов гниения и брожения в кишечнике и развитию метеоризма; г) дефицит жирорастворимых витаминов (А, Д, Е, К), приводящий к нарушению суме- речного зрения, деминерализации костей с развитием остеомаляции и переломов, снижению эффективности системы антиоксидантной защиты тканей, развитию геморрагического синдрома; д) обесцвеченный кал вследствие снижения или отсутствия желчи в кишечнике. 7. Печеночная желтуха: этиология и патогенез паренхимозной формы. Печеночная желтуха Различают инфекционные и неинфекционные причины возникновения печёночных желтух. • Инфекционные причины. К ним относят вирусы, бактерии, плазмодии. • Неинфекционные причины печёночных желтух: органические и неорганические гепатотоксические вещества (например, четырёххлористый углерод, этанол, парацетамол и др.), гепатотропные АТ, цитотоксические лимфоциты и макрофаги, новообразования. Характер и выраженность нарушений функций печени зависит от степени альтерации и массы повреждённых гепатоцитов. В значительной части случаев повреждение, начинаясь с изменения структуры клеточных мембран и/или подавления активности ферментов, нарастает и может завершиться деструкцией печёночных клеток. В любом случае при повреждении паренхимы печени происходят расстройства желчеобразования и желчевыведения. Характер расстройств и степень их выраженности на разных этапах (стадиях) патологического процесса (следовательно — выраженности желтухи) различны. •Стадии_желтухи. † Первая стадия (преджелтушная) 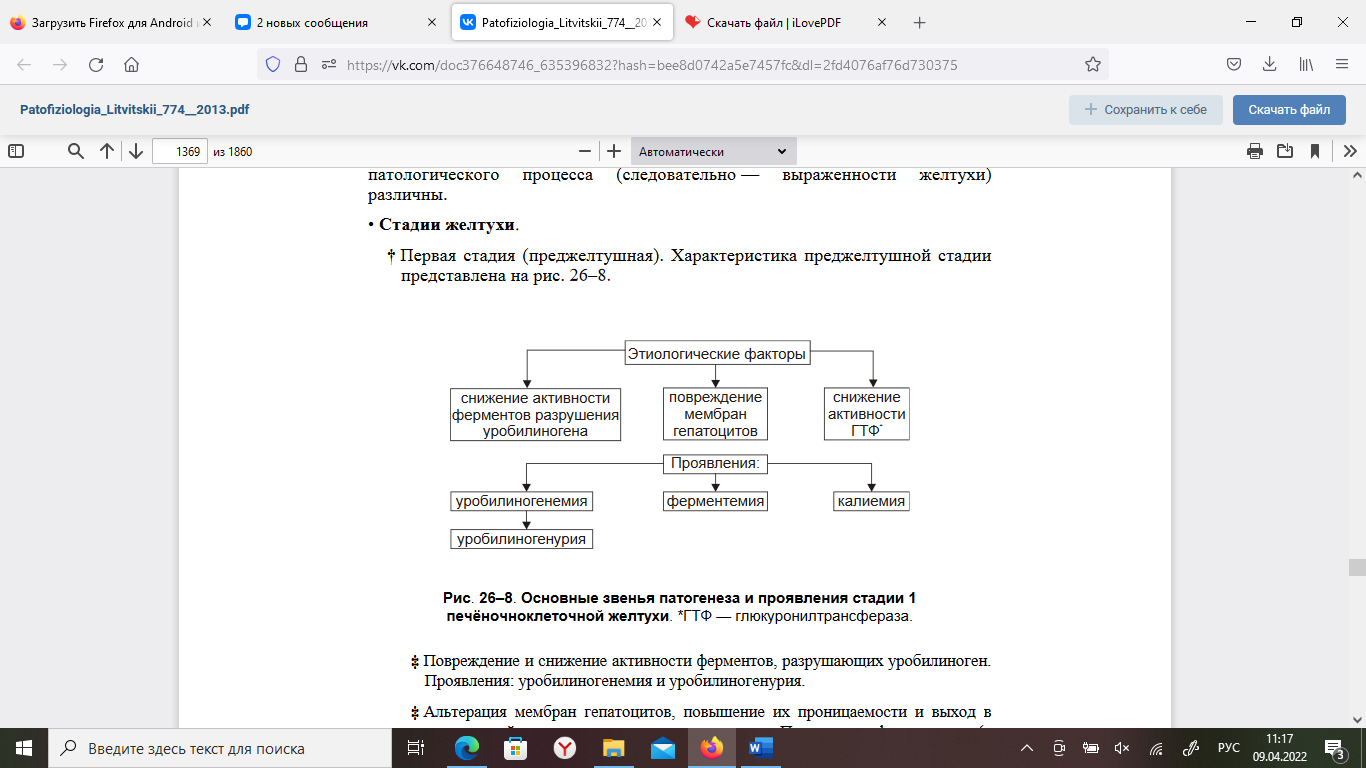 Повреждение и снижение активности ферментов, разрушающих уробилиноген. Проявления: уробилиногенемия и уробилиногенурия. ‡ Альтерация мембран гепатоцитов, повышение их проницаемости и выход в интерстиций и кровь компонентов цитоплазмы. Проявления: ферментемия (в крови увеличивается активность трансаминаз АЛТ и АСТ, а также других ферментов, характерных для печени) и гиперкалиемия (вызвана повреждением большого числа гепатоцитов). ‡ Снижение активности глюкуронилтрансферазы. Проявления: уменьшение образования прямого билирубина и как следствие — содержания стеркобилиногена в крови, моче и экскрементах. † Вторая стадия (желтушная). 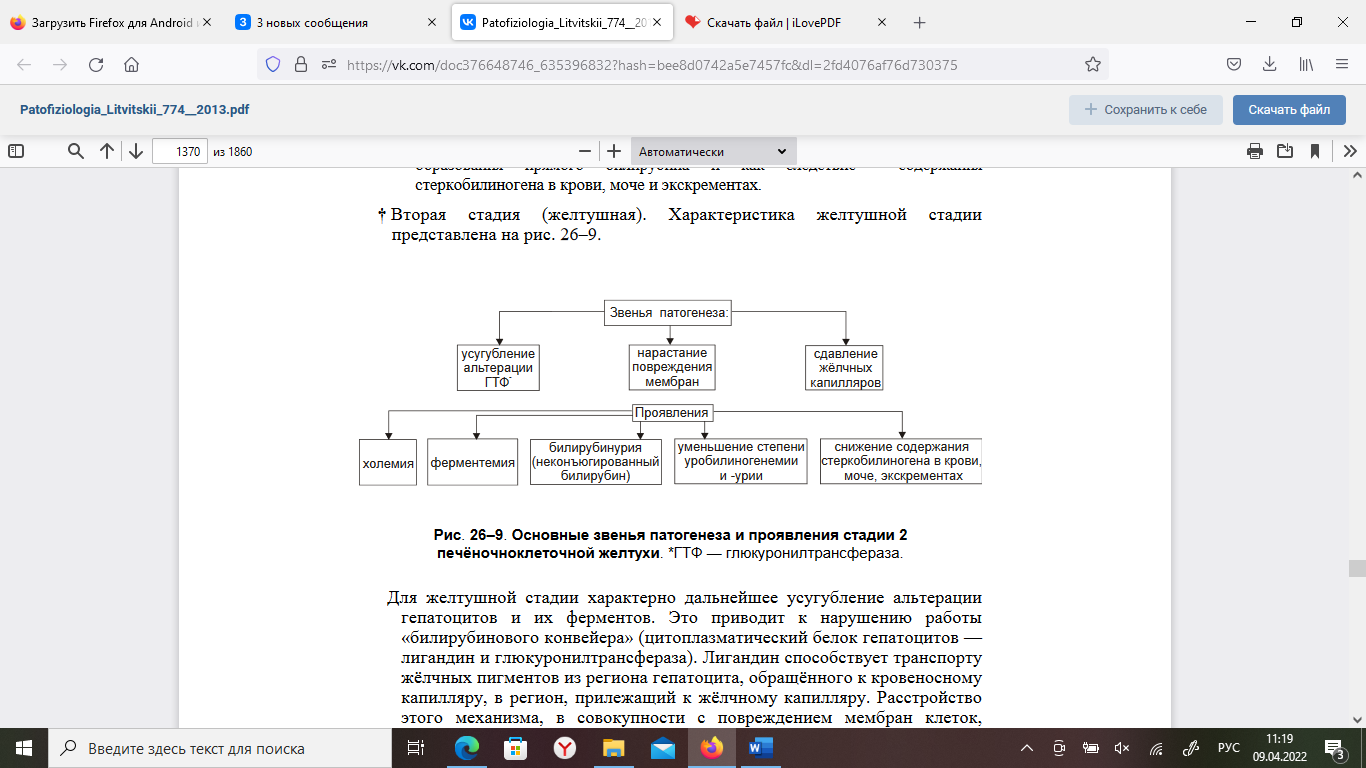 Для желтушной стадии характерно дальнейшее усугубление альтерации гепатоцитов и их ферментов. Это приводит к нарушению работы «билирубинового конвейера» (цитоплазматический белок гепатоцитов — лигандин и глюкуронилтрансфераза). Лигандин способствует транспорту жёлчных пигментов из региона гепатоцита, обращённого к кровеносному капилляру, в регион, прилежащий к жёлчному капилляру. Расстройство этого механизма, в совокупности с повреждением мембран клеток, обусловливает нарушение однонаправленного транспорта билирубина. Проявления: выход прямого билирубина в кровь и развитие билирубинемии, фильтрация прямого билирубина почками и его экскреция с мочой, попадание компонентов жёлчи в кровь и развитие холемии. † Третья стадия печёночной желтухи. 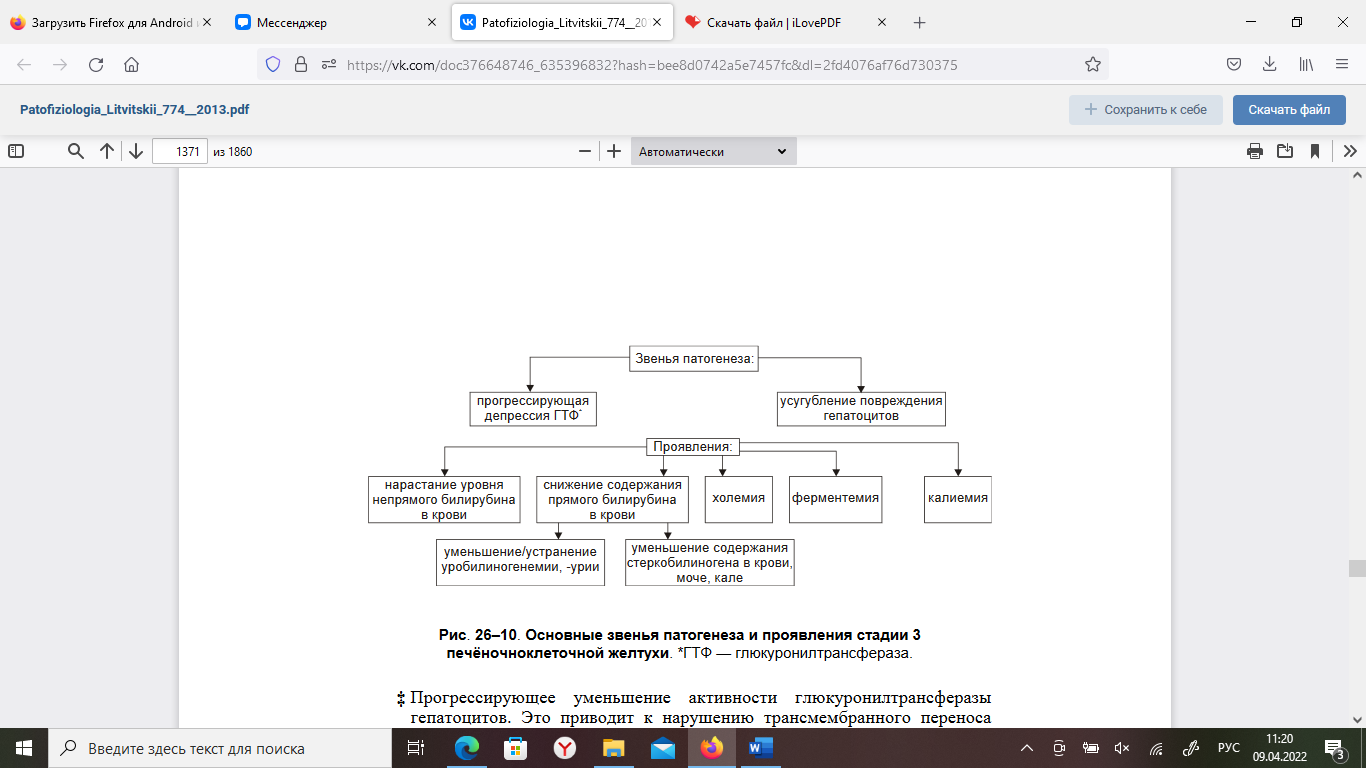 ‡ Прогрессирующее уменьшение активности глюкуронилтрансферазы гепатоцитов. Это приводит к нарушению трансмембранного переноса конъюгированного билирубина в гепатоциты и торможению процесса глюкуронизации билирубина. Проявления: нарастание уровня непрямого билирубина в крови, уменьшение содержания в крови прямого билирубина (как результат подавления реакции глюкуронизации), снижение (в связи с этим) концентрации стеркобилиногена в крови, моче и экскрементах, уменьшение содержания уробилиногена (вплоть до исчезновения) в крови и как результат — в моче. Последнее является результатом малого поступления прямого билирубина в желчевыводящие пути и кишечник. ‡ Нарастающее усугубление повреждения структур и ферментов гепатоцитов. Проявления: нарастание холемии, сохранение ферментемии и гиперкалиемии, прогрессирование печёночной недостаточности, чреватой развитием комы ИЗ ЛЕКЦИИ Печеночная желтуха (паренхиматозная или гепатоцеллюлярная) развивается при острых и хронических заболеваниях печени любой этиологии (вирусной, алкогольной, аутоиммунной), а также при тяжело протекающих инфекциях (тифы, малярия, острая пневмония), сепсисе, отравлениях грибами, фосфором, хлороформом и другими ядами. В результате поражения гепатоцитов лизосомы печеночных клеток выделяют желчь в лимфатические и кровеносные сосуды. Возможно и обратное всасывание желчи из желчных протоков в кровь. В крови отмечается гипербилирубинемия как за счет прямого, так и непрямого билирубина, что связано со снижением активности глюкуронилтрансферазы в поврежденных клетках и нарушением образования глюкуронидов билирубина. Развивается холемический синдром, возникающий из-за поступления желчных кислот в кровь. Он характеризуется брадикардией и снижением артериального давления вследствие воздействия желчных кислот на рецепторы и центр блуждающего нерва, синусовый узел сердца и кровеносные сосуды. Токсическое дей- ствие желчных кислот на центральную нервную систему проявляется в виде астении, раздражительности, нарушения ритма сна, головной боли и повышенной утомляемо- сти. Раздражение чувствительных нервных окончаний кожи желчными кислотами приводит к кожному зуду. Моча имеет темный цвет за счет билирубинурии (прямой билирубин) и уробилинурии(нарушено превращение уробилиногена, всасывающегося в кровь из тонкой кишки и поступающего в печень). В моче определяются желчные кислоты и следы стеркобилиногена вследствие снижения его образования в кишечни- ке, куда мало поступает глюкуронидов билирубина. В группе печеночных желтух различают печеночно-клеточную, холестатическую и эн- зимопатическую желтухи. При печеночно-клеточной желтухе имеет место комплексное нарушение функций печени, касающееся как метаболизма, так и транспорта билирубина. В ее основе лежит повреждение функции и структуры гепа- тоцитов - цитолитический синдром, приводящий к печеночно-клеточной недостаточности. 8. Энзимопатические желтухи: виды этиология, патогенез. Энзимопатические желтухи обусловлены нарушением метаболизма билирубина в гепатоцитах. Речь идет о парциальной форме печеночной недостаточности, связанной с уменьшением или невозможностью синтеза ферментов, участвующих в пигментном обмене. По происхождению эти желтухи, как правило, наследственные. Различают энзимопатические желтухи наследуемые (первичные) и приобретённые (вторичные) 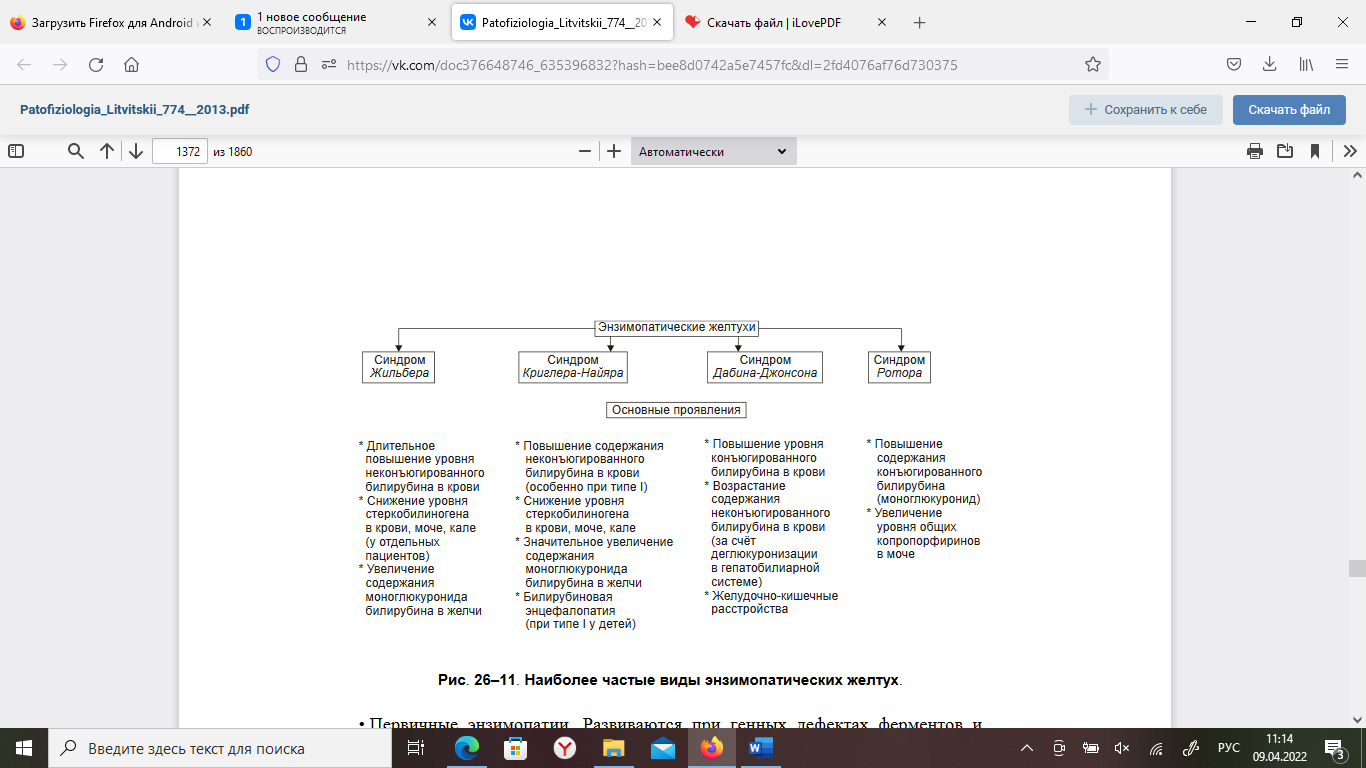 В зависимости от механизма развития выделяют следующие формы желтух: Синдром Жильбера - носит семейный характер и отличается доброкачественной хронически протекающей неконъюгированной гипербилирубинемией, связанной с час- тичным дефицитом УДФ-глюкуронилтрансферазы. Обычно этот синдром проявляется в возрасте не ранее 20 лет. Как правило, уровень билирубина повышается только до 30 мкмоль/л и редко превышает 50 мкмоль/л (лишь 20% общего билирубина будет конъ- югированным). Клинически эта патология чаще не проявляется и устанавливается при лабораторном исследовании. Интенсивность желтухи преходящая, то исчезает, то уси- ливается. Последнее наблюдается после продолжительного голодания либо соблюде- ния низкокалорийной диеты, после интеркуррентной инфекции, хирургических вме- шательств, приема алкоголя. Прием фенобарбитала, увеличивая активность фермента, приводит к нормализации уровня билирубина. Синдром Криглера-Найяра. Известны две формы этого заболевания: тип I - клинически тяжелая форма, связанная с полным отсутствием глюкуронилтрансферазы, и тип II, связанный с частичным ее дефицитом. I тип встречается редко. Характеризуется появлением желтухи с первых дней жизни ребенка, резким повышением содержания непрямого билирубина в крови, поражением центральной нервной системы. Уровень неконъюгированного билирубина у детей достигает высоких цифр - 200-450 мкмоль/л. Функциональное состояние печени не страдает, однако в ней отсутствует конъюгирующий фермент. В связи с тем что печень не синтезирует связанный билирубин, желчь у таких детей бесцветна. Лечение фенобарбиталом безрезультатно. Больные дети обычно погибают на первом году жизни из-за поражения головного мозга (билирубиновая энцефалопатия). У больных со II типом синдрома отмечается только частичный дефицит глюкуронил- трансферазы, что выражается в повышенном уровне неконъюгированного билирубина до 60-200 мкмоль/л. Лечение фенобарбиталом дает временный эффект. Заболевание относится к протекающим относительно благоприятно в случаях, если уровень били- рубина не превышает 200 мкмоль/л. Возможен приобретенный дефицит глюкуронил- трансферазы, возникающий у новорожденных в связи с ингибированием этого фермента рядом лекарственных препаратов (левомицетин, новобиоцин или витамин К). При синдроме Криглера-Найяра и гемолитической болезни новорожденных (резус- несовместимость эритроцитов матери и плода) может развиться билирубиновая энце- фалопатия вследствие так называемой ядерной желтухи. «Ядерная» желтуха - тяжелая форма желтухи новорожденных, при которой желчные пигменты и дегенеративные изменения обнаруживают в ядрах больших полушарий и стволах головного мозга (свободный билирубин, не включенный в связь с альбуми- ном, проникает через гематоэнцефалический барьер и окрашивает ядра головного моз- га - отсюда термин «ядерная» желтуха). Данная желтуха характеризуется следующим: у новорожденных на 3-6 день жизни исчезают спинальные рефлексы, отмечается ги- пертонус мышц туловища, резкий плач, сонливость, беспокойные движения конечностей, судороги, нарушение дыхания, может наступить его остановка и смерть. Если ребенок выживает, то могут развиться глухота, параличи, отставание умственного раз- вития. Синдром Дабина-Джонсона. Данный вариант желтухи возникает вследствие дефекта ферментов, участвующих в экскреции билирубиндиглюкуронида через мембрану печеночных клеток в желчные капилляры. В результате этого прямой билирубин поступает не только в желчные капилляры но и частично в кровь. Клинически проявляется желтухой с умеренным увеличением содержания в крови прямого билирубина и появ- лением его в моче. При биопсии печени в гепатоцитах обнаруживают темный, буро- оранжевый пигмент (липохром). Синдром Ротора (конъюгированная гипербилирубинемия). Клинически сходен с пре- дыдущим синдромом, но в отличие от него при синдроме Ротора отсутствует накопле- ние патологического пигмента в клетках печени. Синдром имеет доброкачественное течение, наследуется по аутосомно-рецессивному типу. Первичные энзимопатии. Развиваются при генных дефектах ферментов и некоторых белков, обеспечивающих метаболизм пигментного обмена в гепатоцитах. Существует несколько нозологических форм, относящихся к этой группе желтух. Характеристика синдрома Жильбера (семейная негемолитическая желтуха), синдрома Дабина-Джонсона, синдрома Криглера-Найяра и синдрома Ротора приведена на рис. 25–11 и в статьях «Желтуха» и «Синдром» приложения «Справочник терминов». • Приобретённые (вторичные) нарушения свойств ферментов, участвующих в метаболизме жёлчных пигментов и синтезе компонентов мембран гепатоцитов. Развиваются вследствие: † интоксикации организма, особенно гепатотропными ядами (например, этанолом или четырёххлористым углеродом), некоторыми ЛС (например, парацетамолом, левомицетином), веществами для холецистографии; † инфекционных поражений печени (например, вирусами, бактериями, их эндо- и экзотоксинами), † повреждений гепатоцитов АТ, цитотоксическими лимфоцитами и макрофагами. |
