Батурицкая Н. В., Фенчук Т. Д. Удивительные опыты с растениями. 1991. Батурицкая Н. В., Фенчук Т. Д. Удивительные опыты с растениями. Удивительные опыты с растениями
 Скачать 0.92 Mb. Скачать 0.92 Mb.
|
|
13.Обнаружение катехинов в клетках растений Этот опыт по сравнению с предыдущими может показаться несколько сложным. Для опыта нужны 10-процентный раствор нитрата натрия, 20-процентный раствор мочевины, 9—10-процентный раствор уксусной кислоты, 2-процентный раствор гидроксида нат- 44 рия, срезы молодых побегов ольхи, ивы, сосны, острый нож или лезвие Тонкие срезы молодых веток поместите последовательно в равные объемы растворов: сначала нитрата натрия, затем мочевины и наконец уксусной кислоты. Выдержите 3— 5 мин в каждом Затем перенесите срезы в раствор гидроксида натрия, объем которого в 2 раза превышает объем уксусной кислоты. При наличии веществ из группы катехинов на срезах появится вишнево-красное окрашивание. Задание. Исследуйте на содержание катехинов кору ели, осины, сухой околоплодник граната, плюски незрелых грецких орехов. 14. Получение чернил из растительного материала В результате полимеризации катехинов в растениях образуются дубильные вещества, которые в присутствии солей железа (5—10 г на 100 г растительного сырья) дают зеленые, синие или черные соединения. На этом основано получение растительных чернил. Для опыта нужно 50—100 г растительного сырья, богатого дубильными веществами, например, дубовой коры, корней лапчатки прямостоячей или щавеля курчавого, плодов конского каштана обыкновенного или бузины черной, концентрированный настой чайного листа, сульфат железа (II), воронка, фильтровальная бумага. Чтобы получить чернила из чая, возьмите 2 г чайного листа, 20-процентный раствор сульфата железа (II), 1—2 г сахара. Залейте 45 чай 50 мл горячей воды и нагревайте 30—40 мин на кипящей водяной бане. Раствор отфильтруйте, к осадку добавьте еще 20—25 мл воды, прокипятите и отфильтруйте. Фильтраты объедините и упарьте до объема 8—10 мл. Получится интенсивно окрашенная коричневая жидкость. К 2 мл теплого фильтрата добавьте 0,5—1 мл 20-процентного раствора сульфата железа (II) до появления черного цвета. 1— 2 г сахарного песка сделают чернила густыми. Чернила из чая стойки, не выцветают. Чернила из зеленых плюсок каштана готовятся так. Возьмите 200 г плюсок и проварите в течение 60—80 мин в 1 л воды. После того как раствор приобретет коричневую окраску, отфильтруйте его и немного уварите. К фильтрату добавьте 2 г сульфата железа (II) и 1 г железоаммиачных квасцов. Почернение раствора происходит постепенно, через 1—2 дня чернила готовы. Чем больше будет добавлено сульфата железа (II), тем темнее будет цвет чернил. Чтобы получить чернила из дубовой коры, залейте ее таким количеством воды, чтобы она только покрывала кору, и прокипятите около часа. Когда жидкость окрасится в темно-коричневый цвет, раствор отфильтруйте, добавьте порциями порошок сульфата железа (II) и оставьте на 1—2 дня. Вместо сульфата железа (II) можно добавить хлорное железо FеС13. Чернила приобретут темно-синий оттенок. Для приготовления чернил из плодов черной бузины возьмите 100 г ягод, отожмите из них сок, добавьте 5 г 9-процентной уксусной кислоты, 2 г железоаммиачных квасцов и 5 г сульфата 46 железа (II). Для увеличения вязкости добавьте 1—2 г сахара. Получите чернила черного цвета. Высокое содержание дубильных веществ (до 30%) свойственно корневищам лапчатки прямостоячей. Найти это растение не трудно. Цветки желтые, но в отличие от других видов лапчаток четырехлепестковые. В народной медицине больше известно под названием «калган» (рис. 6) Осенью выкопайте корневища, измельчите, залейте водой с избытком и приготовьте насыщенный отвар. Добавляя к теплому отвару небольшими порциями порошок железного купороса, получите превосходные черные чернила.  Рис. 6. Лапчатка прямостоячая. Возможность получения черного красителя из различных растений, свидетельствует о широком распространении катехинов и дубильных 47 веществ в растительном мире. В каждом растении они представлены сложным комплексом близких по составу соединений. Поэтому оттенок получаемых чернил будет зависеть от вида растения, даже если вы приготавливаете их по единой методике. 15. Почему органы растений после гибели чернеют Изучите влияние солей железа на окраску различных органов растения. Для опыта нужен 5—20-процентный раствор сульфата железа (II), опавшие листья различных видов растений, плоды дуба, каштана, химические стаканы или кристаллизатор. Опавшие листья, плоды поместите в химические стаканы, чашки Петри или кристаллизатор и залейте раствором железного купороса, чтобы он только покрывал материал. Уже через несколько дней станет заметным изменение их окраски. Причем, чем выше концентрация раствора сульфата железа (II) и содержание дубильных веществ, тем быстрее проявляется черный цвет. Железо содержится, хотя и в небольших количествах (10-5—10-6 % от сырой массы) во всех органах растения. Оно входит в состав ферментов, без которых невозможно осуществление таких физиологических процессов, как дыхание и фотосинтез. Дубильные вещества также широко представлены в растениях. Однако, пока растение здорово, взаимодействия между железом и дубильными веществами в живых клетках не происходит. Если листья, стебли, плоды повреждаются и после 48 отмирания попадают во влажную среду, насыщенную солями железа, это взаимодействие осуществляется легко и приводит к появлению черного цвета. Чем выше содержание дубильных веществ в живых клетках, тем интенсивнее их черная окраска после отмирания. По этой же причине чернеют в воде мертвые листья рдеста, очень богатые дубильными веществами. Плоды дуба и конского каштана, пролежавшие долгое время в воде или в сыром месте, также становятся черными. Задание. Положите несколько листьев, плодов, семян во влажную среду в природных условиях, например у кромки берега, на влажной земле. Сравните скорость (в днях), с которой будет происходить изменение цвета различных органов. 16. Многие ли растения содержат дубильные вещества Для опыта нужны 5-процентный раствор хлорида или сульфата железа (II) или 10-процентный раствор железоаммиачных квасцов, спиртовка, пробирка, стеклянная палочка, предметное стекло, лист белой бумаги. Качественной реакцией на наличие дубильных веществ является почернение тканей при обработке разбавленными растворами солей железа, например, хлорида, сульфата железа, железоаммиачных квасцов. Опыт можно провести 3 способами. 1 способ. 1—2 г растительного материала прокипятите в пробирке с 5—6 мл воды. При этом дубильные вещества переходят в раст- 49 вор. К вытяжке добавьте 1—2 капли хлорида железа. // способ. Предметное стекло положите на лист белой бумаги. На предметное стекло нанесите каплю сока, выжатого из исследуемого растения, и прибавьте каплю соли железа. /// способ. Приготовьте срезы исследуемого органа. На срез нанесите каплю соли железа. Независимо от способа исследования при наличии в клетках дубильных веществ появляется темное окрашивание. Хлорид железа и железоаммиачные квасцы дают темно-зеленое окрашивание, а сульфат железа (II) — черное. Степень почернения выразите по трехбалльной системе (слабое, среднее и сильное), которая характеризует количество дубильных веществ в исследуемом органе. Результаты изучения оформите в виде таблицы:
Начинать работу лучше с растениями, содержащими много дубильных веществ (дуб, ива, каштан конский, щавель курчавый), а затем перейти к исследованию других растений. Задание. Исследуйте, содержатся ли дубильные вещества в органах комнатных растений. Где их больше: в листе, стебле, корне, цветке? 17. В какой части стебля накапливаются дубильные вещества Для этого опыта понадобится микроскоп, 10-процентный водный раствор железоаммиачных квасцов или 5-процентный свежеприготовленный раствор хлорида железа, острый нож, предметное стекло, молодые побеги ольхи клейкой, сосны и других растений. Острым ножом или лезвием приготовьте тонкие срезы молодых побегов сосны и ольхи. Поместите срезы в раствор хлорида железа или железоаммиачных квасцов на 2—3 мин, промойте водой, поместите на предметное стекло, рассмотрите под микроскопом при малом увеличении. Клетки, содержащие дубильные вещества, окрашиваются в темно-зеленый цвет. Хорошо заметно, что в стеблях сосны и ольхи больше всего дубильных веществ содержится в клетках коры и сердцевины. Задание. Проверьте, есть ли дубильные вещества в стеблях и листьях ели, лиственницы, горца, ревеня. ЗЕЛЕНЫЙ ЦВЕТ Зеленые стебли, позеленевшие на свету клубни картофеля, зеленые плоды и, разумеется, зеленые листья своим цветом обязаны пигменту хлорофиллу (от греч. «хлорос» — зеленоватый, «филлон» — лист). В отличие от обширных групп антоцианов, каротиноидов, 51 флавонов и флавонолов, в клетках всех высших растений имеется только 2 формы хлорофилла— зеленый с синеватым оттенком, хлорофилл а и зеленый с желтоватым оттенком, хлорофилл б. У некоторых водорослей в очень малых количествах обнаружены еще 3 формы хлорофилла. Других пигментов зеленого цвета у растений нет, только у некоторых видов древесных растений слои старой древесины могут приобретать зеленоватый оттенок в результате взаимодействия дубильных веществ с солями железа. Для листьев различного возраста, различных видов растений характерно многообразие оттенков зеленого цвета. Объясняется это тем, что в формировании окраски листа принимают участие не только хлорофилл, но и другие содержащиеся в листе пигменты: желтые каротиноиды, красные антоцианы. Убедиться в том, что в листьях зеленого цвета присутствуют и желтые пигменты можно, проделав следующий опыт. 18. Какие пигменты содержатся в зеленом листе Для опыта нужны свежие листья злаков или комнатных растений, 95-процентный этиловый спирт, бензин, ступка фарфоровая, пробирка, воронка, ножницы, фильтровальная бумага. Прежде всего получите вытяжку пигментов. Лучше, если вытяжка будет концентрированной, темно-зеленой. Можно использовать листья любых травянистых, но удобнее всего 52 комнатных теневыносливых растений. Они мягче, легче растираются, содержат, как все теневыносливые растения, больше хлорофилла. Хорошим объектом являются листья каллы (белокрыльника), аспидистры, пеларгонии. Менее пригодны для получения хлорофилльных вытяжек листья бегонии, содержащие в вакуолях много органических кислот, которые при растирании листьев могут частично разрушить хлорофилл. К измельченным листьям (для опыта достаточно 1—2 листа пеларгонии) добавьте 5—10 мл этилового спирта, на кончике ножа СаСО3 (мел) для нейтрализации кислот клеточного сока и разотрите в фарфоровой ступке до однородной зеленой массы. Прилейте еще этилового спирта и осторожно продолжайте растирание, пока спирт не окрасится в интенсивно-зеленый цвет. Полученную спиртовую вытяжку отфильтруйте в чистую сухую пробирку или колбу. Убедиться в том, что спиртовая вытяжка пигментов листа, помимо зеленых, содержит еще и желтые пигменты, можно 2 способами. / способ. На фильтровальную бумагу нанесите стеклянной палочкой каплю полученной спиртовой вытяжки пигментов листа. Через 3—5 мин на бумаге образуются цветные концентрические круги: в центре зеленый (хлорофилл), снаружи—желтый (каротиноиды). // способ. Полоску фильтровальной бумаги шириной примерно в 1 см и длиной 20 см погрузите одним концом в пробирку с вытяжкой. Через несколько минут на бумаге появится зеленая полоса хлорофилла, а выше нее — желтые полосы каротиноидов (каротина и ксантофилла). 53 Разделение пигментов обусловлено их различной адсорбцией (поглощением в поверхностном слое) на фильтровальной бумаге и неодинаковой растворимостью в растворителе, в данном случае — этиловом спирте. Каротиноиды хуже, по сравнению с хлорофиллом, адсорбируются на бумаге, больше растворимы в спирте, поэтому передвигаются по фильтровальной бумаге дальше хлорофилла. Таким образом, в создании цвета листа участвуют 2 группы пигментов — зеленые и желтые Количество хлорофилла в сформировавшихся листьях примерно в 3 раза выше, чем каротиноидов, поэтому желтый цвет каротиноидов маскируется зеленым цветом хлорофилла Количественное соотношение хлорофилла и каротиноидов непостоянно, зависит от возраста листа, физиологического состояния растений Если содержание хлорофилла уменьшается, листья приобретают желто-зеленый, желтый цвет. Кроме описанных выше, существуют другие методы разделения пигментов. 19. Разделение пигментов по методу Крауса Убедиться в том, что в спиртовой вытяжке наряду с хлорофиллом присутствуют желтые пигменты, можно, используя их различную растворимость в спирте и бензине. Из пигментов группы каротиноидов в 54 хлоропластах находятся преимущественно желто-оранжевый каротин и золотисто-желтый ксантофилл. Все пигменты можно выделить из листа спиртом, но растворимость хлорофилла и каротина в бензине выше, чем в спирте. Ксантофилл в бензине не растворяется. Для опыта нужны спиртовая вытяжка пигментов, бензин, пробирки, пипетка, цветные карандаши. В пробирку налейте 2—3 мл вытяжки, столько же бензина и 1—2 капли воды. Закройте большим пальцем пробирку, энергично взболтайте в течение 2—3 мин и дайте отстояться. Жидкость в пробирке разделится на 2 слоя; бензин, как более легкий, будет наверху, спирт — внизу. Оба слоя приобретут различную окраску: бензиновый — зеленую, спиртовой — желтую Желтый цвет спиртовому раствору придает пигмент ксантофилл. В бензиновом слое находятся 2 пигмента: хлорофилл и каротин, который не заметен из-за интенсивно-зеленого цвета хлорофилла Зарисуйте результаты опыта, отметив на рисунке расположение слоев растворителей и пигментов, которые в них растворены. Убедиться в том, что в бензиновом слое действительно находится пигмент каротин, можно, проделав реакцию взаимодействия хлорофилла со щелочью. 20. Действие щелочи на хлорофилл По химическому строению хлорофилл представляет собой сложный эфир дикарбоновой кислоты хлорофиллина и двух спиртов — 55 метилового и фитола. При взаимодействии сложных эфиров со щелочами (реакция омыления) происходит разрыв сложноэфирных связей с образованием соли данной кислоты и спиртов. В результате реакции омыления хлорофилла образуется соль хлорофиллина и 2 спирта: метиловый и фитол. 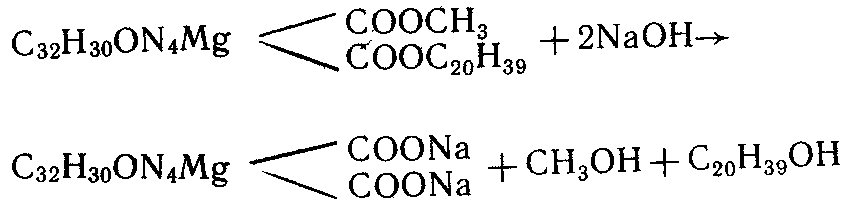 Для проведения этой реакции нужны спиртовая вытяжка пигментов листа, бензин, 20-процентный раствор гидроксида натрия или гидроксида калия, пробирка Налейте в пробирку 2—3 мл спиртовой вытяжки пигментов, добавьте 4—5 капель 20-процентного раствора щелочи, взболтайте смесь. Происходит реакция взаимодействия хлорофилла со щелочью. Цвет раствора не меняется, так как соли хлорофиллина имеют зеленую окраску. Добавьте бензин, чтобы общий объем жидкости в пробирке увеличился в 2 раза, взболтайте и дайте отстояться. Нижний спиртовой слой окрасится в зеленый цвет благодаря присутствию в нем натриевой соли хлорофиллина, которая, в отличие от хлорофилла, в бензине не растворима. Здесь же, в спиртовом слое находится пигмент ксантофилл, но его окраска маскируется интенсивно зеленым цветом натриевой соли хлорофиллина. 56 Верхний слой бензина будет окрашен в желтый цвет пигментом каротином. Опыты по разделению пигментов спиртовой вытяжки листа показывают, что она содержит 2 желтых пигмента: каротин и ксантофилл. Количественное соотношение их в растениях примерно равное. Итак, цвет листа зависит от сочетания и количественного соотношения желтых пигментов каротиноидов (каротин, ксантофилл) и зеленого хлорофилла, изменяясь от желто-зеленого у молодых до интенсивно-зеленого у взрослых и ярко-желтого цвета у опадающих осенних листьев. Но можно ли с уверенностью говорить, что хлорофилл — зеленый? 21. Какого цвета хлорофилл Цвет хлорофилла, как и любого окрашенного вещества, обусловлен сочетанием тех лучей, которые пигмент не поглощает. В спектре поглощения света растворами хлорофилла максимумы поглощения расположены в сине-фиолетовой (430 нм у хлорофилла а и 450 нм у хлорофилла б) и красной частях (660 нм у хлорофилла а и 650 нм у хлорофилла б). Эти лучи поглощаются хлорофиллом полностью. Поглощение голубых, желтых, оранжевых лучей определяется концентрацией хлорофилла в растворе: при\низких концентрациях они поглощаются частично, при высоких могут быть поглощены полностью. Минимум поглощения лежит в зоне зеленых лучей. Совершенно не поглощается хлорофиллом только небольшая часть красных лучей, которые в спектре 57 расположены на границе с инфракрасными лучами Это так называемые дальние красные лучи Исследуйте зависимость цвета вытяжки от концентрации молекул хлорофилла в ней. Для опыта нужна настольная лампа без абажура или фонарь, высокая пробирка, темно-зеленая спиртовая вытяжка пигментов, черная бумага. Пробирку, завернутую в черную бумагу, чтобы свет сбоку не попадал на раствор, поместите над лампой Свет от лампы должен проходить через раствор хлорофилла снизу вверх Если смотреть в пробирку сверху, постепенно добавляя в нее (не над лампой') маленькими порциями раствор хлорофилла, можно наблюдать удивительную картину изменения окраски раствора от ярко-зеленой до вишнево-красной Объясняется это тем, что по мере увеличения высоты столба жидкости в пробирке изменяются условия освещения молекул хлорофилла, а следовательно, и поглощение ими света Пока вытяжки в пробирке немного, она имеет в проходящем свете характерный для хлорофилла изумрудно-зеленый цвет, обусловленный сочетанием непоглощенных зеленых, части голубых, желтых и дальних красных лучей. По мере увеличения количества хлорофилла в пробирке молекулы хлорофилла постепенно поглощают сначала голубые и желтые, а затем и зеленые лучи Остаются непоглощенными только дальние красные лучи Поэтому в очень большом слое раствор хлорофилла в проходящем свете имеет не зеленый, а вишне- 58 во-красный цвет (рис 7). Так иногда в густом лесу можно видеть красное свечение, исходящее из-под полога леса. Этот опыт показывает, что зеленый цвет хлорофилла — сочетание различных, проходящих через молекулу пигмента участков солнечного спектра Измененный солнечный свет, в котором мало лучей, хорошо поглощаемых хлорофиллом,— одна из причин того, почему светолюбивые растения не могут жить под пологом других растений.  Рис 7. Поглощение света хлорофиллом в зависимости от концентрации пигмента: а—в разбавленном растворе (поглощаются средняя часть красного и сине фиолетовая области спектра) цвет раствора же.лто-зеленый; б—в растворе повышенной концентрации (поглощаются голубые, желтые, оранжевые лучи) цвет раствора изумрудно-зеленый; в— в сильно концентрированном растворе (попощаются все видимые лучи солнечного спектра за исключением дальних красных лучей); цвет раствора вишнево красный. Задание Проверьте, содержат ли хлорофилл красные листья ирезинии, бегонии королевской и др. Для этого часть листа поместите в пробирку, залейте водой и прокипятите до полного исчезновения красной окраски Приготовьте спиртовую вытяжку пигментов Сделайте выводы 59 22. Взаимодействие хлорофилла с кислотой Характерное для хлорофилла поглощение света определяется химической структурой его молекулы. Система сопряженных двойных связей играет большую роль в поглощении сине-фиолетовых лучей. Присутствие магния в ядре молекулы обусловливает поглощение в красной области. Нарушение структуры, например удаление из молекулы магния, приводит к изменению цвета хлорофилла. Удалить из хлорофилла магний можно, проделав реакцию взаимодействия хлорофилла с кислотой. Для опыта нужна спиртовая вытяжка хлорофилла, 10-процентный раствор соляной кислоты, уксуснокислый цинк, спиртовка, пипетка, 3 пробирки. П 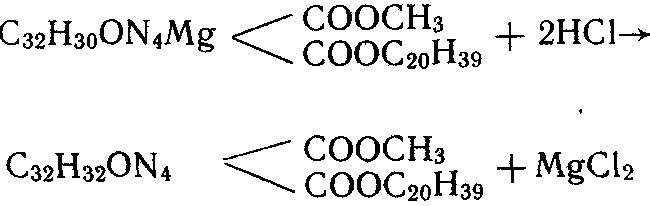 риготовьте спиртовую вытяжку хлорофилла и разлейте в пробирки по 2—3 мл. Одна из пробирок контрольная. В две другие добавьте по 2—3 капли соляной кислоты. В результате взаимодействия хлорофилла с кислотой магний замещается двумя атомами водорода и образуется вещество бурого цвета — феофитин. Одну из пробирок с феофитином оставьте для контроля, а в другую внесите на кончике ножа уксуснокислый цинк и нагрейте на водяной бане до кипения. Бурый цвет раствора 60 меняется на зеленый: вместо двух атомов водорода в молекулу входит атом цинка и занимает то место, где раньше был магний. Вместо уксуснокислого цинка можно взять соли меди, ртути. Во всех случаях металл входит в ядро молекулы феофитина, восстанавливается металлоорганическая связь и зеленая окраска. Следовательно, цвет хлорофилла зависит от наличия металлоорганической связи в его молекуле. Производные хлорофилла с цинком, медью или ртутью в природных условиях пока не обнаружены, а феофитин образуется в листьях, поврежденных заморозками, промышленными кислыми газами, в процессе старения. 23. Письмо на зеленом листе Свойство хлорофилла изменять цвет под действием кислот можно использовать для написания текста на зеленом листе. Выше описывалась методика нанесения рисунка на лепестки. Для опыта нужны «чернила» — 10-процентная соляная кислота, листья фикуса, палочка. Заостренный конец палочки смочите соляной кислотой и нанесите на лист нужный текст. На зеленом фоне листа постепенно появляется надпись бурого цвета. Скорость изменения цвета в месте нанесения кислоты зависит от плотности покровов листа. Появление бурой окраски обусловлено проникновением кислоты внутрь клеток и образованием в них феофитина. 61 Газообразные выделения промышленных предприятий часто содержат сернистый ангидрид SО2, который, проникая через устьица в листья, растворяется в цитоплазме клеток и образует сернистую кислоту Н2SО3. Накопление ее в больших количествах в цитоплазме вызывает разнообразные нарушения обмена веществ в клетках, в том числе и разрушение хлорофилла. Внешне такие повреждения могут выражаться в появлении на листьях бурых пятен. Задание. Сравните время «проявления» письма на листьях различных растений. С чем это связано? 24. Образование колец отмирания на листьях Образование феофитина в листьях многих растений может происходить также и при нагревании листа выше 70—80 °С. Д  ля опыта нужны зеленые листья различных растений, спиртовка, препаровальная игла, стеклянная палочка. ля опыта нужны зеленые листья различных растений, спиртовка, препаровальная игла, стеклянная палочка.Пятикопеечную монету, закрепив так, чтобы не обжечься, нагрейте в пламени спиртовки. Горячую монету опустите на лист. Через несколько минут вокруг монеты появится бурое пятно неправильной формы, при этом часть листа непосредственно под монетой может остаться зеленой. Рис. 8. Кольца отмирания. Видоизмените опыт: прикоснитесь к листу концом сильно нагретой стеклянной палочки, либо проколите его раскаленной препаровальной иглой. Во всех случаях возникают своеобразные изменения окраски листа: зеленые круги с неровными бурыми кольцами. Наиболее наглядные результаты дают растения с кислой 62 реакцией клеточного сока. Появление бурых колец обусловлено поступлением кислот клеточного сока из вакуолей в цитоплазму, а затем в хлоропласты. Под действием кислот происходит образование феофитина и появление бурого окрашивания. Поскольку химический состав листьев различных растений имеет свои особенности, можно получить различные картины колец отмирания (рис. 8). Желтые, коричневые пятна отмирания появляются на листьях и в природных условиях под влиянием сильного перегрева, засухи. Задание. Получите кольца отмирания на листьях нескольких растений и сделайте гербарий. 63 25. Получение отпечатков, фотографий с помощью раствора хлорофилла (по К. А. Тимирязеву) Способность хлорофилла к поглощению света лежит в основе процесса фотосинтеза. Однако при высокой интенсивности освещения, особенно под влиянием ультрафиолетовых лучей, может происходить необратимое разрушение хлорофилла, которое приводит к обесцвечиванию, выцветанию его. Особенно быстро под действием солнечного света обесцвечивается выделенный из листьев хлорофилл. На этом основан опыт К. А. Тимирязева, который был приведен в его знаменитой Крунианской лекции, прочитанной в 1903 г. в Лондонском Королевском обществе: «Вот отпечаток листа папоротника, полученный при помощи хлорофилла. Лист был наложен на пластинку из коллодиума, окрашенного хлорофиллом. После непродолжительной экспозиции на солнце все поле выцвело, а части, защищенные листом, сохранили свою оригинальную окраску. Изображение фиксировалось непродолжительным погружением в баню из медного купороса» (рис. 9). Повторите опыт К. А. Тимирязева. Для его проведения необходима спиртовая вытяжка хлорофилла, коллодий или фильтровальная бумага, 10-процентный раствор медного купороса CuSO4, лист растения. Приготовьте спиртовую вытяжку пигментов. Если нет коллодия, можно использовать фильтровальную бумагу. Пропитайте ее раствором хлорофилла и прикрепите лист растения, отпечаток которого вы хотите получить. Перенесите в освещенное солнцем место. 64  Рис. 9. Отпечаток листа папоротника. Через 1—2 ч под действием света происходит обесцвечивание хлорофилла на участках фильтровальной бумаги, незащищенных листом растения. Для закрепления изображения опустите фильтровальную бумагу с отпечатком листа в горячий (50—60 °С) 10-процентный раствор CuSO4 на несколько минут. О  бесцвечивание хлорофилла при избытке света происходит в результате взаимодействия возбужденных светом молекул хлорофилла с кислородом и последующего необратимого окисления молекул пигмента. Необратимое фотоокисление хлорофилла происходит не только в условиях чрезмерно высокой интенсивности освещения, но и при увеличении доли ультрафиолетовой радиации в потоке солнечного света. В природе такие условия бывают довольно часто, например, растения бесцвечивание хлорофилла при избытке света происходит в результате взаимодействия возбужденных светом молекул хлорофилла с кислородом и последующего необратимого окисления молекул пигмента. Необратимое фотоокисление хлорофилла происходит не только в условиях чрезмерно высокой интенсивности освещения, но и при увеличении доли ультрафиолетовой радиации в потоке солнечного света. В природе такие условия бывают довольно часто, например, растения65 Рис. 10. Колеус. гор обитают в мощном потоке ультрафиолетового излучения. У этих растений в процессе эволюции возникли защитные механизмы в виде сопутствующих хлорофиллу пигментов (антоцианы, каротиноиды), которые поглощают избыточную солнечную радиацию и превращают ее в тепло. Не случайно высокогорные растения содержат в листьях больше антоцианов, чем растения долин. Установить связь между количеством антоцианов в листе и условиями освещения достаточно легко. Для этого необходимы 2 растения колеуса гибридного, можно взять 2 укорененных черенка (рис. 10). Одно растение поставьте на яркий солнечный свет, другое — в условия рассеянного освещения. На свету окраска листьев становится значительно 66 ярче, краснее, а при рассеянном освещении листья зеленеют. То же происходит и с фиолетовыми листьями традесканции зебровидной. 26. Фотография жизнью (по К. А. Тимирязеву) Название этого опыта, как и описание, даны К. А. Тимирязевым в его знаменитой книге «Солнце, жизнь и хлорофилл». Цель опыта — показать, что для образования хлорофилла в листе обязательно нужен свет. Достичь цели просто: выращивая растения, клубни картофеля на свету и в темноте. Через 2—6 дней после начала прорастания сравните цвет проростков. Летом это сделать еще проще: достаточно рассмотреть траву под большим камнем, доской, бревном. Она будет совершенно обесцвечена. Климент Аркадьевич Тимирязев выбрал самый эффектный вариант. Вот описание опыта: «Всякий знает, что в темном погребе растение получается не зеленое, а бледно-желтое, этиолированное, как выражаются ботаники, таков, например, наш зимний салат-цикорий и т. д. Возьмем плоский деревянный ящик, на дно его положим кусок войлока и, посеяв по нему обыкновенный кресс-салат, оставим все в совершенной темноте. Кресс скоро вытянется и представит густую щетку — почти сплошную поверхность из своих первых, совершенно желтых листьев. Теперь вырежем в листе картона сквозными буквами какое-нибудь слово (Тимирязев выбрал слово «свет») и, прибив гвоздиками этот картон к краям ящика, вынесем все на свет (но не 6  7 7Рис. 11. Схема опыта К. А. Тимирязева. на солнце). Через несколько часов, сняв картон, увидим на желтом фоне нашего газона из кресс-салата надпись, выступающую зелеными буквами» (рис. 11). Четкий стиль изложения, умение простым, понятным языком объяснить научные понятия — характерная особенность работ К. А. Тимирязева. Кресс-салат был выбран ученым за быстроту прорастания, мелкость семядольных листочков, что важно для создания однородного фона. Вместо кресс-салата можно использовать семена быстро и легко прорастающих растений: салата, горчицы, ржи, пшеницы. Войлок был использован К. А. Тимирязевым потому, что хорошо впитывает воду, семена на нем лежат ровно, дружно прорастают. Его можно заменить несколькими слоями фильтровальной бумаги либо поролоновым матрасиком. Результаты опыта свидетельствуют, что без 68 света у покрытосеменных растений хлорофилл не образуется. В то же время хвойные, папоротники и многие зеленые водоросли способны синтезировать хлорофилл в полной темноте. Биосинтез молекулы хлорофилла включает 15 последовательных реакций, одна из которых — присоединение 2 атомов водорода по месту разрыва двойной связи в четвертом пиррольном кольце — происходит на завершающей стадии биосинтеза хлорофилла. Поэтому для позеленения этиолированных проростков достаточно нескольких часов освещения. Задание. Повторите опыт с проростками салата или горчицы. 27. Фотографии на листьях Световая энергия, поглощенная пигментами хлоропластов, расходуется на образование из углекислого газа и воды органического вещества. Используя четкие фотографические негативы, убедимся в том, что количество образующегося в листе крахмала пропорционально количеству света, падающего на лист. Для опыта нужны растения, накапливающие в листьях крахмал — примула, гортензия, фасоль обыкновенная, настурция большая, четкий фотографический негатив, черная бумага, ножницы, пинцет, водяная баня, химический стакан, 95-процентный этиловый спирт, раствор йода в йодиде калия (раствор Люголя), чашки Петри, лампа накаливания мощностью 100—200 Вт (или лампы дневного света). Определить, подходит ли растение для опыта, можно пробой на крахмал. Для этого кусочек листа (взять во второй половине дня) 69 прокипятите в воде 2—3 мин, выдержите в горячем спирте до полного удаления хлорофилла из листа, промойте горячей водой и погрузите в раствор йода в йодиде калия, который готовят следующим образом: 2 г йодида калия растворяют в 10 мл воды, вносят 1 г кристаллического йода, тщательно размешивают и доводят до 300 мл водой. Хранят в темном месте. Можно приобрести в аптеке готовый раствор Люголя, который включает те же компоненты, но в более высокой концентрации. Если под действием йода кусочек листа посинел, растение для опыта пригодно. Важный этап опыта — предварительное обескрахмаливание листа. Обычно трех суток выдерживания растения в темноте достаточно для того, чтобы весь крахмал, находящийся в листьях, превратился в глюкозу и перешел из листьев в другие органы. Скорость передвижения органических веществ по растению достаточно велика—до 1 м/ч. Проще поместить в темное место все растение, но длительное пребывание без света для растения неблагоприятно. Поэтому лучше склеить темные внутри и светлые снаружи (для отражения света) пакетики и изолировать отдельные листья (лучше молодые). Во многих случаях обескрахмаливание идет быстрее, чем за трое суток. В связи с этим можно закрыть пакетиками на 3 листа больше, чем планируется сделать фотографий. Через 12, 24 ч затемнения можно сделать пробу на крахмал и приступать к опыту. На верхнюю сторону листа наложите фотографический негатив эмульсией вверх, а нижнюю сторону тщательно закройте черной бумагой (бумагу и негатив можно по краям сшить). 70 В осенне-зимний период естественного освещения для интенсивного фотосинтеза явно недостаточно. Поэтому для получения хорошего отпечатка на листе, его надо дополнительно освещать. Лампа не должна располагаться слишком близко к листу (температура вблизи листа 25—30 °С). Негатив должен плотно прилегать к поверхности листа и равномерно освещаться лампой. 3—6 ч освещения обычно достаточно для накопления крахмала в экспериментальном листе. Методика «проявления» фотографии обычна: пакет снимите, лист опустите на 2—3 мин в кипяток, затем выдержите в горячем спирте до полного удаления хлорофилла (стаканчик со спиртом нагревать только на водяной бане!). Промойте горячей водой, осторожно положите в чашку Петри или тарелку и залейте раствором йода. После появления изображения раствор слейте, промойте лист холодной водой и просушите фильтровальной бумагой. На свету даже у высушенного отпечатка окраска постепенно светлеет, выгорает, но ее можно восстановить, вновь обработав лист раствором йода. 28. Окрашивание цветков искусственными красителями Применив ряд искусственных красителей, можно придать лепесткам цветков необычную для данного вида расцветку. Для опыта нужны белые или окрашенные в светлые тона цветки различных видов рас- 71 тений (например, нарциссы, сирень обыкновенная, жасмин садовый (чубушник), виола трехцветная), красители: эозин, метиленовый синий, малахитовый зеленый, метиловый фиолетовый, либо содержащие данные красители красные, зеленые, синие, фиолетовые, черные чернила «Радуга-2», пробирки, штатив для пробирок. Приготовленные для окрашивания цветков растения погрузите в пробирки с разбавленными растворами красителя. Начинать работу лучше с красных чернил, которые содержат краситель эозин. Эозин способен быстро (через 15—30 мин) проникать в лепестки, окрашивая их в розовые и красные тона. Первоначально краситель накапливается в сосудах, благодаря чему становится заметной густая сеть жилок, пронизывающих лепестки. Постепенно, по мере того как краситель из сосудов начинает проникать в клетки, лепестки окрашиваются полностью (рис. 12, а). Используя чернила других цветов, можно белые лепестки превратить в синие, даже зеленые, что для мира растений — редкость. Если несколько видоизменить опыт, можно получить цветки или соцветия причудливой мозаичной окраски. Для этого расщепите вдоль стебель соцветия или цветоножку. Одну половину стебля погрузите в пробирку с раствором красителя, например эозина, а вто- 72  Рис. 12. Цветки-химеры. рую — в пробирку с водой. В этом случае в красный цвет окрасится только часть соцветия или цветка. Мозаичное окрашивание хорошо удается на соцветиях белой сирени, жасмина садового, рябины обыкновенной (рис. 12, б). На окрашенных лепестках видно, что входящие в них проводящие пучки (жилки) различным образом ветвятся, между ними образуются перемычки. Благодаря густой сети проводящих пучков любая клетка лепестка оказывается близко от источника воды. По мере накопления красителя можно рассмотреть окончания отдельных тонких жилок. Вода из сосудов легко поступает в близлежащие клетки, но проникновение в них растворенных в воде веществ определяется свойствами наружной мембраны клеток. По- 73 этому, помещенные в растворы различных красителей, цветки одного и того же вида растений будут окрашиваться с различной скоростью. Быстро поступает в клетки красный эозин, значительно медленнее — метиловый фиолетовый. В процессе старения клеток проницаемость мембран возрастает, поэтому скорость окрашивания цветков зависит еще и от их возраста. Например, в одном из опытов цветки маргаритки многолетней, находившиеся в растворе зеленых чернил (разбавление 1:2), окрасились в зеленый цвет только на седьмой день. Передвижение воды вверх по сосудам растений происходит благодаря процессу испарения воды с поверхности листьев, лепестков. Поэтому скорость движения воды может колебаться от 0,1 до 100 м/ч в зависимости от вида растения и условий внешней среды. Используя эозин, можно определить скорость передвижения воды по стеблю или цветоножке. Для этого в раствор красителя нужно опустить только нижнюю часть стебля, измерить расстояние от уровня красителя до цветка и определить время, необходимое для появления красителя в лепестках. Задание. Определите скорость передвижения различных красителей по стеблю нивяника обыкновенного (составьте букет из розовых, голубых, зеленоватых ромашек), сравните скорость движения воды по сосудам при различных погодных условиях. РОСТ РАСТЕНИЙ Ростовые явления у растений проявляются прежде всего в образовании новых органов, тканей, клеток и их компонентов. В отличие от животных, рост растений продолжается в течение всей их жизни. Неограниченность роста обусловлена тем, что, в отличие от других организмов, деление клеток у растений приурочено к определенным зонам, называемым меристемами (от греч. «меристес»—делитель). В меристемах происходит не только деление клеток, но и образование зачатков органов. За счет деления клеток верхушечных меристем происходит рост стебля и корня в длину,образование листьев, цветков. Боковые меристемы обеспечивают рост осевых органов в толщину У злаков рост стебля обусловлен делением клеток вставочных меристем, расположенных в основании междоузлий Характерной чертой роста растения является его неравномерность, периодичность. Рост клеток растений включает несколько следующих друг за другом процессов: фазы деления, растяжения и дифференциации. Фаза деления (эмбриональная фаза) проходит в зоне меристем. Образующиеся в ре- 75 зультате деления дочерние клетки первоначально имеют размеры вдвое меньше материнской, но затем быстро растут за счет увеличения объема цитоплазмы. | ||||||||
