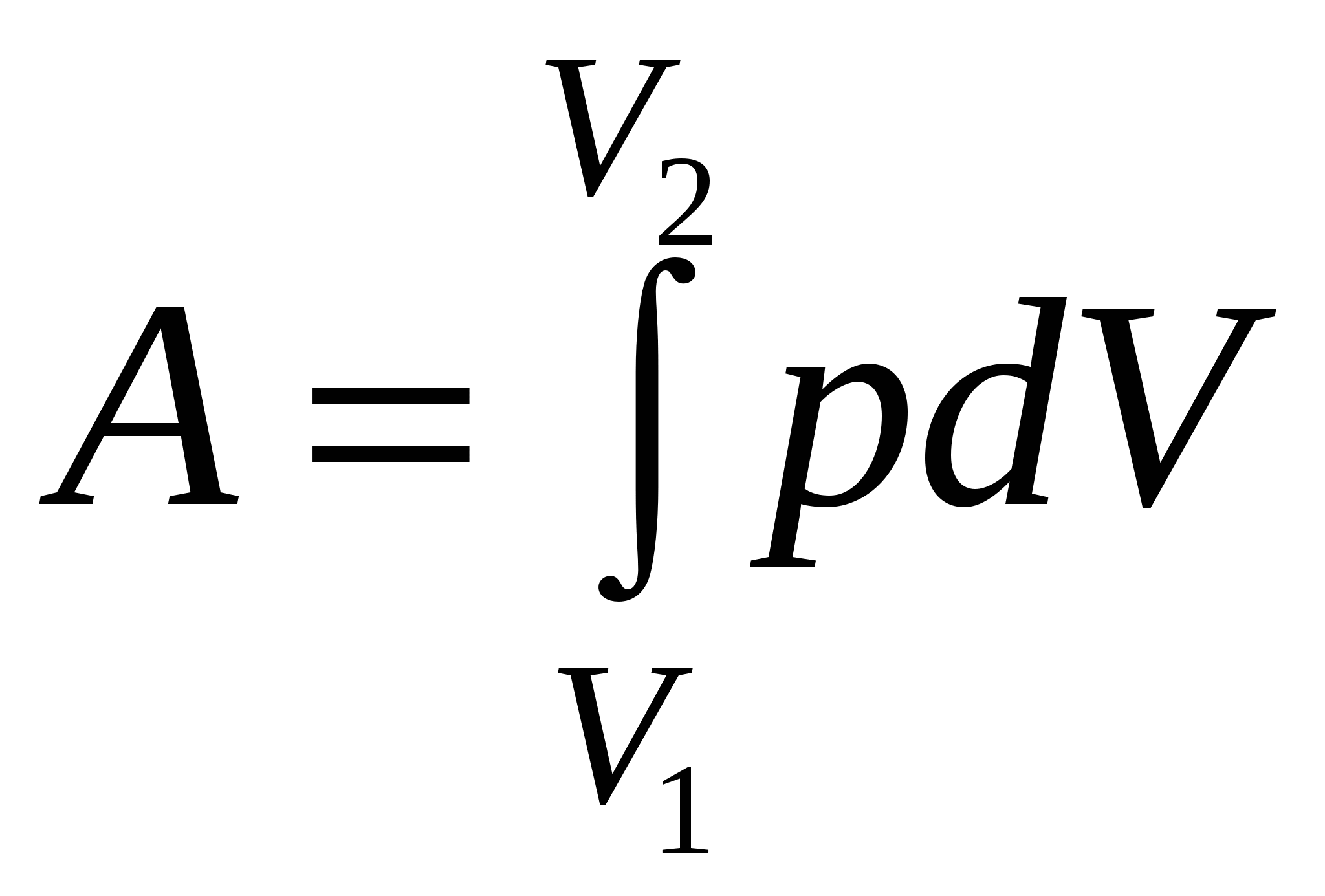|
|
Сборник задач по механике. Уфимский государственный авиационный технический университет
6. Молекулярно-кинетическая теория идеальных газов
Концентрация частиц (молекул, атомов и т.п.) однородной системы
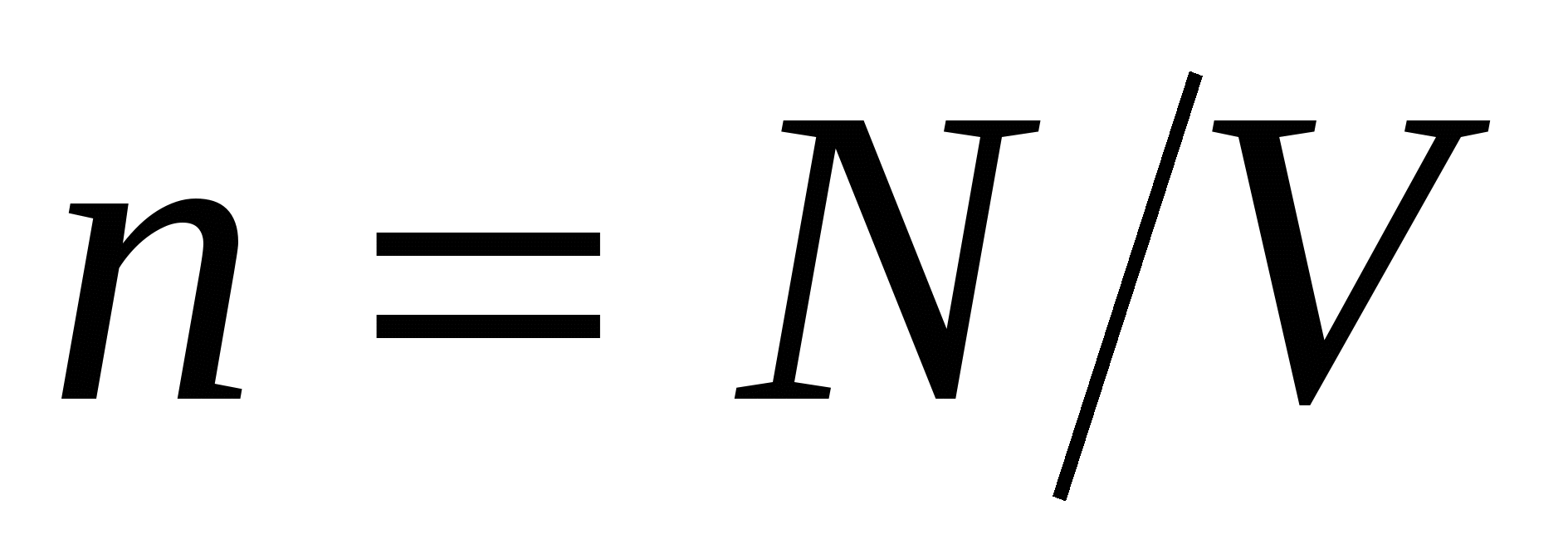
где V-объём системы
Основное уравнение кинетической теории газов
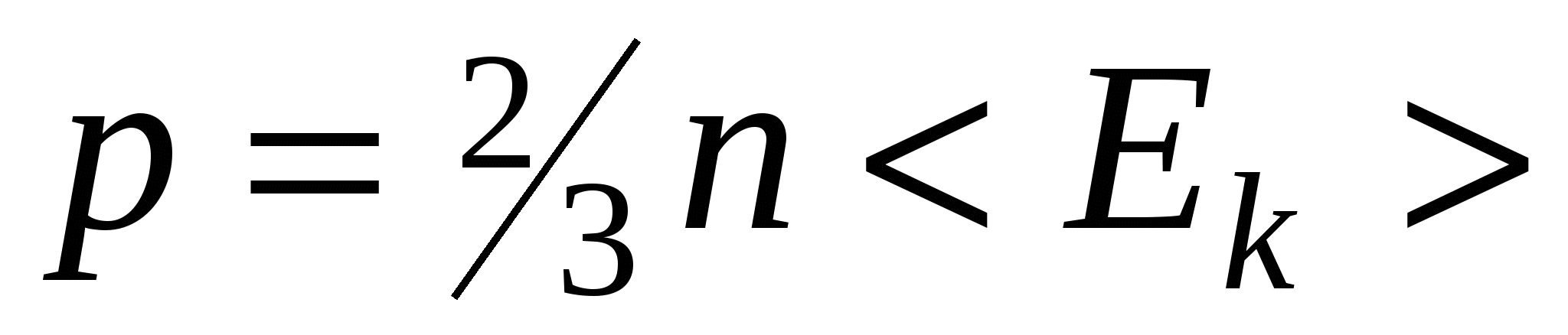
где p — давление газа; <Ek>-средняя кинетическая энергия поступательного движения молекулы.
Средняя кинетическая энергия:
приходящаяся на одну степень свободы молекулы
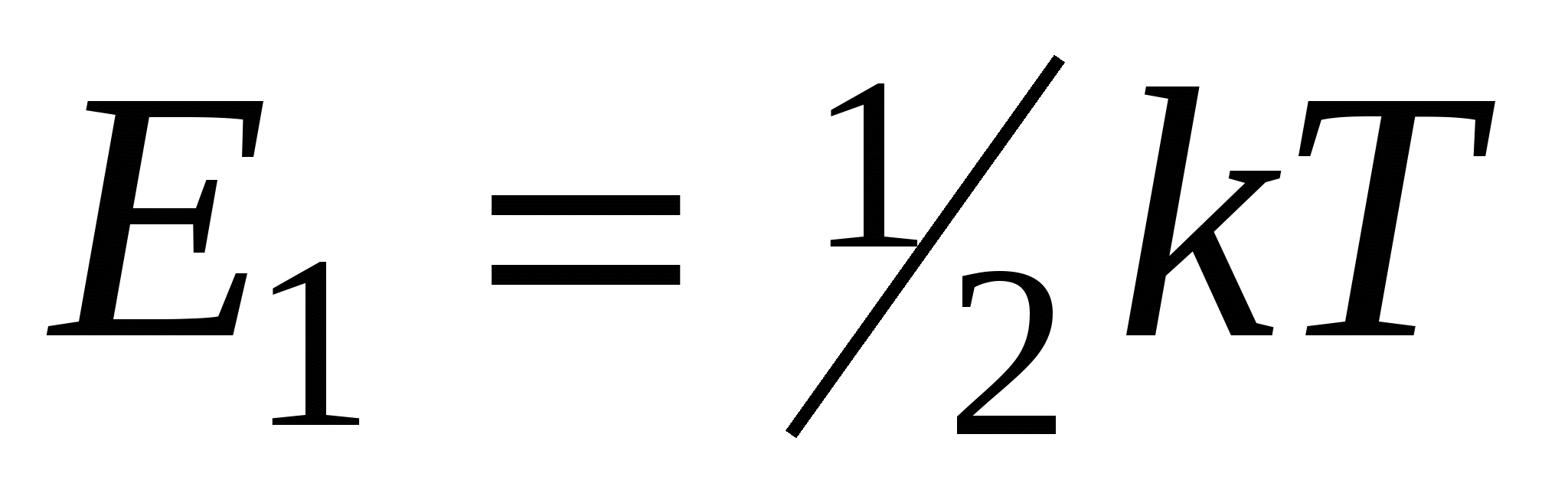
приходящаяся на все степени свободы молекулы (полная энергия молекулы)
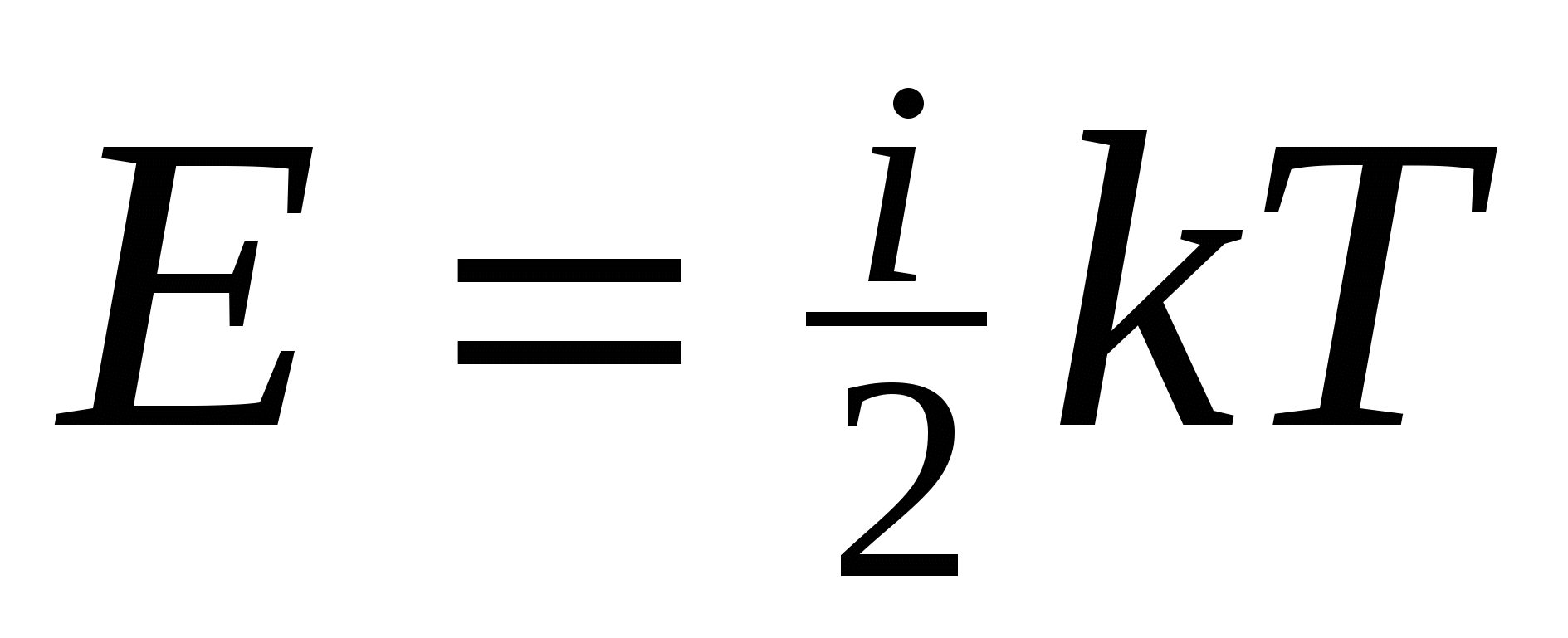
поступательное движение молекулы
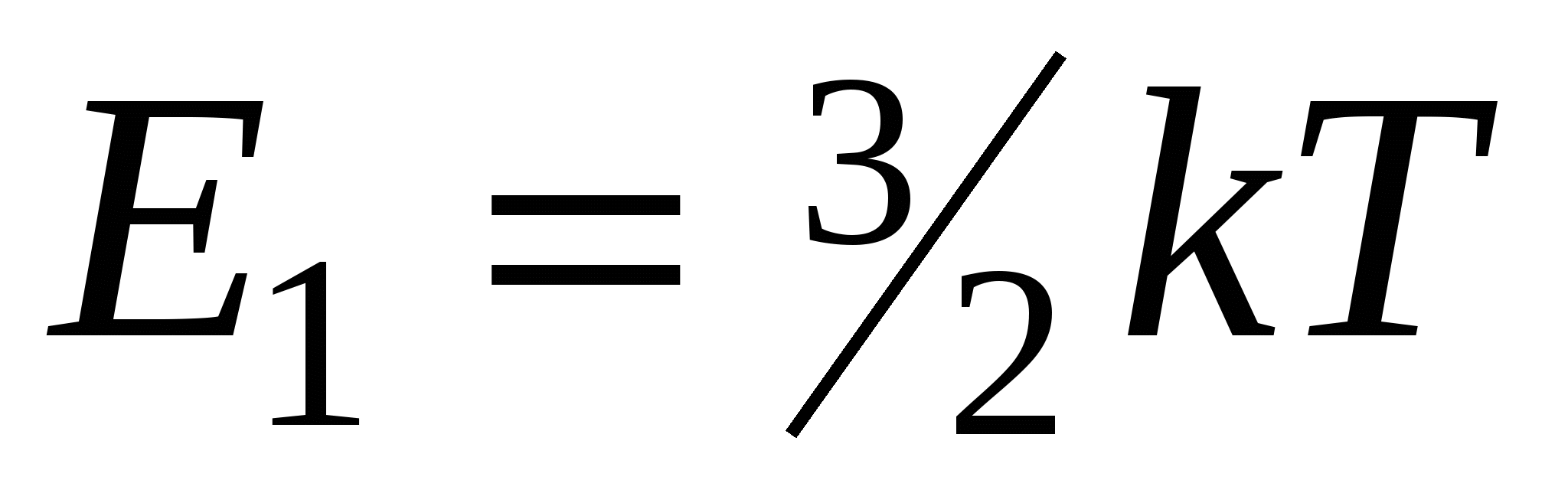
где k-постоянная Больцмана; T-термодинамическая температура; i-число степеней свободы молекулы;
Энергия вращательного движения молекулы
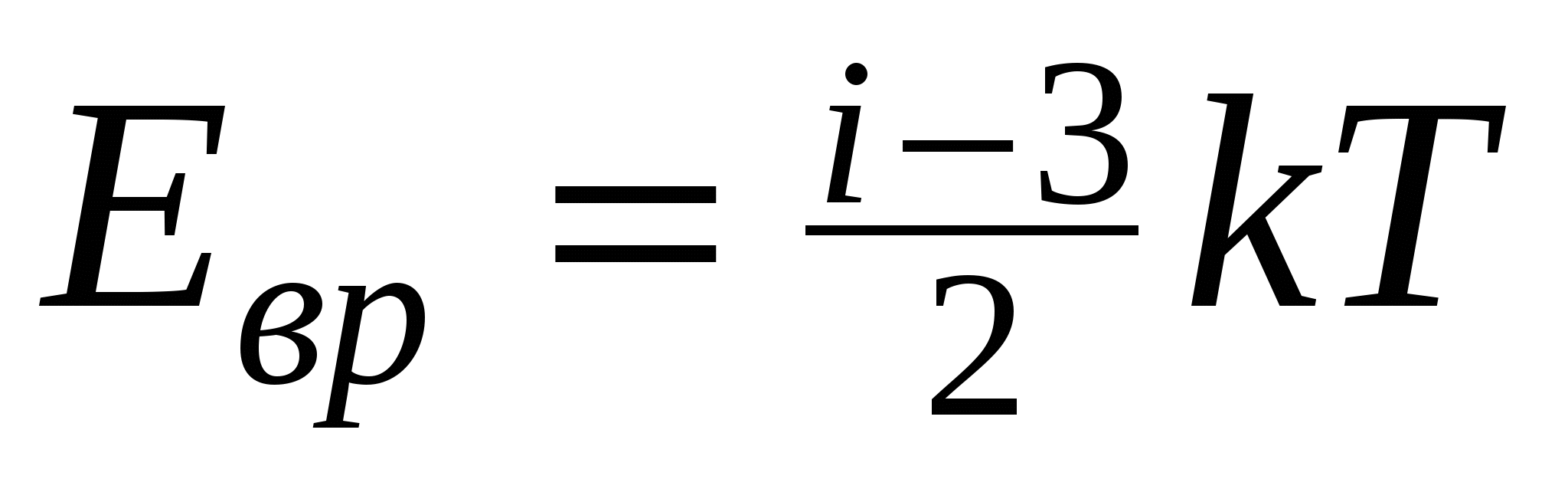
Зависимость давления газа от концентрации молекул и температуры
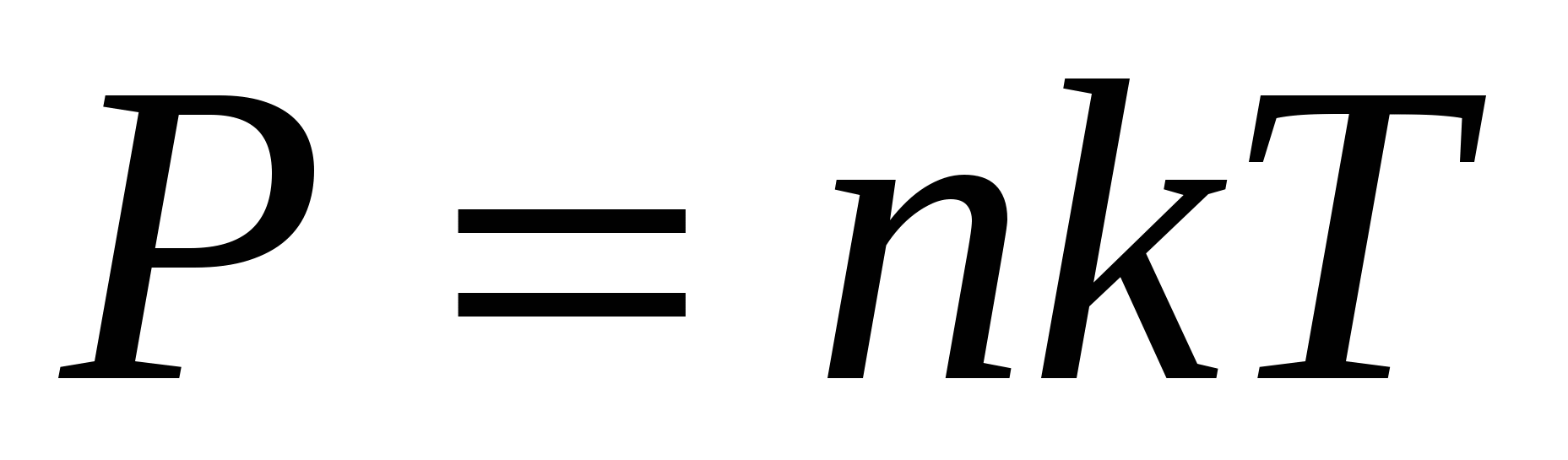
средняя квадратичная
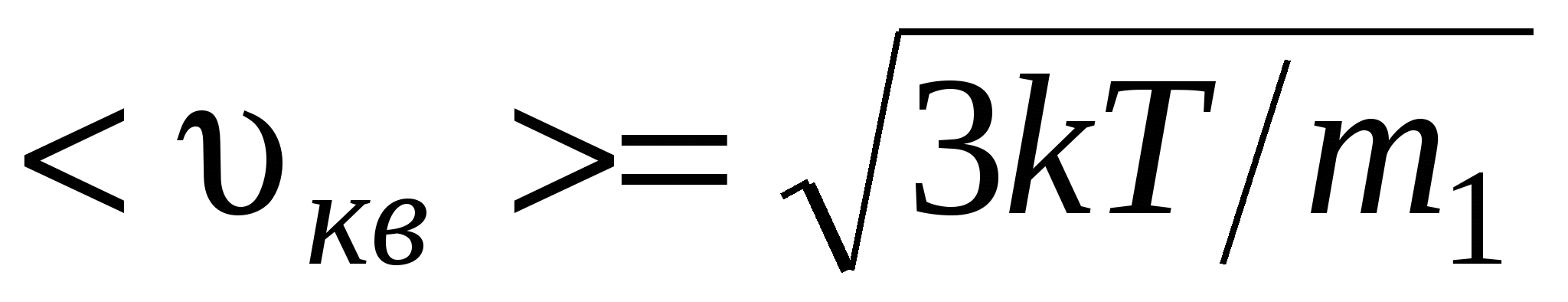 , или , или 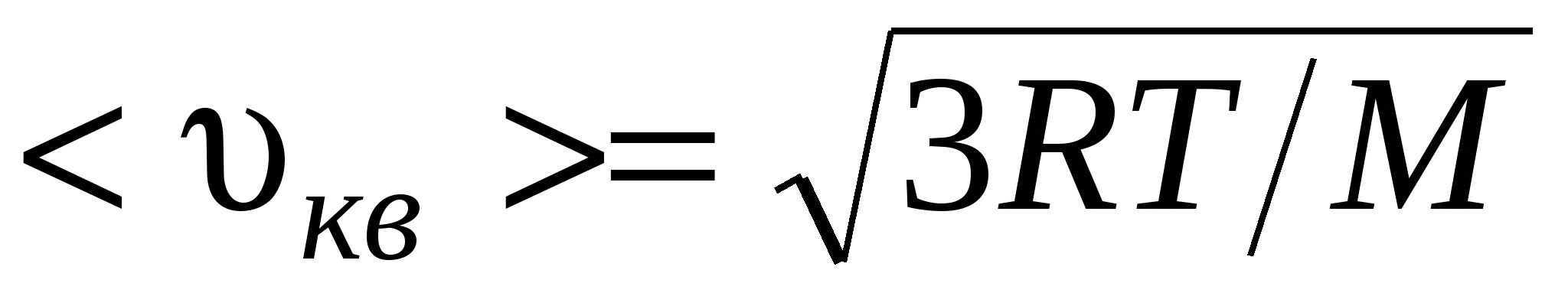
средняя арифметическая
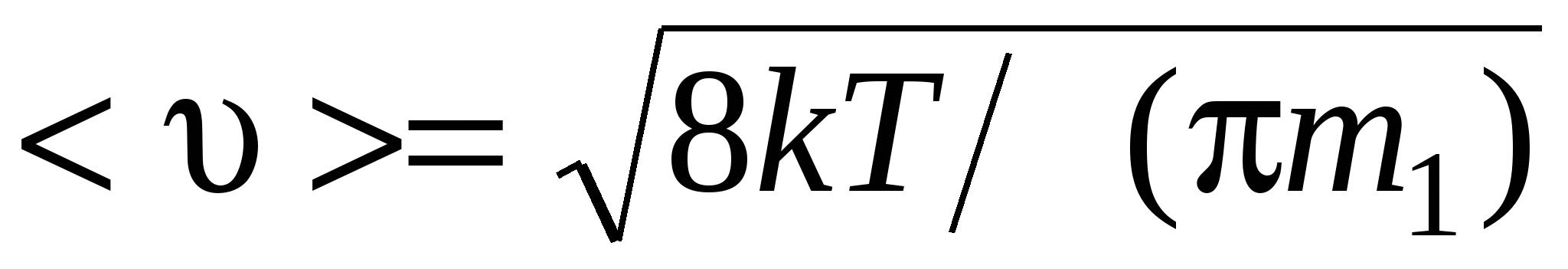 , или , или 
наиболее вероятная
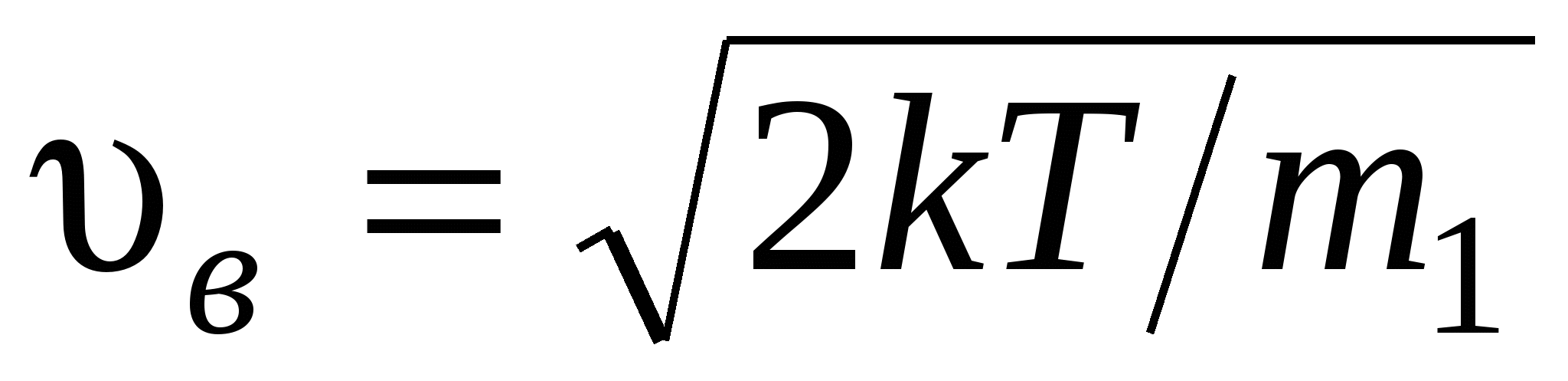 , или , или 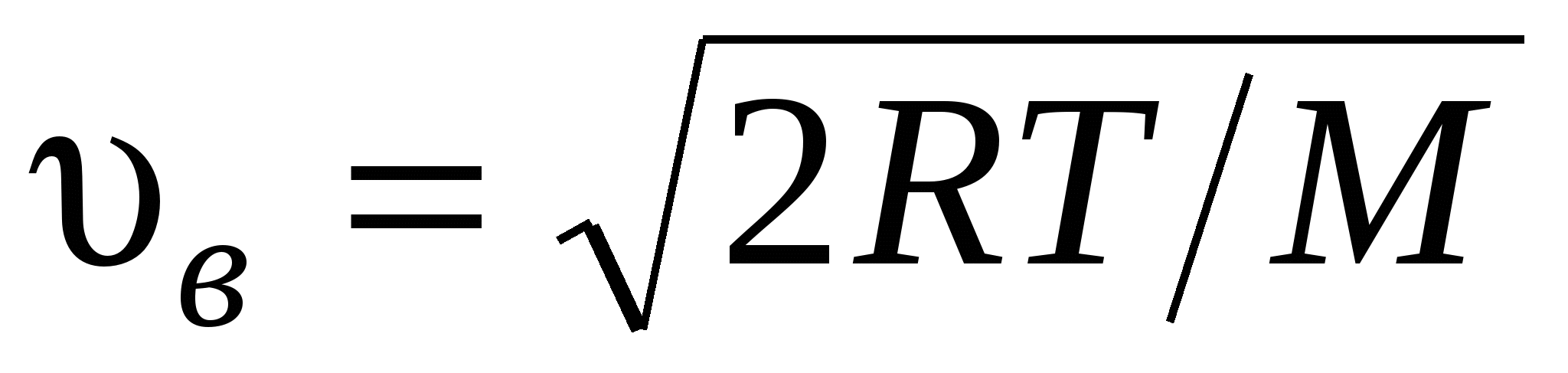
где m1 – масса одной молекулы.
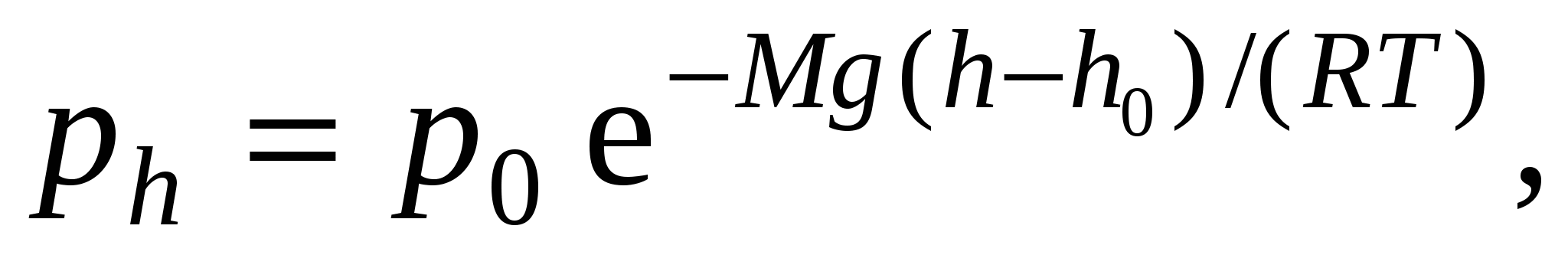
где ph и p0 – давление газа на высоте h и h0.
Распределение Больцмана во внешнем потенциальном поле
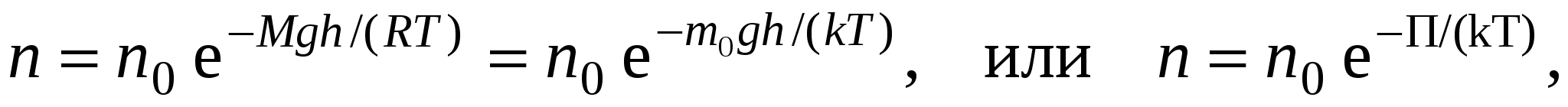
где n и n0 – концентрация молекул на высоте h и h=0; П=m0gh – потенциальная энергия молекулы в поле тяготения.
Среднее число соударений, испытываемых молекулой газа за 1 с 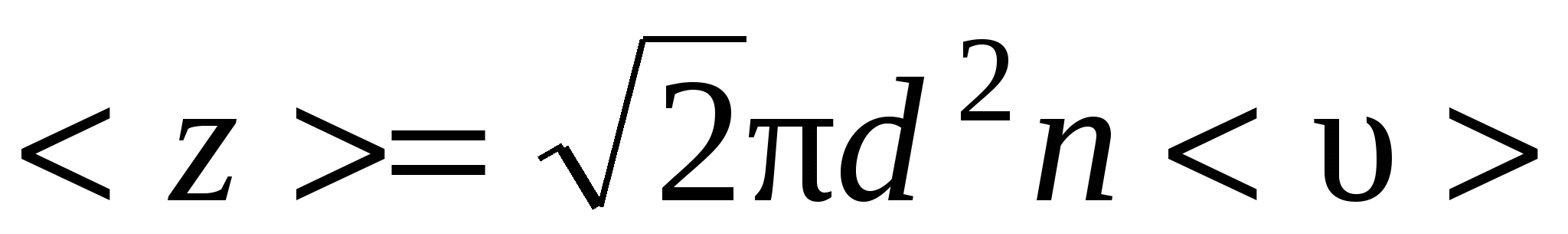 , ,
где d – эффективный диаметр молекулы; n – концентрация молекул; <υ> - средняя арифметическая скорость молекул.
Средняя длина свободного пробега молекул газа
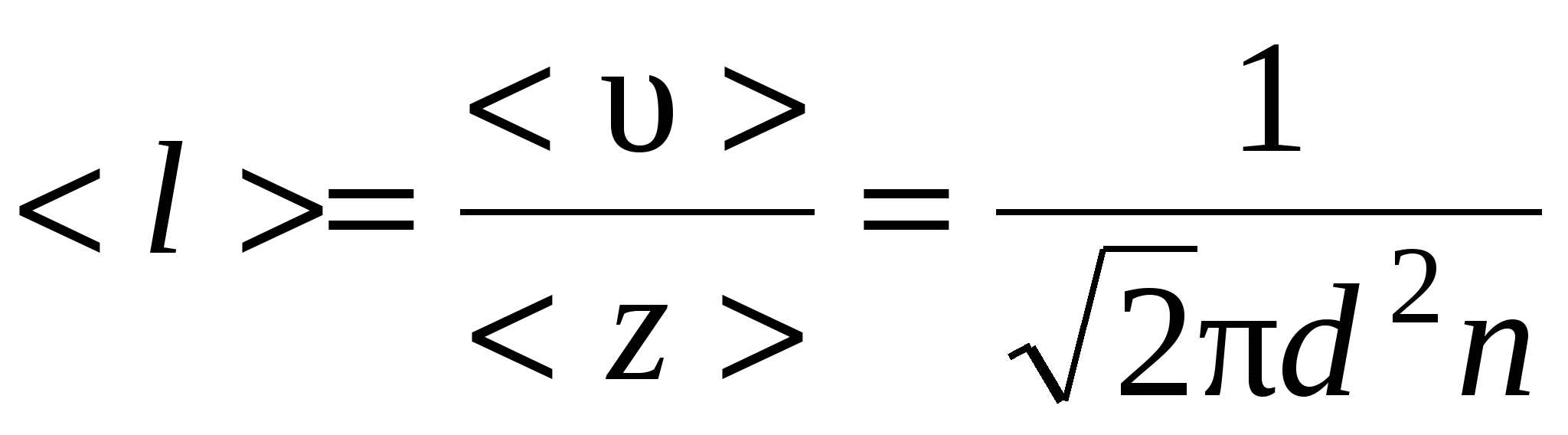 . .
Закон теплопроводности Фурье
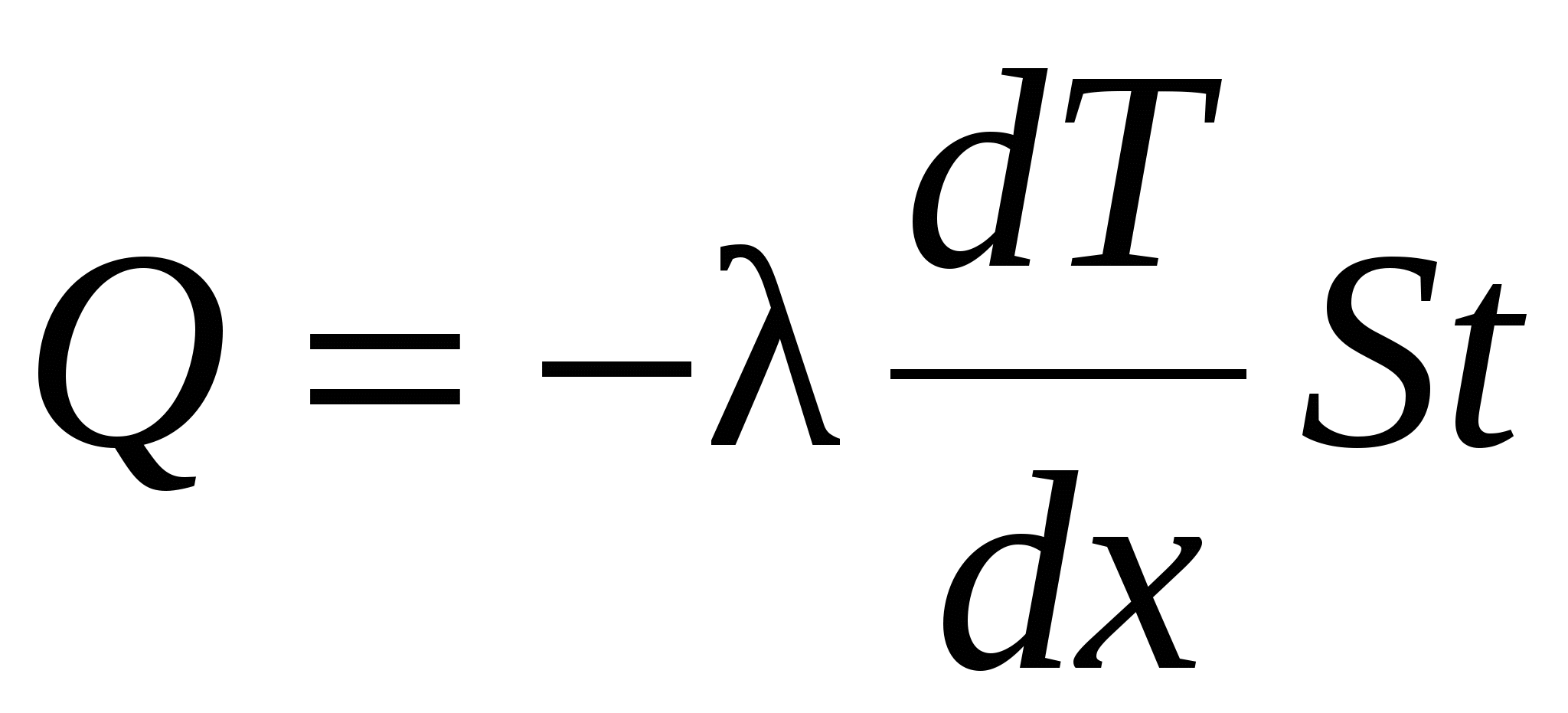 , ,
где Q – теплота, прошедшая посредством теплопроводности через площадь S за время t; dT/dx – градиент температуры; λ – теплопроводность:
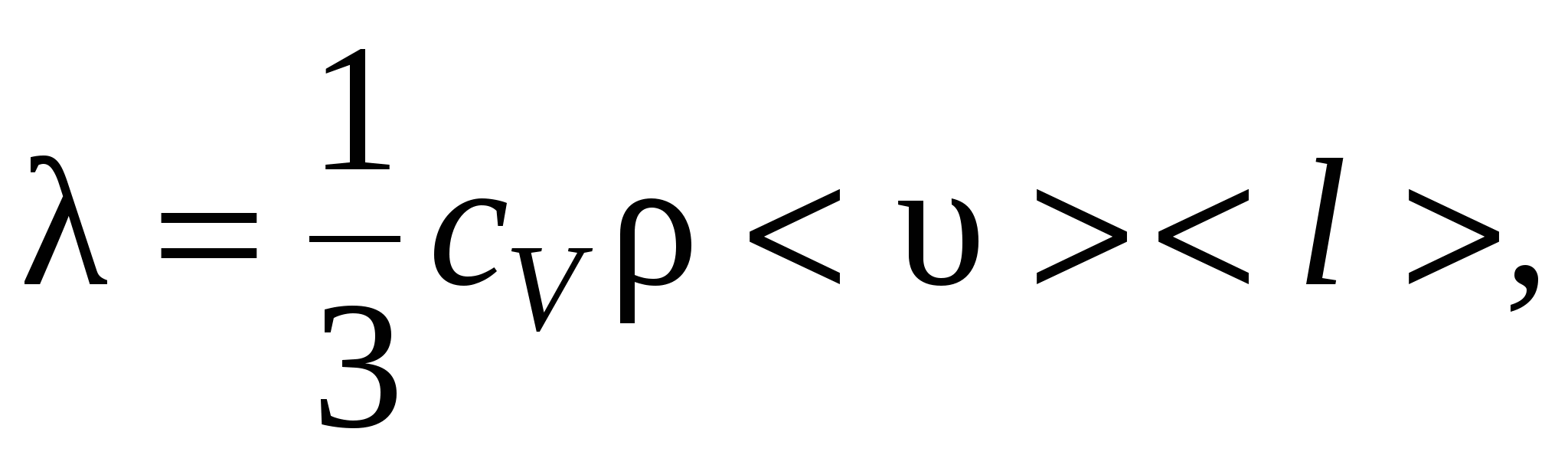
где cV – удельная теплоемкость газа при постоянном объеме; ρ – плотность газа; <υ> - средняя арифметическая скорость теплового движения его молекул; <l> - средняя длина свободного пробега молекул.
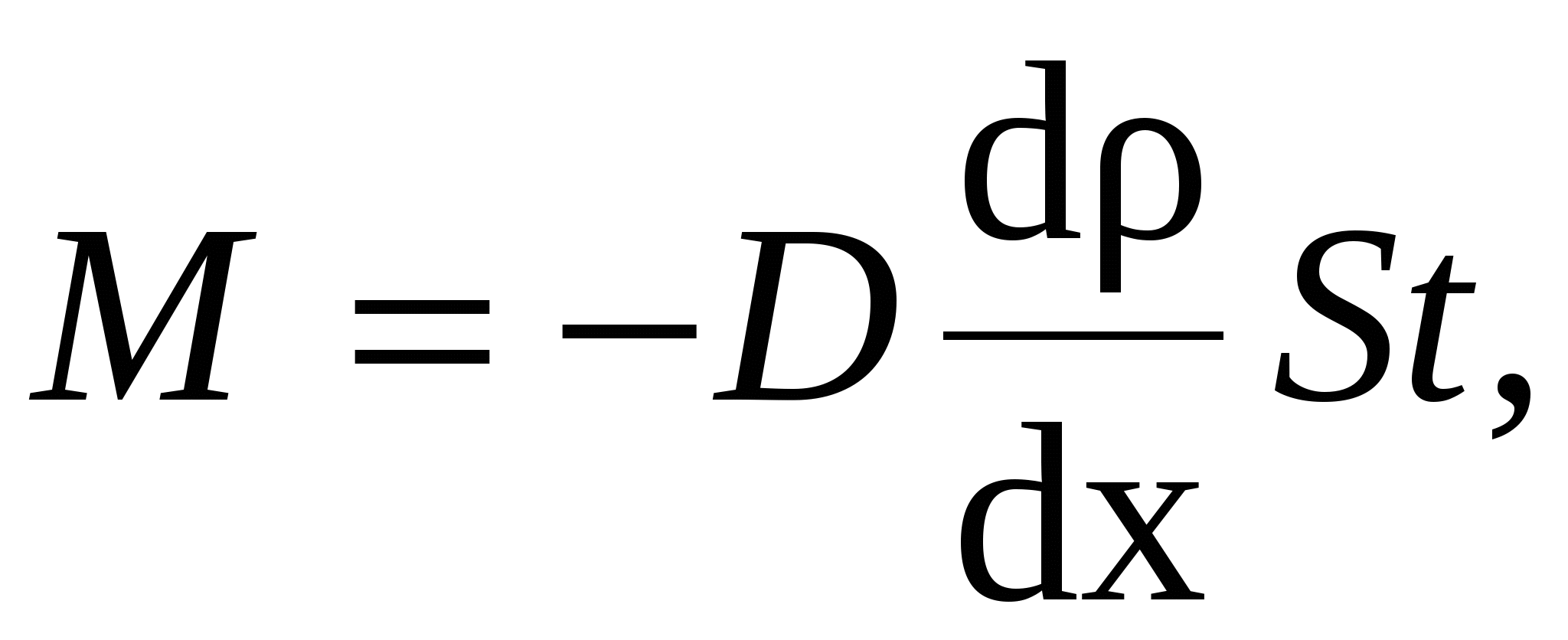
где M – масса вещества, переносимая посредством диффузии через площадь S за время t; dρ/dx – градиент плотности; D – диффузия:
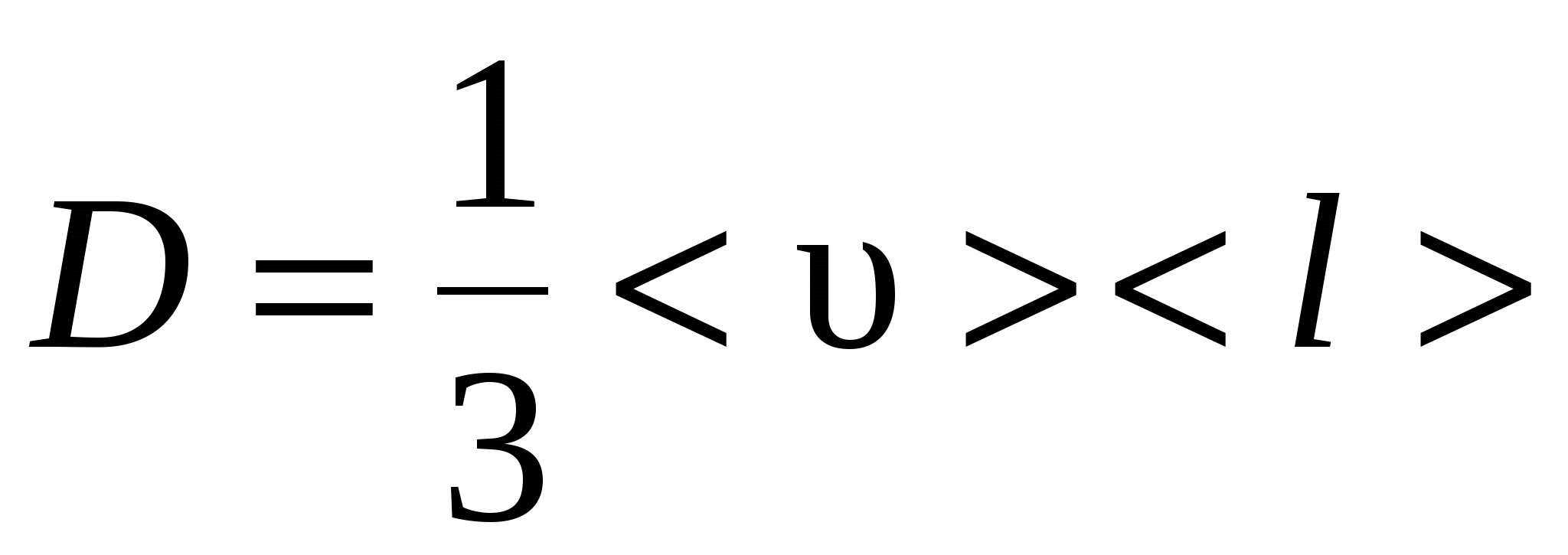 . .
Закон Ньютона для внутреннего трения (вязкости)
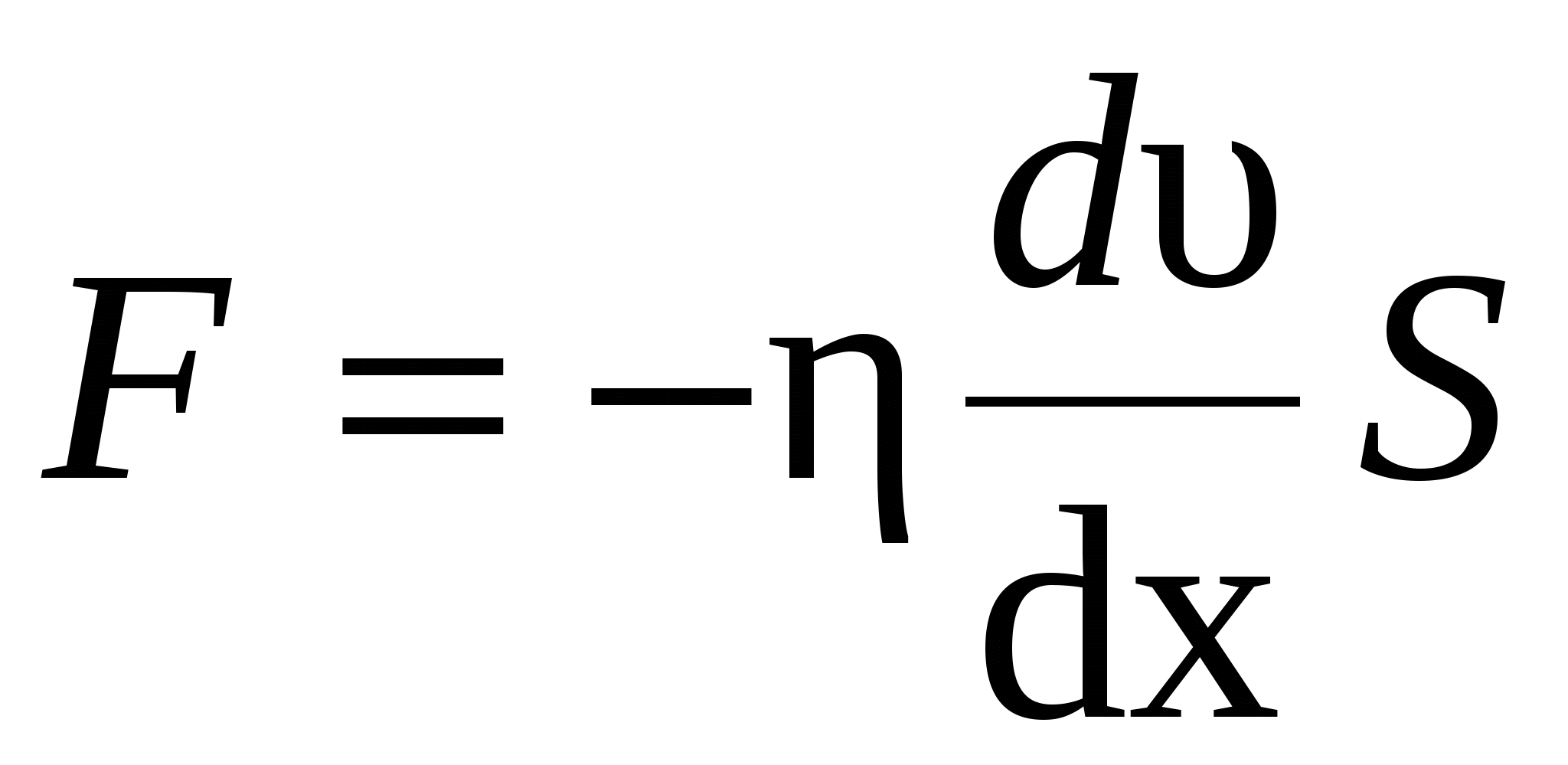 , ,
где F – сила внутреннего трения между движущимися слоями площадью S; dυ/dx – градиент скорости; η – динамическая вязкость:
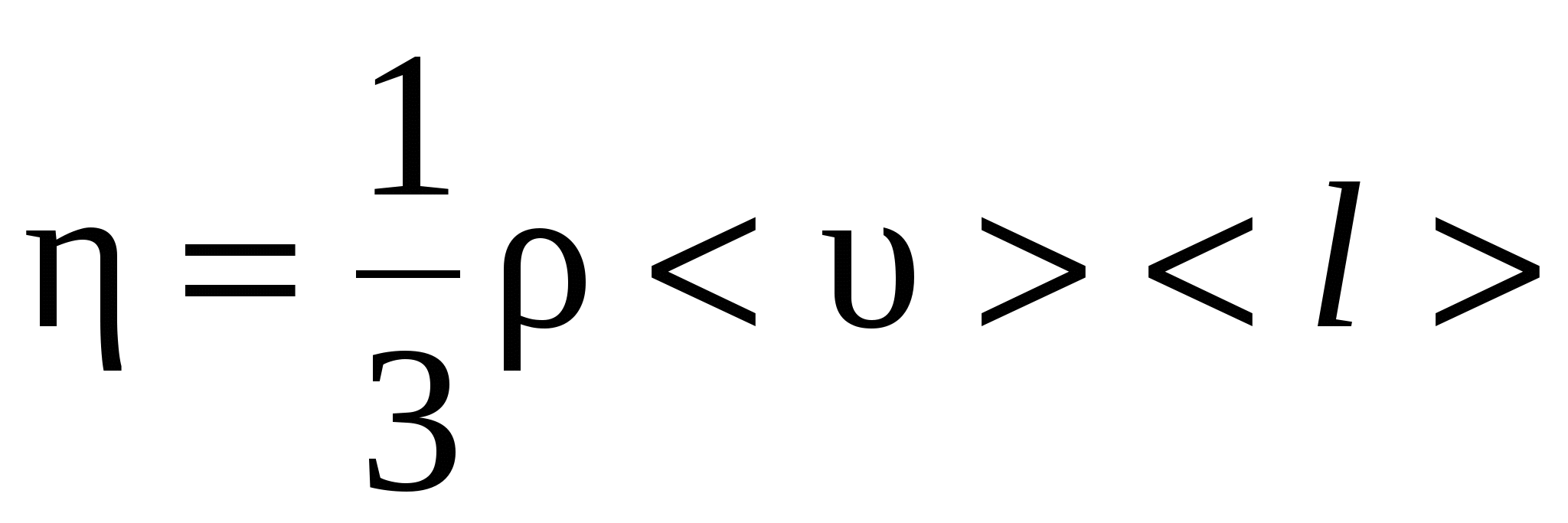 . .
Начертить графики изотермического, изобарного и изохорного процессов в координатах P и V, P и Т, Т и V.
Определить число N атомов в 1 кг водорода и массу одного атома водорода. Ответ: Н = 3,01·1026; т0 = 3,32.10-27 кг.
В закрытом сосуде вместимостью 20 л находятся водород массой 6 г и гелий массой 12 г. Определить: 1) давление; 2) молярную массу газовой смеси в сосуде, если температура смеси Т = 300 К. Ответ: 1) P = 0,75 кПа; 2) М = 3·10-3 кг/моль.
Определить плотность смеси газов водорода массой m1 = 8 г и кислорода массой m2 = 64 г при температуре Т = 290 К и при давлении 0,1 МПа. Газы считать идеальными. Ответ: 0,498 кг/м3.
Баллон вместимостью V = 20 л содержит смесь водорода и азота при температуре 290 К и давлении 1 МПа. Определить массу водорода, если масса смеси равна 150 г. Ответ: 6,3 г.
В сосуде вместимостью 1 л находится кислород массой 1 г. Определить концентрацию молекул кислорода в сосуде. Ответ: 1,88.1025 м-3.
Определить наиболее вероятную скорость молекул газа, плотность которого при давлении 40 кПа составляет 0,35 кг/м3. Ответ: 478 м/с.
Определить среднюю кинетическую энергию <E0> поступательного движения молекул газа, находящегося под давлением 0,1 Па. Концентрация молекул газа равна 1013 см-3. Ответ: 1,5·10-19 Дж.
Используя закон распределения молекул идеального газа по скоростям, найти формулу наиболее вероятной скорости υB. Ответ: υB = 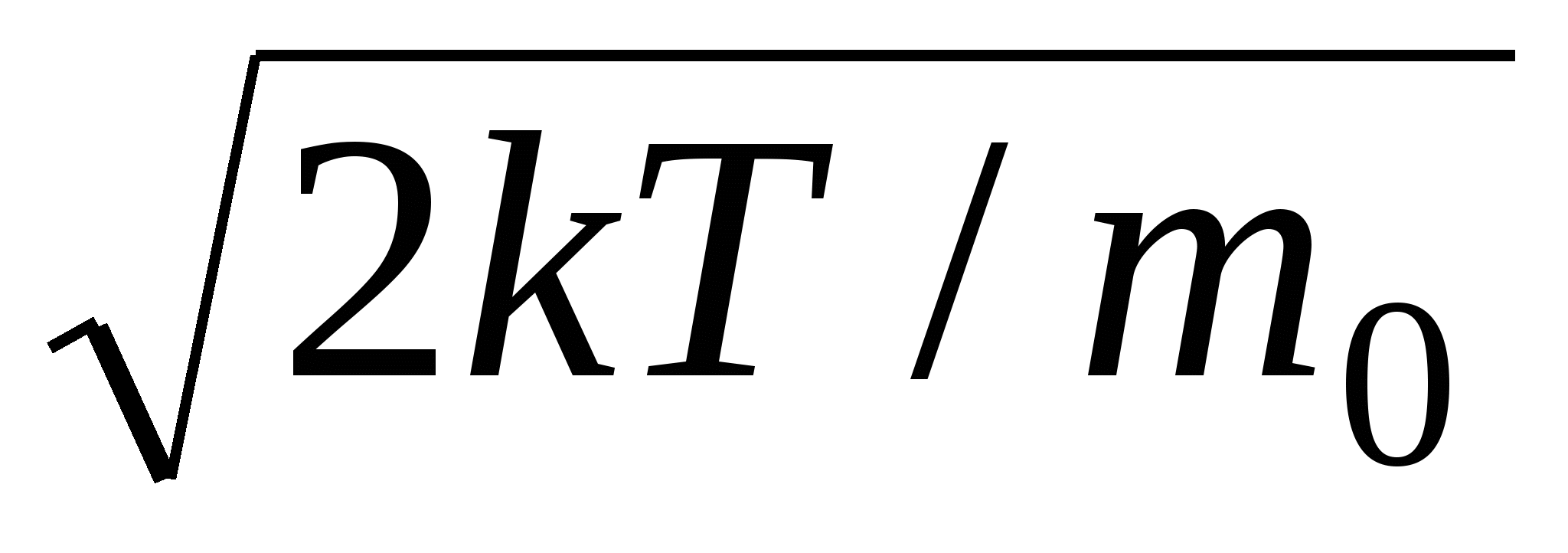
Используя закон распределения молекул идеального газа по скоростям, найти закон, выражающий распределение молекул по относительным скоростям и (u = υ/υв). Ответ: f(u) = 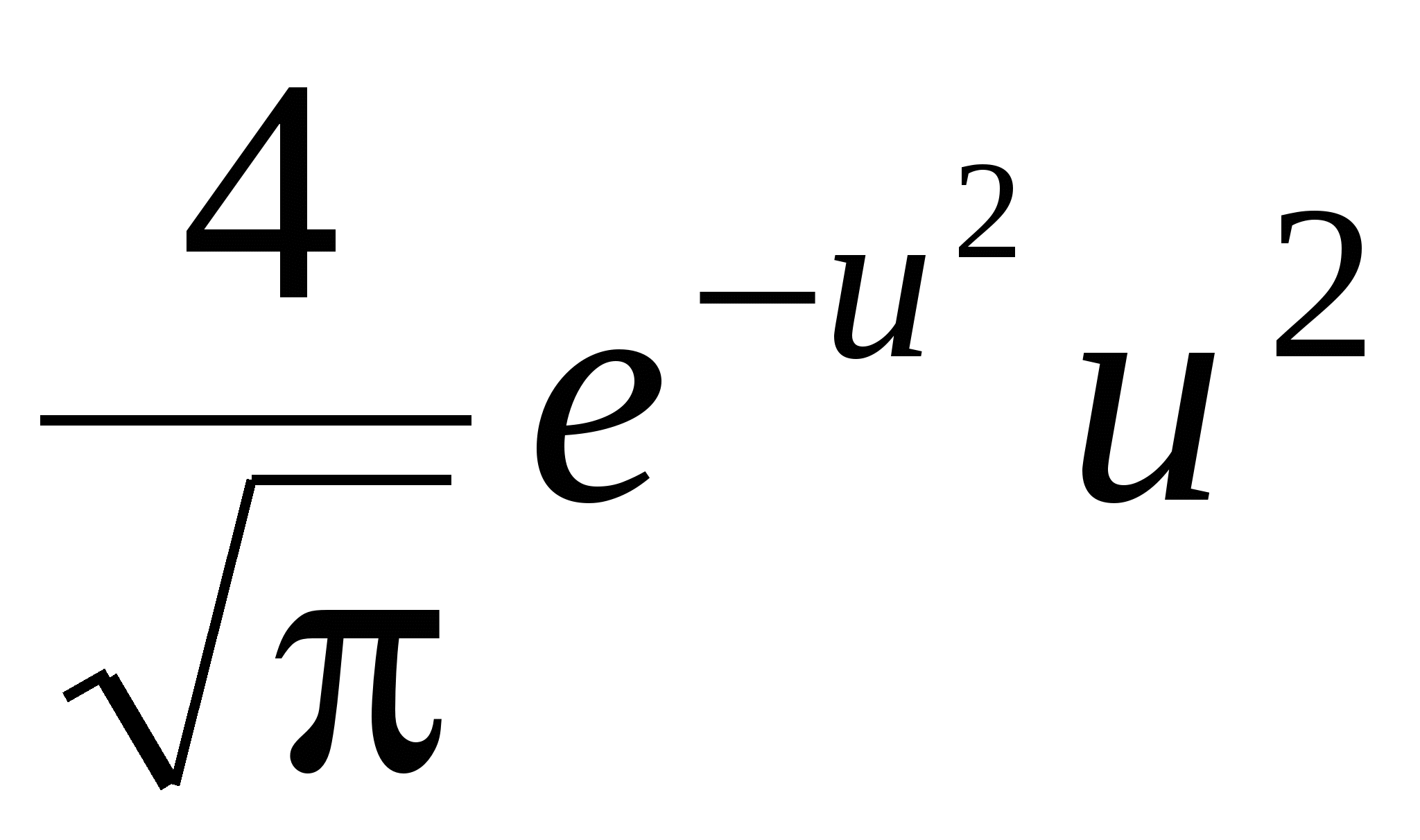 . .
На какой высоте давление воздуха составляет 60 % от давления на уровне моря? Считать, что температура воздуха везде одинакова и равна 10 °С. Ответ: 4,22 км.
Каково давление воздуха в шахте на глубине 1 км, если считать, что температура по всей высоте постоянная и равна 22 °С, а ускорение свободного падения не зависит от высоты. Давление воздуха у поверхности Земли принять равным P0. Ответ: 1,12 P0.
Определить отношение давления воздуха на высоте 1 км к давлению на дне скважины глубиной 1 км. Воздух у поверхности Земли находится при нормальных условиях, и его температура не зависит от высоты Ответ: 0,78.
На какой высоте плотность воздуха в е раз (е — основание натуральных логарифмов) меньше по сравнению с его плотностью на уровне моря? Температуру воздуха и ускорение свободного падения считать не зависящими от высоты. Ответ: 7,98 км.
Определить среднюю длину свободного пробега <l> молекул кислорода, находящегося при температуре 0 °С, если среднее число <z> столкнрвений, испытываемых молекулой в 1 с, равно 3,7·109. Ответ: 115 нм.
При каком давлении средняя длина свободного пробега молекул водорода равна 2,5 см, если температура газа равна 67 °С? Диаметр молекулы водорода принять равным 0,28 нм. Ответ: 0,539 Па.
Определить среднюю продолжительность <τ> свободного пробега молекул водорода при температуре 27 °С и давлении 5 кПа. Диаметр молекулы водорода' принять равным 0,28 нм. Ответ: 13,3 нс.
Средняя длина свободного пробега <l> молекул водорода при нормальных условиях составляет 0,1 мкм. Определить среднюю длину их свободного пробега при давлении 0,1 мПа, если температура газа остается постоянной. Ответ: 101 м.
При температуре 300 К и некотором давлении средняя длина свободного пробега <l> молекул кислорода равна 0,1 мкм. Чему равно среднее число <z> столкновений, испытываемых молекулами в 1 с, если сосуд откачать до 0,1 первоначального давления? Температуру газа считать постоянной. Ответ: 4,45.108 с-1.
Определить коэффициент теплопроводности λ азота, находящегося в некотором объеме при температуре 280 К. Эффективный диаметр молекул азота принять равным 0,38 нм. Ответ: 8,25 мВт/(м.К).
Кислород находится при нормальных условиях. Определить коэффициент теплопроводности λ кислорода, если эффективный диаметр его молекул равен 0,36 нм. Ответ: 8,49 мВт/(м·К).
Пространство между двумя параллельными пластинами площадью 150 см2 каждая, находящимися на расстоянии 5 мм друг от друга, заполнено кислородом. Одна пластина поддерживается при температуре 17 °С, другая – при температуре 27 °С. Определить количество теплоты, прошедшее за 5 мин посредством теплопроводности от одной пластины к другой. Кислород находится при нормальных условиях. Эффективный диаметр молекул кислорода считать равным 0,36 нм. Ответ: 76,4 Дж.
Определить коэффициент диффузии D кислорода при нормальных условиях. Эффективный диаметр молекул кислорода принять равным 0,36 нм. Ответ: 9,18.10-6 м2/с.
Определить массу азота прошедшего вследствие диффузии через площадку 50 см2 за 20 с, если градиент плотности в направлении, перпендикулярном площадке, равен 1 кг/м4. Температура азота 290 К, а средняя длина свободного пробега его молекул равна 1 мкм. Ответ: 15,6 мг.
Определить коэффициент теплопроводности λ азота, если коэффициент динамической вязкости η для него при тех же условиях равен 10 мкПа.с Ответ: 7,42 мВт/(м.К).
7. Основы термодинамики
Связь между молярной (Cm) и удельной (c) теплоёмкостями газа
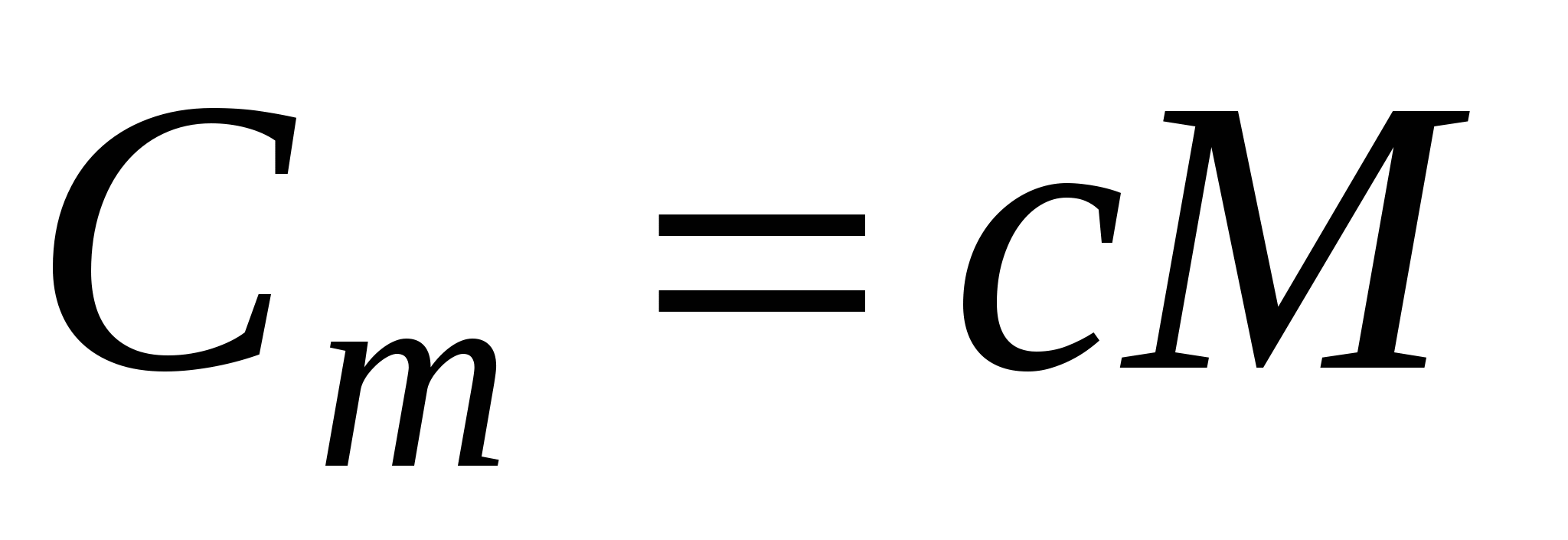
где M-молярная масса газа.
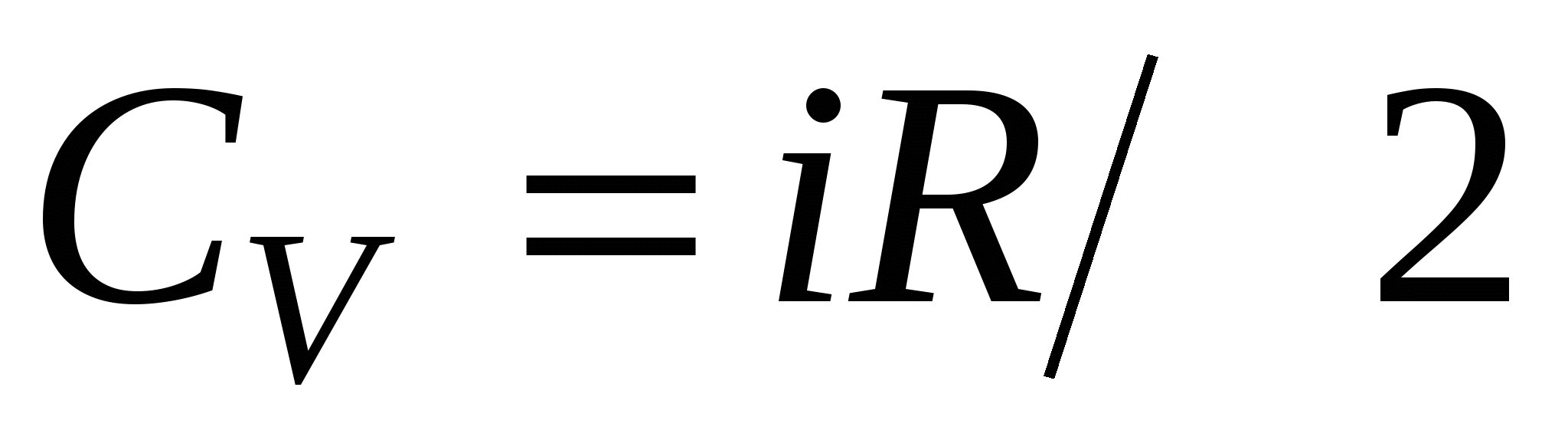 ; ; 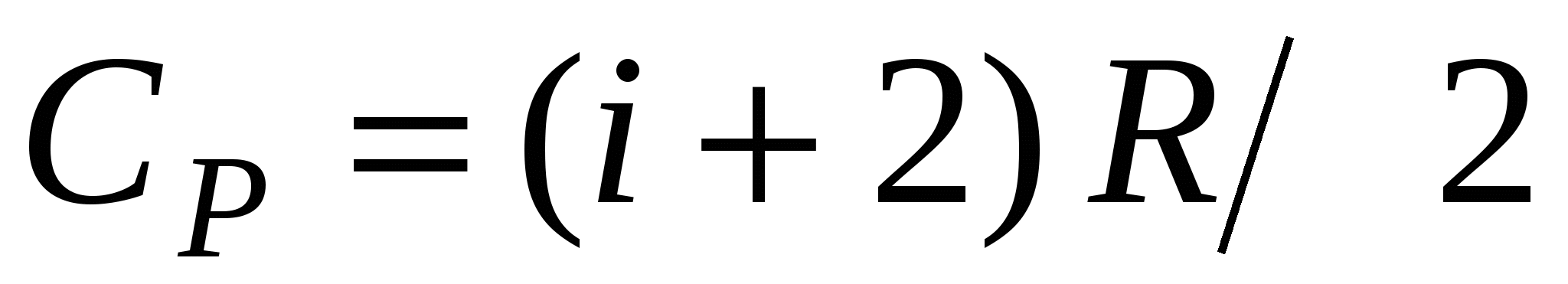
где i-число степеней свободы; R-молярная газовая постоянная.
Удельные теплоемкостью при постоянном объёме и постоянном давлении соответственно равны
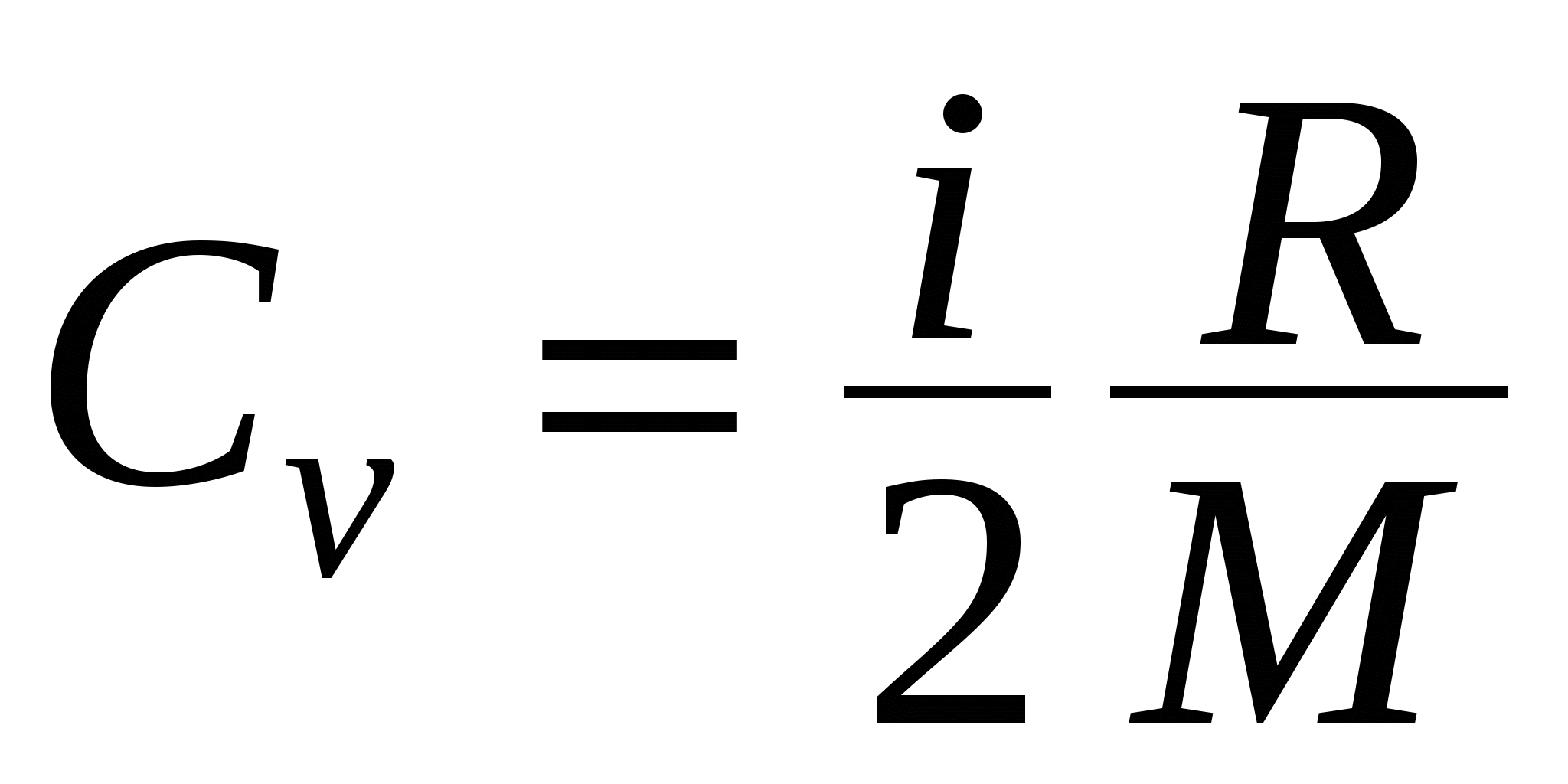 ; ; 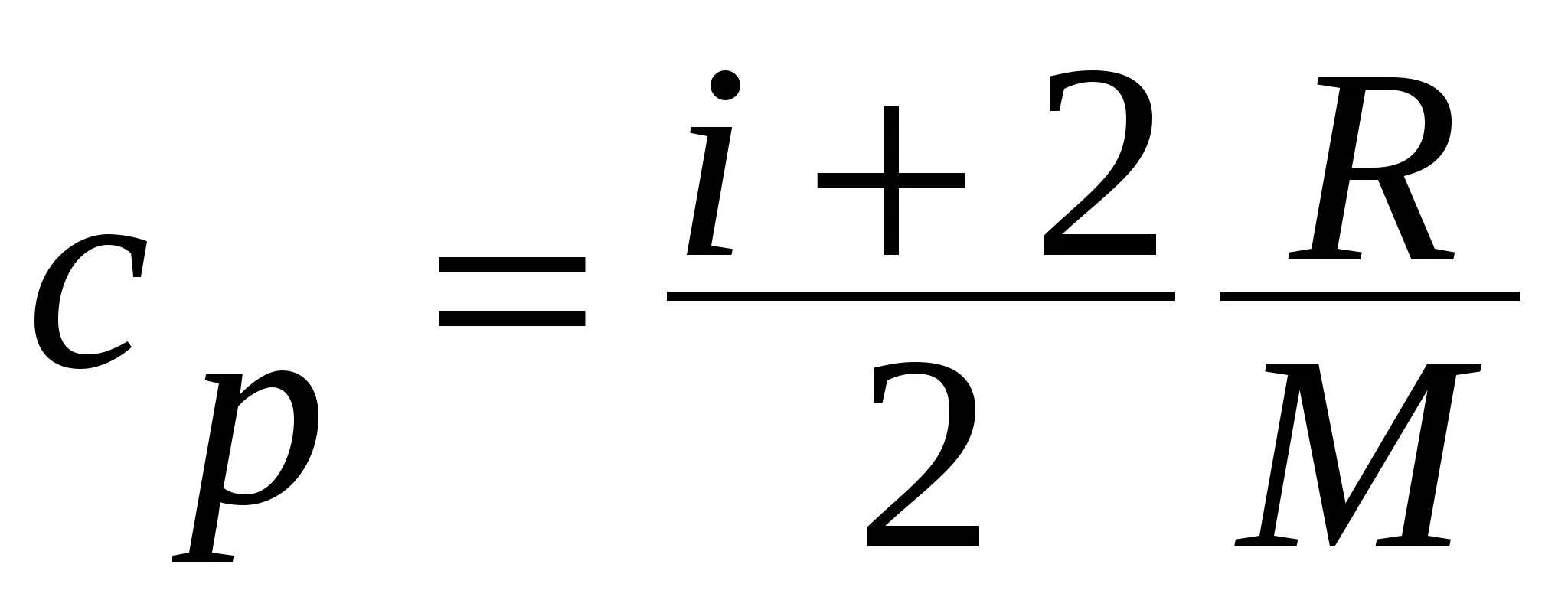
Уравнение Майера 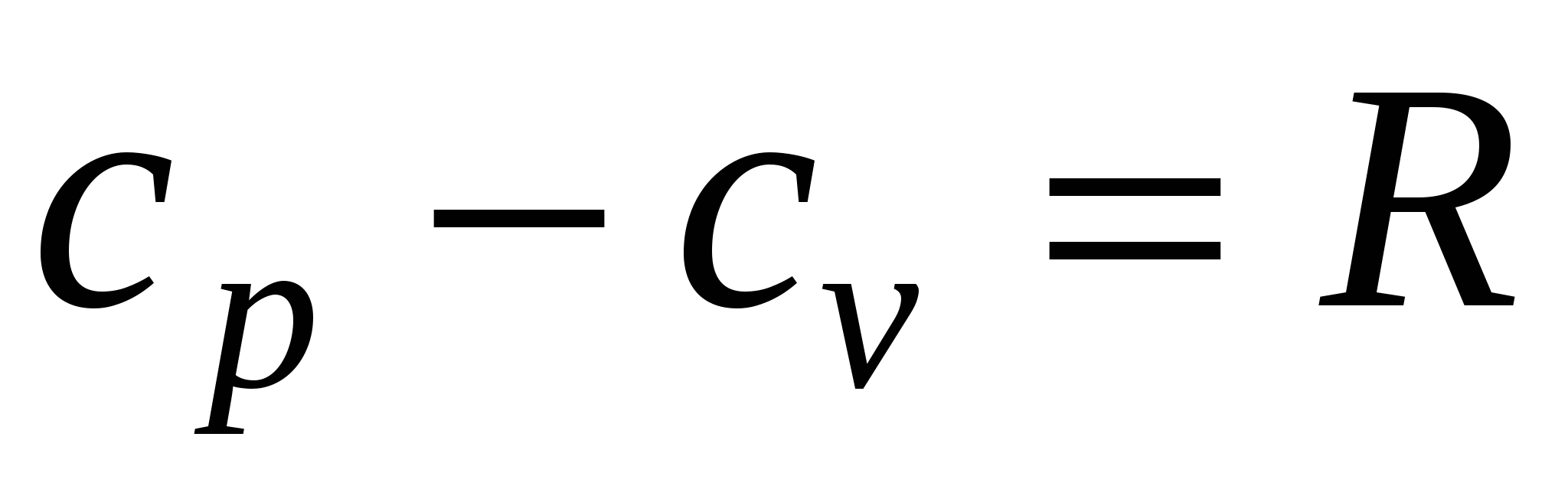
Показатель адиабаты
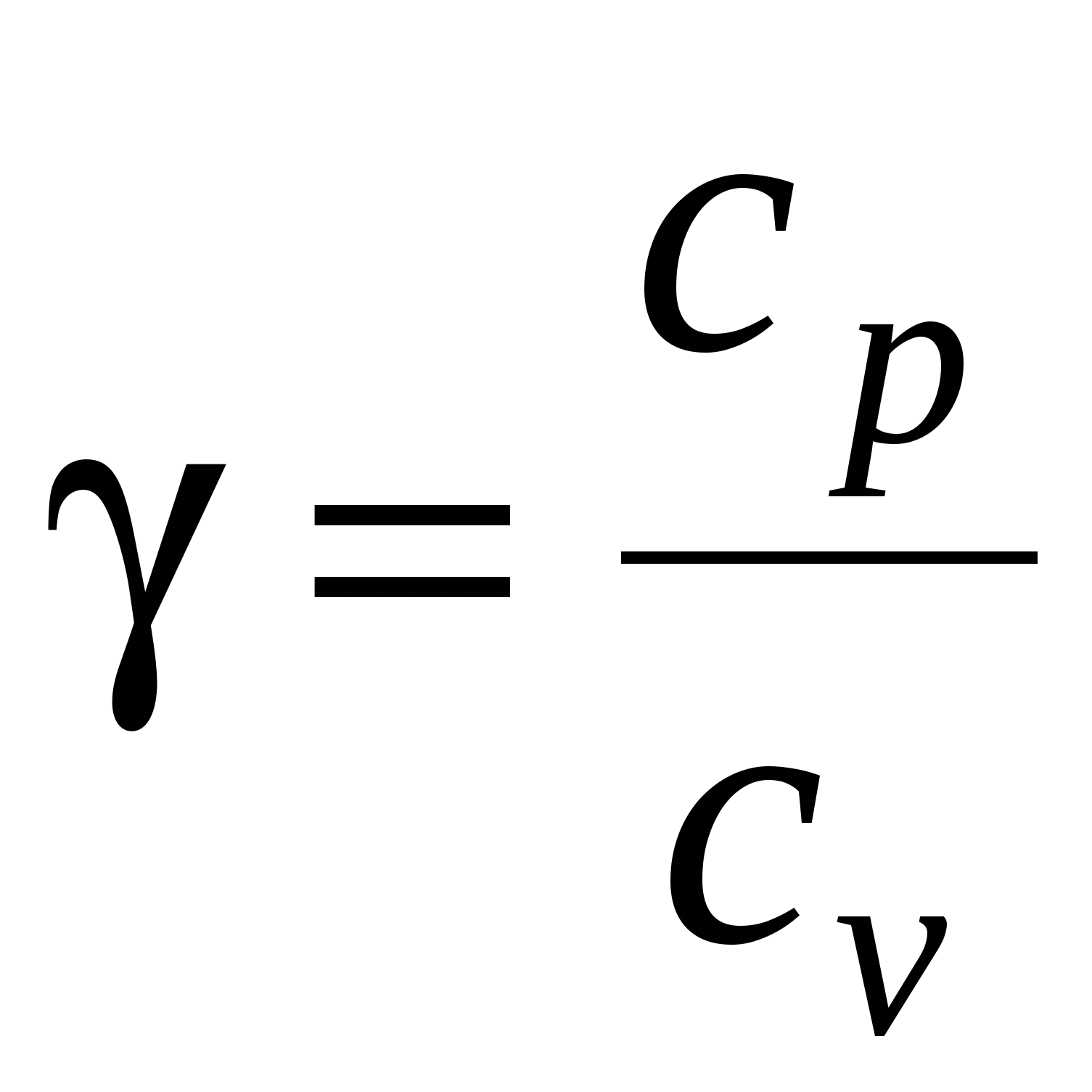 , или , или 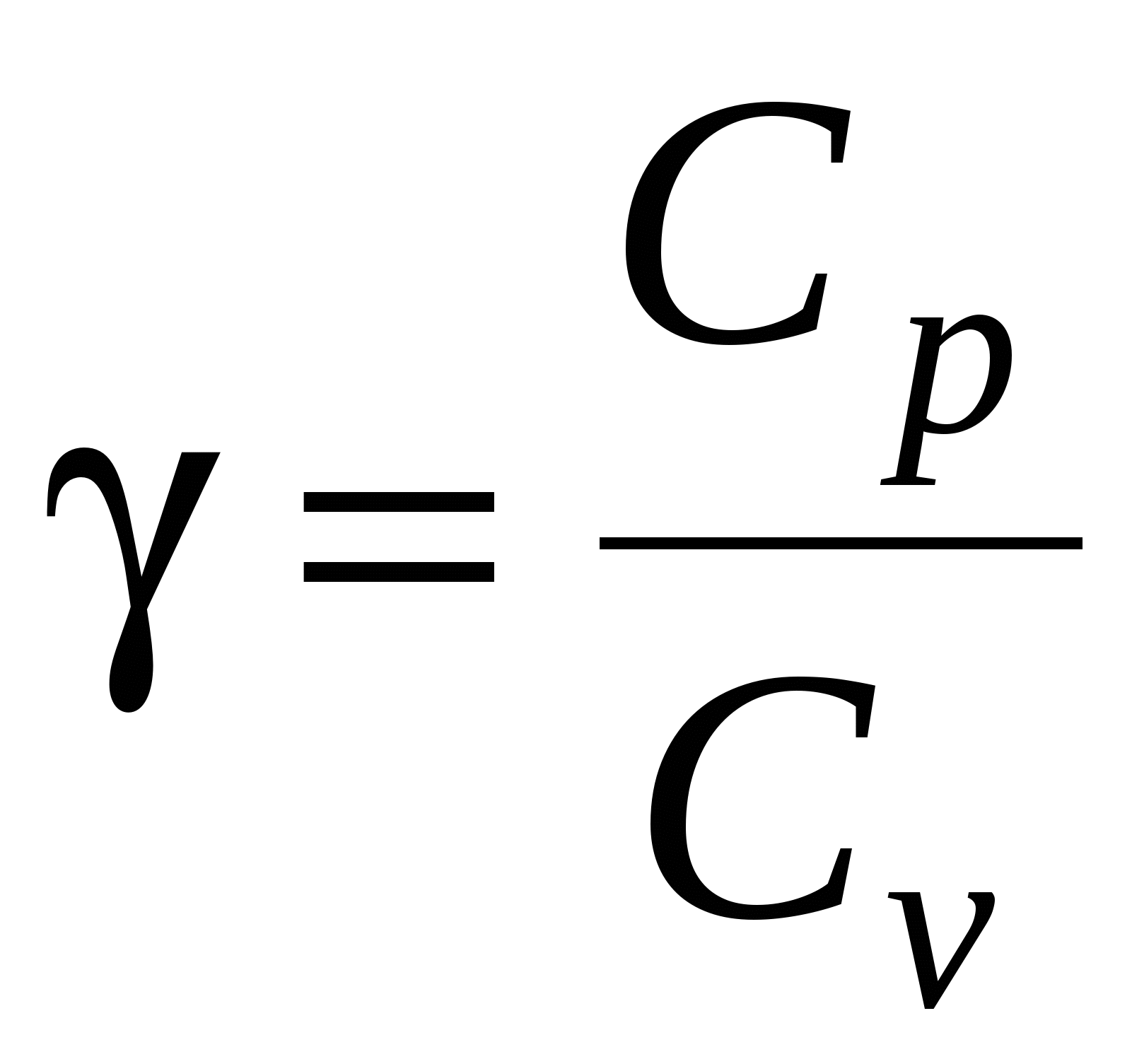 , или , или 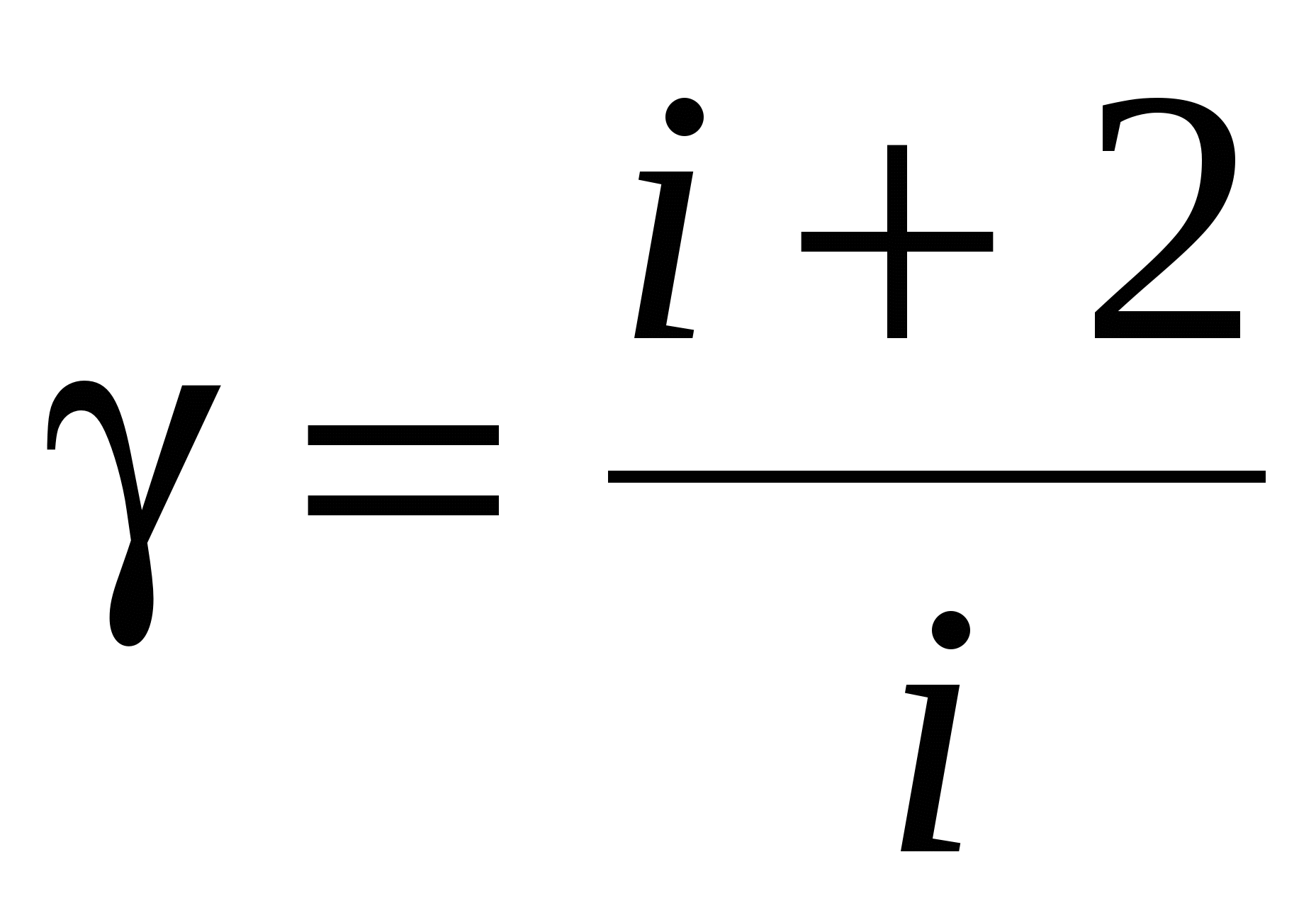 . .
Внутренняя энергия идеального газа
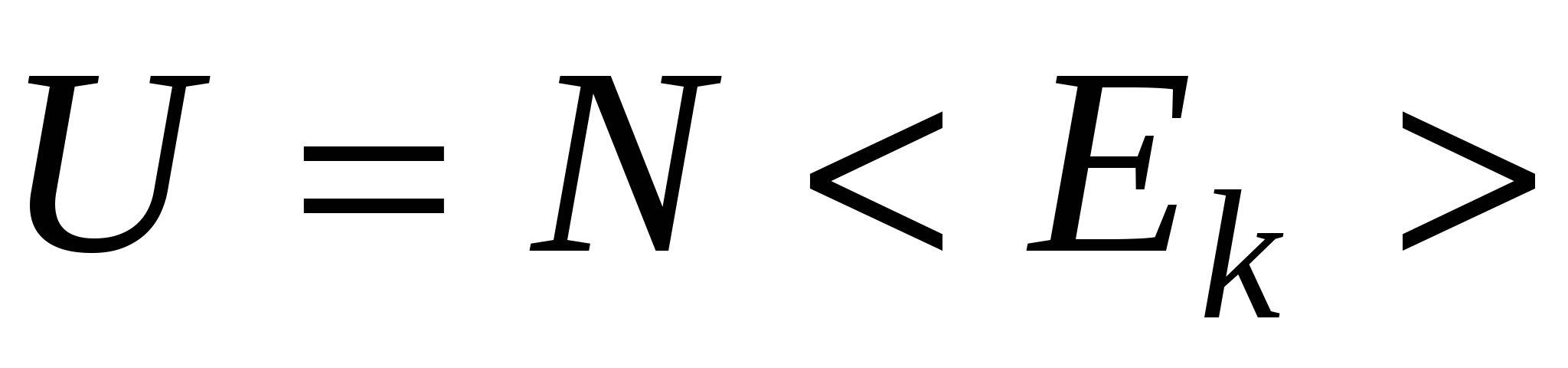 , или , или 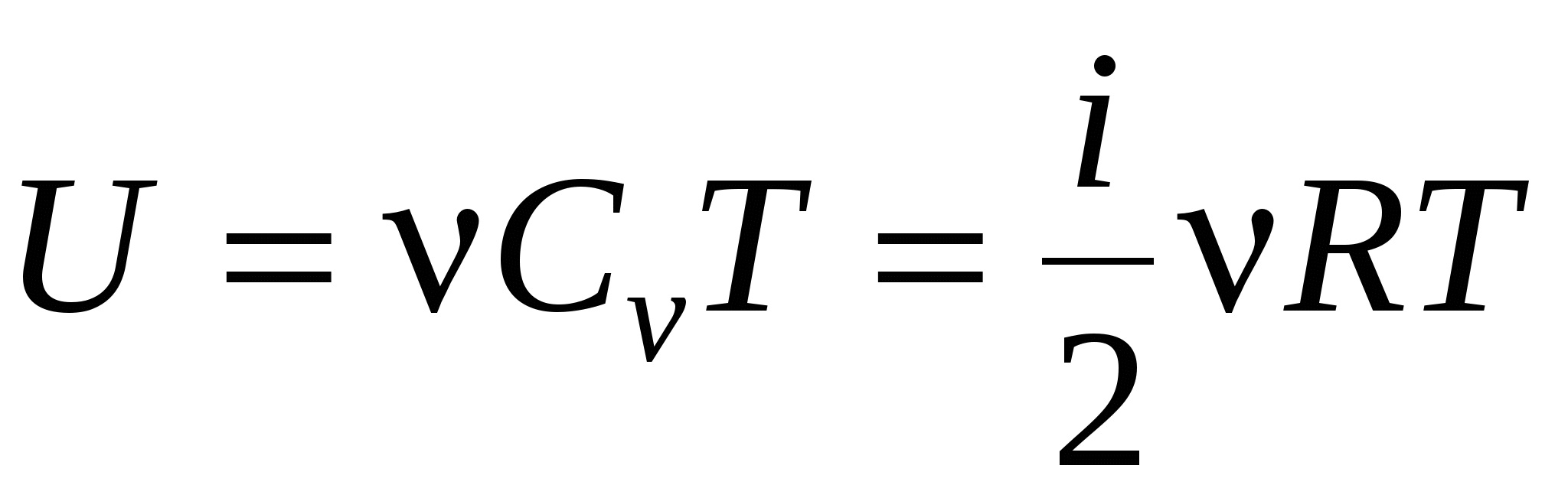 , ,
где <Ek>-средняя кинетическая энергия молекулы; N-число молекул газа; k-количество вещества, 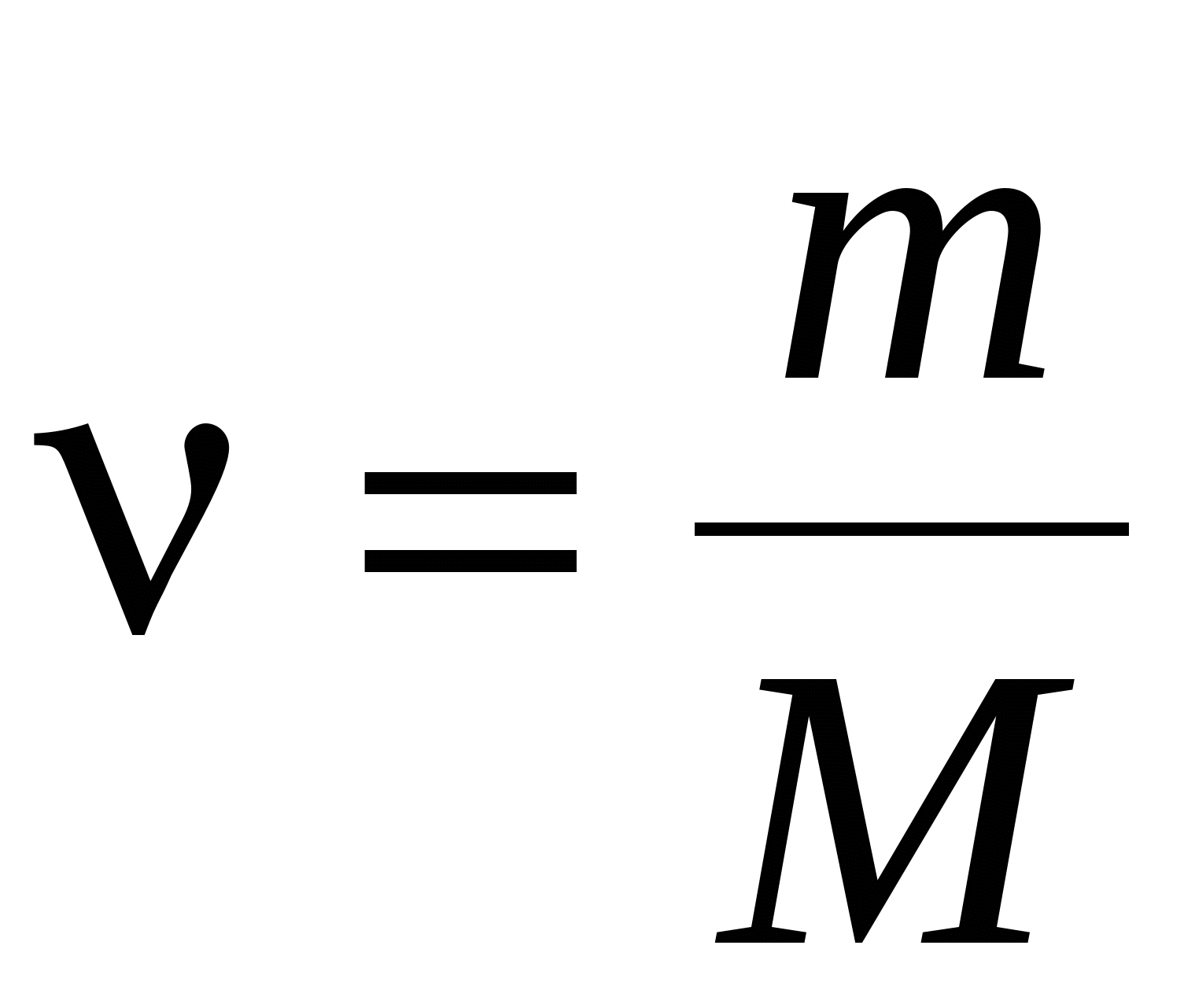 . .
Работа, связанная с изменением объёма газа, в общем случае вычисляется по формуле
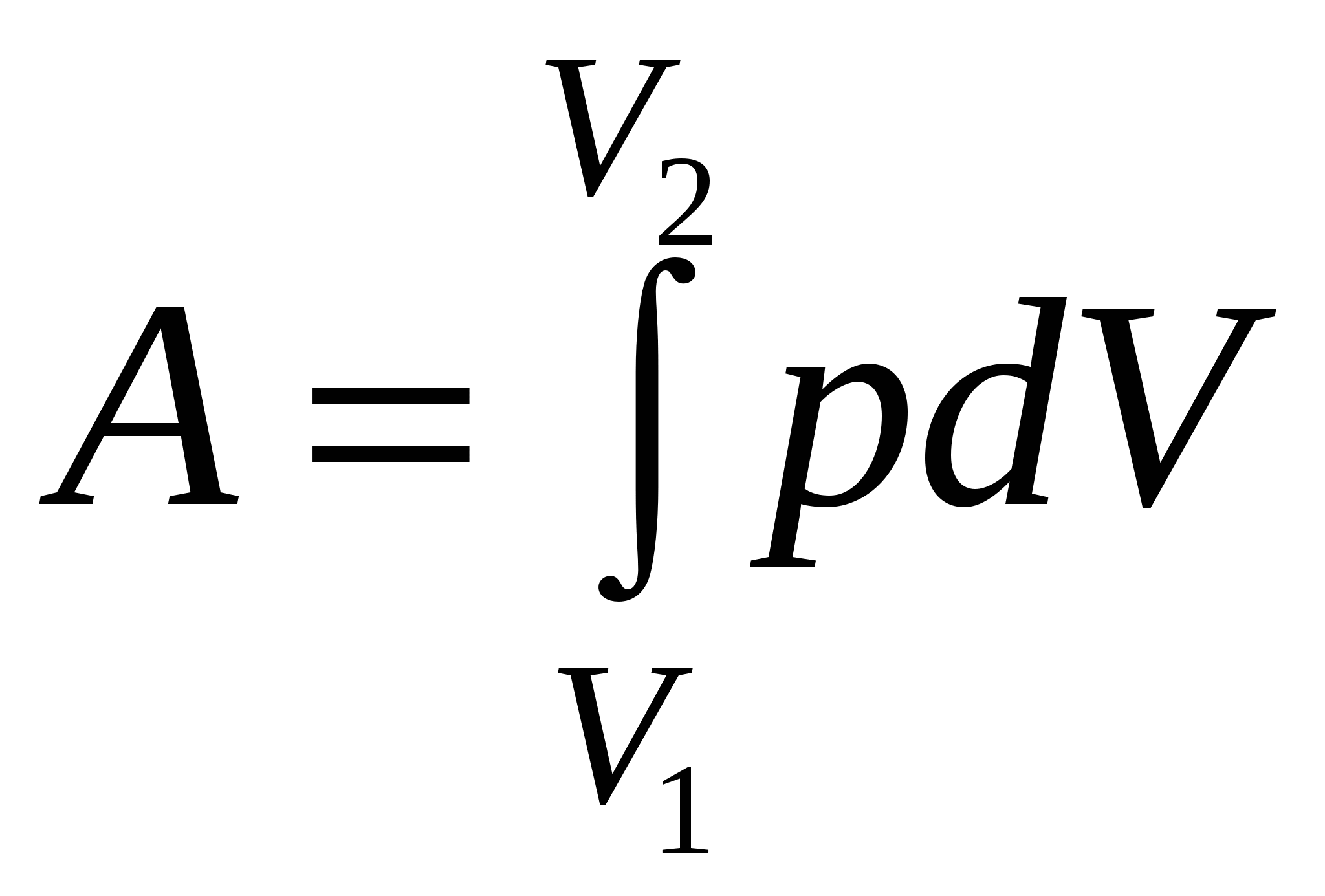
где – V1 начальный объём газа; V2- его конечныё объём.
Работа газа;
а) при изобарном процессе (p=const)
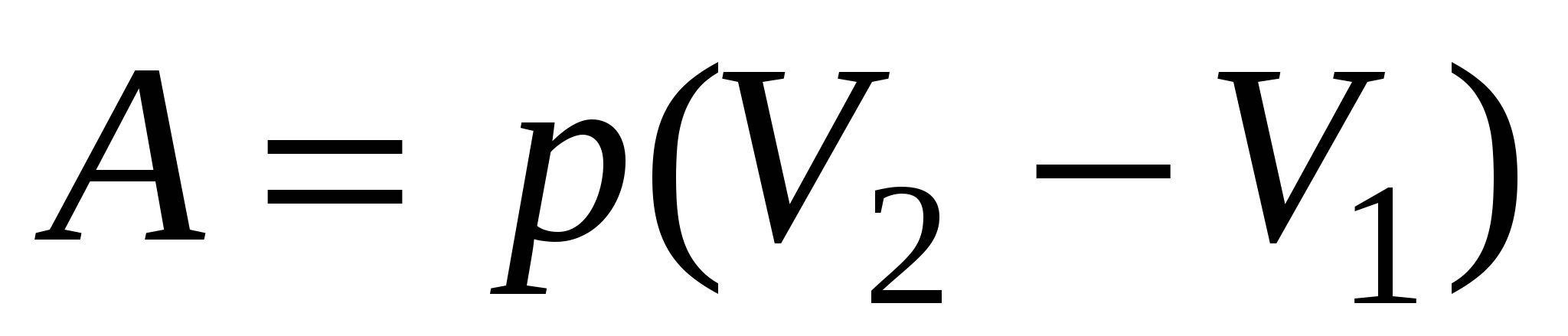
б) при изотермическом процессе (T=const)
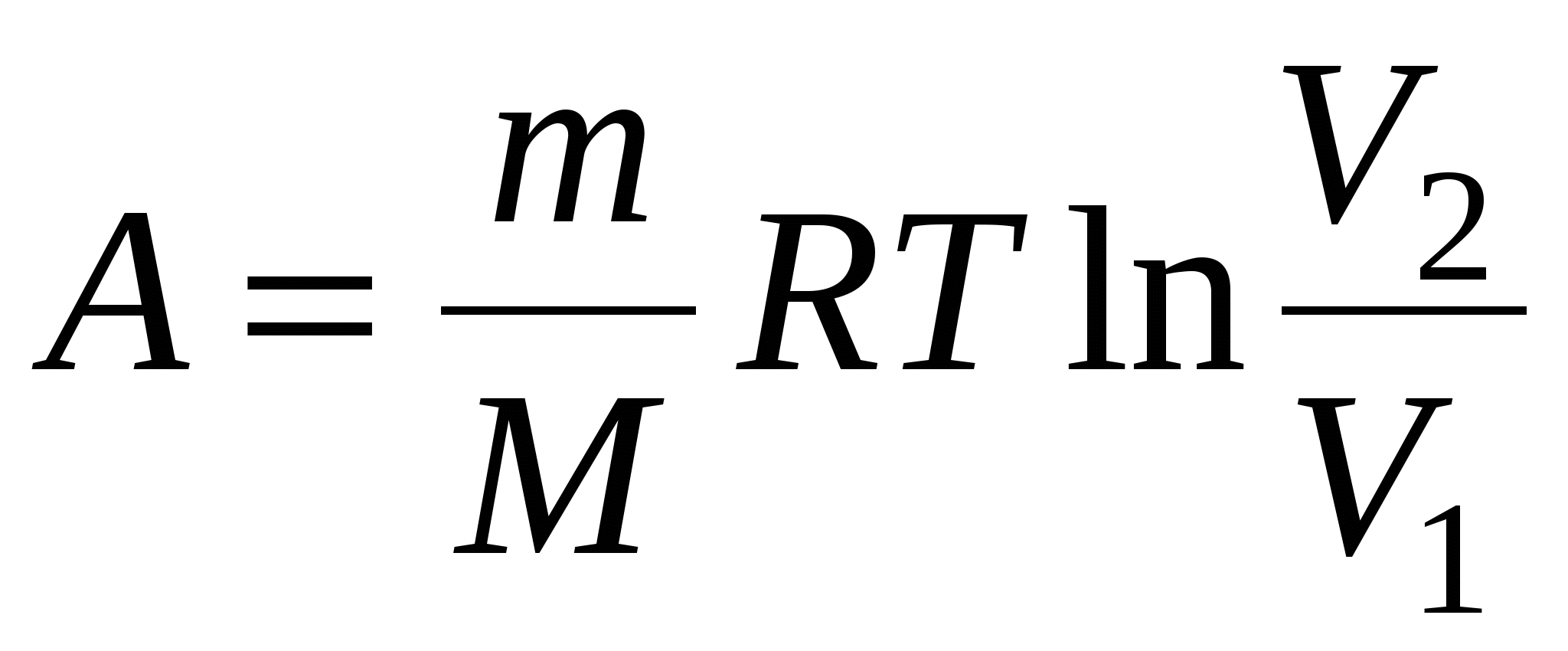
в) при адиабатном процессе
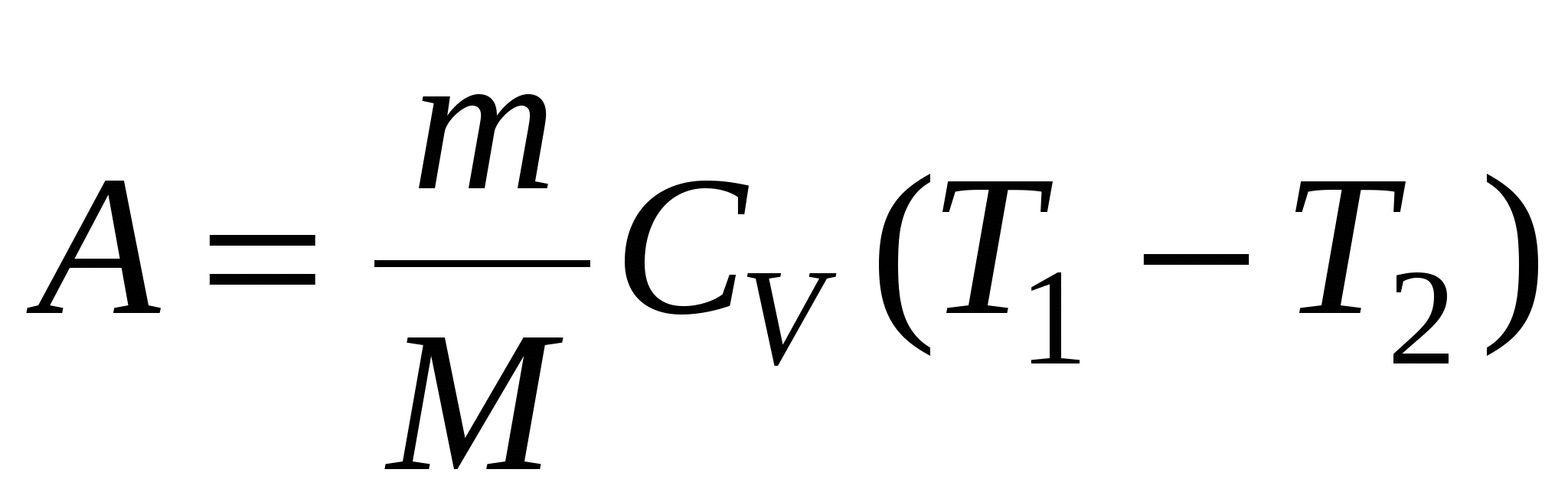
где T1 –начальная температура газа; T2 –ого конечная температура.
Уравнение Пуассона (уравнение газового состояния при адиабатном процессе)
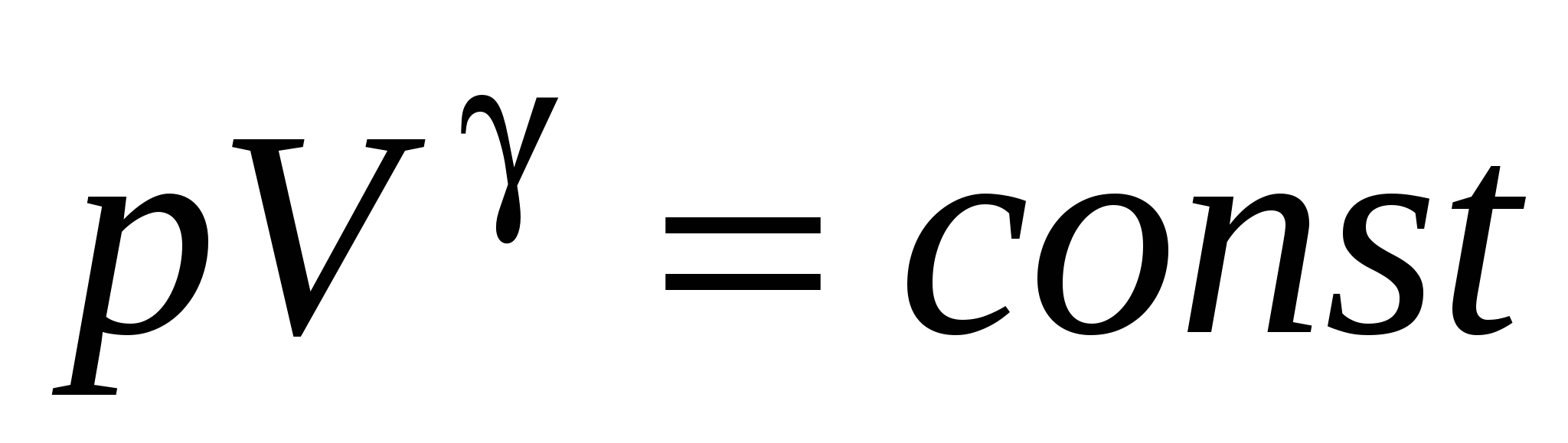
Связь между начальным и конечным значениями параметров состояния газа при адиабатном процессе:
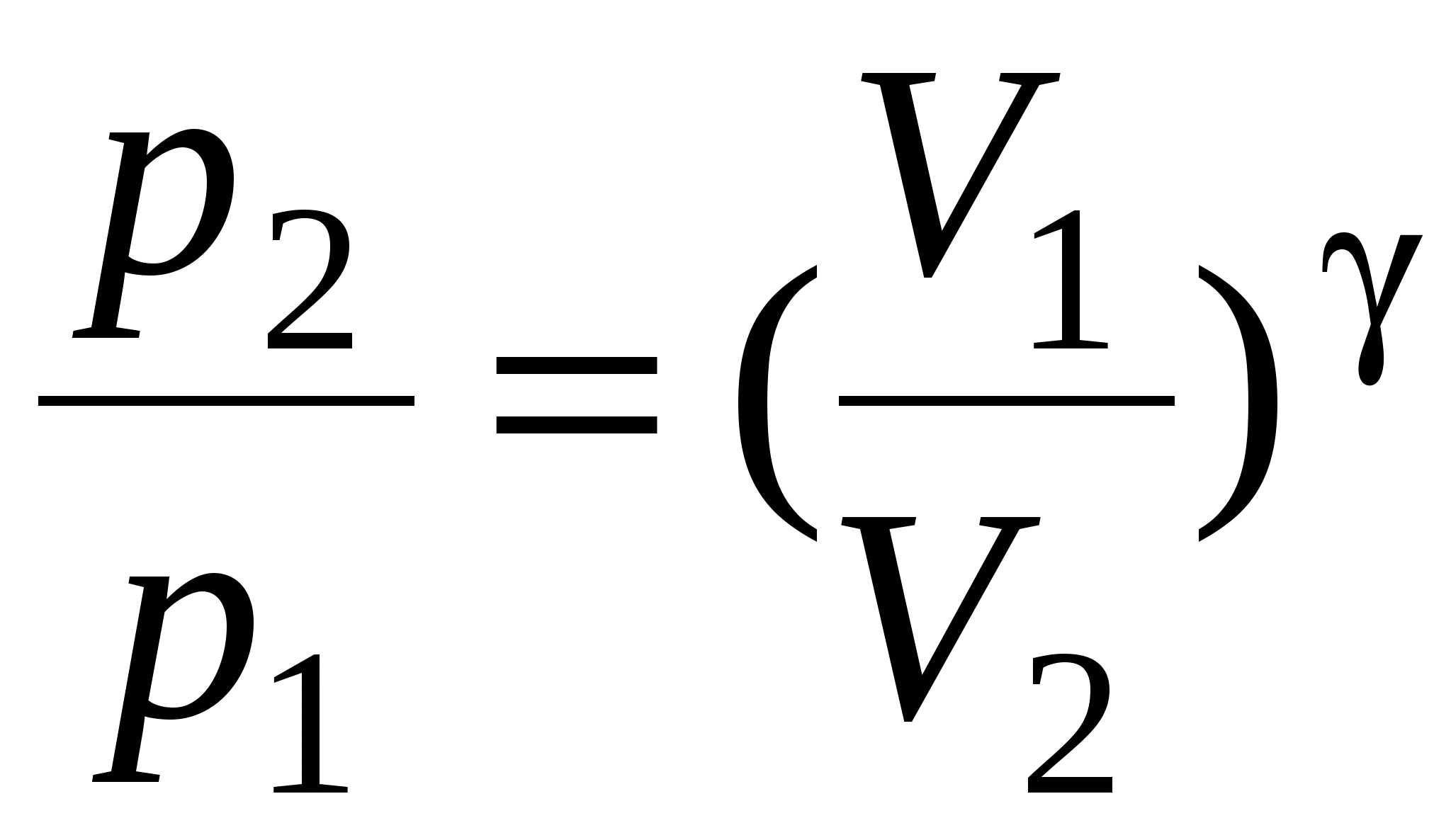 ; ; 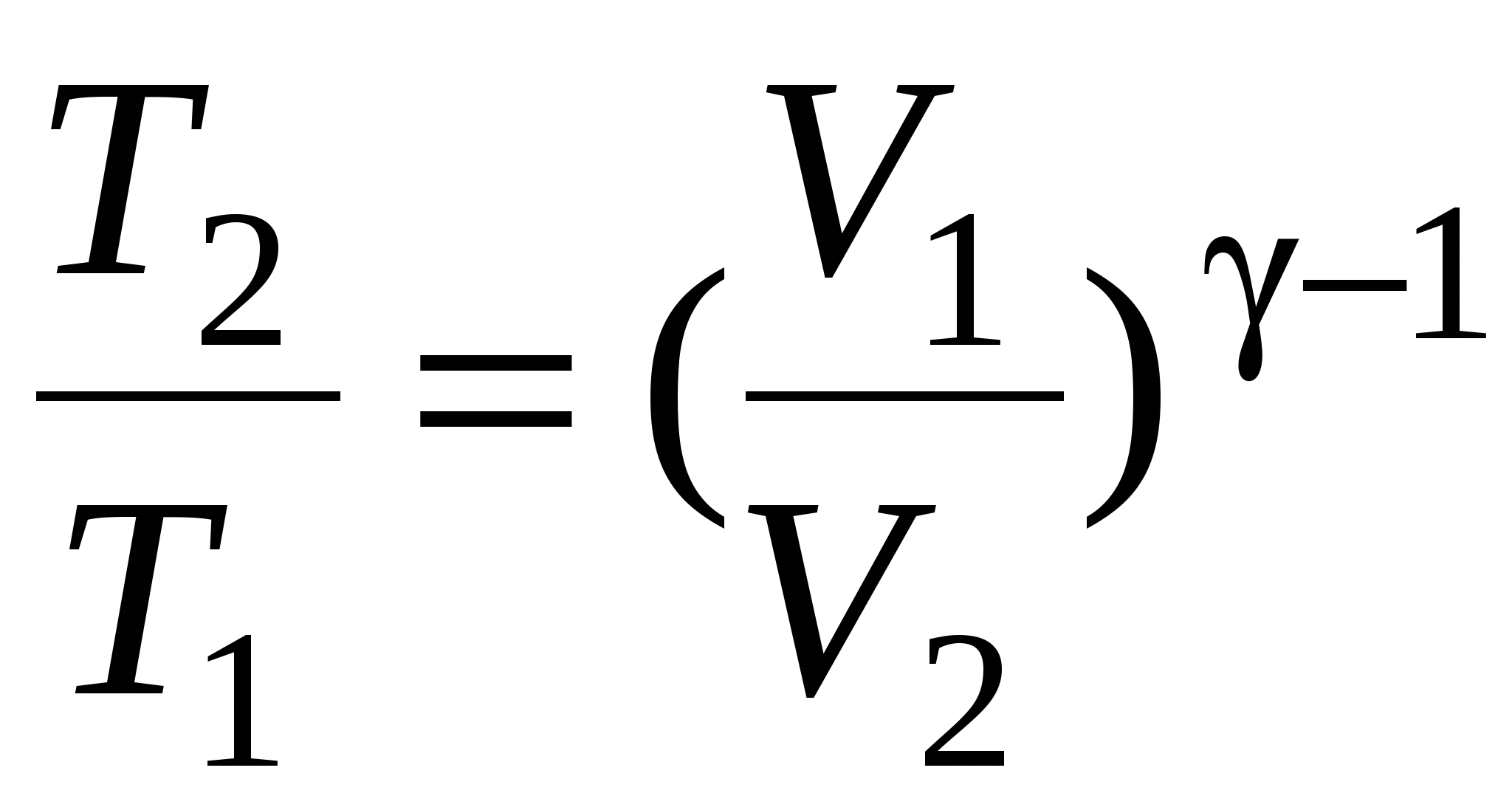 ; ; 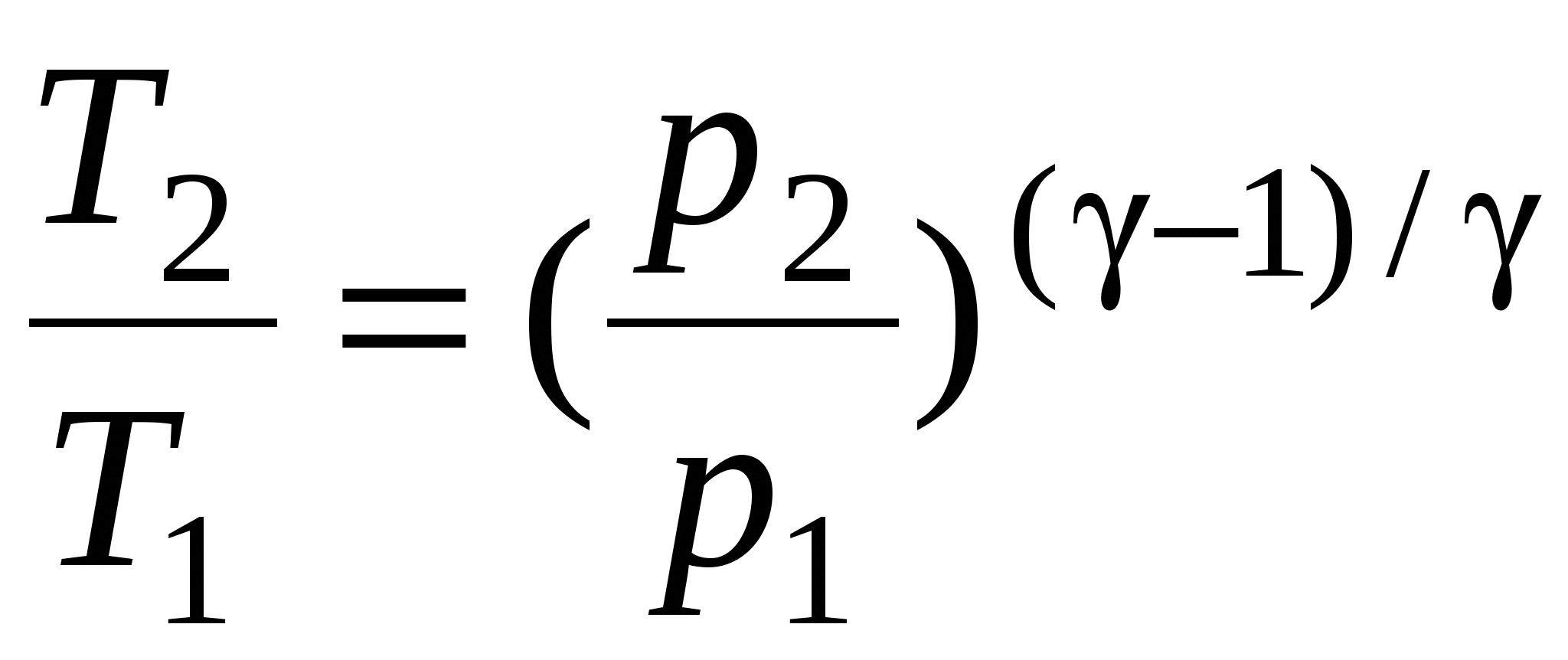
Первое начало термодинамики в общем случае записывается в виде
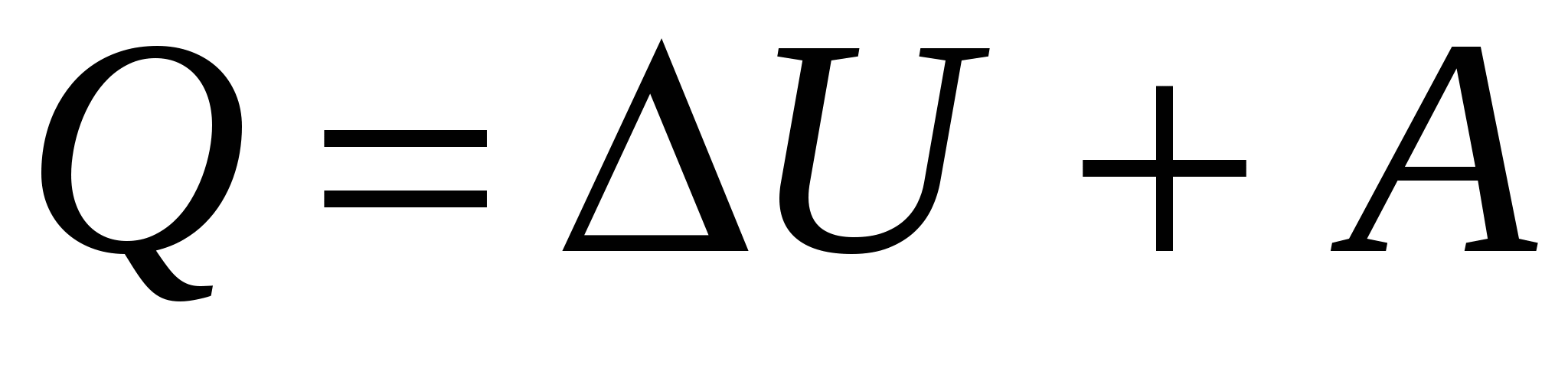
где Q-количество теплоты, сообщение газу; ∆U-изменение его внутренней энергии; A-работа, совершаемая газом против внешних сил.
Первое начало термодинамики:
а) при изобарном процессе
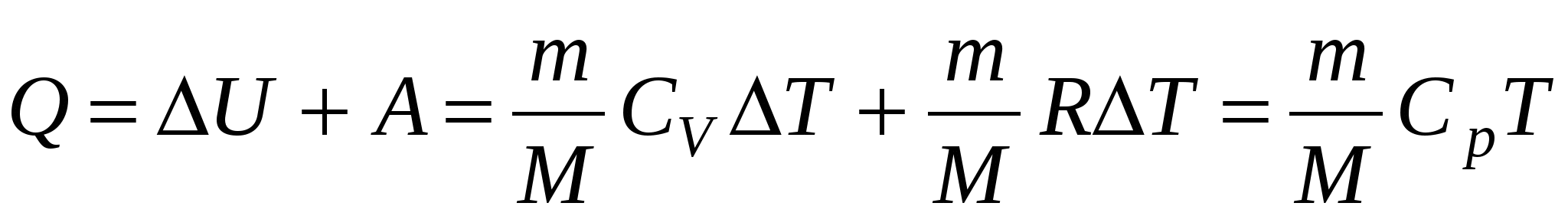
б) при изохорном процессе (A=0)
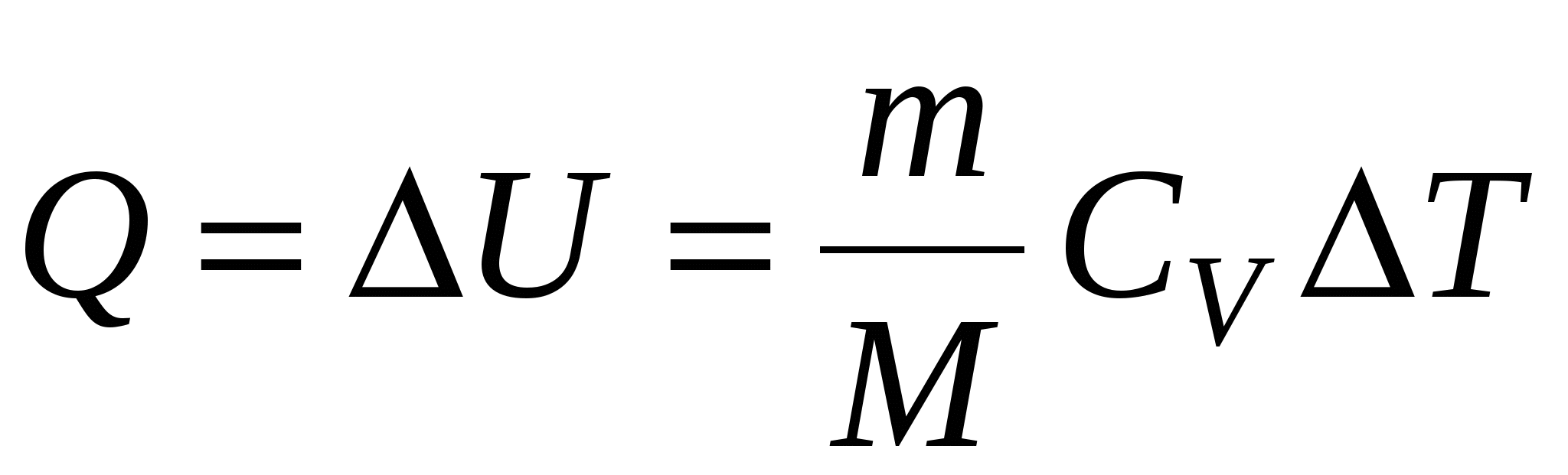
в) при изотермическом процессе (∆U=0)
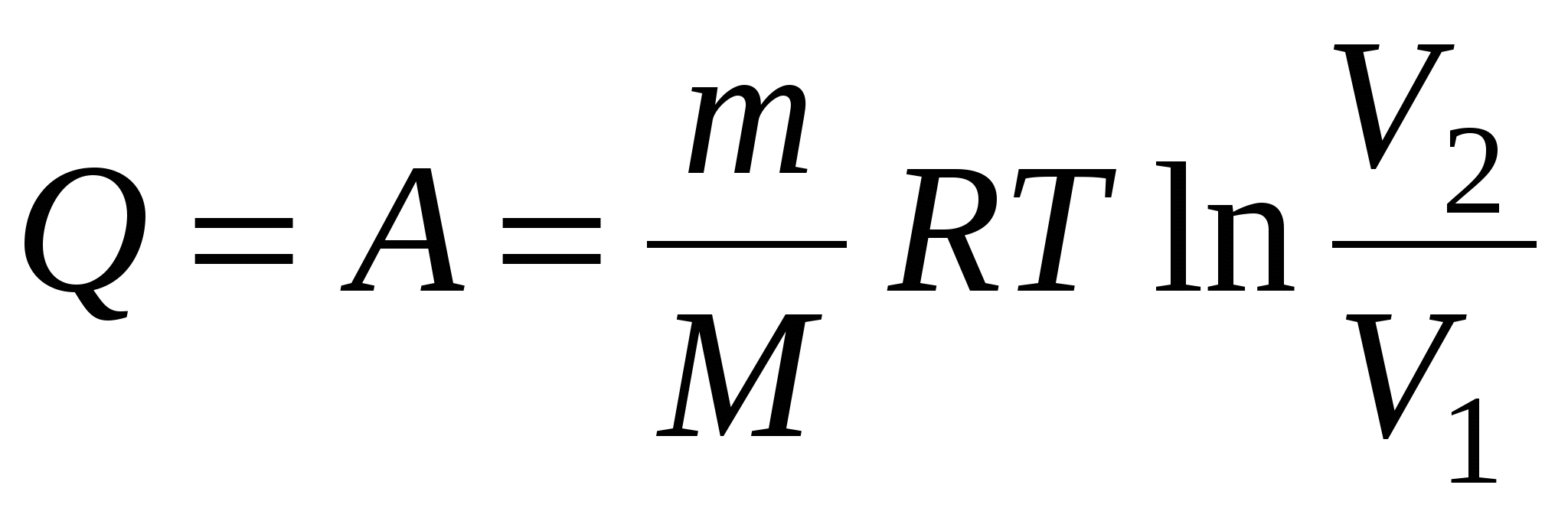
г) при адиабатном процессе (Q=0)
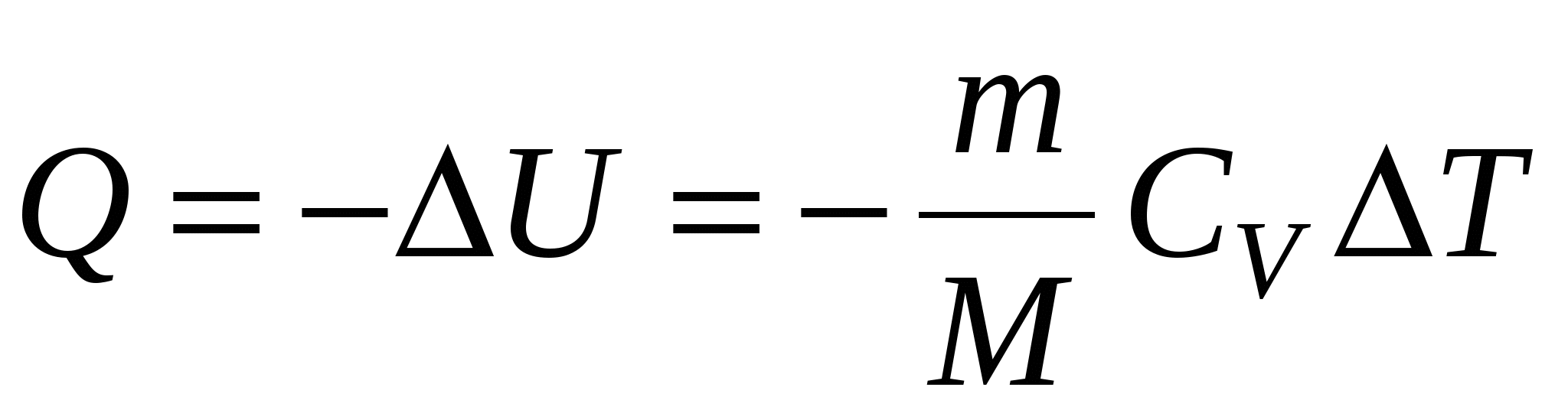
Термический коэффициент полезного действия (КПД) цикла в общем случае
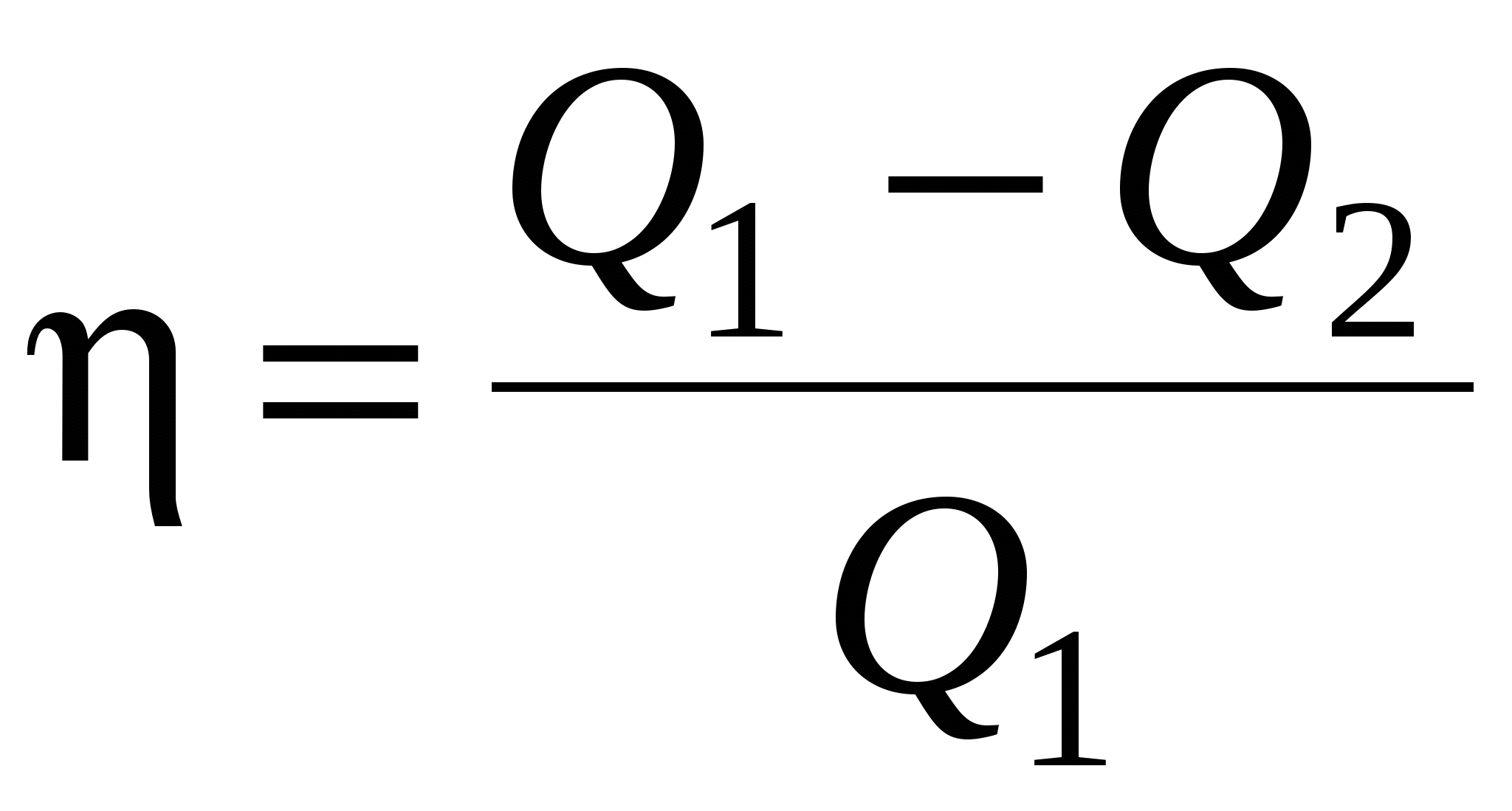
где Q1 – количество теплоты, полученное рабочим телом (газом) от нагревателя; Q2 – количество теплоты, переданное рабочим телом охладителю.
КПД цикла Карно
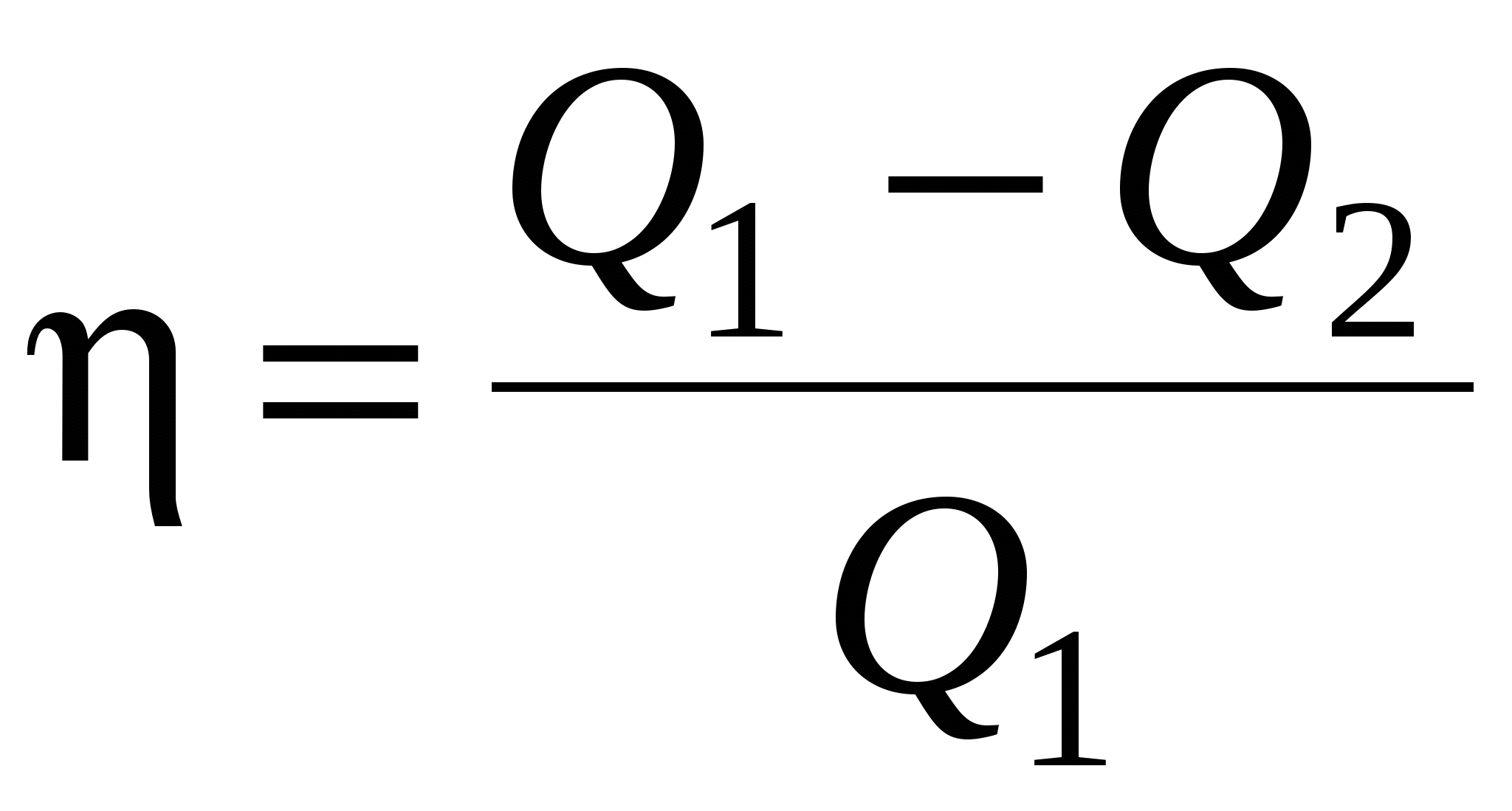 , или , или 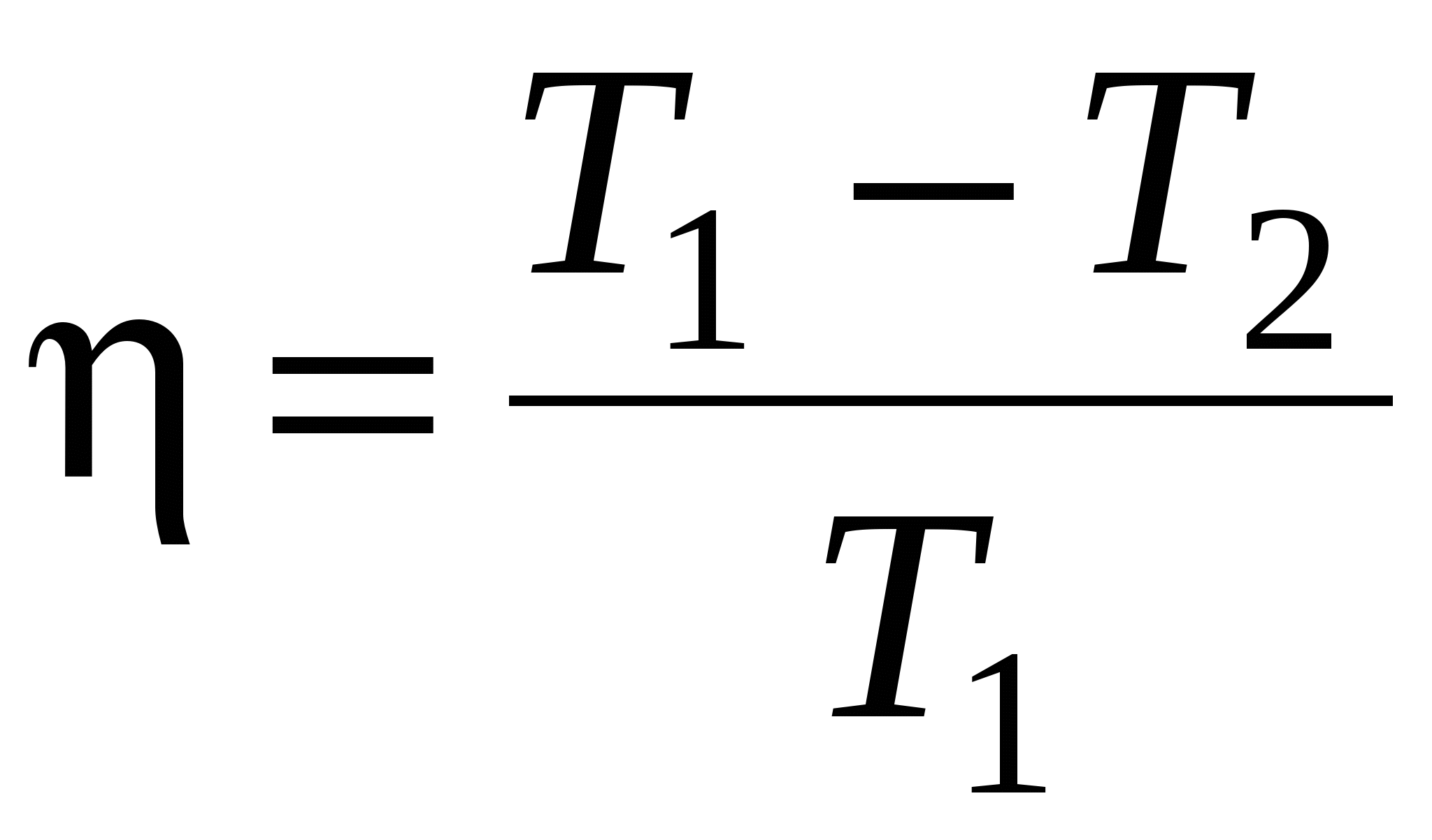
где T1 – температура нагревателя; T1 – температура охладителя.
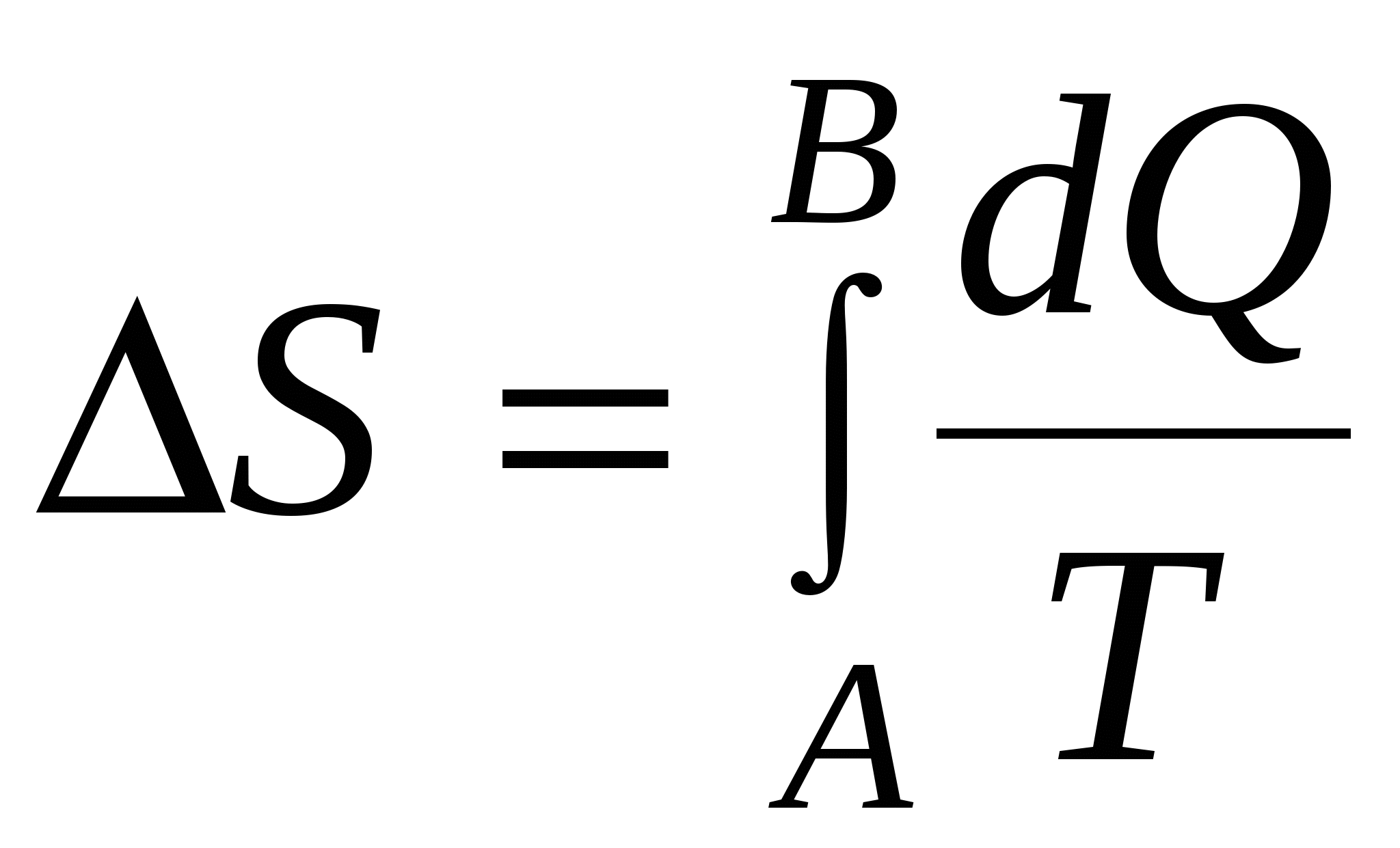 , ,
где А и В – пределы интегрирования, соответствующие начальному и конечному состоянию системы. Так как процесс равновесный, то интегрирование проводится по любому пути.
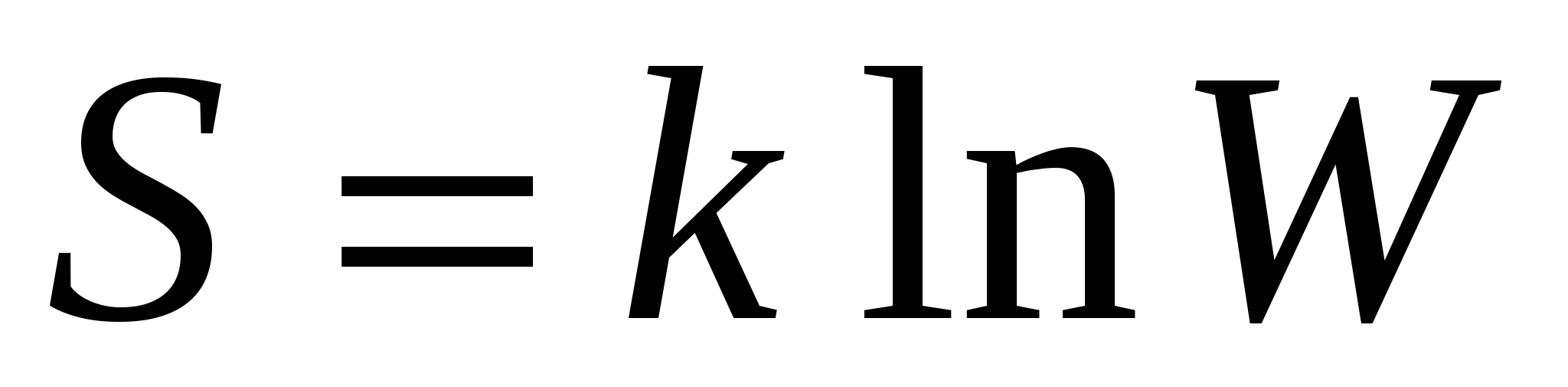 , ,
где S – энтропия системы; W – термодинамическая вероятность её состояния; k – постоянная Больцмана.
Азот массой m = 10 г находится при температуре Т = 290 К. Определить: 1) среднюю кинетическую энергию одной молекулы азота; 2) среднюю кинетическую энергию вращательного движения всех молекул азота. Газ считать идеальным. Ответ: 1) 10-20 Дж; 2) 860 Дж.
Кислород массой m = 1 кг находится при температуре Т = 320 К. Определить: 1) внутреннюю энергию молекул кислорода; 2) среднюю кинетическую энергию вращательного движения молекул кислорода. Газ считать идеальным. Ответ: 1) 208 кДж; 2) 83,1 кДж.
В закрытом сосуде находится смесь азота массой m1 = 56 г и кислорода массой m2 = 64 г. Определить изменение внутренней энергии этой смеси, если ее охладили на 20°. Ответ: 1,66 кДж.
Считая азот идеальным газом, определить его удельную теплоемкость: 1) для изобарного процесса; 2) для изохорного процесса. Ответ: 1) cV = 742 Дж/(кг.К); 2) cр = 1,04 кДж/(кг.К).
Определить удельные теплоемкости cV и cр, если известно, что некоторый газ при нормальных условиях имеет удельный объем V= 0,7 м3/кг. Что это за газ? Ответ: cV = 649 Дж/(кг·К), ср = 909 Дж/(кг·К).
Определить удельные теплоемкости cv и ср смеси углекислого газа массой m1 = 3 г и азота массой m2 = 4 г. Ответ: cV = 667 Дж/(кг.К), сp = 918 Дж/(кг.К).
Определить показатель адиабаты г для смеси газов, содержащей гелий массой m1 = 8 г и водород массой m2 = 2 г Ответ: 1,55.
Применяя первое начало термодинамики и уравнение состояния идеального газа, показать, что разность удельных теплоемкостей ср – cV= R/M.
Кислород массой 32 г находится в закрытом сосуде под давлением 0,1 МПа при температуре 290 К. После нагревания давление в сосуде повысилось в 4 раза. Определить: 1) объем сосуда; 2) температуру, до которой газ нагрели; 3) количество теплоты, сообщенное газу. Ответ: 1) 2,4.10-2 м3; 2) 1,16 кК; 3) 18,1 кДж.
Определить количество теплоты, собщенное газу, если в процессе изохорного нагревания кислорода объемом V = 20 л его давление изменилось на ΔP = 100 кПа. Ответ: 5 кДж.
Двухатомный идеальный газ (ν = 2 моль) нагревают при постоянном объеме до температуры T1 = 289 К. Определить количество теплоты, которое необходимо сообщить газу, чтобы увеличить его давление в n = 3 раза. Ответ: 24 кДж.
При изобарном нагревании некоторого идеального газа (ν = 2 моль) на ΔT = 90 К ему было сообщено количество теплоты 2,1 кДж. Определить: 1) работу, совершаемую газом; 2) изменение внутренней энергии газа; 3) величину γ = Cp/ CV. Ответ: 1) 1,5кДж; 2) 0,6 кДж; 3) 1,4.
Азот массой m = 280 г расширяется в результате изобарного процесса при давлении P = 1 МПа. Определить: 1) работу расширения; 2) конечный объем газа, если на расширение затрачена теплота Q = 5 кДж, а начальная температура азота T1 = 290 К. Ответ: А = 1,43 кДж; V2= 0,026 м3.
Кислород объемом 1 л находится под давлением 1 МПа. Определить, какое количество теплоты необходимо сообщить газу, чтобы: 1) увеличить его объем вдвое в результате изобарного процесса; 2) увеличить его давление вдвое в результате изохорного процесса. Ответ: 1) 3,5 кДж; 2) 2,5 кДж.
Некоторый газ массой m = 5 г расширяется изотермически от объема V1 до объема V2 = 2V1. Работа расширения А = 1 кДж. Определить среднюю квадратичную скорость молекул газа. Ответ: 930 м/с.
Азот массой m = 14 г сжимают изотермически при температуре Т = 300 К от давления P1 = 100 кПа до давления P2 = 500 кПа. Определить: 1) изменение внутренней энергии газа; 2) работу сжатия; 3) количество выделившейся теплоты. Ответ: 1) 0; 2) –2,01 кДж; 3) 2,01 кДж.
Некоторый газ массой 1 кг находится при температуре Т = 300 К и под давлением P1 = 0,5 МПа. В результате изотермического сжатия давление газа увеличилось в два раза. Работа, затраченная на сжатие, А = –432 кДж. Определить: 1) какой это газ; 2) первоначальный удельный объем газа. Ответ: 2) 1,25 м3/кг.
Азот массой m = 50 г находится при температуре T1= 280 К. В результате изохорного охлаждения его давление уменьшилось в n= 2 раза, а затем в результате изобарного расширения температура газа в конечном состоянии стала равной первоначальной. Определить: 1) работу, совершенную газом; 2) изменение внутренней энергии газа. Ответ: 1) 2,08 кДж; 2) 0.
Работа расширения некоторого двухатомного идеального газа составляет А = 2 кДж. Определить количество подведенной к газу теплоты, если процесс протекал: 1) изотермически; 2) изобарно. Ответ: 1) 3 кДж; 2) 7 кДж.
При адиабатическом расширении кислорода (ν = 2 моль), находящегося при нормальных условиях, его объем увеличился в n = 3 раза. Определить: 1) изменение внутренней энергии газа; 2) работу расширения газа. Ответ: 1) –4,03 кДж; 2) 4,03 кДж.
Азот массой m = 1 кг занимает при температуре T1 = 300 К объем V1 = 0,5 м3. В результате адиабатического сжатия давление газа увеличилось в 3 раза. Определить: 1) конечный объем газа; 2) его конечную температуру; 3) изменение внутренней энергии газа. Ответ: 1) 0,228 м3; 2) 411 К; 3) 82,4 кДж.
Азот, находившийся при температуре 400 К, подвергли адиабатическому расширению, в результате которого его объем увеличился в n = 5 раз, а внутренняя энергия уменьшилась на 4 кДж. Определить массу азота. Ответ: 28 г.
Двухатомный идеальный газ занимает объем V1 = 1 л и находится под давлением P1 = 0,1 МПа. После адиабатического сжатия газ характеризуется объемом V2 и давлением P2. В результате последующего изохор-ного процесса газ охлаждается до первоначальной температуры, а его давление P3 = 0,2 МПа. Определить: 1) объем V2; 2) давление P2. Начертить график этих процессов. Ответ: 1) 0,5л; 2) 264 кПа.
Кислород, занимающий при давлении P1 = 1 МПа объем V1= 5 л, расширяется в n = 3 раза. Определить конечное давление и работу, совершенную газом. Рассмотреть следующие процессы: 1) изобарный; 2) изотермический; 3) адиабатический. Ответ: 1) 1 МПа, 10 кДж; 2) 0,33 МПа, 5,5 кДж; 3) 0,21 МПа, 4,63 кДж.
Рабочее тело – идеальный газ – теплового двигателя совершает цикл, состоящий из последующих процессов: изобарного, адиабатического и изотермического.
В результате изобарного процесса газ нагревается от T1 = 300 К до Т2 = 600 К. Определить термический к.п.д. теплового двигателя. Ответ: 30,7 %.
Азот массой 500 г, находящийся под давлением P1 = 1 МПа при температуре T1= 127 °С, подвергли изотермическому расширению, в результате которого давление газа уменьшилось в n = 3 раза. После этого газ подвергли адиабатическому сжатию до начального давления, а затем он был изобарно сжат до начального объема. Построить график цикла и определить работу, совершенную газом за цикл. Ответ: –11,5 кДж.
Идеальный газ, совершающий цикл Карно, 70 % количества теплоты, полученной от нагревателя, отдает холодильнику. Количество теплоты, получаемое от нагревателя, равно 5 кДж. Определить: 1) термический к.п.д. цикла; 2) работу, совершенную при полном цикле. Ответ: 1) 30%; 2) 1,5 кДж.
Идеальный газ совершает цикл Карно. Газ получил от нагревателя количество теплоты 5,5 кДж и совершил работу 1,1 кДж. Определить: 1) термический к.п.д. цикла; 2) отношение температур нагревателя и холодильника. Ответ: 1) 20%; 2) 1,25.
Идеальный газ совершает цикл Карно, термический к.п.д. которого равен 0,4. Определить работу изотермического сжатия газа, если работа изотермического расширения составляет 400 Дж. Ответ: –240 Дж.
Идеальный газ совершает цикл Карно. Температура нагревателя Т1 = 500 К, холодильника Т2 = 300 К. Работа изотермического расширения газа составляет 2 кДж. Определить: 1) термический к.п.д. цикла; 2) количество теплоты, отданное газом при изотермическом сжатии холодильнику. Ответ: 1) 40 %; 2) 0,6 кДж.
Многоатомный идеальный газ совершает цикл Карно, при этом в процессе адиабатического расширения объем газа увеличивается в n = 4 раза. Определить термический к.п.д. цикла. Ответ: 37 %.
Во сколько раз необходимо увеличить объем V = 5 моль идеального газа при изотермическом расширении, если его энтропия увеличилась на 57,6 Дж/К? Ответ: 4.
При нагревании двухатомного идеального газа (ν = 3 моль) его термодинамическая температура увеличилась в n = 2 раза. Определить изменение энтропии, если нагревание происходит: 1) изохорно; 2) изобарно. Ответ: 1) 28,8 Дж/К; 2) 40,3 Дж/К.
Идеальный газ (ν = 2 моль) сначала изобарно нагрели, так что объем газа увеличился в n1 = 2 раза, а затем изохорно охладили, так что давление его уменьшилось в n = 2 раза. Определить приращение энтропии в ходе указанных процессов. Ответ: 11,5 Дж/К.
Азот массой 28 г адиабатически расширили в n = 2 раза, а затем изобарно сжали до первоначального объема. Определить изменение энтропии газа в ходе указанных процессов.
Ответ: –0,2 Дж/К.
8. Реальные газы, жидкости и твердые тела
Уравнение Ван-дер-Ваальса для одного моля газа
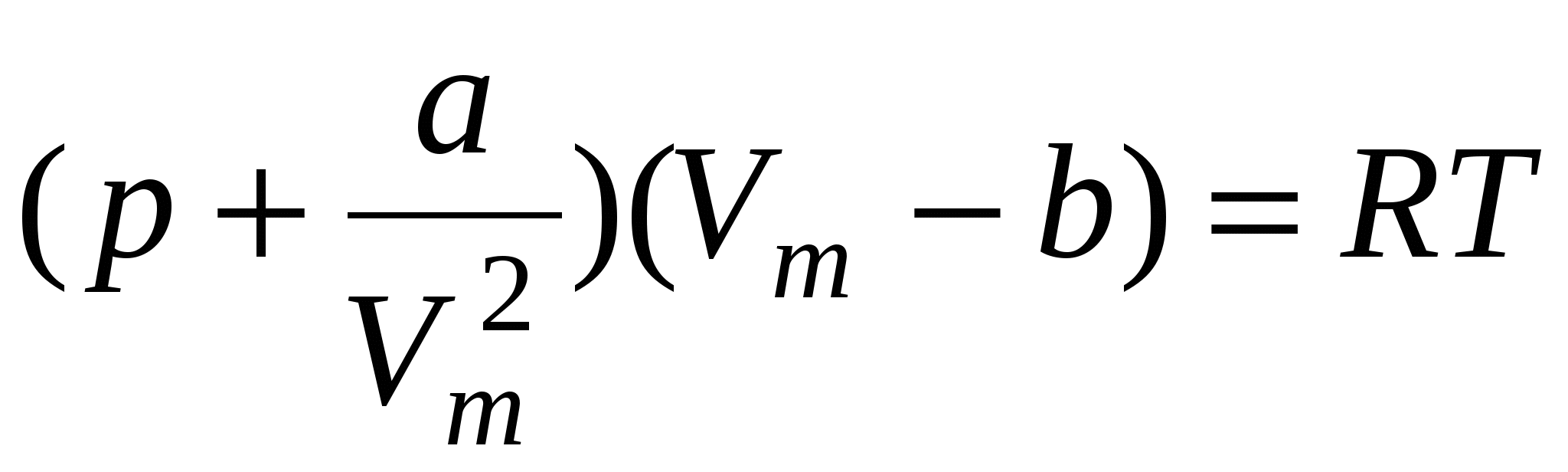 , ,
для произвольного количества вещества ν газа
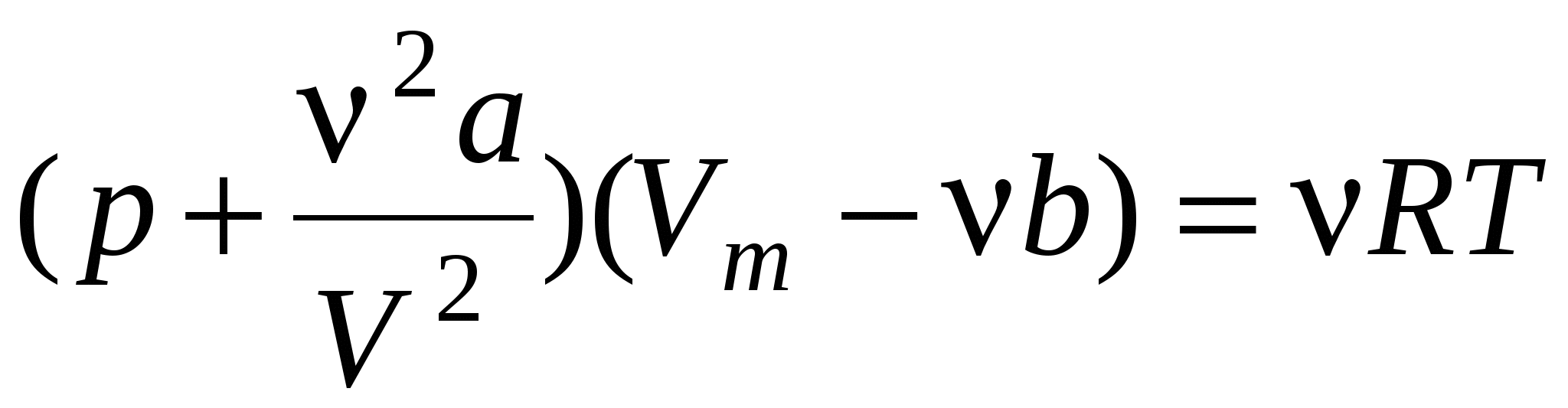 , ,
где а и b– постоянные Ван-дер-Ваальса (рассчитанные на один моль газа); V – объём, занимаемый газом; Vm – молярный объём;
p - давление газа на стенки сосуда.
Внутреннее давление, обусловленное силами взаимодействия молекул,
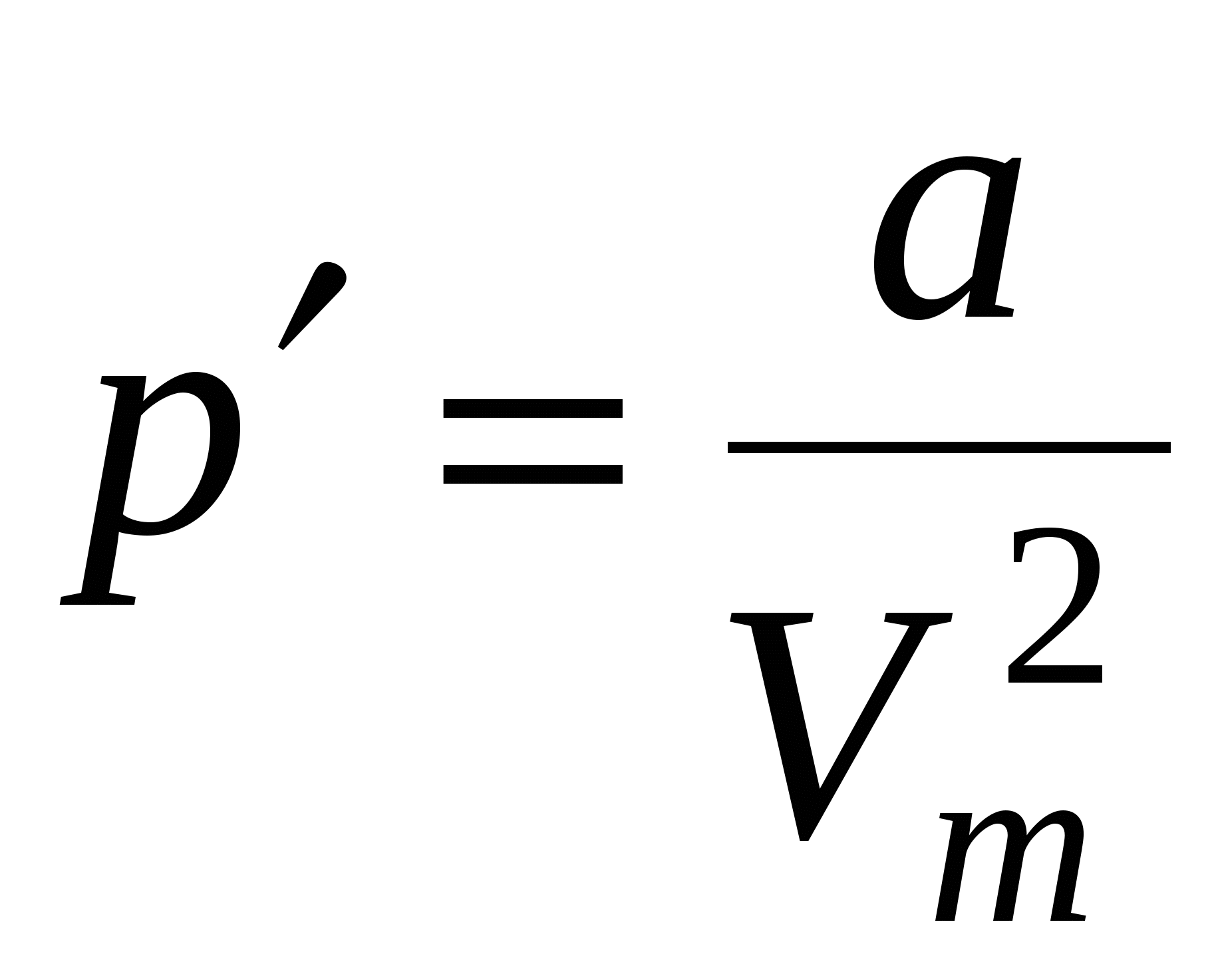 , или , или 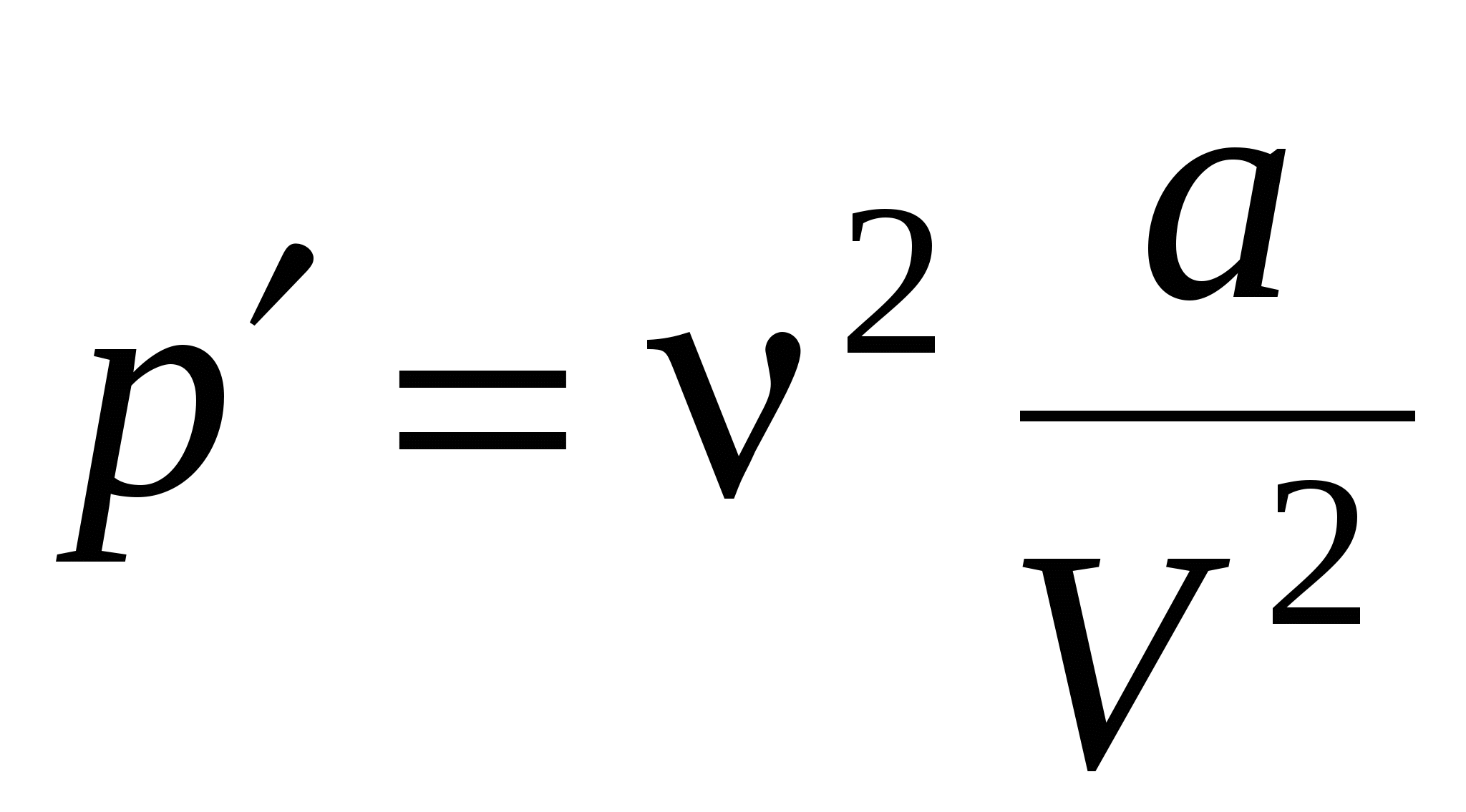 . .
Связь критических параметров – объёма, давления и температуры газа – с постоянными а и b Ван-дер-Ваальса:
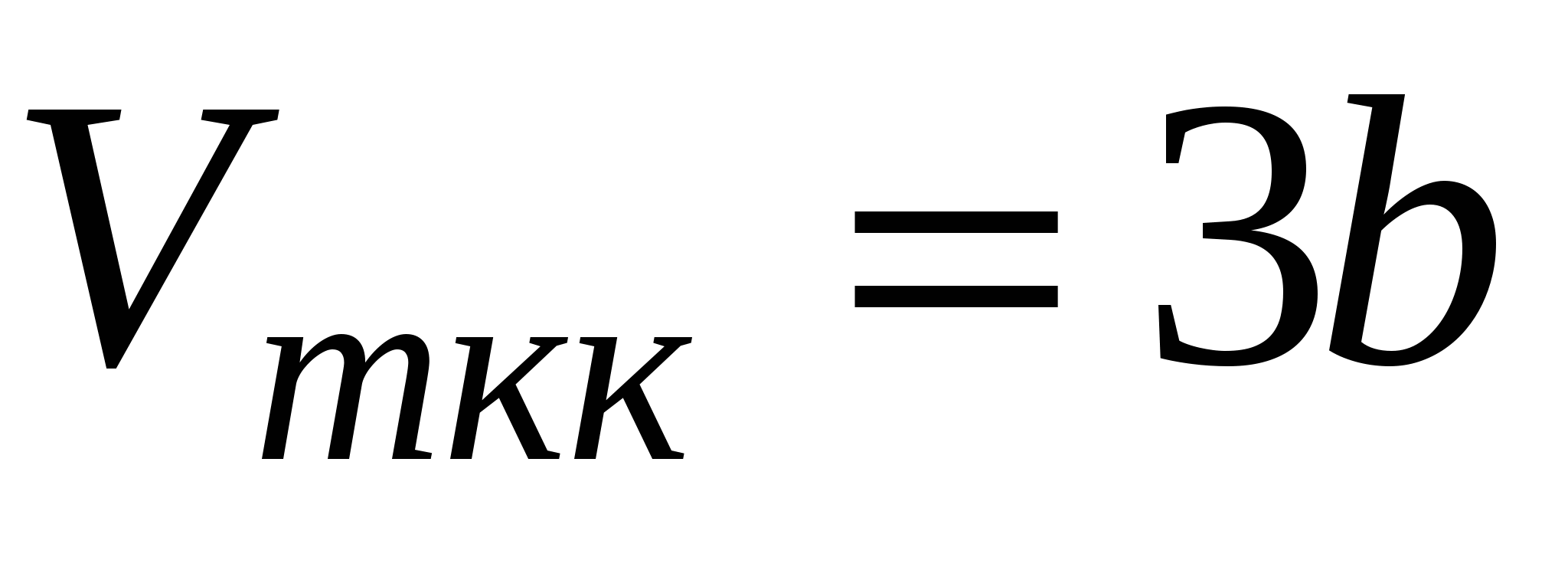 ; ; 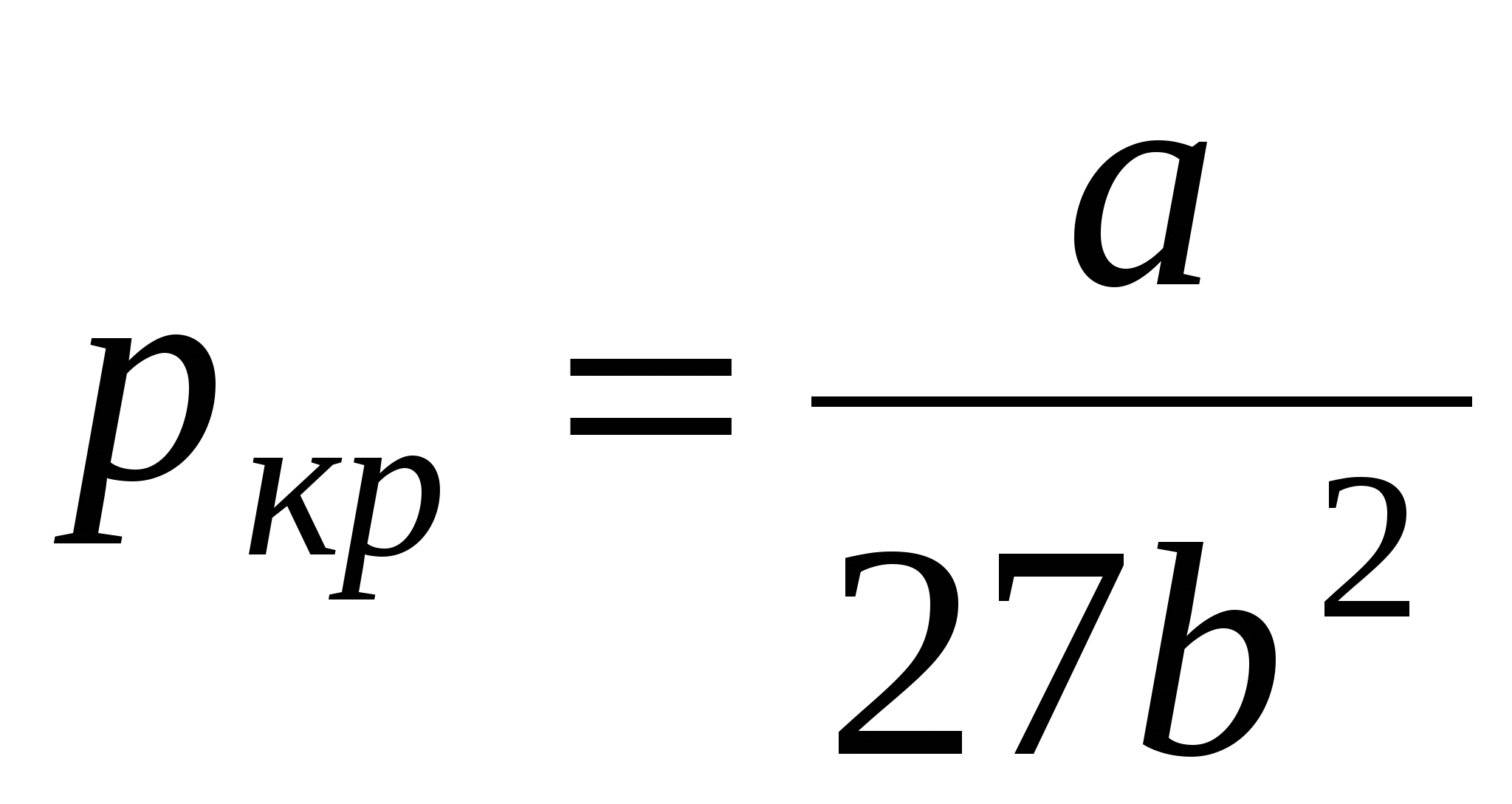 ; ; 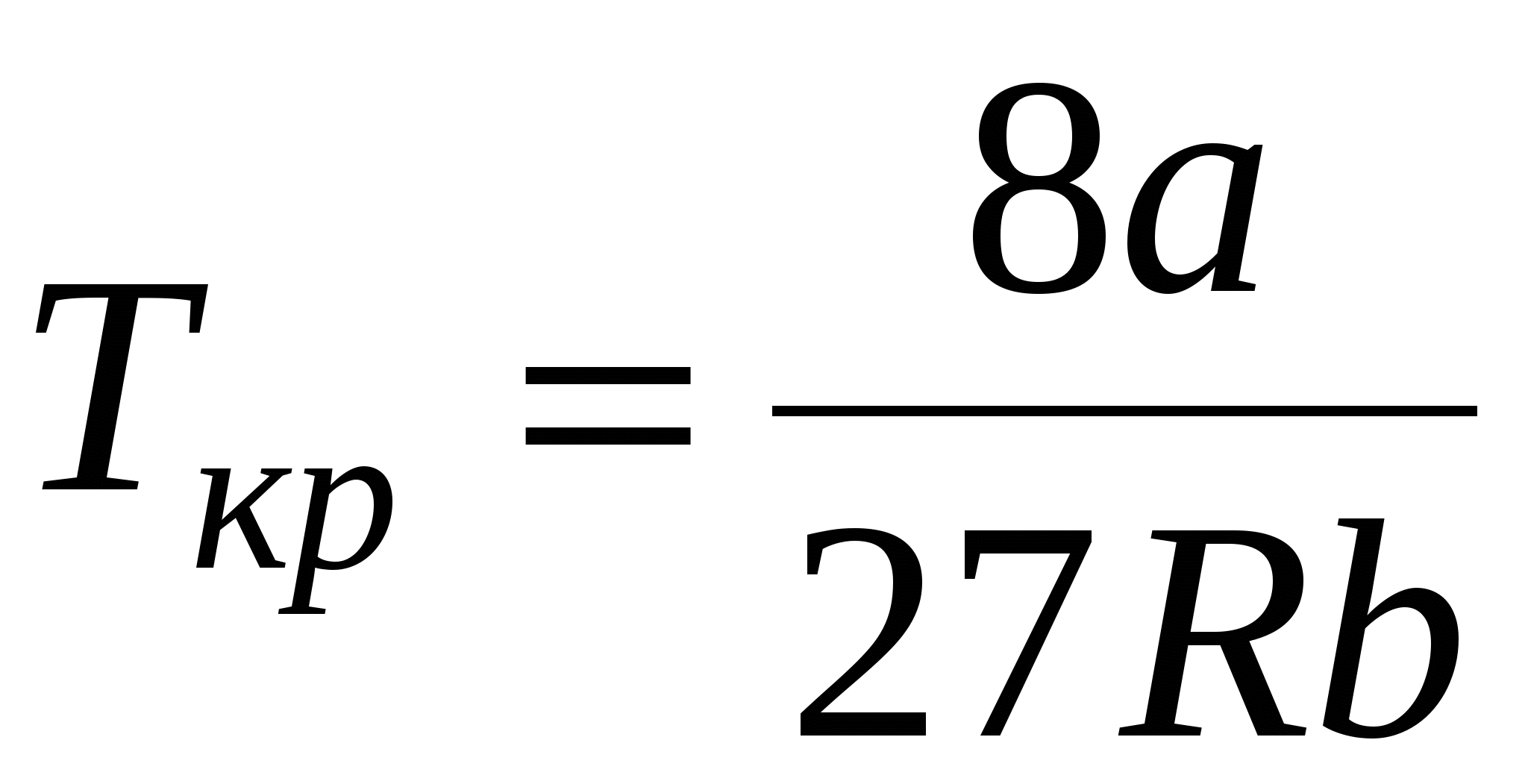
Внутренняя энергия реального газа
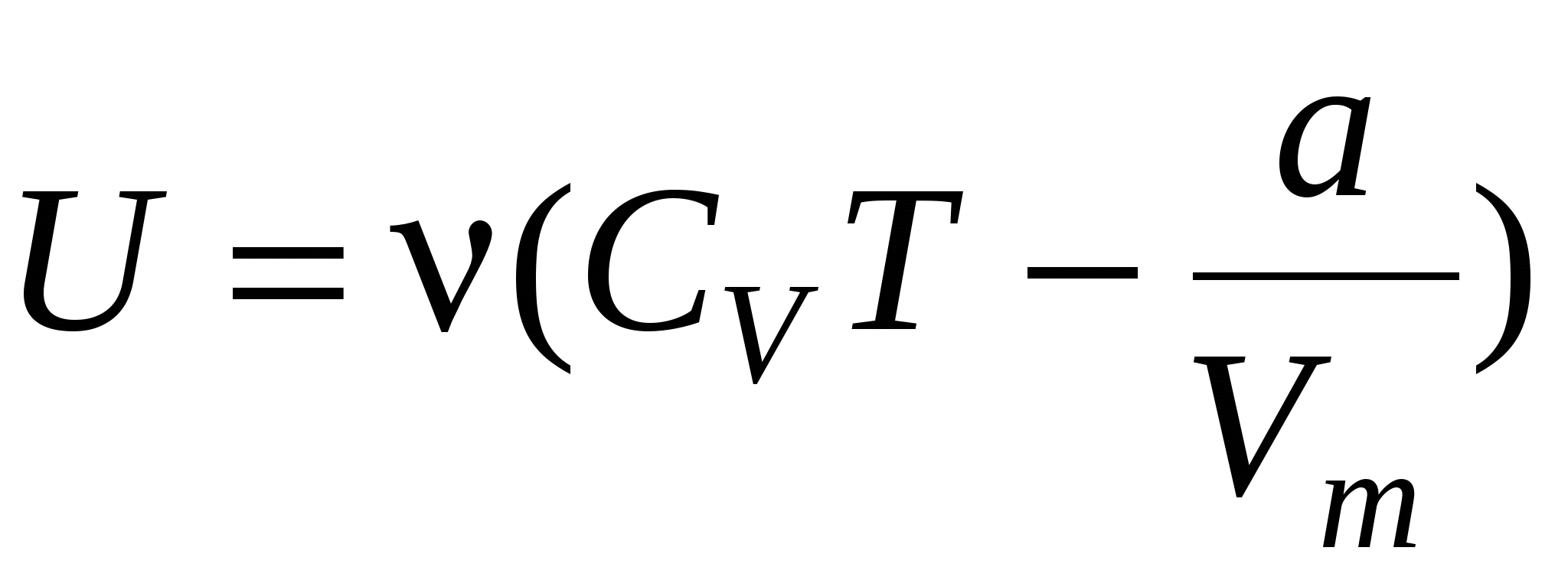
где СV –молярная теплоёмкость газа при постоянном объёме.
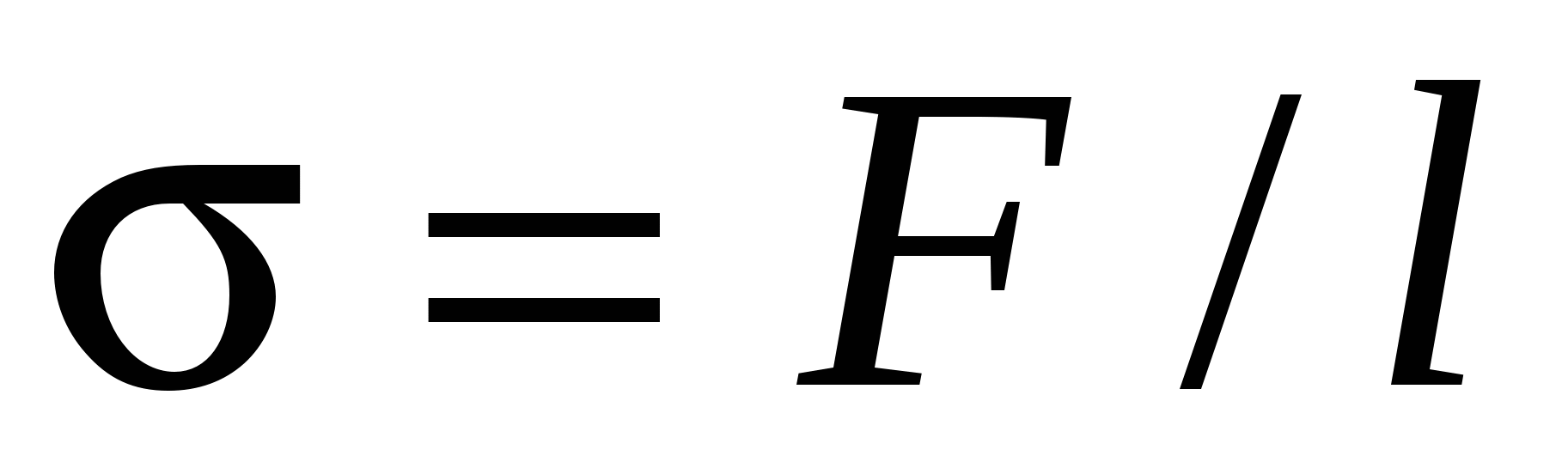
где F – сила поверхностного натяжения, действующая на контур l, ограничивающий поверхность жидкость, или
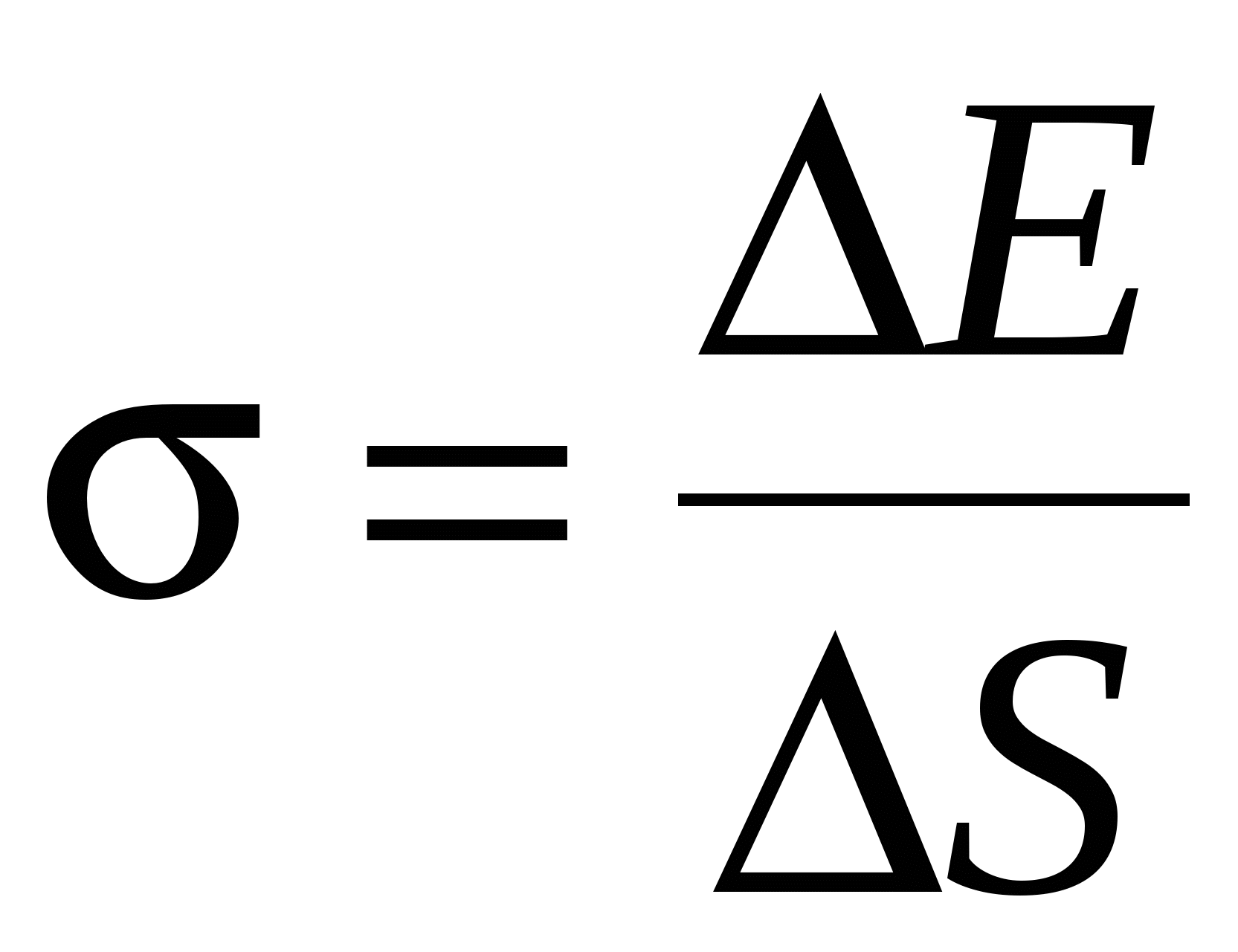 , ,
где ∆E – изменение свободной энергии поверхностной плёнки жидкости, связанное с изменением площади ∆S – поверхности этой плёнки.
Формула Лапласа в общем случае записывается в виде
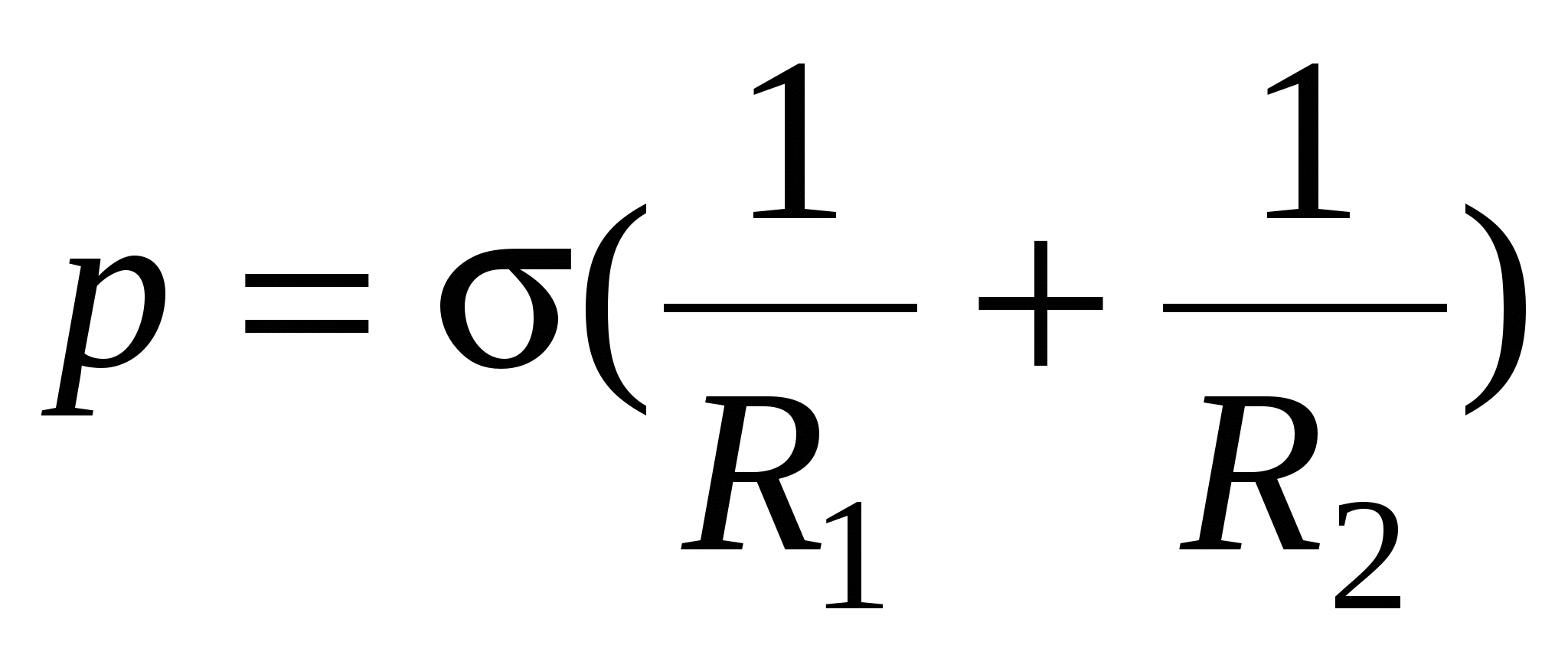
где p-давление, создаваемое изогнутой поверхностью жидкости; σ - поверхностное натяжение; R1 и R2 – радиусы кривизны двух взаимно перпендикулярных сечений жидкости, а в случае сферической поверхности
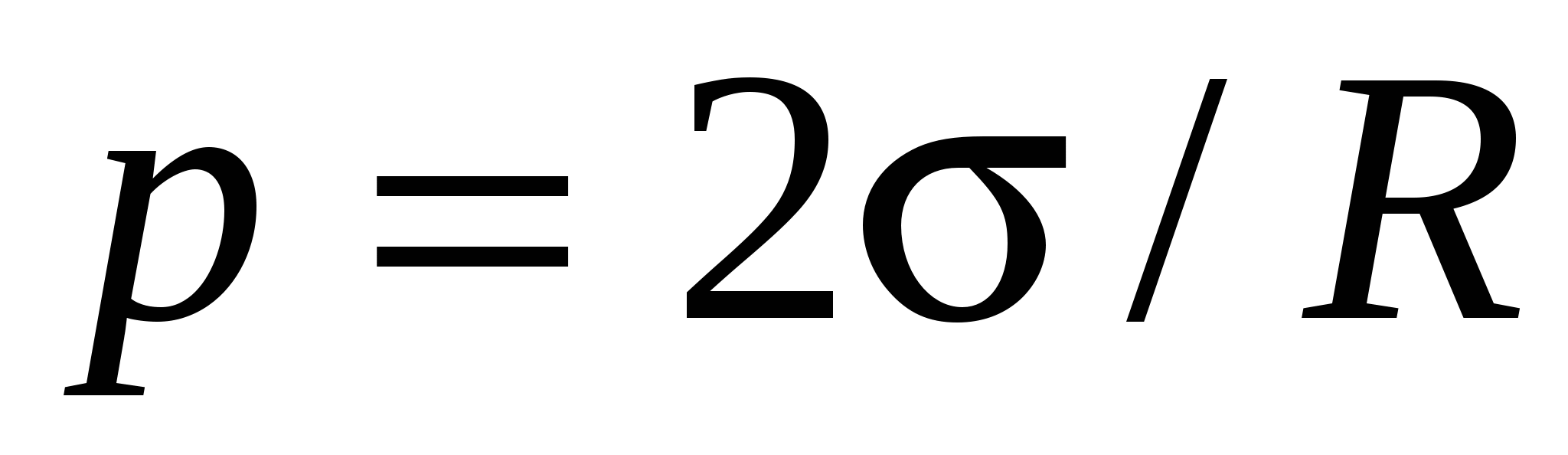
Высота подъёма жидкости в капилярной трубке
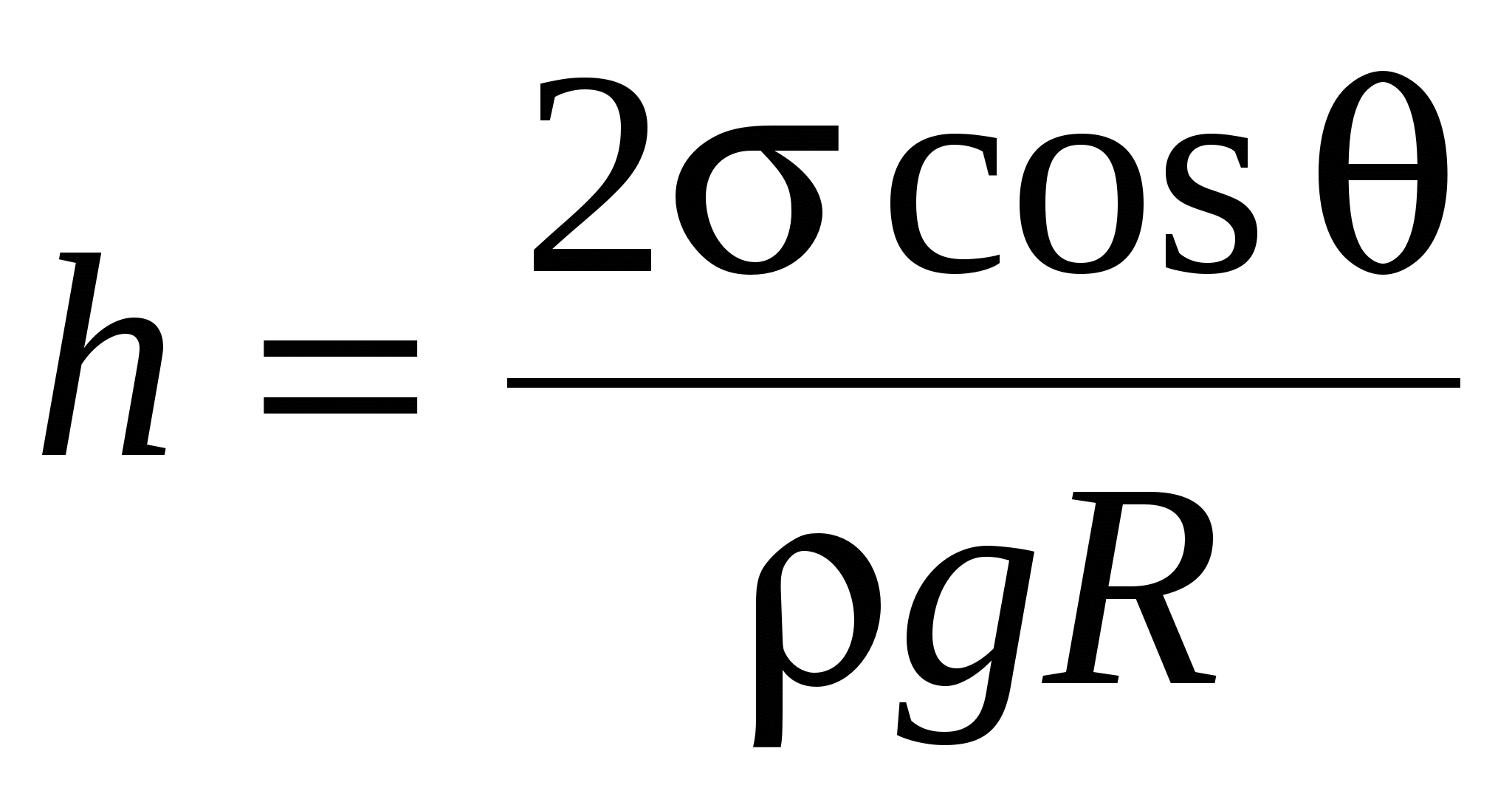
где θ – краевой угол; R-радиус канала трубки; ρ-плотность жидкости; g-ускорение свободного падения.
Высота подъёма жидкости между двумя близкими и параллельными плоскостями
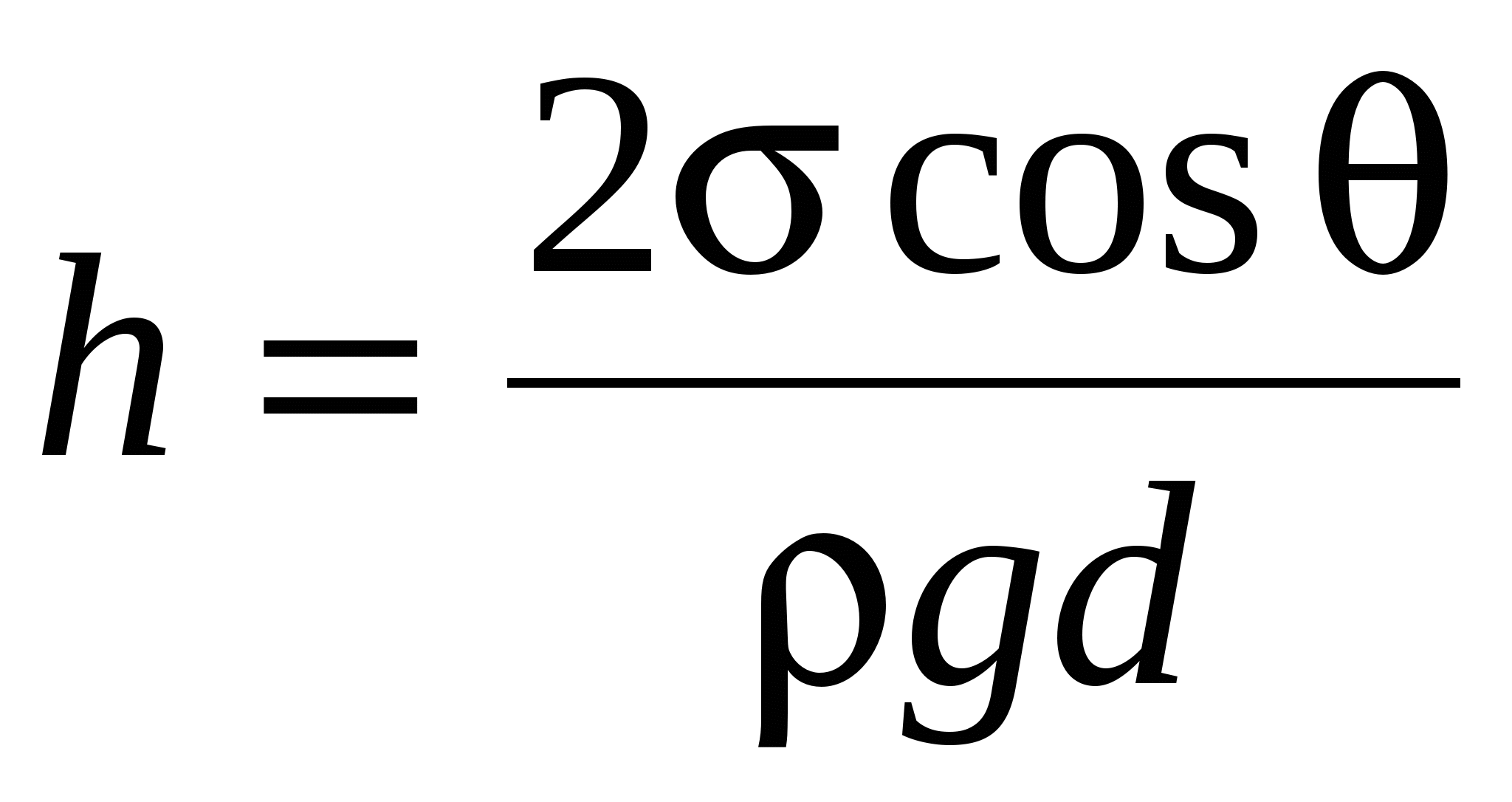 , ,
где d- расстояния между плоскостями.
CV = 3R,
где CV – молярная (атомная) теплоемкость химически простых твердых тел.
Кислород (ν = 10 моль) находится в сосуде объемом V = 5 л. Определить: 1) внутреннее давление газа; 2) собственный объем молекул Поправки а и b принять равными соответственно 0,136 Н.м4/моль2 и 3,17.10-5 м3/моль. Ответ: 1) 544 кПа; 2) 79,3 см3.
Углекислый газ массой 6,6 кг при давлении 0,1 МПа занимает объем 3,75 м3. Определить температуру газа, если: 1) газ реальный; 2) газ идеальный. Поправки a и b принять равными соответственно 0,361 Н.м4/моль2 и 4,28.10-5 м3/моль. Ответ: 1) 302 К; 2) 301 К.
Углекислый газ массой 2,2 кг находится при температуре 290 К в сосуде вместимостью 30 л. Определить давление газа, если: 1) газ реальный; 2) газ идеальный. Поправки a и b принять равными соответственно 0,361 Н.м4/моль2 и 4,28.10-5 м3/моль. Ответ: 1) 3,32 МПа; 2) 4,02 МПа.
Плотность азота ρ = 140 кг/м3, его давление P = 10 МПа. Определить температуру газа, если: 1) газ реальный; 2) газ идеальный. Поправки aиb принять равными соответственно 0,135 Н.м4/моль2 и 3,86.10-5 м3/моль. Ответ: 1) 260 К; 2) 241 К.
Азот (ν = 3 моль) расширяется в вакуум, в результате чего объем газа увеличивается от V1 = 1 л до V2 = 5 л. Какое количество теплоты Q необходимо сообщить газу, чтобы его температура осталась неизменной? Поправку a принять равной 0,135 Н.м4/моль2. Ответ: 972 Дж.
Углекислый газ массой 88 г занимает при температуре 290 К объем 1000 см3. Определить внутреннюю энергию газа, если: 1) газ идеальный; 2) газ реальный. Поправку а принять равной 0,361 Н.м4/моль2. Ответ: 1) 14,5 кДж; 2) 13 кДж.
Кислород (ν = 2 моль) занимает объем V1 = 1 л. Определить изменение температуры кислорода, если он адиабатически расширяется в вакууме до объема V2 = 10 л. Поправку a принять равной 0,136 Н.м4/моль2. Ответ: –11,8 К.
Азот (ν = 2 моль) адиабатически расширяется в вакуум. Температура газа при этом уменьшается на 1 К. Определить работу, совершаемую газом против межмолекулярных сил притяжения. Ответ: 83,1 Дж.
Кислород (ν = 1 моль) (реальный газ), занимавший при T1 = 400 К объем V1 = 1 л, расширяется изотермически до V2 = 2V1. Определить: 1) работу при расширении; 2) изменение внутренней энергии газа. Поправки a и b принять равными соответственно 0,136 Н·м4/моль2 и 3,17·10-5 м3/моль. Ответ: 1) 2,29 кДж; 2) 68 Дж.
Определить радиус R капли спирта, вытекающей из узкой вертикальной трубки радиусом r = 1 мм. Считать, что в момент отрыва капля сферическая. Поверхностное натяжение спирта σ = 22 мН/м, а его плотность ρ = 0,8 г/см3. Ответ: 1,61 мм.
Давление воздуха внутри мыльного пузыря на ΔP = 200 Па больше атмосферного. Определить диаметр d пузыря. Поверхностное натяжение мыльного раствора σ = 40 мН/м. Ответ: 1,6 мм.
Воздушный пузырек диаметром d = 0,02 мм находится на глубине h = 25 см под поверхностью воды. Определить давление воздуха в этом пузырьке. Атмосферное давление принять нормальным. Поверхностное натяжение воды σ = 73 мН/м, а ее плотность ρ = 1 г/см3. Ответ: 118 кПа.
Вертикальный капилляр погружен в воду. Определить радиус кривизны мениска, если высота столба воды в трубке h = 20 мм. Плотность воды ρ = 1 г/см3, поверхностное натяжение σ = 73мН/м. Ответ: 744мкм.
Широкое колено U-образного манометра имеет диаметр d1 = 2 мм, узкое – d2 = 1 мм. Определить разность Δh уровней ртути в обоих коленах, если поверхностное натяжение ртути σ = 0,5 Н/м, плотность ртути ρ = 13,6 г/см2, а краевой угол θ = 138°. Ответ: 5,6 мм.
Используя закон Дюлонга и Пти, определить удельную теплоемкость: 1) натрия; 2) алюминия. Ответ: 1) 1,08 кДж/(кг·К); 2) 0,924 кДж/(кг·К).
Пользуясь законом Дюлонга и Пти, определить, во сколько раз удельная теплоемкость железа больше удельной теплоемкости золота. Ответ: 3,52.
Для нагревания металлического шарика массой 10 г от 20 до 50 °С затратили количество теплоты, равное 62,8 Дж. Пользуясь законом Дюлонга и Пти, определить материал шарика. Ответ: Олово, так как М = 0,119 кг/моль.
Изменение энтропии при плавлении 1 моль льда составило 25 Дж/К. Определить, насколько изменится температура плавления льда при увеличении внешнего давления на 1 МПа? Плотность льда ρ1 = 0,9 г/см3, воды ρ2 = 1 г/см3. Ответ: ΔT = –0,08 К.
Литература
Волькенштейн В.С. Сборник задач по курсу физики. – СПб.: СпецЛит, 2001.
Трофимова Т.И. Сборник задач по курсу физики для втузов. – М.: «Оникс 21 век», «Мир и Образование», 2003.
Чертов А.Г., Воробьев А.А. Задачник по физике. – М.: Интеграл-пресс, 1977.
Индивидуальные задания.
Тема 1. Кинематика
1
|
1.1, 1.31, 1.10
|
11
|
1.11, 1.27, 1.17
|
21
|
1.21, 1.3, 1.37
|
2
|
1.2, 1.32, 1.11
|
12
|
1.12, 1.26, 1.18
|
22
|
1.22, 1.4, 1.36
|
3
|
1.3, 1.33, 1.12
|
13
|
1.13, 1.25, 1., 2
|
23
|
1.23, 1.5, 1.35
|
4
|
1.4, 1.34, 1.20
|
14
|
1.14, 1.24, 1.3
|
24
|
1.24, 1.6, 1.34
|
5
|
1.5, 1.35, 1.21
|
15
|
1.15, 1.23, 1.4
|
25
|
1.25, 1.7, 1.33
|
6
|
1.6, 1.36, 1.22
|
16
|
1.16, 1.22, 1.5
|
26
|
1.26, 1.8, 1.32
|
7
|
1.7, 1.37, 1.23
|
17
|
1.17, 1.21, 1.6
|
27
|
1.27, 1.9, 1.31
|
8
|
1.8, 1.30, 1.24
|
18
|
1.18, 1.20, 1.7
|
28
|
1.28, 1.10, 1.15
|
9
|
1.9, 1.29, 1.15
|
19
|
1.19, 1.1, 1.8
|
29
|
1.29, 1.11, 1.6
|
10
|
1.10, 1.28, 1.16
|
20
|
1.20, 1.2, 1.30
|
30
|
1.30, 1.12, 1.17
|
Тема 2. Динамика материальной точки
1
|
2.1, 2.10, 2.59
|
11
|
2.11, 2.20, 2.51
|
21
|
2.10, 2.30, 2.40
|
2
|
2.2, 2.11, 2.58
|
12
|
2.12, 2.21, 2.50
|
22
|
2.11, 2.31, 2.41
|
3
|
2.3, 2.12, 2.57
|
13
|
2.13, 2.22, 2.49
|
23
|
2.12, 2.32, 2.42
|
4
|
2.4, 2.13, 2.56
|
14
|
2.14, 2.23, 2.48
|
24
|
2.13, 2.33, 2.43
|
5
|
2.5, 2.14, 2.55
|
15
|
2.15, 2.24, 2.47
|
25
|
2.14, 2.34, 2.44
|
6
|
2.6, 2.15, 2.54
|
16
|
2.16, 2.25, 2.46
|
26
|
2.15, 2.35, 2.45
|
7
|
2.7, 2.16, 2.53
|
17
|
2.17, 2.26, 2.45
|
27
|
2.16, 2.36, 2.46
|
8
|
2.8, 2.17, 2.52
|
18
|
2.18, 2.27, 2.44
|
28
|
2.17, 2.37, 2.47
|
9
|
2.9, 2.18, 2.53
|
19
|
2.19, 2.28, 2.43
|
29
|
2.18, 2.38, 2.48
|
10
|
2.10, 2.19, 2.52
|
20
|
2.20, 2.29, 2.42
|
30
|
2.19, 2.39, 2.49
|
Тема 3. Динамика вращательного движения
|
|
|
 Скачать 0.66 Mb.
Скачать 0.66 Mb.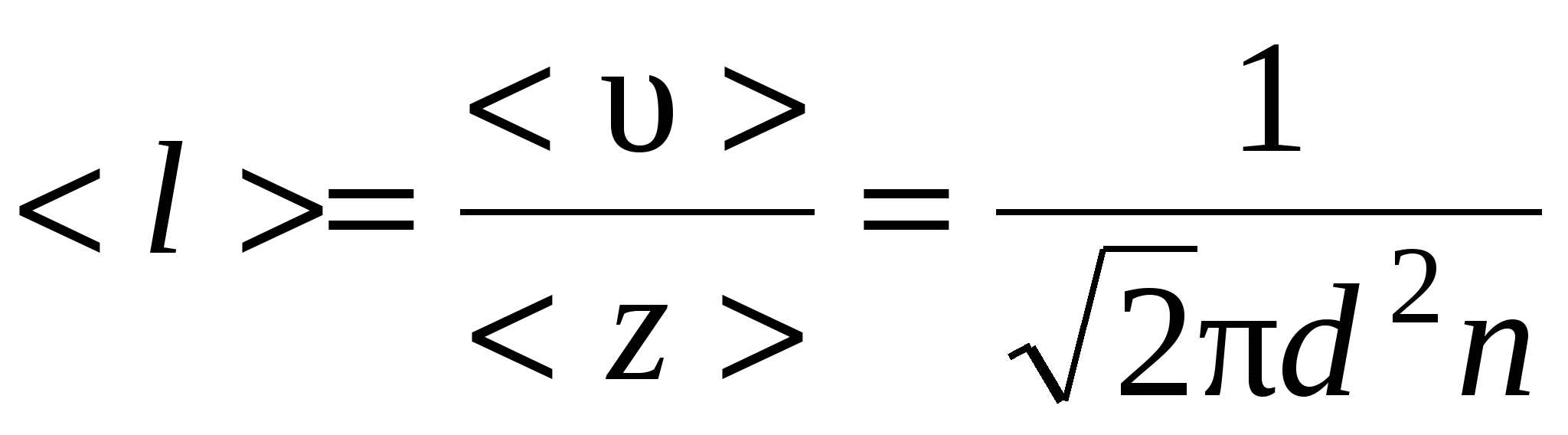 .
.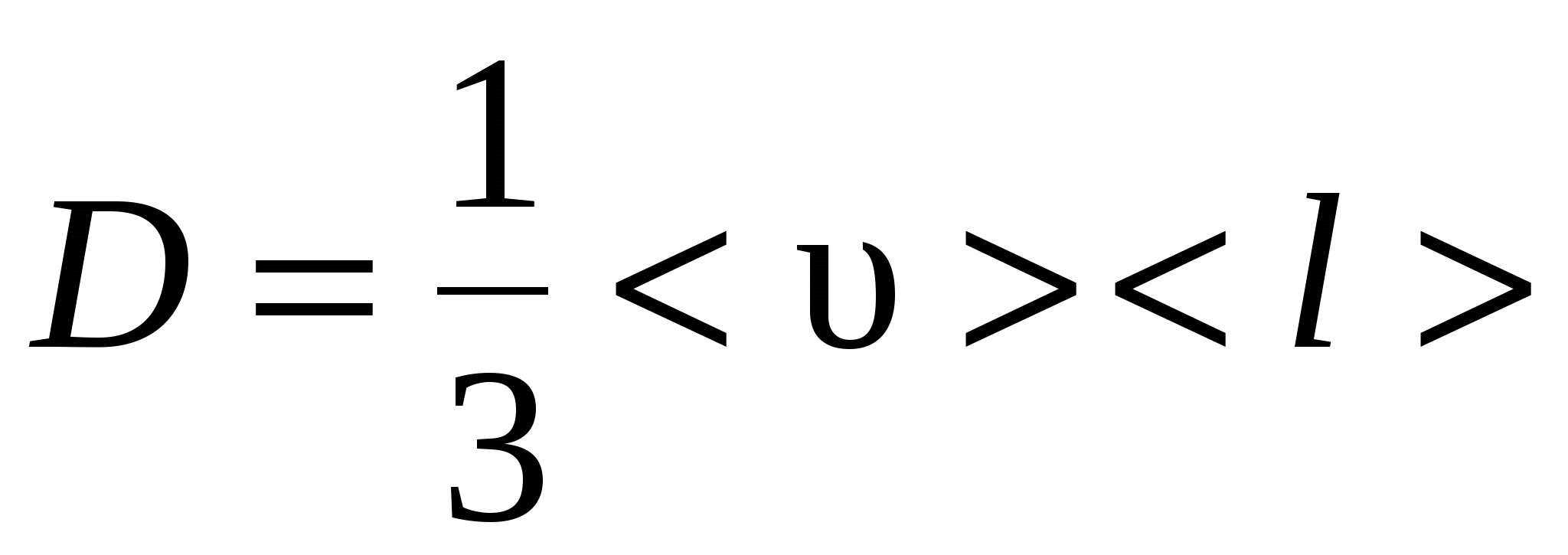 .
.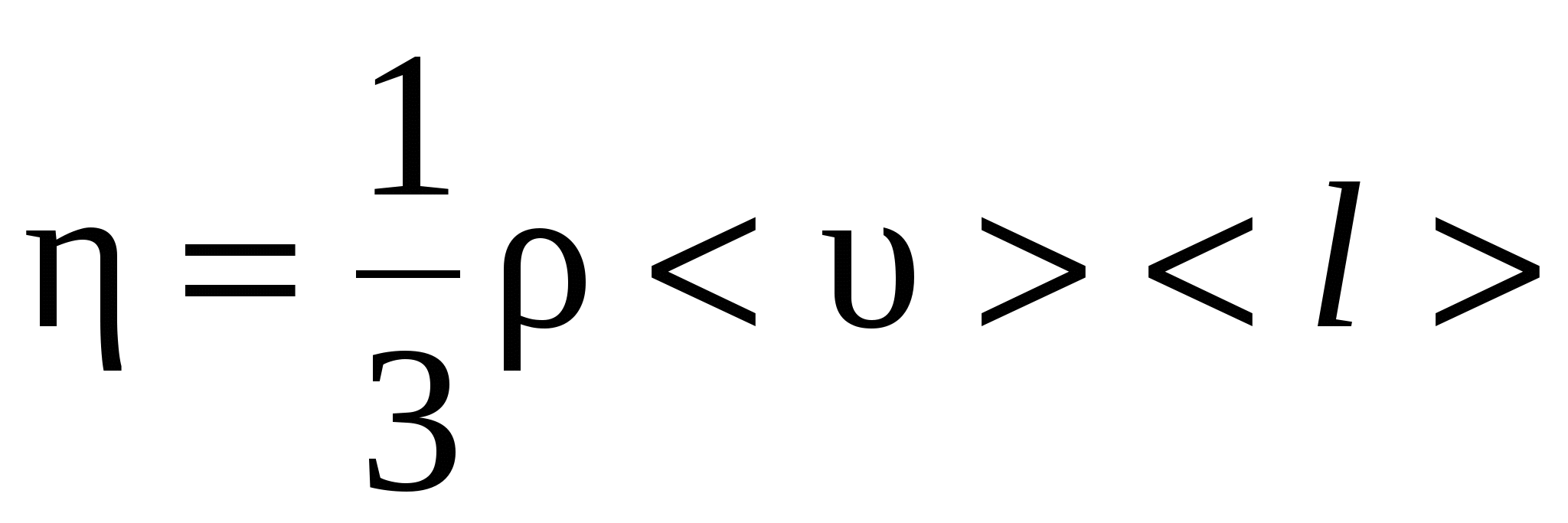 .
.