Гемолитики доклад. гемолитики доклад. Вещества, вызывающие гемолиз
 Скачать 53.65 Kb. Скачать 53.65 Kb.
|
|
Действие химических веществ на организм, приводящее к повреждению биологических механизмов энергетического обеспечения процессов жизнедеятельности, называется общеядовитым. Это действие отмечается у многих химических веществ. Выделяют также группу общеядовитых веществ, в реализации токсического эффекта которых существенное место занимает повреждающее влияние на сам эритроцит. Такие вещества называются гемолитиками. Гемолитики разрушают эритроциты, и гемоглобин выходит в плазму крови. При это наблюдается: Существенное повышение коллоидно-осмотического давления плазмы крови (содержание белка возрастает с 7 до 20%); Ускоренное разрушение гемоглобина, уже через сутки уровень Hb составляет менее 30% от нормы; Ухудшение оксигенации тканей вследствие затруднения диссоциации оксигемоглобина из-за существенно более низкого содержания бисфосфоглицерата в плазме крови, чем в эритроцитах; Нефротоксическое действие гемоглобина, свободно циркулирующего в плазме крови, ведущее к развитию острой почечной недостаточности. Именно поражение почек при действии гемолитических ядов практически определяет судьбу пораженных. Формируется пигментный гемоглобинурийный нефроз, приводящий к необратимому нарушению функции почек и к гибели больных от уремии. Из сказанного ясно, почему вещества этой подгруппы можно лишь с большой долей условности назвать общеядовитыми. Общая классификация веществ, вызывающих гемолиз, представлена в таблице 1. Таблица 1. Вещества, вызывающие гемолиз.
Лечение острых отравлений строится по следующим принципам: Прекращение дальнейшего поступления токсиканта в организм; Связывание или обезвреживание яда, затруднение его дальнейшего всасывания, удаление не всосавшегося токсиканта из организма Восстановление и поддержание нарушенных жизненно-важных функций организма; Применение антидотов; Устранение отдельных симптомов интоксикации. Рассмотрим лечение поражений гемолитиками в соответсвии с данными принципами на примере арсина и стибина. 1. Прекращение дальнейшего поступления токсиканта в организм. Арсин и стибин попадают в организм ингаляционно, поэтому, прежде всего, необходимо надеть на пострадавшего противогаз и немедленно эвакуировать из зоны химического заражения, после чего немедленно начать лечение. Важным мероприятием медицинской защиты является скорейшее выявление пораженных, до развития у них выраженного гемолиза, и скорейшая эвакуация их в лечебные учреждения. 2. Применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью и дееспособности в ходе оказания медицинской помощи. При содержании гемоглобина в плазме крови более 1,5 мг/мл показано обменное переливание крови. В раннем периоде интоксикации особенно показан гемодиализ в сочетании с введением унитиола (200-300 мл 5%), так как комплексы мышьяк-унитиол имеют меньшие размер, чем комплексы яд-белок, благодаря чему значительно лучше диализируются (метод искусственной детоксикации). Применяют симптоматические средства борьбы с развивающимися анемией, кислородным голоданием и поражением почек: кровопускание (300 - 400 мл), внутривенное введение 40% раствора глюкозы, физиологического раствора, других кровезаменяющих жидкостей (инфузионная терапия). Гемодиализ и инфузионная терапия способствуют постепенному снижению концентрации мышьяка в биологических средах. При отравлениях гемолитическими ядами показано ощелачивание крови в сочетании с водной нагрузкой. С этой целью в/в капельно вводят 500— 1500 мл/сут 4% раствора гидрокарбоната натрия с одновременным контролем кислотно-основного состояния для поддержания постоянной щелочной реакции мочи (рН более 8,0). Использование форсированного диуреза позволяет в 5—10 раз ускорить выведение токсических веществ из организма, что способствует профилактике нефропатии и гепатопатии. Поскольку гемолиз сопровождается нарушением кислородотранспортной функции крови с последующим развитием гипоксии, проводятся ингаляции кислорода. Терапия токсической нефропатии и гепатопатии. В токсикогенной стадии острого отравления, когда структурные нарушения в печени и почках ещё формируются, основное значение имеет ускоренное удаление токсичных веществ из организма. Кроме того, необходимы экстренная патогенетическая терапия экзотоксического шока, применение специфических антидотов и «печёночных» лекарственных препаратов. В соматогенной стадии, когда развёртывается клиническая картина острой почечно-печёночной недостаточности, основное значение приобратают мероприятия, обеспечивающие временное замещение утраченных функций этих органов (в расчёте на их высокую регенераторную способность), а также симптоматическое лечение. Даже при тяжёлых формах отравления рано начатые мероприятия по ускоренному выведению токсических веществ из организма (гемодиализ, перитонеальный диализ, форсированный диурез и другие) способствуют благоприятному исходу, предотвращают острую почечно-печёночную недостаточность. Эффективным средством профилактики и лечения токсической гепато- и нефропатии является метод форсированного диуреза с помощью осмотических диуретиков (мочевина, маннитол) или салуретиков (фуросемид). Основными лечебными факторами форсированного диуреза являются: уменьшение концентрации нефро- и гепатотоксичных веществ в первичной моче, ускорение освобождения организма от этих токсичных веществ, уменьшение гемодинамического сопротивления почечных канальцев с восстановлением их проходимости при закупорке (гемоглобинурия, миогемоглобинурия, кристаллурия), восстановление почечного кровотока и оксигенация почечной ткани. «Печёночная терапия» направлена на ликвидацию патогенетических факторов развивающейся печёночно-почечной недостаточности независимо от вида химического вещества. Применяются так называемые липотропные лекарственные препараты, уменьшающие жировую инфильтрацию печени, углеводную нагрузку и коферменты, которые сохраняют своё лечебное действие и при дальнейшем течении патологического процесса в соматогенной фазе. Использование этих лекарственных препаратов не имеет каких-либо особенностей, свойственных терапии острых отравлений. Обоснованием их полезности при токсической гепатопатии является клинический опыт. В качестве липотропных лекарственных препаратов обычно применяются витамины группы В (В1, В6, В12, В15); для восстановления запасов гликогена используется 5—11 % раствор глюкозы (до 1 г на кг массы тела пациента в сутки) с инсулином (8—12 ЕД). Вводится комплекс кофермента А (200—240 мг в сутки), кокарбоксилазу (150 мг), альфа-липоевую кислоту (100—200 мг) и никотинамид (200 мг) для предупреждения накопления продуктов обмена пировиноградной кислоты (ацетоин, 2,3-бутиленгликоль и другие), которые играют важную роль в патогенезе печёночной энцефалопатии. Большое значение для усиления репаративных процессов в печени имеет длительное курсовое применение эссенциале, что помогает восстановить фосфолипидные потери клеток. Антидотная терапия Эффективность проводимой «печёночной» и антидотной терапии острых отравлений гепато- и нефротоксическими веществами значительно увеличивается при внутрипортальном способе введения лекарственных препаратов, который успешно применяется в клинической практике. Внутрипортальные (трансумбиликальные) инфузии создают более высокую концентрацию лекарственных препаратов в печени, чем обычные методы введения. Попадая в организм через воротную вену, лекарственные препараты минуют физиологические фильтры (лёгкие, кишечник и другие), которые они преодолевают при парентеральном введении или приёме внутрь. Унитиол (основной антидот, применяемый для снижения степени поражения печени и почек) вводят в пупочную вену со скоростью 60-100 капель в минуту в виде 5% раствора по 50-150 мл/сут в растворах глюкозы. Продолжительность введения антидота 4-6 суток. 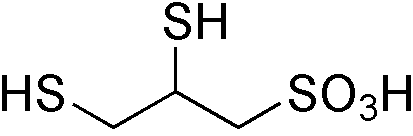 Рисунок 1. Формула унитиола. Также в качестве антидота применяется мекаптид (антарсин). Мекаптид выпускается в ампулах по 1 мл 40% раствора в абрикосовом или персиковом масле. Вводится п/к и в/м в виде 40% масляного раствора в количестве 1 мл (что составляет примерно 70 мг чистого препарата на 10 кг массы тела больного). Вводить следует как можно раньше. В первые сутки производят 2–3 инъекции раствора препарата с промежутками в 4–5 часов, на вторые и третьи сутки делают 2 инъекции с интервалом в 8–10 часов в зависимости от состояния больного. При тяжёлых интоксикациях мышьяковистым водородом первая инъекция производится в дозе 2 мл 40% раствора. Как антидот Мекаптид эффективен только при отравлениях мышьяковистым водородом. При интоксикациях прочими соединениями мышьяка неактивен. Указанная избирательность действия Мекаптида обусловлена особенностями его хим. строения (наличие тиоэфирной связи и ароматического ядра), обеспечивающими высокое сродство препарата к мышьяковистому водороду. Благодаря выраженной липоидотропности и поверхностной активности, Мекаптид быстро проникает через мембраны эритроцитов и взаимодействует с мышьяковистым водородом, образуя малотоксичные водорастворимые соединения (тиоарсениты), которые выводятся через почки. Определенное значение имеет способность Мекаптида (благодаря наличию у него двух реакционноспособных SH-групп) нормализовать содержание сульфгидрильных групп белков крови и тканей и в связи с этим восстанавливать активность ряда ферментов 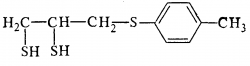 Рисунок 2. Формула мекаптида. Источники Токсикология и медицинская защита [Электронный ресурс]/ А.Н. Гребенюк [и др.].— Электрон. текстовые данные.— Санкт-Петербург: Фолиант, 2016.— 672 c.— Режим доступа: http://www.iprbookshop.ru/60949.html.— ЭБС «IPRbooks» Гребенюк, А. Н. Антидотная фармакотерапия в чрезвычайных ситуациях / А.Н. Гребенюк, Н.В. Шперлинг, Н.Л. Денисов, О.Ю. Стрелов // Издательство СПХФА. – 2017г. – 92 с. Сложный для дифференциальной диагностики случай острого случайного отравления соединением мышьяка у подростка. URL: https://medi.ru/pp/2016/03/7980/ (дата обращения: 03.11.2020). Токсическая нефропатия. URL: https://studfile.net/preview/4333182/page:21/ (дата обращения: 03.11.2020). Острые отравления. Принципы оказания неотложной помощи. URL: https://matveynator.ru/lib/spv/book/16.htm (дата обращения: 03.11.2020). | ||||||||||||
