Вопросы для самоподготовки к контрольной работе 1 по разделу 1
 Скачать 1.25 Mb. Скачать 1.25 Mb.
|
|
Вопросы для самоподготовки к контрольной работе №1 по разделу №1 1. Сторонники физической модели процесса растворения: С. А. Аррениус, Я.Х.Вант-Гофф, В.Ф.Оствальд. Суть физической теории и ее применение. -------- Сторонники физической модели процесса растворения: С. А. Аррениус, Я.Х.Вант-Гофф, В.Ф.Оствальд. Суть физической теории и ее применение. Физическая теория растворов, возникшая главным образом на основе трудов Вант-Гоффа, Аррениуса и Оствальда, опиралась на экспериментальное изучение коллигативных свойств разбавленных растворов (осмотическое давление, новышение температуры кипения, понижение температуры замерзания раствора и т. п.), зависящих главным образом от концентрации растворенного вещества, а не от его природы. Количественные законы (законы Вант-Гоффа, Рауля) были открыты в предположении, что в разбавленных растворах молекулы растворенного вещества подобны молекулам идеального газа. Отступления от этих законов, наблюдаемые для растворов электролитов, были объяснены на основе теории электролитической диссоциации Аррениуса. Простота представлений физической теории и успешное применение ее как для объяснения свойств растворов электролитов, так и для количественного изучения электрической проводимости растворов обеспечили быстрый успех этой теории. Растворение – процесс диффузии. 2. Сторонники химической модели процесса растворения: Д.И. Менделеев, Каблуков И.А., Н.С. Курнаков и др. Суть химической теории. Образование сольватов (гидратов). ----------- Сторонники химической модели процесса растворения: Д.И. Менделеев, Каблуков И.А., Н.С. Курнаков рассматривали процесс растворения как процесс химического взаимодействия растворяемого вещества с водой- процесс гидратации.Если в качестве растворителя какой-нибудь другой, то будет называться процессом сольватацией. Главную роль в образовании сольватов играет водородная связь. СОЛЬВАТЫ - продукты присоединения растворителя к растворенным веществам. Сольваты (гидраты) образуются за счет ион-дипольного, донорно-акцепторного взаимодействий, образования водородных связей и т.д. Признаки химических явлений: 1. выделение и поглощение теплоты при растворении различных веществ. При растворении в воде концентрированной серной кислоты выделяется большое количество теплоты. 2. Изменение окраски некоторых веществ при растворении. Безводный сульфат меди( II ) белый, а в водном растворе он голубой. 3. Понятия: раствор, растворитель, растворенное вещество. -----В растворах протекает большее количество химических реакций организма. Раствор – это идеальная транспортная система, которая доставляет необходимые лекарственные средства непосредственно во внутреннюю среду организма. Также растворённые препараты лучше усваиваются организмом. Раствор- это гомогенная система переменного состава, состоящая из двух и более независимых компонентов и продуктов их взаимодействия. Растворитель- компонент, агрегатное состояние которого не изменяется при образовании раствора. При одинаковых агрегатных состояниях компонентов растворителем считают то вещество, содержание которого в растворе больше. Растворенное вещество-компонент, молекулы или ионы которого равномерно распределены в объеме растворителя. 4. Классификация растворов: по природе растворителя, по размерам частиц и степени однородности растворенного вещества, по агрегатному состоянию, по возможности к электролитической диссоциации (по поведению вещества в растворе), по концентрации (относительному количеству компонентов), по растворимости (насыщенные, ненасыщенные и пересыщенные). Классификация растворов: По природе растворителя: водные и неводные По размерам частиц и степени однородности растворенного вещества: 1. Истинные растворы (гомогенные системы с размером частиц 10-10-10-9м). 2. Коллоидные растворы (неоднородные гетерогенные системы с размером частиц 10-9-10-6 м) . По агрегатному состоянию: газовые, твёрдые и жидкие По возможности к электролитической диссоциации (по поведению вещества в растворе): растворы электролитов (растворы низкомолекулярных электролитов и растворы высокомолекулярных электролитов - полиэлектролитов); растворы неэлектролитов (углеводы); растворы амфолитов (аминокислоты, основания Al,Zn и др.) и полиамфолитов (гепарин, полиадениловая кислота, полиаспаргиновая кислота). По концентрации (относительному количеству компонентов): Разбавленные: < 10% Концентрированные: > 10% По растворимости (насыщенные, ненасыщенные и пересыщенные): 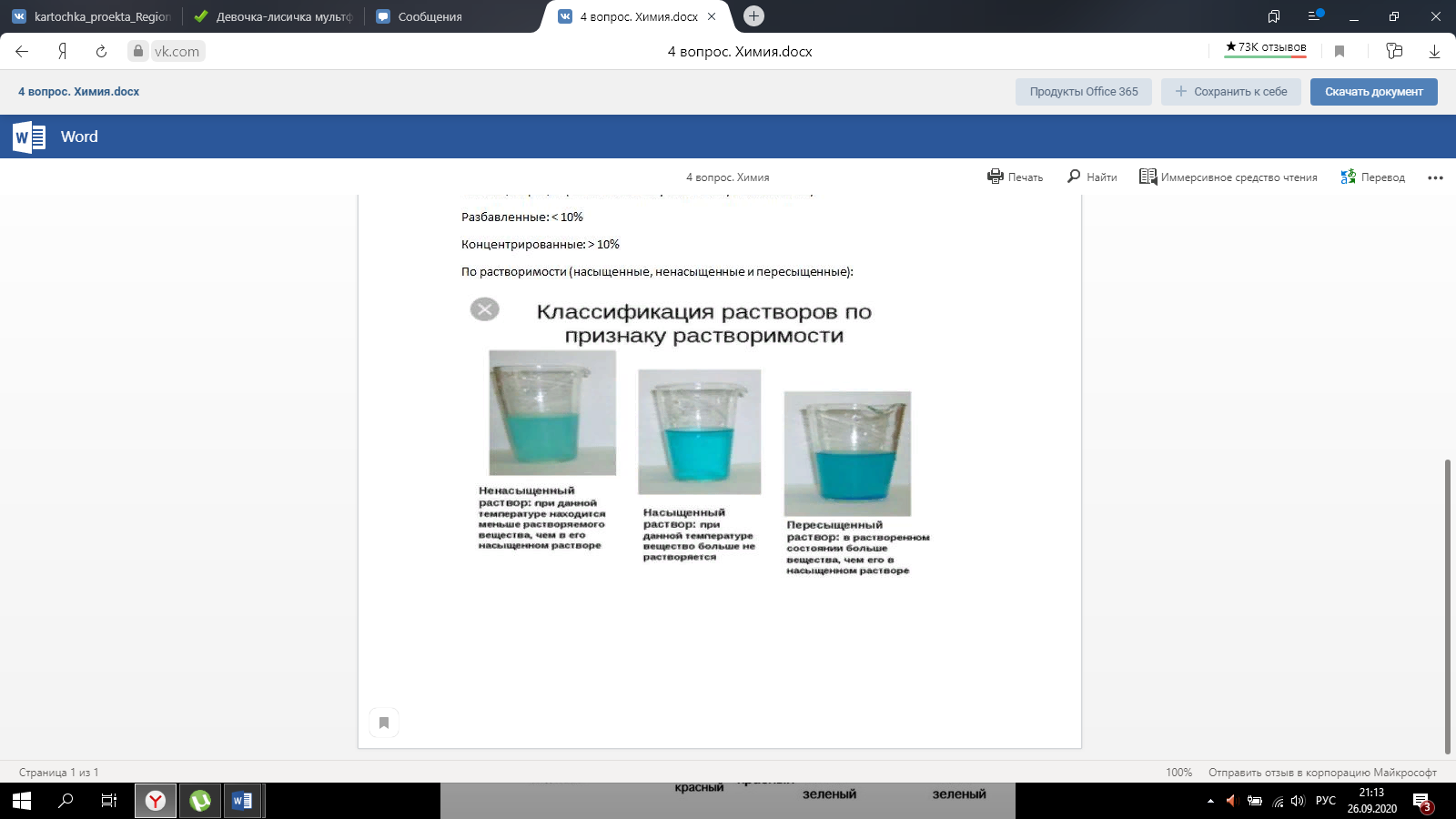 5. Растворимость - понятие, факторы влияющие на растворимость: природа растворенного вещества и растворителя, температура, давление.   6. Зависимость растворимости твердых веществ и газов в жидкостях от температуры. ------ С ростом температуры растворимость твёрдых и жидких веществ увеличивается. Растворимость газов в жидкостях с ростом температуры уменьшается.Пример: кипячение раствора – способ удалить газы 2. От температуры: для твёрдых веществ растворимость зависит от теплоты растворения если 3. Для всех газов характерен экзотермический процесс, идущий с выделением теплоты Q, если Эту Закономерность используют для удаления СО2 из воды кипячением. Исключение составляют благородные газы, при растворимости в некоторых органических растворителях наблюдается эндотермический процесс, то есть t 7. Растворимость жидких веществ в жидкостях. Привести примеры неограниченной и ограниченной растворимости. Рассмотреть примеры полной нерастворимости. ---------- Растворимость жидкостей в жидкостях зависит от природы растворителя и растворяемого вещества, температуры, присутствия в растворе посторонних веществ. На растворимость жидкостей в жидкостях давление почти не влияет, поскольку при растворении объемные эффекты невелики. При смешивании двух жидкостей можно наблюдать самую различную их взаимную растворимость: от практически полной нерастворимости друг в друге (ртуть - вода) до неограниченной смешиваемости (ацетон - вода). Неограниченно растворяются в воде все жидкие неорганические кислоты (HNO3, HClO4, HCN, HNCS, и др.), простейшие органические кислоты (НСООН, СН3СООН и др.), простейшие спирты и кетоны (СН3ОН, С2Н5OН, СН3СОСН3 и др.). Жидкости, неограниченно растворимые друг в друге • Примерами таких жидкостей являются этанол – вода, метанол – вода, метанол – этанол, бензол – толуол и т.д. Ограниченно растворимыми жидкостями называются жидкости, которые в пределах определенной концентраций и температур образуют одну гомогенную фазу; в другой области концентраций и температур эта система становится гетерогенной. (триэтиламин-вода, анилин –вода) Однако, в некоторых случаях взаимная растворимость жидкостей настолько мала, что их можно считать практически нерастворимыми друг в друге. Смеси нерастворимых жидкостей при перемешивании образуют эмульсии (серный эфир и вода) Наконец, вода и бензин совсем не смешиваются (пример практической нерастворимости одной жидкости в другой). 8. Зависимость растворимости газов в жидкостях от давления. Законы Генри-Дальтона-Сеченова, формулировки и математические формулы. Медико-биологическое значение этих законов. ---------- Давление влияет только на расторимость газов и описывается законом Генри: Растворимость газа в жидкостях прямо пропорциональна его давлению над жидкостью: С = kP, где C - концентрация газа в жидкости. k - константа Генри; коэффицент пропорциональности, зависящий от природы газа (моль/(Па×л)). Из уравнения следует, что с повышением давления растворимость газов в жидкостях увеличивается. Закон Дальтона: Закон Дальтона утверждает, что общее давление всех газов вместе взятых равно сумме парциальных давлений каждого газа по отдельности. p = p1+p2+p3. Закон Дальтона (для смеси газов) Растворимость каждого из компонентов газовой смеси при T = const пропорциональга парциальному давлению компонента над жидкостью и не зависит от общего давления смеси и индивидуальности других компонентов: Pi = Pобщ. × N(xi), где Pi - парциальное давление компонента Pобщ - общее давленре газовой смеси N (xi) - мольная доля компонента. Закон Сеченова: Растворимость газов в жидкостях в присутствии электролитов понижается: ln No/N = KC, где No - мольная доля газа в чистой воде N - мольная доля газа в растворе соли C - молярная концентрация соли K - константа Сеченова, зависящая от природы газа, электролита и температуры. Медико-биологическое значение этих законов: Законы Генри-Дальтона и Сеченова имеют большое практическое значение как в медицине, так и в спорте. Изменение растворимости газов в крови при изменении давления может вызывать тяжелые заболевания 9.Способы выражения состава растворов: массовая доля, молярная концентрация, молярная концентрация эквивалента (нормальная концентрация), моляльная концентрация, титр, мольная доля. Привести математические формулы, дать определение и рассмотреть физический смысл каждого наименования. Способы выражения концентрации растворов: · Массовая доля- это отношение массы растворенного вещества к общей массе раствора. Массовую долю выражают в долях единицы или в процентах (например - ω = 0,05 или 5%) ω = m в-ва / mр-ра · Мольная доля – это отношение количества растворенного вещества к общему количеству вещества всех компонентов раствора: N = n в-ва / (nв-ва + nрастворителя) Размерность – доли единицы или проценты. · Молярная концентрация вещества (молярность) – отношение количества растворенного вещества к объему раствора: См = n в-ва / Vр-ра Cм=m в-ва/ M*V Размерность: моль/л. · Молярная концентрация эквивалента вещества (эквивалентная концентрация, нормальная концентрация, нормальность) , – отношение количества растворенного вещества к объему раствор Cн= m в-ва/ Э*V Размерность: моль-экв/л. · Моляльная концентрация вещества (моляльность) – отношение количества растворенного вещества к массе растворителя: Cm=m в-ва*1000/m р-ля*М в-ва Размерность – моль/1 кг р-ля. · Титр– отношение массы растворенного вещества к объему раствора: T=m в-ва/ V р-ра Размерность- г/мл 10. Закон эквивалентов. Следствие из закона эквивалентов. Расчетные формулы, определение, физический смысл. -------- Закон эквивалентов: m1/m2=Э1/Э2 Определение:массы реагирующих друг с другом веществ прямо пропорциональны их эквивалентным массам Физический смысл:вещества взаимодействуют в эквивалентных количествах Следствие из закона эквивалентов: V1×Сн1=V2×Сн2 (Сн-молярная концентрация эквивалента, нормальность) Определение: объёмы растворов реагирующих веществ обратно пропорциональны их нормальности Физический смысл:вещества взаимодействуют в эквивалентных количествах 11. Приготовление разбавленных растворов кислот из более концентрированных и их количественное определение (титриметрия) алкалиметрическим методом. Рассмотреть приготовление растворов на примере НСl, а титрование с применением в качестве титранта NaOH/ ----- Приготовление разбавленных растворов кислот из более концентрированных и их количественное определение (титриметрия) алкалиметрическим методом. Рассмотреть приготовление растворов на примере НСl, а титрование с применением в качестве титранта NaOH/ растворы готовятся в мерных колбах в соответствии с задачей. при приготовлении растворов берется определенное количество кислоты hcl, и мерная колба нужного обьема. для приготовления раствора необходимо добавить необходимый оьем кислоты в мерную колбу, эти обьемы указаны в задаче, после этого в три этапа нужно добавить воду, первый этап- добавление 1/3 от обьема колбы и перемешивание , второй- добавление воды почти до мерной линии, третий этап- наполнение с помощью глазной пипетки до линии мерной, стоит держать мерную колбу на уровне глаз, для точного и правильного создания расствора. после создания раствора, который и будет использоваться в титриметрии, после чего приготовить бюретку, наполнить ее до отметки 0. начать титриметрию. для этого в коническую колбу необходимо добавить определенный обьем раствора кислоты, к этому расствору добавить индикатор- фенолфталеин. покапельно добавлять щелочь в коническую колбу. прекратить титрирование после добавления капли которая запустила процесс окрашивания расствора, исходя из следствия закона эквивалентов, мы можем получить нормальность расствора кислоты, а из нормальности раствора уже точно также, по следствию закона эквивалентов получить и нормальность изначального расствора. 12.Коллигативные свойства растворов. Дать понятие и привести примеры. ------------ .Коллигативные свойства растворов. Дать понятие и привести примеры. Коллигативные свойства растворов -это такие свойства, на которые не оказывает влияние природа растворенного вещества, а зависят они исключительно от количества частиц этого растворенного вещества. Примеры: • 1) понижение давления насыщенного пара над раствором по сравнению с растворителем; • 2) повышение температуры кипения и понижение температуры замерзания (кристаллизации) растворов по сравнению с растворителем; • 3) осмотические явления 13. Первый закон Рауля, две трактовки закона. Рассмотреть давление насыщенного пара над раствором в зависимости от мольной доли растворителя и мольной доли растворенного вещества. Привести математические формулы. --------- Первый закон Рауля, две трактовки закона. Рассмотреть давление насыщенного пара над раствором в зависимости от мольной доли растворителя и мольной доли растворенного вещества. Привести математические формулы. Первый закон Рауля Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе: • p = p0 · χр-ль= p0 · n2 / n2 + n1 • p — давление пара над раствором, Па; • p0 — давление пара над чистым растворителем, Па; • χр-ль — мольная доля растворителя • n1 – количество растворенного вещества (моль); n2 – количество растворителя (моль). Закон Рауля (иная трактовка) • Относительное понижение давления пара растворителя над раствором нелетучего неэлектролита равно мольной доле растворенного вещества: • где Р – давление насыщенного пара растворителя над раствором • (атм; Па; мм. рт. ст.); • Р0 – давление насыщенного пара над чистым растворителем • (атм; Па; мм. рт. ст.); • n1 – количество растворенного вещества (моль); • n2 – количество растворителя (моль). 14. Понятие- насыщенный пар. Зависимость давления насыщенного пара от температуры. -------- Насыщенный пар- пар, находящийся в динамическом равновесии со своей жидкостью, т.е кол-во молекул, покидающих жидкость за некоторый промежуток времени, равно кол-ву молекул пара, возвращающихся обратно в жидкость. При увеличении температуры, молекулы жидкости будут иметь большую кинетическую энергию и все большее кол-во молекул сможет вырваться из жидкости, следовательно, будет расти концентрация пара и его давление. 15.Второй закон Рауля. Рассмотреть температуры кипения и замерзания растворов от моляльной концентрации раствора. Физический смысл эбулиоскопической (Е, Кэ) и криоскопической констант (Кз). Зависимость их значений от природы растворителя. ------ Тот факт, что давление паров над раствором отличается от давления паров над чистым растворителем, существенно влияет на процессы кристаллизации и кипения. Из первого закона Рауля выводятся два следствия, касающиеся понижения температуры замерзания и повышения температуры кипения растворов, которые в объединённом виде известны как второй закон Рауля. Понижение температуры кристаллизации растворов Условием кристаллизации является равенство давления насыщенного пара растворителя над раствором давлению пара над твёрдым растворителем. Поскольку давление пара растворителя над раствором всегда ниже, чем над чистым растворителем, это равенство всегда будет достигаться при температуре более низкой, чем температура замерзания растворителя. Так, океанская вода начинает замерзать при температуре около −2 °C. Разность между температурой кристаллизации растворителя T°fr и температурой начала кристаллизации раствора Tfr есть понижение температуры кристаллизации. Понижение температуры кристаллизации бесконечно разбавленных растворов не зависит от природы растворённого вещества и прямо пропорционально моляльной концентрации раствора. Поскольку по мере кристаллизации растворителя из раствора концентрация последнего возрастает, растворы не имеют определённой температуры замерзания и кристаллизуются в некотором интервале температур. Повышение температуры кипения растворов Жидкость кипит при той температуре, при которой общее давление насыщенного пара становится равным внешнему давлению. Если растворённое вещество нелетуче (то есть давлением его насыщенных паров над раствором можно пренебречь), то общее давление насыщенного пара над раствором равно парциальному давлению паров растворителя. В этом случае давление насыщенных паров над раствором при любой температуре будет меньше, чем над чистым растворителем, и равенство его внешнему давлению будет достигаться при более высокой температуре. Таким образом, температура кипения раствора нелетучего вещества Tb всегда выше, чем температура кипения чистого растворителя при том же давлении T°b. Повышение температуры кипения бесконечно разбавленных растворов нелетучих веществ не зависит от природы растворённого вещества и прямо пропорционально моляльной концентрации раствора Криоскопическая и эбулиоскопическая константы Коэффициенты пропорциональности К и Е в приведённых выше уравнениях — соответственно, криоскопическая и эбулиоскопическая постоянные растворителя, имеющие физический смысл понижения температуры кристаллизации и повышения температуры кипения раствора с концентрацией 1 моль/кг. Для воды они равны 1,86 и 0,52 K·моль−1·кг, соответственно. Поскольку одномоляльный раствор не является бесконечно разбавленным, второй закон Рауля для него в общем случае не выполняется, и величины этих констант получают экстраполяцией зависимости из области малых концентраций до m = 1 моль/кг. Для водных растворов в уравнениях второго закона Рауля моляльную концентрацию иногда заменяют молярной. В общем случае такая замена неправомерна, и для растворов, плотность которых отличается от 1 г/см³, может привести к существенным ошибкам. Второй закон Рауля даёт возможность экспериментально определять молекулярные массы соединений, неспособных к диссоциации в данном растворителе; его можно использовать также для определения степени диссоциации электролитов. Растворы электролитов Законы Рауля не выполняются для растворов (даже бесконечно разбавленных), которые проводят электрический ток — растворов электролитов. Для учёта этих отклонений Вант-Гофф внёс в приведённые выше уравнения поправку — изотонический коэффициент i, неявно учитывающий диссоциацию молекул растворённого вещества: Неподчинение растворов электролитов законам Рауля и принципу Вант-Гоффа послужили отправной точкой для создания С. А. Аррениусом теории электролитической диссоциации.  16. Закон Вант - Гоффа: определение и его математическое выражение для не электролитов и электролитов. Изотонический коэффициент, понятие, определение и его зависимость от концентрации раствора. 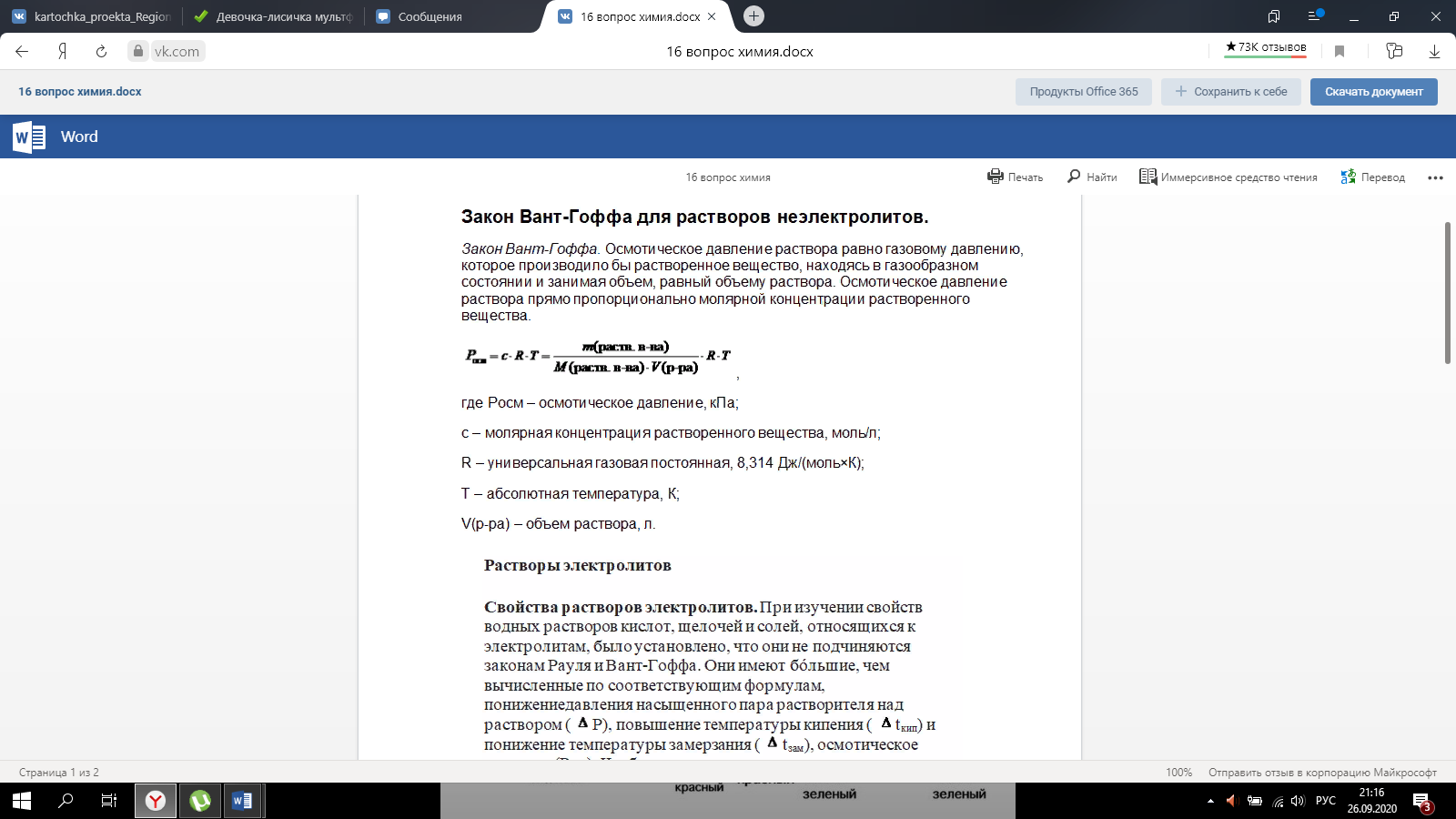 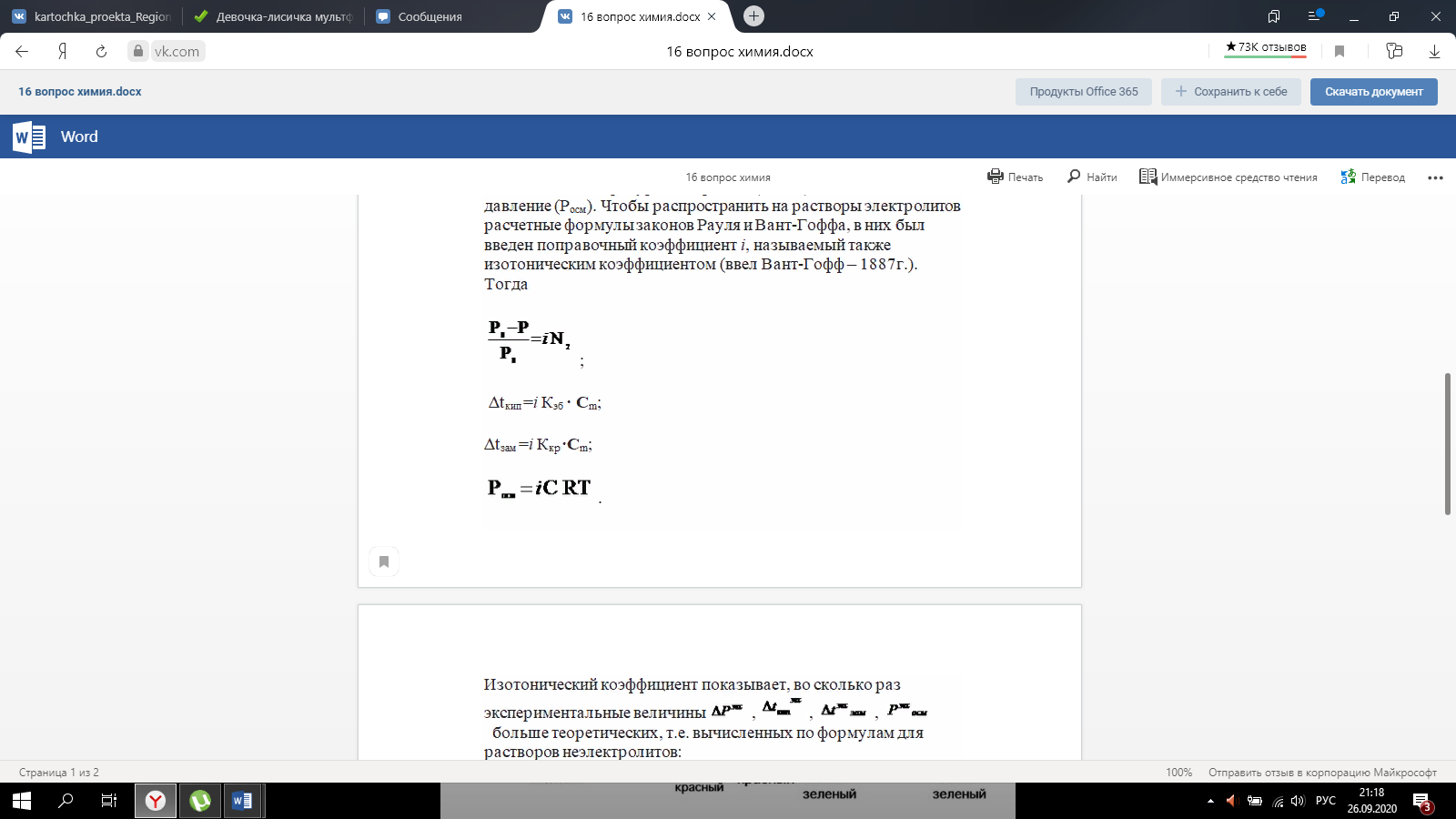 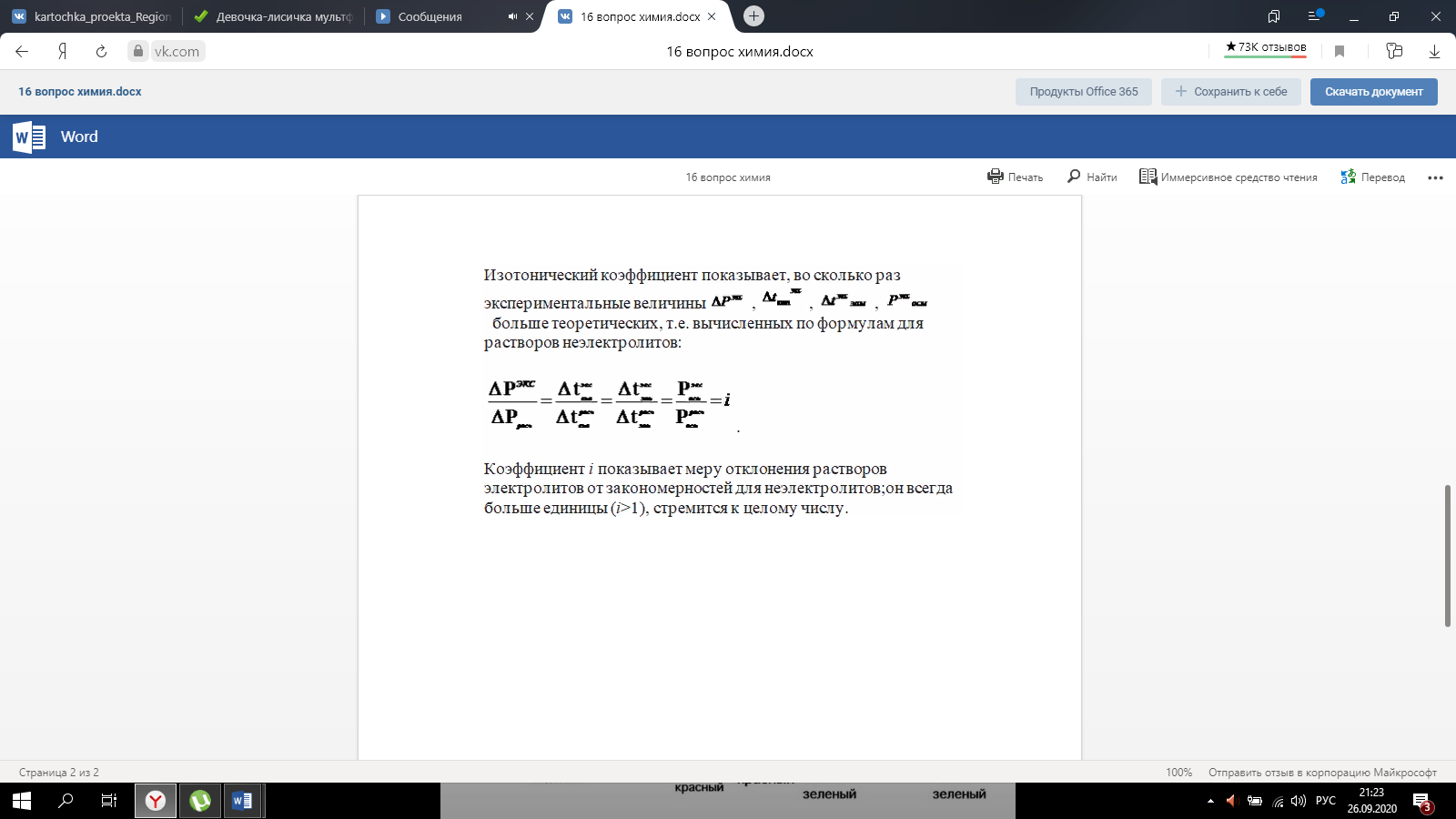 17. Определение осмоса и осмотического давления; факторы, влияющие на осмотическое давление; формула для расчёта осмотического давления. Роль осмоса в биологии и медицине. 18.Понятия: эндоосмос, экзоосмос, изоосмия. В каких растворах наблюдаются эти процессы? Что при этом происходит? Гемолиз, плазмолиз, тургор. Их значение в медицине и биологии. Эндосмос и экзосмос, частные случаи явления осмоса. Осмос состоит в следующем: если два раствора различных концентраций или раствор и чистый растворитель отделены друг от друга полупроницаемой перепонкой (пергамент, животный пузырь и т. п.), то растворитель переходит от более слабого раствора в более крепкий, растворённое же вещество через перепонку не проходит; процесс перехода растворителя продолжается до тех пор, пока или не выравняются концентрации или не возникнет достаточное давление в более крепком растворе, прекращающее ток растворителя через перепонку (см. растворы, XXXV, 681/82). В прежнее время явления перехода растворителя в раствор (или переход его из слабого раствора в более крепкий) называли эндосмосом; если к раствору приложить извне давление, превышающее его осмотическое давление, то растворитель станет уходить из раствора через перепонку в сосуд с чистым растворителем (или в более слабый раствор); такое явление получило название экзосмоса. Эти термины в настоящее время почти вышли из употребления. Изоосмия - относительное постоянство осмотического давления в жидких средах и тканях организма, обусловленное поддержанием на данном уровне концентраций содержащихся в них веществ: электролитов, белков и т. д. Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. При эндо и экзосмосе наблюдается перенос растворителя в среду с большей концентрацией растворенного вещества Гемо́лиз — разрушение эритроцитов крови с выделением в окружающую среду гемоглобина. В норме физиологический гемолиз завершает жизненный цикл эритроцитов (120 суток) и происходит в организме человека и животных непрерывно. Плазмолиз - это процесс, при котором клетки теряют воду в гипертоническом растворе. Обратный процесс, деплазмолиз или цитолиз , может происходить, если клетка находится в гипотоническом растворе, что приводит к более низкому внешнему осмотическому давлению и чистому потоку воды в клетку. Значение данных процессов состоит в том, что при длительной засухе растение может при помощи плазмолиза выделять из своих клеток запасы воды на поверхность листьев, дабы защитить от чрезмерного влияния солнечных лучей. А когда идут дожди - происходит деплазмолиз и клетки вновь наполняются водой. Ту́ргор тка́ней — напряжённое состояние оболочек живых клеток. Тургорное давление — внутреннее давление, которое развивается в растительной клетке, когда в неё в результате осмоса входит вода и цитоплазма прижимается к клеточной стенке; это давление препятствует дальнейшему проникновению воды в клетку. 19. Изотонические, гипо- и гипертонические растворы. Какие процессы происходят с клеткой в этих растворах? Где эти растворы используются в медицинской практике? ----- . Гипертонические растворы- растворы, Осмотическое давление которых выше осмотического давления в растительных или животных клетках и тканях. В зависимости от функциональной, видовой и экологической специфики клеток осмотическое давление в них различно, и раствор, гипертоничный для одних клеток, может оказаться изотоничным или даже гипотоничным для др. При погружении растительных клеток в Г. р. он отсасывает воду из клеток, которые уменьшаются в объёме, а затем дальнейшее сжатие прекращается и протоплазма отстаёт от клеточных стенок Эритроциты крови человека и животных в Г. р. также теряют воду и уменьшаются в объёме. Г. р. в сочетании с гипотоническими растворами и изотоническими растворами применяют для измерения осмотического давления в живых клетках и тканях. Медицина - Перечень патологий, от которых удаётся успешно избавиться, применяя гипертонический раствор, достаточно велик, поэтому такое средство многие по-настоящему считают уникальным. Солевой раствор воды способен вылечить:1. головные боли и мигрень; 2.воспалительные заболевания носоглотки;3. ОРЗ; 4.бронхиальную астму;5. ангину; 6.гипертонию; 7.приступы гипертензии; 8.отёчность; 9.остеохондроз; 10.гематомы;11. поражения суставов; 12.патологические изменения в тканях; 13.гинекологические заболевания. 2.Гипотонические растворы - в биологии, различные растворы, Осмотическое давление которых ниже, чем в клетках растительных или животных тканей. В Г. р. клетки насасывают воду, увеличиваясь в объёме, и теряют часть осмотически активных веществ (органических и минеральных). Эритроциты крови животных и человека в Г. р. разбухают до такой степени, что их оболочки лопаются и они разрушаются. Это явление называют Гемолизом. Медицина-1.Для полоскания (ангины, тонзиллиты, воспалительные заболевания носоглотки). 2.Для обработки гнойных ран (повязки, компрессы). 3.При отеках. 4.В гинекологии.5. 10% раствор вводится внутривенно при желудочных, кишечных и легочных кровотечениях.6. 5% раствор применяют в виде клизмы. 7.Оказывает терапевтический эффект при приеме ванн. 8.В косметологии для укрепления ногтей, волос, при грибковых заболеваниях. 3.Изотонические растворы(от Изо... и греч. tónos — напряжение)- растворы с одинаковым осмотическим давлением в биологии и медицине — природные или искусственно приготовленные растворы с таким же осмотическим давлением, как и в содержимом животных и растительных клеток, в крови и тканевых жидкостях. В нормально функционирующих животных клетках внутриклеточное содержимое обычно изотонично внеклеточной жидкости. При сильном нарушении изотоничности растворов в растительной клетке и окружающей среде вода и растворимые вещества свободно перемещаются в клетку или обратно, что может привести к расстройству нормальных функций клетки . Как правило, по своему составу и концентрации И. р. близки к морской воде. Для теплокровных животных изотоничны 0,9%-ный раствор NaCl и 4,5%-ный раствор глюкозы. И. р., близкие по составу, pH, буферности и другим свойствам к сыворотке крови, называются физиологическими растворами (раствор Рингера для холоднокровных животных и растворы Рингера — Локка и Рингера — Тироде для теплокровных животных). В кровезамещающие И. р. для создания коллоидно-осмотического давления вводят высокомолекулярные соединения (декстран, поливинол и др.). Медицина - 1.Для восполнения жидкости в организме ( понос, рвота, при кровопотере, ожогах, высокой температуре тела).2 В качестве дезинтоксикационной терапии (различные инфекционные заболевания, отравления). 3.Для ингаляций ( в чистом виде и в сочетании с другими лекарственными средствами).4. Для промывания носа, глаз, контактных линз. Как растворитель для целого ряда лекарственных средств. 20. Диффузия и скорость диффузии. Сравнение диффузии с осмосом. |
