6 ьема. Введение Понятие железодефицитной анемии
 Скачать 0.49 Mb. Скачать 0.49 Mb.
|
Обмен железаВ организме человека железо не синтезируется. При рождении ребенок имеет около 300-500 мг железа, полученного от матери через плаценту. После рождения ребенка запас железа увеличивается за счет поступления пищевого железа: сначала — из лактоферрина молочных продуктов, в дальнейшем — за счет гемового железа и железа растительных продуктов. После достижения возрастной нормы (3-5 г), содержание железа поддерживается на постоянном уровне. В норме ежедневно теряется около 2 мг железа. Эти потери включают железо, удаляющееся со слущивающимся эпителием кожи и ЖКТ, с потоотделением. Примерно такое же количество железа ежедневно поступает с пищей. Процесс всасывания регулируется гепсидином: если содержание железа в организме избыточно, железо задерживается в энтероцитах и в дальнейшем удаляется из организма вместе со слущивающимся эпителием. В случае недостатка железо поступает в кровоток и соединяется с трансферрином Включение железа в трансферрин возможно при наличии двух условий: 1) выход железа из энтероцита обеспечивается ферропортином; 2) двухвалентное железо переводится в трехвалентное гефестином. В составе трансферрина всосавшееся железо поступает через систему воротной вены в печень, где часть железа остается в гепатоцитах и хранится в виде запасного фонда, преимущественно внутриклеточно в составе ферритина. Печень располагает наиболее значительными запасами железа, которое при необходимости может быстро освобождаться для метаболических процессов. Большая часть железа транспортируется в костный мозг для синтеза гемоглобина. Меньшая часть железа доставляется другим клеткам-потребителям, имеющим трансферриновые рецепторы. В основном это активно пролиферирующие клетки с высокой потребностью в железе. Утилизация железа, доставленного трансферрином к клеткам потребителям, осуществляется с помощью трансферриновых рецепторов, которые расположенны на поверхностной мембране клетки. С помощью эндоцитоза комплекс железа с трансферрином попадает в клетку, имеющую трансферриновые рецепторы. В клетке ионы железа освобождаются, а комплекс трансферрина с рецепторами расщепляется, вслед за чем рецепторы возвращаются на поверхность клетки, а в плазму поступает белковая часть трансферритина, лишенная железа, называемая апотрансферрином. Большая часть железа, поступившего в цитоплазму клетки, используется для синтеза гемоглобина, а в неэритроидных клетках — для синтеза ДНК, РНК и железосодержащих ферментов. Из костного мозга железо в составе эритроцитов поступает в кровоток, где циркулирует в течение 3–4 мес. В дальнейшем специализированные макрофаги селезенки и печени захватывают и разрушают состарившиеся (или поврежденные) эритроциты, осуществляют деградацию гемоглобина и освобождение железа, которое затем вновь поступает в плазму и связывается с трансферрином. Соединение железа с трансферрином возможно при наличии ферропортина, который обеспечивает выход железа из макрофага в плазму, и церулоплазмина, который окисляет двухвалентное железо в трехвалентное. Далее железо вновь поступает в плазму и повторно утилизируется, т. е. доставляется к активно пролиферирующим, преимущественно эритроидным клеткам костного мозга, синтезирующим гемоглобин. Ежедневно для эритропоэза требуется около 20–30 мг железа, тогда как ежедневное поступление пищевого железа из кишечника составляет всего 1–2 мг. Необходимые 20–30 мг железа ежедневно возвращаются в циркуляцию макрофагами селезенки и печени. Этот процесс носит название «рециркуляция железа». Процессы всасывания, рециркуляции и хранения запасов железа регулируются гепсидином, который продуцируется клетками печени. После соединения гепсидина с молекулами ферропортина, расположенными на поверхностной мембране клетки, комплекс гепсидин–ферропортин поступает внутрь клетки и разрушается в лизосомах. В результате выключения функции ферропортина железо накапливается внутри энтероцитов, макрофагов и гепатоцитов, т. е. блокируются процессы всасывания, рециркуляции и освобождения железа из запасных фондов, что ведет к снижению содержания железа в плазме. В физиологических условиях продукция гепсидина клетками печени регулируется уровнем железа в крови и степенью оксигенации ткани печени. Повышение концентрации железа в крови сопровождается повышением продукции гепсидина, что ведет к внутриклеточной секвестрации железа и, как следствие, к развитию гипоферремии. Снижение концентрации железа в крови подавляет продукцию гепсидина, что обусловливает восстановление функции ферропортина, активацию всасывания и рециркуляции, повышение уровня железа в крови. Таким образом, поддерживается баланс между поступлением и потреблением железа в норме. При патологических условиях продукция гепсидина регулируется провоспалительными цитокинами. Схема всасывания железа. При всасывании железа большую роль играет слизистая кишечника. Гемовое железо всасывается как железопорфириновый комплекс с помощью специальных рецепторов. Не подвержено влиянию различных факторов в просвете кишечника. Негемовое железо всасывается как разновидность железа поступающего из солей железа. Всасывается в виде железа, образующегося из комплексов Fe (III). Находятся под влиянием обмена таких железо-связывающих белков, как трансферрин, муцины, интегрины, и мобилферрин. Обе формы усваиваются на уровне эпителиоцитов двенадцатиперстной кишки и проксимального отдела тощей кишки. В желудке возможна абсорбция только негемового железа, на долю которого приходится не более 20%. В принципе, все клетки имеют трансферриновые рецепторы и захват железа клетками определяется количеством трансферриновых рецепторов. В норме заняты не более, чем 30 % железосвязывающих рецепторов трансферрина плазмы. В эпителиоцитах гемовое железо распадается на ионизированное железо, окись углерода и билирубин, причем усвоение его не связано с кислотнопептической активностью желудочного сока. Оксигеназа гема, специальный фермент, стимулирует распад комплекса железа и порфирина. Негемовое железо, поступившее с пищей, находится в окисленной форме Fe3+. Основной барьер для железа – это мембрана между энтероцитом и капилляром, где присутствует специфический переносчик двухвалентных катионов, связывающий Fе2+. Данный белок синтезируется только в криптах двенадцатиперстной кишки. Железо захватывается апикальной поверхностью энтероцита и при помощи дуоденального цитохрома В восстанавливается в Fe2+ и движется к базолатеральной поверхности энтероцита с помощью дивалентного (дуоденального) металлотранспортера (DМТ1), далее транспортируется ферропортином через мембрану в плазму. В транспорте железа через мембрану принимает участие, кроме ферропортина, также и гефестин, который окисляет Fe2+ в Fe3+, поскольку ферропортин может взаимодействовать лишь с Fe2+, а трансферрин связывает лишь Fe3+ и доставляет его к тканям, органам и костному мозгу. Следующий механизм всасывания железа: альтернативный железотранспортный (интегрин-мобилферриновый) путь - характерен только для трехвалентного железа. Fe3+ связывается с муцином, который передает его на интегрин с последующим переходом в энтероцит и взаимодействует с мобилферрином. Схема всасывания представлена на рисунке 1. 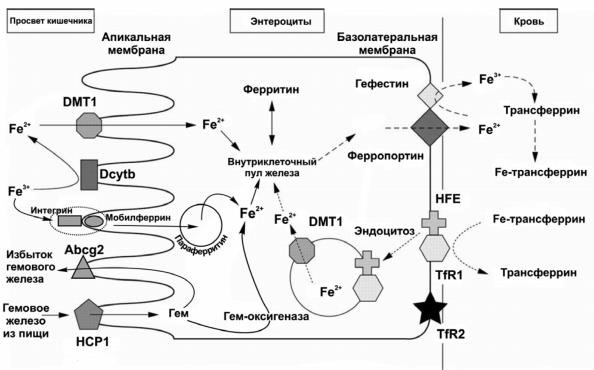 |
