Методичка по биологии. Методичка по биологии Костюков А.А.. Занятие 15 Сцепленное наследование признаков. Наследование признаков, контролируемых генами х и ухромосом человека
 Скачать 1.35 Mb. Скачать 1.35 Mb.
|
|
Оперон состоит из следующих частей: Оператор – участок ДНК, связанный с белком-репрессором. До тех пор, пока эта связь не нарушена, РНК-полимераза не будет считывать информацию. Промотор – определенная последовательность нуклеотидов, которая связывается с ферментом РНК-полимеразой. Процесс связывания является первым этапом в последующей транскрипции. Ряд структурных генов, кодирующих информацию о синтезе какого-либо вещества. Терминатор – участок ДНК, на котором заканчивается считывание. Ген регулятор кодирует синтез белка репрессора. Этот белок взаимодействует с оператором и блокирует его. Если заблокирован оператор, то блокируется и часть промотора. РНК-полимераза не может присоединиться к промотору, поэтому транскрипция не происходит и синтез белка не идёт. Это не активное состояние оперона. При связывании белка репрессора ген оператор и промотор открыты, РНК-полимераза начинает процесс транскрипции, и происходит синтез белка. Что же связывает белок репрессор? -- вещества, которые могут находиться в клетке или поступающие в неё извне. Эти вещества называются индукторами (индукция – наведение, запуск). Допустим, что индуктором является поступившая в клетку глюкоза. Индуктор связывается с белком репрессором и блокирует его. Теперь ген оператор освобождается от белка репрессора и запускает процесс синтеза белка фермента, который будет переваривать глюкозу. Такое состояние оперона называется активным. Синтез белка будет идти до тех пор, пока образовавшийся белок (фермент) не переварит всю глюкозу. При этом освобождается репрессор, который блокирует ген оператор и прекращает процесс транскрипции. У эукариот выделяют несколько уровней регуляции экспрессии генов. на уровне инициации транскрипции на уровне процессинга первичного транскрипта в зрелую мРНК РНК – интерференция на уровне трансляции посттрансляционные механизмы регуляции (на уровне процессинга белка) Регуляция экспрессии генов на уровне инициации транскрипции. В этом процессе принимают участие дополнительные регуляторные элементы: промоторы, энхансеры, сайленсеры и инсуляторы. промоторы – последовательности нуклеотидов, расположенные близко от кодирующих последовательностей гена. Промоторы связывают РНК полимеразу. энхансеры (усилители) и сайленсеры (глушители). Они могут располагаться от гена на расстоянии в несколько тысяч пар нуклеотидов. Их действие основано на связывании со специфическими белками-регуляторами. Белок-регулятор может усиливать (в энхансере) или ослаблять (в сайленсере) инициацию транскрипции путём изменения активности промотора. Энхансеры в свою очередь находятся под контролем инсуляторов. Инсуляторы – последовательности ДНК, которые способны блокировать взаимодействие между энхансером и промотором, но только в том случае, если находятся между ними. Регуляция экспрессии генов на уровне процессинга. Это регуляция функциональных генов в результате альтернативного сплайсинга. При альтернативном сплайсинге образуются различные формы мРНК из одного и того же гена и, как результат, образование разных белков (изоформ белка) РНК–интерференция – подавление экспрессии генов у эукариот на посттранскрипционном уровне, вызванное короткими интерферирующими РНК (миРНК). Регуляторные малые интерферирующее РНК – это двухцепочные РНК длиной 19-25 п.н., которые вызывают разрушение мРНК. Они дают сигнал ферментам (эндонуклеазам), которые разрушают мРНК, а, значит, блокируют трансляцию и прекращают работу генов. РНК–интерференция обнаружена у большинства эукариотов, включая человека. Регуляция экспрессии генов на уровне трансляции осуществляется в трёх вариантах. позитивной и негативной регуляции. 1. позитивная регуляция осуществляется на основе сродства мРНК с факторами инициации. Факторы инициации (специфические белки) катализируют образование инициаторного комплекса. 2. негативная регуляция осуществляется с помощью белков-репрессоров, которые связываясь с мРНК, блокируют инициацию трансляции. 3. подавление трансляции с помощью регуляторных микроРНК, которые связываются с мРНК-мишенью, блокируют трансляцию и запускают процесс разрушения мРНК. мкРНК – одноцепочные РНК длиной 18-24 нуклеотида, кодируемые специальными генами. Посттрансляционные механизмы регуляции. Синтезируемые при трансляции полипептиды подвергаются многочисленным превращениям и модификациям: сборка белка (фолдинг) – процесс, при котором белок принимает характерную для его функционирования пространственную структуру отщепление фрагментов полипептидной цепи химические изменения белка, заключающиеся в присоединении фосфатной группы (фосфорилирование), ацетильной группы СН3-СО- (ацетилирование) или остатков сахаров – пентоз или гексоз (гликозилирование). достижение места своего функционирования 4. Классификация генов: структурные и регуляторные. Все гены клетки в организме можно разделить на 2 группы, это: – структурные гены, которые отвечают за все белки организма, за рРНК, и тРНК. – регуляторные гены, которые соответственно регулируют работу структурных генов. 5. Цитоплазматическая наследственность. Главная роль в передаче наследственных свойства принадлежит хромосомам. С ними связаны закономерности, открытые Г. Менделем. Но ряд органоидов, расположенных в цитоплазме содержит ДНК (митохондрии, пластиды). Их ДНК способна к репликации, и с ней может быть связана передача цитоплазматической наследственности. Существуют сорта львиного зева, ночной красавицы и некоторых других растений, у которых наряду с зелёными листьями встречаются пёстрые, с белыми пятнами – участкам, лишёнными хлорофилла. В связи с тем, что организм, образуемый вследствие оплодотворения, получает цитоплазматические структуры главным образом от яйцеклетки, цитоплазматическое наследование признаков осуществляется по материнской линии. В клетках прокариот и эукариот обнаруживаются плазмиды – отрезки ДНК, имеющие кольцевую или линейную форму и способные к самостоятельной (независимо от ядра) репликации. У бактерии наблюдается передача плазмид от клетки к клетке при их непосредственном контакте, а распределение их по дочерним клеткам при делении происходит случайно. Наличие плазмид может обеспечивать устойчивость бактерий к определённым антибиотикам. У растений и животных плазмиды могут существенно влиять на свойства многоклеточного организма. ЗАНЯТИЕ 19 Изменчивость. Формы изменчивости. Генные мутации. Понятие о генных болезнях. Определение изменчивости. Классификация ее форм. Изменчивость – есть общее свойство живых организмов, заключающееся в изменении наследственных признаков в ходе онтогенеза (индивидуального развития). Изменчивость организмов делят на два крупных типа: 1. фенотипическую, не затрагивающую генотип и не передающуюся по насл-ву 2. генотипическую, изменяющую генотип и поэтому передающуюся по насл-ву. Генотипическая изменчивость подразделяется на комбинативную и мутационную. Мутационная изменчивость включает геномные, хромосомные и генные мутации. Геномные мутации подразделяется на полиплоидию и анеуплоидию Хромосомные мутации подразделяется на делеции, дупликации, инверсии, транслокации Фенотипическая изменчивость. Норма реакции генетически детерминированных признаков. Адаптивный характер модификаций. Фенокопии. Фенотипическая изменчивость (или ненаследственная, модификационная) – это изменение фенотипических признаков организма под действием факторов внешней среды, без изменения генотипа. Например: окраска шерсти у гималайского кролика в зависимости от температуры среды обитания: на выбритом месте при температуре выше + 2С0, вырастает белая шерсть; при температуре ниже + 2С0 вырастает чёрная шерсть. Норма реакции – это диапазон изменчивости, в пределах которого один и тот же генотип способен давать различные фенотипы. широкая норма реакции – когда колебания признака идут в широких пределах (например: загар, количество молока). узкая норма реакции – когда колебания признака незначительны (например: жирность молока). однозначная норма реакции – когда признак не изменяется, ни при каких условиях (например: группы крови, цвет глаз, разрез глаз). Адаптивный характер модификаций заключается в том, что модификационная изменчивость позволяет организму приспособиться к изменяющимся условиям среды. Поэтому модификации всегда полезны. Если во время эмбриогенеза на организм воздействуют неблагоприятные факторы, то могут появляться фенотипические изменения, выходящие за пределы нормы реакции и не носящие адаптивного характера; их называют морфозы развития. Например, ребёнок рождается без конечностей или с заячьей губой. Фенокопии – это морфозы развития, которые очень трудно отличить от наследственных изменений (заболеваний). Например: если беременная женщина переболела краснухой, у неё может родиться ребёнок с катарактой. Но эта патология может появиться и в результате мутации. В первом случае речь идет о фенокопии. Диагноз «фенокопия» важен для будущего прогноза, так как при фенокопии генетический материал не изменяется. Следовательно, у ребёнка с катарактой, рождённого больной краснухой женщиной, свои дети не будут больны катарактой. Комбинативная изменчивость. Значение комбинативной изменчивости в обеспечении генетического разнообразия людей. Комбинативная изменчивость – это возникновение у потомков новых комбинаций генов, которых не было у их родителей. Комбинативная изменчивость связана: с кроссинговером в профазу мейоза 1. с независимым расхождением гомологичных хромосом в анафазу мейоза 1. со случайным сочетанием гамет при оплодотворении. Значение комбинативной изменчивости – обеспечивает генетическое разнообразие особей в пределах вида, что важно для естественного отбора и эволюции. Мутационная изменчивость. Основные положения теории мутаций. Гюго де Фриз голландский ученый ввел в 1901 году термин "мутация". Мутация – это явление прерывистого скачкообразного изменения наследственного признака. Процесс возникновения мутаций называется мутагенез, а организм, который приобретает новые признаки в процессе мутагенеза, называется – мутант. Основные положения теории мутаций по Гюго де Фризу. мутации возникают внезапно без всяких переходов. возникшие формы вполне устойчивы. мутации являются качественными изменениями. мутации происходят в различных направлениях: они могут быть полезными, вредными и нейтральными. одни и те же мутации могут возникать повторно. Классификация мутаций. По происхождению. Спонтанные мутации. Самопроизвольные мутации или естественные, возникают в обычных природных условиях. Индуцированные (наведённые) мутации. Они возникают при воздействии на организм мутагенных факторов. физические (ионизирующие лучи, УФЛ, высокая температура и т.п.) химические (соли тяжёлых Ме, азотистая кислота, свободные радикалы, бытовые и промышленные отходы, лекарства). биологические (вирусы, продукты жизнедеятельности паразитов). По месту возникновения. Соматические мутации возникают в соматических клетках и наследуются потомками тех клеток, в которых возникли. Из поколения в поколение не передаются. Генеративные мутации возникают в половых клетках и передаются из поколения в поколение. По характеру изменений фенотипа. Морфологические мутации, характеризующиеся изменением строения органа или организма в целом (заячья губа, волчья пасть, шестипалость). Физиологические мутации, характеризующиеся изменением функций органа или организма в целом (при отсутствии тех или иных ферментов возникают болезни обмена веществ). Биохимические мутации, связанные с изменением структуры белка. По влиянию на жизнеспособность организма. 1. Летальные – организм погибает на эмбриональной стадии (100%) 2. Полулетальные – организм погибает до размножения (смертность 50-90%) 3. Условно летальные мутации, в одних условиях организм погибает, а в других условиях выживает (галактоземия). 4. Полезные мутации повышают жизнеспособность организма (используются в селекции). По характеру изменения наследственного материала. Генные мутации. Хромосомные мутации. геномные мутации Генные мутации. Механизмы возникновения спонтанных генных мутаций. Генные мутации или точковые мутации – это мутации, которые возникают в генах на уровне нуклеотидов, при этом изменяется структура гена, изменяется молекула мРНК, изменяется последовательность аминокислот в белке, в организме изменяется признак. Виды генных мутаций: миссенс мутации – замена 1 нуклеотида в триплете на другой приведет к тому, что в полипептидную цепь белка будет включаться другая аминокислота, которой в норме не должно быть, а это приведет к тому, что изменятся свойства и функции белка. Пример: замена глутаминовой кислоты на валин в молекуле гемоглобина. ЦТТ – глутаминовая кислота, ЦАТ – валин Если такая мутация происходит в гене, который кодирует β цепь белка гемоглобина, то в β цепь вместо глютаминовой кислоты включается валин. В результате такой мутации изменяются свойства и функции белка гемоглобина – вместо нормального HbA появляется HbS. В итоге у человека развивается серповидноклеточная анемия (форма эритроцитов изменяется). нонсенс мутации – замена 1 нуклеотида в триплете на другой приведет к тому, что генетически значащий триплет превратится в стоп кодон, что приводит к обрыву синтеза полипептидной цепи белка. Пример: УАЦ – тирозин. УАА – стоп кодон. мутации со сдвигом рамки считывания наследственной информации. Если в результате генной мутации у организма будет появляться новый признак (например, полидактилия), то они называются неоморфные. если в результате генной мутации организм утрачивает признак (например, при ФКУ исчезает фермент) то они называются аморфные. сеймсенс мутации – замена нуклеотида в триплете приводит к появлению триплета-синонима, который кодирует тот же самый белок. Это связано с вырожденностью генетического кода. Например: ЦТТ – глютамин ЦТЦ – глютамин. Механизмы возникновения генных мутаций (замена, вставка, выпадение). ДНК состоит из 2-х полинуклеотидных цепей. Сначала изменение возникает в 1-й цепи ДНК – это полумутационное состояние или “первичное повреждение ДНК”. Каждую секунду в клетке имеет место 1 первичное повреждение ДНК. Когда повреждение переходит на вторую цепь ДНК то, говорят о том, что произошла фиксация мутации, то есть возникла “полная мутация”. Первичные повреждения ДНК возникают при нарушении механизмов репликации, транскрипции, кроссинговера Частота генных мутаций. Мутации прямые и обратные, доминантные и рецессивные. У человека частота мутаций = 1х10–4 – 1х10–7, то есть в среднем 20–30% гамет у человека в каждом поколении являются мутантными. У дрозофилы частота мутаций = 1х10–5, то есть 1 гамета из 100 тысяч несет генную мутацию. Прямая мутация (рецессивная) – это мутация гена из доминантного состояния в рецессивное состояние: А → а. Обратная мутация (доминантная) – это мутация гена из рецессивного состояния в доминантное состояние: а → А. Генные мутации встречаются у всех организмов, гены мутируют в различных направлениях, а также с различной частотой. Гены, которые редко мутируют называются – стабильные, а гены, которые часто мутируют называются – мутабельные. Закон гомологических рядов в наследственной изменчивости Н.И.Вавилова. Мутирование происходит в самых различных направлениях, т.е. случайно. Однако эти случайности подчиняются закономерности, обнаруженной в 1920г. Вавиловым. Он сформулировал закон гомологичных рядов в наследственной изменчивости. "Виды и роды генетически близкие характеризуются сходными рядами наследственной изменчивости с такой правильностью, что, зная ряд форм в пределах одного вида, можно предвидеть существование параллельных форм у других видов и родов". Этот закон позволяет предсказать наличие определённого признака у особей различных родов одного семейства. Так было предсказано наличие в природе безалкалоидного люпина, т.к. в семействе бобовых есть роды бобов, гороха, фасоли, не содержащие алкалоиды. В медицине закон Вавилова позволяет использовать животных, генетически близких человеку, в качестве генетических моделей. На них ставят эксперименты по изучению генетических болезней. Например, катаракта изучается на мышах и собаках; гемофилия – на собаках, врождённая глухота – на мышах, морских свинках, собаках. Закон Вавилова позволяет предвидеть появление индуцированных мутаций, неизвестных науке, которые могут использоваться в селекции для создания ценных для человека форм растений. Антимутационные барьеры организма. Точность репликации ДНК. Иногда в ходе репликации возникают ошибки, тогда включаются механизмы самокоррекции, которые направлены на устранение неправильного нуклеотида. Важную роль играет фермент ДНК-полимераза, и частота ошибок снижается в 10 раз (с 10–5до 10–6). Вырожденность генетического кода. 1 аминокислоту могут кодировать несколько триплетов, поэтому замена 1 нуклеотида в триплете в ряде случаев не искажает наследственную информацию. Например, ЦТТ и ЦТЦ – глутаминовая кислота. Экстракопирование некоторых генов отвечающих за важные макромолекулы: рРНК, тРНК, белки гистоны, т.е. образуется много копий этих генов. Эти гены входят в состав умеренно повторяющихся последовательностей. Избыточность ДНК – 99% является избыточной и мутагенный фактор чаще попадает в эти 99% бессмысленных последовательностей. Парность хромосом в диплоидном наборе. В гетерозиготном состоянии многие вредные мутации не проявляются. Выбраковка мутантных половых клеток. Репарация ДНК. Репарация генетического материала. Репарация ДНК – удаление первичных повреждений из ДНК и замена их нормальными структурами. Выделяют две формы репарации: световую и темновую А. Световая репарация (или ферментативная фотореактивация). Ферменты репарации активны только в присутствии света. Эта форма репарации направлена на удаление первичных повреждений ДНК вызванных действием УФЛ. П  од действием УФЛ в ДНК активируются пиримидиновые азотистые основания, что приводит к тому, что возникают связи между пиримидиновыми азотистыми основаниями, которые располагаются рядом в одной цепи ДНК, то есть образуются пиримидиновыедимеры. Чаще всего возникают связи: Т=Т; Т=Ц; Ц=Ц. од действием УФЛ в ДНК активируются пиримидиновые азотистые основания, что приводит к тому, что возникают связи между пиримидиновыми азотистыми основаниями, которые располагаются рядом в одной цепи ДНК, то есть образуются пиримидиновыедимеры. Чаще всего возникают связи: Т=Т; Т=Ц; Ц=Ц.В норме в ДНК пиримидиновых димеров нет. Образование их приводит к тому, что искажается наследственная информация и нарушается нормальный ход репликации и транскрипции, что приводит впоследствии к генным мутациям. Суть фотореактивации: в ядре существуют специальный (фотореактивирующий) фермент, который активен только в присутствии света, этот фермент разрушает пиримидиновые димеры, то есть разрывает связи, которые возникли между пиримидиновыми азотистыми основаниями под действием УФЛ. Темновая репарация происходит в темноте и на свету, то есть активность ферментов не зависит от присутствия света. Она делится на дорепликативная репарацию и пострепликативную репарацию. Дорепликативная репарация происходит до репликации ДНК, в этом процессе участвует много ферментов: Эндонуклеаза Экзонуклеаза ДНК- полимераза ДНК - лигаза Допустим, в ДНК имеется первичное повреждение. 1  этап. Фермент эндонуклеаза находит поврежденный участок и разрезает его. этап. Фермент эндонуклеаза находит поврежденный участок и разрезает его. 2  этап. Фермент экзонуклеаза удаляет поврежденный участок из ДНК (эксцизия) в результате образуется брешь. этап. Фермент экзонуклеаза удаляет поврежденный участок из ДНК (эксцизия) в результате образуется брешь. 3 этап. Фермент ДНК полимераза синтезирует недостающий участок. Синтез происходит по принципу комплементарности. 4  этап. Фермент лигаза соединяют или сшивают вновь синтезированный участок с цепью ДНК. Таким образом, первичное повреждение в ДНК устраняется. этап. Фермент лигаза соединяют или сшивают вновь синтезированный участок с цепью ДНК. Таким образом, первичное повреждение в ДНК устраняется. Пострепликативная репарация. Допустим, в ДНК имеется первичное повреждение. 1  этап. Начинается процесс репликации ДНК. Фермент ДНК-полимераза синтезирует новую цепь полностью комплементарную старой неповрежденной цепи. этап. Начинается процесс репликации ДНК. Фермент ДНК-полимераза синтезирует новую цепь полностью комплементарную старой неповрежденной цепи. 2  этап. Фермент ДНК полимераза синтезирует другую новую цепь, но участок, где находится повреждение, он обходит. В результате во второй новой цепи ДНК образовалась брешь. этап. Фермент ДНК полимераза синтезирует другую новую цепь, но участок, где находится повреждение, он обходит. В результате во второй новой цепи ДНК образовалась брешь. 3  этап. По окончании репликации фермент ДНК полимераза синтезирует недостающий участок комплементарно новой цепи ДНК. этап. По окончании репликации фермент ДНК полимераза синтезирует недостающий участок комплементарно новой цепи ДНК. 4   этап. Затем фермент лигаза соединяют вновь синтезированный участок с цепью ДНК, где имелась брешь. Таким образом, первичное повреждение ДНК не перешло на другую новую цепь, то есть не произошла фиксация мутации. этап. Затем фермент лигаза соединяют вновь синтезированный участок с цепью ДНК, где имелась брешь. Таким образом, первичное повреждение ДНК не перешло на другую новую цепь, то есть не произошла фиксация мутации.В дальнейшем первичное повреждение ДНК может быть ликвидировано в ходе дорепликативной репарации. Мутации, связанные с нарушением репарации ДНК и их роль в патологии. Способность к репарации у организмов выработалась и закрепилась в ходе эволюции. Чем выше активность репарирующих ферментов, тем стабильнее наследственный материал. За ферменты репарации отвечают соответствующие гены, поэтому если происходит мутация в этих генах, то снижается активность репарирующих ферментов. У человека при этом возникают тяжелые наследственные заболевания, которые связаны со снижением активности репарирующих ферментов. Таких заболеваний у человека больше 100. Некоторые из них: Анемия Фанкони – уменьшение количества эритроцитов, потеря слуха, нарушения в ССС, деформация пальцев, микроцефалия. Сидром Блума – малый вес новорождённого, замедление роста, повышенная восприимчивость в вирусной инфекции, повышенный риск онкологических заболеваний. Характерный признак: при непродолжительном пребывании на солнечном свету на коже лица появляется пигментация в форме бабочки (расширение кровеносных капилляров). Пигментная ксеродермия – на коже от света появляются ожоги, которые скоро перерождаются в рак кожи (у таких больных рак возникает в 20.000 раз чаще). Больные вынуждены жить при искусственном освещении. Частота заболевания – 1 : 250.000 (Европа, США), и 1 : 40.000 (Япония) Два вида прогерий – преждевременное старение организма. Генные болезни, механизмы их развития, наследования, частота возникновения. Генные болезни (или молекулярные болезни) достаточно широко представлены у человека, их насчитывается более 1000. Особую группу среди них составляют врожденные дефекты обмена веществ. Впервые эти заболевания описал А. Гарод в 1902 году. Симптоматика этих заболеваний различна, но всегда имеет место нарушение превращения веществ в организме. При этом одни вещества будут в избытке, другие в недостатке. Например, в организм поступает вещество (А) и превращается далее под действием ферментов в вещество (В). Далее вещество (В) должно превращаться в вещество (С), но этому мешает мутационный блок,  в результате вещество (С) будет в недостатке, а вещество (В) в избытке. в результате вещество (С) будет в недостатке, а вещество (В) в избытке. А  → В → → В → Примеры некоторых болезней, обусловленных врожденным дефектом обмена веществ. ФКУ (фенилкетонурия, врожденное слабоумие). Генное заболевание, наследуется по аутосомно-рецессивному типу, встречается с частотой = 1:10.000. Фенилаланин является незаменимой аминокислотой для построения белковой молекулы и, кроме того, служит предшественником гормонов щитовидной железы (тироксина), адреналина и меланина. Аминокислота фенилаланин в клетках печени должна превращаться с помощью фермента (фенилаланин-4-гидроксилазы) в тирозин. Если отсутствует фермент, отвечающий за данное превращение, или снижена его активность то содержание фенилаланина в крови будет резко повышено, а содержание тирозина понижено. Избыток фенилаланина в крови приводит к появлению его производных (фенилуксусной, фенилмолочной, фенилпировиноградной и других кетоновых кислот), которые выделяются с мочой, а также оказывают токсическое воздействие на клетки центральной нервной системы, что приводит к слабоумию. При своевременной постановке диагноза и переводе младенца на диету, лишенную фенилаланина, развитие заболевания можно предупредить. Альбинизм общий. Генное заболевание, наследуется по аутосомно-рецессивному типу. В норме аминокислота тирозин участвует в синтезе тканевых пигментов. Если возникает мутационный блок, отсутствует фермент или снижена его активность, то тканевые пигменты не синтезируются. В этих случаях кожа имеет молочно-белый цвет, волосы очень светлые, вследствие отсутствия пигмента в сетчатке просвечивают кровеносные сосуды, глаза имеют красновато-розовый цвет, и повышенную чувствительность к свету. Алькапнонурия. Генное заболевание, наследуется по аутосомно-рецессивному типу, встречается с частотой = 3-5:1.000.000. Заболевание связано с нарушением превращения гомогентизиновой кислоты, в результате чего эта кислота накапливается в организме. Выделяясь с мочой, эта кислота приводит к развитию заболеваний почек, кроме того, подщелоченная моча при этой аномалии быстро темнеет. Также заболевание проявляется окрашиванием хрящевых тканей, в пожилом возрасте развивается артрит. Таким образом, заболевание сопровождается поражением почек и суставов. Генные болезни, связанные с нарушением обмена углеводов. Галактоземия. Генное заболевание, наследуется по аутосомно-рецессивному типу, встречается с частотой = 1:35.000-40.000 детей. В крови новорождённого содержится моносахарид галактоза, который образуется при расщеплении дисахарида молока лактозы на глюкозу и галактозу. Галактоза непосредственно не усваивается организмом, она должна быть переведена специальным ферментом в усваиваемую форму – глюкоза-1-фосфат. Наследственная болезнь галактоземия обусловлена нарушением функции гена, контролирующего синтез белка-фермента, превращающего галактозу в усваиваемую форму. В крови больных детей будет очень мало этого фермента и много галактозы, что устанавливается биохимическим анализом. Если диагноз поставлен в первые дни после рождения ребенка, то его кормят смесями, где нет молочного сахара, и ребёнок нормально развивается. В противном случае ребёнок вырастает слабоумным. Муковисцидоз. Генное заболевание, наследуется по аутосомно-рецессивному типу, встречается с частотой = 1:2.000-2.500. Заболевание связано с мутацией гена, который отвечает за белок-переносчик, встроенный в плазматическую мембрану клеток. Этот белок регулирует проницаемость мембраны к ионам Na и Ca. Если нарушена проницаемость этих ионов в клетках экзокринных желез, то железы начинают вырабатывать густой, вязкий секрет, который закрывает протоки экзокринных желез. Выделяют легочную и кишечную формы муковисцидоза. Синдром Марфана. Генное заболевание, наследуется по аутосомно-доминантному типу. Связано с нарушением обмена белка фибриллина в соединительной ткани, что проявляется комплексом признаков: «паучьи» пальцы (арахнодактилия), высокий рост, подвывих хрусталика, пороки сердца и сосудов, повышенный выброс в кровь адреналина, сутулость, впалая грудь, высокий свод стопы, слабость связок и сухожилий и т.д. Впервые описано в 1896 году французским педиатром Антонио Марфаном. ЗАНЯТИЕ 20 Структурные мутации хромосом. Фенотипический эффект. 1. Структурные мутации хромосом (хромосомные аберрации). Выделяют следующие виды хромосомных аберраций. – делеции – дупликации – инверсии – кольцевые хромосомы – транслокации – транспозиции При данных мутациях изменяется структура хромосом, изменяется порядок расположения генов в хромосомах, изменяется доза генов в генотипе. Эти мутации встречаются у всех организмов, они классифицируются следующим образом. По происхождению: спонтанные – они возникают в нормальных условиях обитания, и их причина пока не ясна индуцированные – природа фактора, вызвавшего мутацию известна По месту возникновения: соматические – затрагивают наследственный материал соматических клеток, не передаются при половом размножении и наследуются только при бесполом размножении генеративные – затрагивают наследственный материала гамет, обязательно передаются потомкам По влиянию на жизнеспособность организма: полезные (крайне редко) вредные (очень часто) Мутации могу быть сбалансированными и несбалансированными: сбалансированные – система генотипа не изменяется, значит, не меняется и фенотип несбалансированные – изменяется система генотипа, значит, изменяется и фенотип Если мутация затрагивает две хромосомы, говорят о межхромосомных перестройках. Если мутация затрагивает 1 хромосому, говорят о внутрихромосомных перестройках. Механизмы возникновения структурных мутаций хромосом. гипотеза «разрыв-соединение». Предполагают, что в одной или нескольких хромосомах происходят разрывы. Образуются участки хромосом, которые затем соединяются, но в иной последовательности. Если разрыв происходит до репликации ДНК, то в этот процесс вовлекаются две хроматиды – это изохроматидный разрыв. Если разрыв происходит после репликации ДНК, то в процесс вовлекается одна хроматида – это хроматидный разрыв. вторая гипотеза: между негомологичными хромосомами происходит процесс подобный кроссинговеру, т.е. негомологичные хромосомы обмениваются участками. Делеции, их сущность, формы, фенотипический эффект. Псевдодоминирование Делеция (нехватка) – потеря участка хромосомы. в хромосоме может произойти один разрыв, и она потеряет концевой участок, который будет разрушен ферментами (дефишенси) в хромосоме может быть два разрыва с потерей центрального участка, который также будет разрушен ферментами (интерстициальная делеция). В гомозиготном состоянии делеции всегда летальны, в гетерозиготном состоянии они проявляются множественными пороками развития. Выявление делеций: дифференциальное окрашивание хромосом по фигуре петли, которая образуется во время коньюгации гомологичных хромосом в профазу мейоза 1. Петля возникает на нормальной хромосоме. Впервые делеция была изучена у мушки дрозофилы, при этом произошла потеря участка Х хромосомы. В гомозиготном состоянии эта мутация летальна, а в гетерозиготном состоянии она проявляется фенотипически вырезкой на крыле (Notch-мутация). При анализе этой мутации было выявлено особое явление, которое получило название псевдодоминирование. При этом фенотипически проявляется рецессивный аллель, так как участок хромосомы с доминантным аллелем утрачен вследствие делеции. У человека делеции чаще происходят в хромосомах с 1 по 18. Например, делеция короткого плеча пятой хромосомы в гетерозиготном состоянии проявляется фенотипически, как синдром "кошачьего крика". Ребёнок рождается с большим числом патологий, живет от 5 дней до месяца (очень редко до 10 лет), его плач напоминает резкое мяуканье кота. В 21 или 22 хромосоме стволовых кроветворных клеток может произойти интерстициальная делеция. В гетерозиготном состоянии она проявляется фенотипически как злокачественная анемия. Дупликации, инверсии, кольцевые хромосомы. Механизм возникновения. Фенотипическое проявление. Дупликация – удвоение какого-то участка хромосомы (этот участок может повторяться многократно). Дупликации могут быть прямыми и обратными. При данных мутациях увеличивается доза генов в генотипе, и в гомозиготном состоянии эти мутации летальны. В гетерозиготном состоянии они проявляются множественными пороками развития. Однако эти мутации могли играть определенную роль в эволюции, благодаря ним могли возникнуть семейства генов гемоглобина. Также дупликации могли обеспечить возникновение многократно повторяющихся последовательностей нуклеотидов. Выявление дупликаций: 1) дифференциальное окрашивание. 2) фигура петли в профазу мейоза 1. Петля возникает на мутировавшей хромосоме. Инверсия – отрыв участка хромосомы, поворот его на 180° и присоединение на старое место. При инверсиях доза генов не меняется, но изменяется порядок расположения генов в хромосоме, т.е. изменяется группа сцепления. Концевых инверсий не бывает. Инверсии бывают 2 видов: парацентрическая инверсия, которая не затрагивает центромеру, т.к. разрывы происходят в пределах одного плеча хромосомы перицентрическая инверсия, которая затрагивает центромеру, т.к. разрывы происходят по обе стороны от центромеры. При перицентрической инверсии может изменяться форма хромосомы (если концы поворачиваемых участков не симметричны). А это делает невозможным в последующем конъюгацию. Выявление инверсий: 1) дифференциальное окрашивание. 2) фигура в виде 2х противоположно расположенных петель в профазу мейоза 1. Фенотипическое проявление инверсий наиболее мягкое по сравнению с другими хромосомными абберациями. Если рецессивные гомозиготы погибают, то у гетерозигот чаще всего наблюдается бесплодие. Кольцевые хромосомы. В норме в кариотипе человека кольцевых хромосом нет. Они могут появляться при действии на организм мутагенных факторов, особенно радиоактивного облучения. При этом в хромосоме происходит два разрыва, и образовавшийся участок замыкается в кольцо. Если кольцевая хромосома содержит центромеру, то образуется – центрическое кольцо. Если центромеры нет, то образуется – ацентрическое кольцо, оно разрушается ферментами и не наследуется. В гомозиготном состоянии эти мутации летальны, а в гетерозиготном состоянии фенотипически проявляются, как делеции. Выявляются кольцевые хромосомы при исследовании кариотипа человека. Кольцевые хромосомы являются маркерами радиоактивного облучения. Чем больше доза радиоактивного облучения, тем больше кольцевых хромосом, и тем хуже прогноз. Транслокации, их сущность. Реципрокные транслокации, их характеристика и медицинское значение. Робертсоновские транслокации и их роль в наследственной патологии. Транслокация – это перемещение участка хромосомы. Бывают взаимные (реципрокные) и не взаимные (транспозиции) транслокации. Реципрокные транслокации происходят в тех случаях, когда две негомологичные хромосомы обмениваются своими участками. Особую группу транслокаций составляют робертсоновские транслокации (центрические слияния). Им подвергаются акроцентрические хромосомы – они теряют короткие плечи, а их длинные плечи соединяются. Причина 4-5% случаев рождения ребёнка-дауника – робертсоновские транслокации. При этом происходит перемещение длинного плеча 21 хромосомы на одну из хромосом группы D (13, 14, 15, чаще вовлекается 14 хромосома). 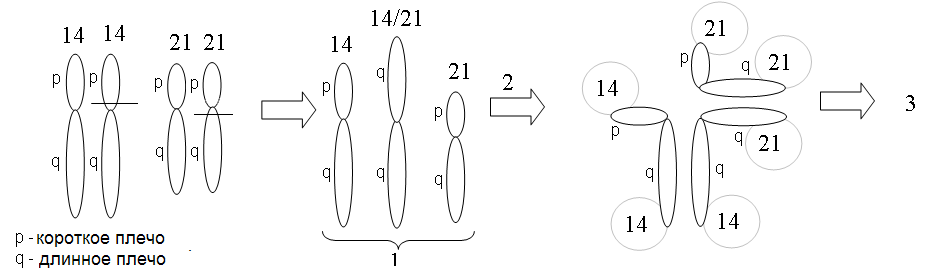 Типы яйцеклеток сперматозоид зигота Последствия 14 + 14, 21 14,14,21 моносомия 21 (леталь) 14/21,21 + 14, 21 14/21,21,14,21 трисомия 21 (дауник) 21 + 14, 21 21,14,21, моносомия 14 (леталь) 14,14/21 + 14, 21 14,14/21,14,21 трисомия 14 (леталь) 14/21 + 14, 21 14/21,14,21 фенотипически здоров (носитель) 14, 21 + 14, 21 14,21,14,21 фенотипически здоров Как видим, женщина с робертсоновской транслокацией, в кариотипе которой 45 хромосом может родить здорового ребенка. Выявление транслокаций: 1) дифференциальное окрашивание 2) фигура креста в профазу мейоза 1. Траспозиции. Мобильные генетические элементы. Механизмы перемещения МГЭ по геному и их значение. Если транслокации не носят характера взаимности, то говорят о транспозиции. Особую группу транспозонов составляют мобильные генетические элементы (МГЭ), или прыгающие гены, которые обнаружены у всех организмов. У мушки дрозофилы они составляют 5% генома. У человека МГЭ объединяют в семейство ALU. МГЭ состоят из 300- 400 нуклеотидов, повторяющихся в геноме у человека 300 тысяч раз. На концах МГЭ находятся повторы нуклеотидов, состоящие из 50-100 нуклеотидов. Повторы могут быть прямыми и обратными. Повторы нуклеотидов, по-видимому, влияют на перемещение МГЭ. Выделяют два варианта перемещения МГЭ по геному. 1. с помощью процесса обратной транскрипции. Для этого необходим фермент обратная транскриптаза (ревертаза). Этот вариант протекает в несколько этапов: на ДНК фермент РНК-полимераза (другое название – транскриптаза) синтезирует мРНК, на мРНК фермент обратная транскриптаза синтезирует одну цепь ДНК, фермент ДНК-полимераза обеспечивает синтез второй цепочки ДНК, синтезированный фрагмент замыкается в кольцо, кольцо ДНК встраивается в другую хромосому или в другое место этой же хромосомы. 2. с помощью фермента транспозазы, который вырезает МГЭ и переносит его в другую хромосому или в другое место этой же хромосомы В ходе эволюции МГЭ играли положительную роль, т.к. они осуществляли перенос генетической информации от одних видов организмов к другим. Важную роль в этом играли ретровирусы, которые содержат в качестве наследственного материала РНК, а также содержат обратную транскриптазу. МГЭ перемещаются по геному очень редко, одно перемещение на сотни тысяч событий в клетке (частота перемещений 1 х 10–5). В каждом конкретном организме МГЭ положительной роли не играют, т.к. перемещаясь по геному, они изменяют работу генов, вызывают генные и хромосомные мутации. Индуцированный мутагенез. Физические, химические и биологические мутагенные факторы. Индуцированные мутации возникают при действии на организм мутагенных факторов, которые делятся на 3 группы: Физические (УФЛ, рентгеновское и радиационное излучения, электромагнитные поля, высокие температуры). Так ионизирующее излучение может действовать непосредственно на молекулы ДНК и РНК, вызывая в них повреждения (генные мутации). Косвенное воздействие этого мутагена на геном клеток заключается в образовании Н2О2, ОН-, О2-, а они уже повреждают ДНК. Химические мутагенные факторы. Существует свыше 2 млн. химических веществ, способных вызывать мутации. Это соли тяжелых металлов, химические аналоги азотистых оснований (5-бромурацил), алкилирующие соединения (СН3, С2Н5). Биологические (вирусы, продукты жизнедеятельности паразитов, МГЭ). Радиационные мутации. Генетическая опасность загрязнения окружающей среды. Радиационные мутации это мутации, вызванные радиацией. В 1927 году американский генетик, Генрих Мелёр впервые показал, что облучение рентгеновскими лучами приводит к существенному увеличению частоты мутаций у дрозофилы. Эта работа положила начало новому направлению в биологии – радиационной генетике. Благодаря многочисленным работам, проведенным за последние десятилетия, мы теперь знаем, что при попадании элементарные частицы (кванты, электроны, протоны и нейтроны) могут вызывать ионизация молекул воды с образованием свободных радикалов (ОН-, О2-). Обладая большой химической активностью свободные радикалы вызывают разрывы ДНК, повреждение нуклеотидов или их разрушение; всё это приводит к возникновению мутаций. Так как человек является открытой системой, то различные факторы загрязнения окружающей среды могут попадать в человеческий организм. Многие из этих факторов могут изменять или повреждать наследственный материал живых клеток. Последствия воздействия этих факторов столь серьезны, что человечество не может игнорировать загрязнение окружающей среды. Мутагенез и канцерогенез. Впервые мутационную теорию рака в 1901 году предложил Гюго Де Фриз. В наши дни существует много теорий канцерогенеза. Одна из них генная теория канцерогенеза. Известно, что в геноме человека содержится более 60 онкогенов, способных регулировать клеточное деление. Они находятся в неактивном состоянии в виде протоонкогенов. Под действием различных мутагенных факторов протоонкогены активируются и переходят в состояние онкогенов, которые вызывают интенсивную пролиферацию клеток и развитие опухолей. ЗАНЯТИЕ 21 Мутации числа хромосом. Фенотипический эффект. |
