1 сем занятие 8. Занятие 8. Общие принципы лечения туберкулеза (гигиенодиетический режим, химиотерапия, патогенетическая и симптоматическая терапия, физиотерапия, коллапсотерапия, хирургическое лечение, медицинская реабилитация).
 Скачать 0.58 Mb. Скачать 0.58 Mb.
|
|
Занятие №8. Общие принципы лечения туберкулеза (гигиено-диетический режим, химиотерапия, патогенетическая и симптоматическая терапия, физиотерапия, коллапсотерапия, хирургическое лечение, медицинская реабилитация). Обоснование этапности лечения (стационарное, амбулаторное, санаторное).Преемственность лечения. Организационные формы лечения и методы контроля за эффективностью лечения. Организация лечения больных туберкулезом. Лечение больных туберкулезом проводят под наблюдением фтизиатра. Весь курс лечения или его отдельные этапы можно проводить в стационаре с круглосуточным или только дневным пребыванием, в амбулаторных условиях или в санатории. Выбор организационной формы лечения должен быть строго индивидуальным. Большое значение имеют эпидемическая опасность, характеристика туберкулезного процесса, социальные и материальные условия жизни больного и его отношение к лечению. Лечение проводят только в специализированном стационаре, если у пациента установили: • остро прогрессирующий туберкулез - милиарный туберкулез, казеозную пневмонию, туберкулезный менингит; • распространенный туберкулез с массивным бактериовыделением; • устойчивость МБТ к противотуберкулезным препаратам; • осложненное течение туберкулеза: легочное кровотечение, спонтанный пневмоторакс, легочно-сердечную недостаточность и др.; • сложные в диагностическом отношении случаи заболевания и необходимость проведения специальных исследований в условиях стационара; • тяжелые сопутствующие заболевания (лекарственная болезнь, сахарный диабет, язвенная болезнь и др.); • социальную дезадаптацию, неблагоприятные социальные и материальные условия жизни; • деградацию личности на почве хронического алкоголизма и наркомании. Контроль эффективности химиотерапиии и оценка результата лечения. До начала химиотерапии проводят комплексное первичное физикальное, лабораторное, рентгенологическое и при необходимости - инструментальное обследование больного. Перед назначением этамбутола необходима консультация офтальмолога, а стрептомицина или других аминогликозидов - оториноларинголога. В процессе лечения лабораторные исследования, а также осмотры офтальмолога и оториноларинголога повторяют ежемесячно в плановом порядке. Плановые контрольные рентгенологические исследования проводят 1 раз в 2 мес. При появлении признаков неудовлетворительной переносимости препаратов лабораторный контроль и консультации специалистов проводят незамедлительно вне зависимости от времени предыдущего обследования. Клиническое излечение от туберкулеза подразумевает полное клиническое благополучие пациента, стойкое отсутствие бактериовыделения и рентгенологических признаков активного туберкулезного воспаления, а также полноценную функцию ранее пораженного органа. Принимают во внимание характер остаточных посттуберкулезных изменений, которые сформировались в исходе туберкулезного процесса. 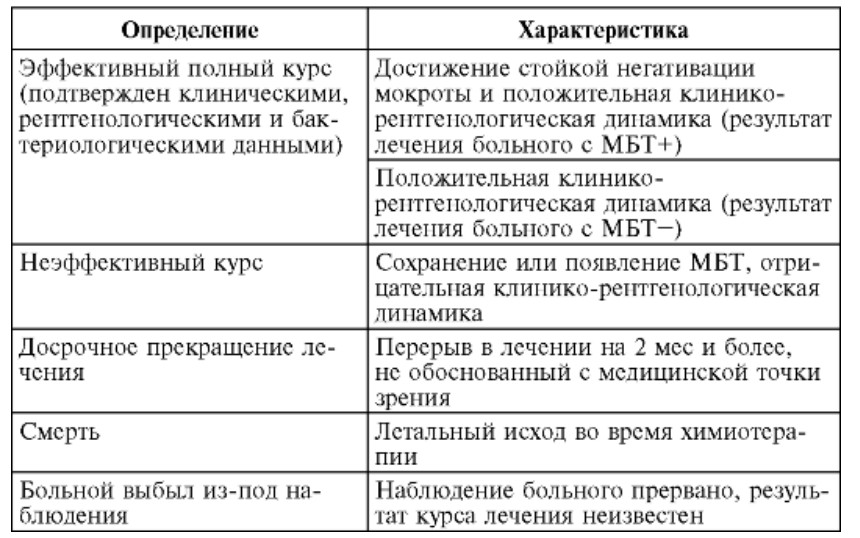 Основные принципы химиотерапии. Основные принципы двухэтапной химиотерапии туберкулеза: • раннее начало лечения; • комбинирование противотуберкулезных препаратов; • оптимальная продолжительность и непрерывность; • комплексность; • контролируемость Противотуберкулезные препараты, классификация, механизм действия на микобактериальную популяцию. Фармакологические характеристики отдельных противотуберкулезных препаратов. Лекарственные препараты, применяемые при химиотерапии туберкулеза, подразделяют на: противотуберкулезные препараты первого ряда (основные, препараты для лечения туберкулеза, вызванного лекарственно чувствительными микобактериями): изониазид**, рифампицин**, рифабутин**, рифапентин**, пиразинамид**, этамбутол**, стрептомицин**; противотуберкулезные препараты второго ряда (резервные, препараты для лечения туберкулеза с МЛУ, пре-ШЛУ, ШЛУ МБТ): бедаквилин**, линезолид**, левофлоксацин**, #моксифлоксацин**, спарфлоксацин**, деламанид**, канамицин**, #амикацин**, капреомицин**, #(имипенем + [циластатин])**, #меропенем**, циклосерин**, теризидон**, протионамид**, этионамид**, аминосалициловая кислота**, тиоуреидоиминометилпиридиния перхлорат**. При этом приоритетными препаратами для включения в схемы терапии являются бедаквилин**, линезолид**, лекарственные препараты группы фторхинолонов, а также циклосерин** или теризидон**[64]. ВОЗ рекомендует деление препаратов для лечения туберкулеза с устойчивостью МБТ к рифампицину** и изониазиду** (или только рифампицину** на 3 группы в зависимости от соотношения их пользы и вреда: Группа А: фторхинолоны (левофлоксацин** и #моксифлоксацин**), бедаквилин** и линезолид** сочтены высокоэффективными и настоятельно рекомендуются для включения во все режимы при отсутствии противопоказаний; Группа B: циклосерин** или теризидон** Группа C: в нее входят все прочие препараты, которые могут использоваться в том случае, если режим не может быть составлен из препаратов групп A и B. Препараты в группе С отсортированы по стандартно ожидаемому от каждого из них относительному балансу пользы и вреда. К группе С относятся: этамбутол**, деламанид**, пиразинамид**, #имипенем + [циластатин]**, #меропенем**, #амикацин**, стрептомицин**, протионамид**, этионамид**, аминосалициловая кислота**. Противотуберкулезные препараты разделяют на 2 группы Основные препараты Изониазид (Н) - гидразид изоникотиновой кислоты - строго специфичный высокоэффективный противотуберкулезный препарат. Он наиболее активен в отношении МБТ человеческого вида. Механизм действия связан с подавлением синтеза ДНК, фосфолипидов и нарушением целостности стенки МБТ. Препарат образует соединения с внеи внутриклеточными катионами железа, жизненно важными для МБТ, и блокирует окислительные процессы. В высоких концентрациях изониазид оказывает бактерицидное действие. Изониазид повышает концентрацию рифампицина и протионамида в крови, замедляет выведение стрептомицина. Изониазид назначают внутрь, но его можно также вводить внутримышечно, внутривенно струйно, внутривенно капельно, интратрахеально, внутрикавернозно, внутриплеврально, эндолюмбально, внутрибрюшинно. Суточная лечебная доза изониазида 5-15 мг/кг. Побочные реакции чаще наблюдаются со стороны центральной и периферической нервной системы или печени. При лечении изониазидом нельзя употреблять алкоголь, поскольку их сочетание резко увеличивает токсичность изониазида. Первичная устойчивость МБТ к изониазиду встречается нечасто, вторичная развивается довольно быстро. В ряде случаев у МБТ возникает перекрестная устойчивость к изониазиду и его гомологам (фтивазиду, метазиду, салюзиду). Перекрестная устойчивость к другим противотуберкулезным препаратам не установлена. Рифампицин (R) - антибиотик широкого спектра действия. На МБТ действует бактерицидно, обладает стерилизующими свойствами. Механизм действия связан с подавлением синтеза РНК путем образования комплекса с ДНК-зависимой РНК-полимеразой. В результате у МБТ нарушается передача генетической информации и их размножение прекращается. хорошо всасывается в кишечнике и проникает в ткани. Выводится из организма в основном с желчью, около 25% - с мочой. У больных, , слезная жидкость, мокрота, моча и кал приобретают красноватооранжевый цвет. Суточная лечебная доза рифампицина 10 мг/кг. Назначают его внутрь ежедневно, но возможно назначение 2-3 раза в неделю. Рифампицин можно вводить внутривенно капельно, интратрахеально и внутрикавернозно. Побочные реакции чаще проявляются желудочно-кишечными расстройствами, нарушением функции печени. Рифампицин чаще других противотуберкулезных препаратов взаимодействует с другими лекарственными средствами, так как он индуцирует микросомальный цитохромный комплекс Р-450 в клетках печени. В результате повышается скорость метаболических превращений многих лекарств и в крови снижается уровень антагонистов кальция, барбитуратов, бетаадреноблокаторов, кортикостероидов, нейролептиков, диазепама, некоторых антикоагулянтов и антиаритмических средств (хинидин), производных сульфонилмочевины, теофиллина, дигоксина, циклоспорина А и др. Интервал между приемом рифампицина и других лекарств целесообразно увеличить. Желательно, чтобы он был не менее 6 ч. После отмены рифампицина необходима повторная коррекция дозы других лекарств. Запрещается употребление алкоголя в период лечения рифампицином. Первичная устойчивость к рифампицину встречается нечасто, вторичная развивается довольно быстро. Перекрестная устойчивость к другим противотуберкулезным препаратам не установлена. Пиразинамид (Z) - синтетический высокоэффективный и строго специфичный противотуберкулезный препарат. Действие пиразинамида на МБТ наиболее выражено в очагах казеозного некроза, имеющих кислую реакцию. Максимальный бактериостатический эффект пиразинамида установлен именно в кислых средах (pH 5,5). В основе бактериостатического и стерилизующего действия пиразинамида на МБТ человеческого вида лежат его превращение в пиразинокарбоновую кислоту и блокада МБТ пиразинамидазникотинамидазы. После приема внутрь пиразинамид быстро всасывается в кровь. Его максимальная концентрация в крови достигается через 1-3 ч после приема. Препарат равномерно распределяется в организме, легко проникает в очаги казеозного некроза. Метаболизируется пиразинамид в печени. Продукты его метаболизма и частично пиразинамид в неизмененном 272 виде выделяются с мочой. Суточную лечебную дозу пиразинамида 25-35 мг/кг назначают перорально. При лечении пиразинамидом часто применяют интермиттирующий режим. Побочные эффекты наблюдаются относительно редко. Возможны боли в суставах, нарушение функции печени, увеличение содержания мочевой кислоты в крови. Вероятность появления побочных эффектов значительно возрастает при одновременном употреблении алкоголя. Пиразинамид несовместим с ацетилсалициловой и аскорбиновой кислотами, пробенецидом, йодсодержащими рентгеноконтрастными препаратами. Кортикостероидные препараты снижают активность пиразинамида в отношении МБТ. Первичная устойчивость МБТ к пиразинамиду наблюдается редко, вторичная развивается относительно медленно. Перекрестная устойчивость к другим противотуберкулезным препаратам не установлена. Этамбутол (E) - синтетический противотуберкулезный препарат, подавляющий синтез и стабилизацию РНК МБТ. В результате обратимо блокируется синтез клеточной стенки микобактерии. Такой эффект возникает при постоянной и достаточно высокой концентрации препарата в крови. Действует этамбутол в основном бактериостатически. Суточную лечебную дозу этамбутола 25 мг/кг назначают внутрь. Однократный прием суточной дозы эффективнее дробного применения. Обычно этамбутол назначают ежедневно, иногда - прерывисто 2-3 раза в неделю. При пероральном приеме всасывается примерно 70% препарата и максимальный уровень в крови создается через 2-3 ч. Этамбутол накапливается в эритроцитах, которые превращаются в своеобразное депо препарата. Постепенно этамбутол равномерно распределяется в тканях. Выводится этамбутол с мочой в основном в неизмененном виде. Побочные реакции при лечении этамбутолом в виде аллергии или нарушения функции желудочно-кишечного тракта наблюдаются довольно редко. Более серьезны возникающие иногда расстройства зрения - снижение его остроты, выпадение полей зрения, изменение цветоощущения. При отмене препарата эти явления обычно проходят самостоятельно. Этамбутол нельзя назначать одновременно с дисульфирамом (тетурамом). Их сочетание приводит к резкому повышению концентрации этамбутола в крови и возникновению токсических эффектов. Этамбутол также несовместим со спермином, спермидином, препаратами магния. Первичная устойчивость МБТ к этамбутолу практически не наблюдается, вторичная развивается очень медленно. Перекрестной устойчивости к другим противотуберкулезным препаратам не бывает. Этамбутол препятствует развитию лекарственной устойчивости возбудителя туберкулеза к другим противотуберкулезным препаратам. Стрептомицин (S) - первый антибиотик, у которого была обнаружена противотуберкулезная активность, до сих пор не утратил своего значения. Механизм действия основан на нарушении белкового синтеза в МБТ. Препарат вступает в соединение с нуклеиновыми кислотами, играющими важную роль в построении ферментов микробной клетки, и нарушает их обмен. Действует стрептомицин бактериостатически и бактерицидно на быстроразмножающиеся штаммы МБТ при прогрессирующем течении заболевания. В кислой среде стрептомицин теряет свою активность. Суточную лечебную дозу стрептомицина 16 мг/кг вводят внутримышечно однократно. При необходимости стрептомицин можно вводить в трахею, плевральную полость, каверну. Для эндолюмбального введения используют стрептомицина хлоркальциевый комплекс. Максимальная концентрация в крови при внутримышечном введении достигается через 0,5-1 ч после введения. В организме стрептомицин распределяется неравномерно: большая часть введенного препарата накапливается в почках, меньшая - в легких, лимфатических узлах, 273 серозных полостях. Препарат почти не проникает в мышцы, кости и центральную нервную систему. В течение 24 ч 60-80% стрептомицина выводится почками. При лечении стрептомицином нередко возникают вестибулярные и кохлеарные нарушения. Снижение слуха часто имеет необратимый характер. Необходимы своевременная диагностика этих побочных реакций и немедленная отмена препарата. Довольно часто наблюдаются побочные аллергические реакции, реже - нефропатия, нарушения кроветворения. Назначение стрептомицина противопоказано при поражении VIII пары черепно-мозговых нервов, нарушении функции почек, гипертонической болезни, облитерирующем эндартериите. Нельзя комбинировать стрептомицин с канамицином, флоримицином, капреомицином, амикацином, так как все эти препараты могут вызвать поражение VIII пары черепно-мозговых нервов. Первичная устойчивость МБТ к стрептомицину встречается значительно чаще, чем к другим противотуберкулезным препаратам, вторичная возникает быстро. Существует неполная перекрестная устойчивость между стрептомицином, канамицином и флоримицином. Перекрестная устойчивость к другим противотуберкулезным препаратам не установлена. Назначение стрептомицина на ранних этапах лечения уменьшает вероятность появления устойчивых к противотуберкулезным препаратам субпопуляций туберкулезного возбудителя. Резервные препараты Протионамид (Рt) - гомолог этионамида, нарушающий обмен микробной клетки. В основном протионамид оказывает бактериостатическое действие, сохраняет свою активность в кислой среде. Протионамид медленно всасывается в желудочно-кишечном тракте. Максимальная концентрация в крови достигается через 1-2 ч после приема. Препарат равномерно распределяется в тканях, хорошо проникает в спинномозговую жидкость. Предположительно 90% препарата метаболизируется в печени. Суточная лечебная доза протионамида 15 мг/кг. Обычно препарат назначают внутрь. Возможно его внутривенное капельное и ректальное введение. Переносимость протионамида у разных людей может существенно различаться. Повидимому, большое значение имеют генетические факторы и особенности метаболизма препарата. Основные побочные эффекты - нарушения со стороны желудочно-кишечного тракта, почек, центральной нервной системы. Реже возникают дисфункция печени и угревая сыпь. Протионамид несовместим с гипотензивными препаратами, фенотиазином. В период лечения протионамидом недопустимо употребление алкоголя Этионамид - противотуберкулезный препарат, полученный раньше протионамида. Основные характеристики этих препаратов и методика применения в значительной степени совпадают. Однако этионамид гораздо более токсичен. Он часто вызывает побочные реакции, что существенно ограничивает его использование. Канамицин (K) - антибиотик из группы аминогликозидов. Бактериостатическое действие канамицина похоже на действие стрептомицина. Оно связано с нарушением синтеза белка в МБТ. Канамицин блокирует специфические протеины рибосом и препятствует правильному включению аминокислот в растущую полипептидную цепь. Действие канамицина на микобактерии слабее, чем стрептомицина. Однако канамицин способен эффективно влиять на устойчивые к стрептомицину штаммы возбудителя. Это свойство определяет ценность канамицина для лечения больных с устойчивостью МБТ к стрептомицину. Амикацин - препарат из группы аминогликозидов, весьма близок к канамицину. До последнего времени амикацин редко применяли во фтизиатрической клинике. Поэтому МБТ, устойчивые к другим противотуберкулезным препаратам, как правило, к амикацину чувствительны. Капреомицин (Cap) включает комплекс из 4 активных компонентов, которые подавляют синтез белка бактериальной клетки. Он является специфическим противотуберкулезным препаратом и оказывает выраженное бактериостатическое действие на МБТ человеческого вида и более слабое на МБТ бычьего вида. Циклосерин (Cs) - препарат широкого спектра действия, в результате которого МБТ теряют кислотоустойчивость и приобретают необычную форму. Механизм действия бактериостатический. Циклосерин сохраняет активность в кислой среде. После приема внутрь циклосерин быстро всасывается. Самый высокий уровень его в крови определяется через 3-4 ч. Препарат равномерно распределяется в организме, выводится с мочой. Суточную лечебную дозу циклосерина 10-20 мг/кг назначают обычно перорально. При необходимости циклосерин можно вводить в трахею, плевральную полость, каверну. Рифабутин (Rb) - полусинтетический антибиотик, который является производным рифампицина. Обладает широким спектром действия, связанного со способностью препарата ингибировать ДНК-зависимую РНК-полимеразу микобактерий. Рифабутин эффективно воздействует на значительную часть штаммов МБТ, устойчивых к рифампицину. Суточная лечебная доза рифабутина 5-10 мг/кг. Препарат назначают перорально. В отличие от рифампицина рифабутин не влияет на ацетилирование изониазида, поэтому при сочетании рифабутина и изониазида усиление гепатотоксичности менее вероятно. Парааминосалициловая кислота (PAS) - химиопрепарат, оказывающий слабое бактериостатическое действие на МБТ. Туберкулостатический эффект ПАСК обусловлен ее конкурентным взаимоотношением с парааминобензойной и пантотеновой кислотами, а также с биотином, которые являются факторами роста микобактерий. Метаболизируется ПАСК главным образом в печени: происходят ацетилирование и соединение ПАСК с глицином. Перорально приходится назначать большое количество препарата, поэтому иногда предпочтение отдают внутривенному капельному введению ПАСК. Ее можно вводить ректально, методом электрофореза, применять местно. Побочные реакции при лечении ПАСК часто возникают со стороны желудочно-кишечного тракта и печени, почек и кожи. Изза частых побочных реакций ПАСК применяют в основном при устойчивости МБТ к другим противотуберкулезным препаратам. Первичная устойчивость МБТ к ПАСК встречается относительно редко, вторичная развивается медленно. Перекрестная устойчивость не установлена. Фторхинолоны (Fq) - ципрофлоксацин, офлоксацин, ломефлоксацин, левофлоксацин, моксифлоксацин, спарфлоксацин, гатифлоксацин) - являются антибиотиками широкого спектра действия. Они ингибируют реакции связывания цепей ДНК, а непосредственное связывание фторхинолонов с ее отдельными цепями приводит к гибели МБТ. Препараты фторхинолонового ряда также способны повреждать внешнюю мембрану микобактерии и оказывать длительное постантибиотическое действие. Молекулы фторхинолонов имеют малые размеры, поэтому хорошо проникают во все органы, ткани, биологические жидкости, а также внутрь клетки. В результате эти препараты способны воздействовать на микобактерии при их любой локализации, активно влияя на МБТ в период роста и в период покоя бактериальной клетки. Различие между максимально переносимой концентрацией препаратов фторхинолонового ряда и их концентрацией, обеспечивающей максимальный бактерицидный эффект, относительно небольшое. Сочетание фторхинолонов с изониазидом приводит к усилению действия на МБТ. Еще более выраженный синергический эффект отмечен при сочетании фторхинолонов с пиразинамидом. Тиоацетазон (тибон) - синтетический противотуберкулезный препарат, механизм действия которого на МБТ связывают с образованием комплексных соединений с микроэлементами меди, входящими в состав микобактерий, и подавлением активности диаминоксидазы. Максимальная концентрация тиоацетозона в крови достигается через 2-4 ч после приема. Бактериостатическая концентрация препарата сохраняется в течение 10-12 ч. Через 24 ч с мочой и калом выводится около 80% принятой дозы. Понятие о режиме химиотерапии. Определение этапов химиотерапии. Режим химиотерапии – это комбинация противотуберкулезных препаратов и антибиотиков, длительность и кратность их приема, сроки и содержание контрольных исследований, а также организационные формы проведения лечения. В лечении туберкулеза используется пять режимов химиотерапии. Режимы химиотерапии назначаются на основании индивидуальных результатов определения лекарственной устойчивости возбудителя: при лекарственной чувствительности возбудителя (режим лекарственно-чувствительного туберкулеза), при устойчивости возбудителя к изониазиду, в том числе полирезистентности (режим изониазид- резистентного туберкулеза), при устойчивости возбудителя к рифампицину** и изониазиду** (или только рифампицину**) с лекарственной чувствительностью к фторхинолонам (режим МЛУ ТБ), при устойчивости возбудителя к рифампицину** и изониазиду** (или только рифампицину**) с лекарственной устойчивостью к фторхинолонам (режим пре-ШЛУ ТБ), при устойчивости возбудителя к рифампицину** и изониазиду** (или только рифампицину**) с лекарственной устойчивостью к фторхинолонам, а также бедаквилину или линезолиду (режим ШЛУ ТБ) 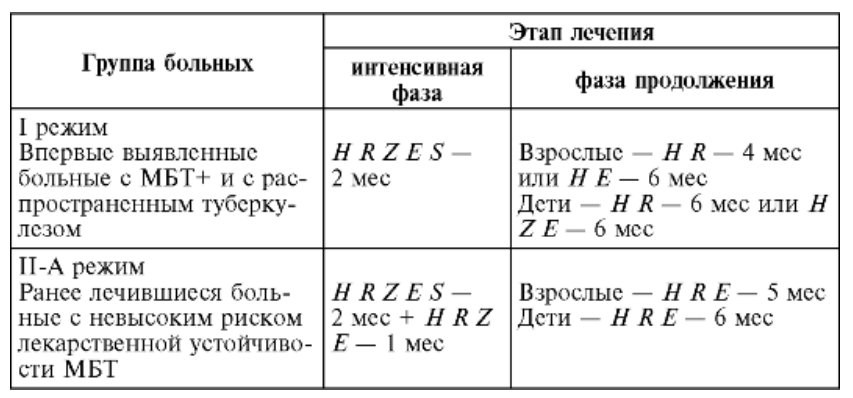 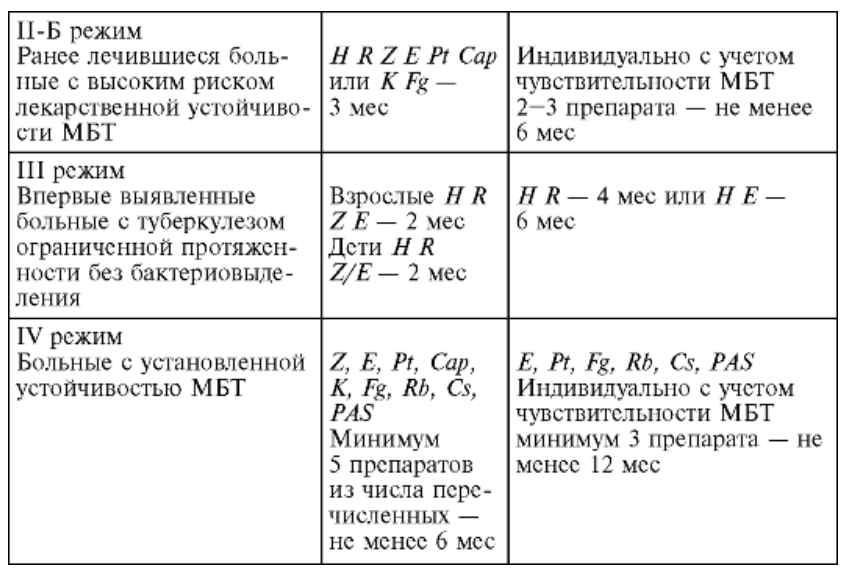 Химиотерапия туберкулеза состоит из 2 этапов. Первый этап - интенсивная фаза лечения. Ее проводят для уничтожения максимально возможного количества МБТ и значительного уменьшения бактериальной популяции. Интенсивная фаза лечения призвана устранить острые проявления болезни, прекратить бактериовыделение и способствовать закрытию полостей распада. Второй этап - фаза продолжения лечения. Она необходима для закрепления достигнутых результатов. На этом этапе воздействуют на сохранившиеся МБТ и предупреждают их размножение. Двухэтапное лечение способствует последовательной инволюции туберкулезного процесса, стойкому клиническому эффекту и предупреждает реактивацию туберкулеза. Клиническое значение и клинические проявления лекарственной резистентности микобактерий туберкулеза. Режимы химиотерапии больных хроническим туберкулезом с лекарственной резистентностью микобактерий. Режимы химиотерапии больных туберкулезом легких с множественной и широкой лекарственной резистентностью микобактерий. Режим химиотерапии МЛУ туберкулеза Рекомендуется при назначении режима химиотерапии МЛУ туберкулеза лечение пациента проводить длительностью не менее 18 месяцев для полного подавления микробной популяции и предотвращения рецидива: интенсивная фаза – не менее 6 месяцев; фаза продолжения лечения – не менее 12 месяцев [40, 77-79, 64, 99]. Общая длительность режима химиотерапии МЛУ туберкулеза может быть увеличена при недостаточном ответе пациента на лечение по решению ВК [30]. Общая длительность индивидуализированного режима химиотерапии МЛУ туберкулеза может быть сокращена у пациентов с впервые выявленным МЛУ туберкулезом, ограниченной формой туберкулеза и ранее не получавших лекарственные препараты группы фторхинолонов по решению ВК, при отсутствии контактов с больными пре-ШЛУ и ШЛУ возбудителя (но не менее 12 месяцев терапии) [100]. Рекомендуется в интенсивной фазе режима химиотерапии МЛУ туберкулеза назначение комбинации, одновременно включающей пять-шесть противотуберкулезных лекарственных препаратов и антибиотиков с доказанной или предполагаемой лекарственной чувствительностью возбудителя, из которых четыре наиболее эффективны [75, 98]. Больному назначается один из лекарственных препаратов группы фторхинолонов, бедаквилин**, линезолид**, циклосерин** или теризидон**, а также один дополнительный препарат с оказанной или предполагаемой лекарственной чувствительностью возбудителя. Уровень убедительности рекомендаций С (уровень достоверности доказательств 5) Рекомендуется назначение левофлоксацина** в составе режима химиотерапии МЛУ туберкулеза для повышения эффективности лечения Рекомедуется назначение #моксифлоксацина** в составе режима химиотерапии МЛУ туберкулеза для повышения эффективности лечения Рекомендуется назначение спарфлоксацина** в составе режима химиотерапии МЛУ туберкулеза при сохранении лекарственной чувсвительности [69, 70]. Рекомендуется назначение бедаквилина** в составе режима химиотерапии МЛУ туберкулеза [101]. Комментарий: при назначении бедаквилина** в составе режима химиотерапии: не следует добавлять препарат к неэффективному режиму химиотерапии (сохранение бактериовыделения, отрицательная клинико- рентгенологическая динамика процесса); назначается на 6 месяцев, по решению ВК по жизненным показаниям продолжительность лечения может быть увеличена при условии информированного согласия пациента; лучше применять с левофлоксацином** (доказанная безопасность их совместного применения) для повышения эффективности лечения и предотвращения развития устойчивости, при применении с #моксифлоксацином** необходим тщательный мониоринг кардиотоксичности [101, 104-106]. Эффективное завершение интенсивной фазы подтверждается получением двух последовательных отрицательных результатов посева мокроты или другого диагностического материала с интервалом в один месяц. Рекомендуется назначение линезолида** в составе режима химиотерапии МЛУ туберкулеза для повышения эффективности лечения [64, 103-107]. Рекомендуется назначение циклосерина** или теризидона** в составе режима химиотерапии МЛУ туберкулеза для повышения эффективности лечения Рекомендуется в схемы терапии дополнительно включать один-два препарата: этамбутол**, пиразинамид**, капреомицин** при сохранении лекарственной чувствительности возбудителя [109-120]. Комментарии: при невозможности составления схемы терапии из вышеперечисленных препаратов в схему терапии могут быть включены деламанид**, протионамид** или этионамид**, #(имипенем + [циластатин])** или #меропенем**, аминосалициловая кислота**, тиоуреидомеилпиридиния пехлорат**. Применение канамицина** или #амикацина**возможно при сохранении к ним лекарственной чувствительности возбудителя. Рекомендуется в фазе продолжения режима химиотерапии МЛУ туберкулеза назначение комбинации, одновременно включающей не менее трех эффективных противотуберкулезных лекарственных препаратов и антибиотиков с сохраненной или предполагаемой лекарственной чувствительностью возбудителя для повышения эффективности лечения [100, 121-123]. 3 Режим химиотерапии ШЛУ туберкулеза Рекомендуется лечение пациента по режиму химиотерапии ШЛУ туберкулеза проводить длительностью не менее 20 месяцев: интенсивная фаза – не менее 8 месяцев; фаза продолжения лечения – не менее 12 месяцев для достижения стойкого эффекта от проводимой терапии [100, 121-123]. : Длительность интенсивной фазы – 8 месяцев или более до получения четырех отрицательных результатов посева на жидких и/или плотных средах с интервалом в один месяц. Рекомендуется в интенсивной фазе режима ШЛУ туберкулеза назначение комбинации, одновременно включающей не менее пяти противотуберкулезных лекарственных препаратов и антибиотиков с предполагаемой или сохраненной лекарственной чувстительностью возбудителя для полного подавления микробной популяции [124, 125]. приоритетными являются бедаквилин** или линезолид** (в зависимости от результатов индивидуального теста лекарственной чувствительности возбудителя), деламанид** и три дополнительных препарата с доказанной или предполагаемой лекарственной чувствительностью возбудителя. Рекомендуется назначение бедаквилина** в составе режима ШЛУ туберкулеза при достоверном сохранении к нему лекарственной чувствительности возбудителя для повышения эффективности лечения [64, 101, 106, 126 ,127]. Уровень убедительности рекомендаций С (уровень достоверности доказательств 4) Рекомендуется назначение линезолида** в составе режима ШЛУ туберкулеза при достоверном сохранении к нему лекарственной чувствительности возбудителя для повышения эффективности лечения [30, 64, 80, 86, 128-129] Рекомендуется в схемы режима ШЛУ туберкулеза дополнительно включать деламанид** для стойкого подавления микробной популяции и повышения эффективности лечения [110-112, 130, 131]. : Применение рекомендуется в течение 6 месяцев, по решению ВК по жизненным показаниям продолжительность лечения может быть увеличена при условии информированного согласия пациента [114-115]. Рекомендуется назначение циклосерина** или теризидона** в составе режима ШЛУ туберкулеза для повышения эффективности лечения [64, 103,108,109] Уровень убедительности рекомендаций А (уровень достоверности доказательств 2) Рекомендуется при необходимости в схемы режима ШЛУ туберкулеза могут быть включены этамбутол**, пиразинамид**, #амикацин**, капреомицин** при сохранении лекарственной чувствительности возбудителя. При резистентности возбудителя к этим препаратам в схему терапии рекомендуется включение #имипенем + [циластатин]** или #меропенема** для повышения эффективности лечения [116, 118, 132]. При невозможности составления схемы терапии из вышеперечисленных препаратов в схему терапии могут быть включены протионамид** или этионамид**, аминосалициловая кислота**, тиоуреидомеилпиридиния пехлорат**. Применение канамицина** возможно при сохранении к нему лекарственной чувствительности возбудителя, #меропенем** или #имипенем + [циластатин]** [70, 133]. Побочные реакции при химиотерапии. Побочные реакции токсического происхождения зависят от фармакологических свойств, дозы препаратов и исходного состояния органов и систем, ответственных за их метаболизм. Токсические побочные реакции часто проявляются моноцитозом, сдвигом лейкоцитарной формулы влево. Иногда в результате токсического действия на костный мозг возникают анемия, лейкопения или тромбоцитопения. Длительное применение препаратов широкого спектра действия может привести к дисбактериозу. Основанием для подозрения на дисбактериоз служат упорные диспепсические расстройства, возникающие через 2-4 мес химиотерапии. После бактериологического подтверждения диагноза необходимы отмена препарата, вызвавшего дисбактериоз, и назначение терапии для восстановления нормальной кишечной флоры. Важно различать устранимые и неустранимые побочные реакции. Устранимые реакции могут быть полностью ликвидированы уменьшением дозы, изменением пути или кратности введения химиопрепарата, а также с помощью различных корригирующих средств. Прекращения курса лечения не требуется. К неустранимым реакциям относятся клинически выраженные побочные реакции, которые не поддаются корректирующим и лечебным воздействиям. При их возникновении дальнейшее применение препаратов, вызывающих эти реакции, практически невозможно. Меры, предпринимаемые для устранения побочных реакций, зависят от их вида и степени тяжести. Слабые и умеренно выраженные аллергические побочные реакции подавляются с помощью десенсибилизирующих средств. При отсутствии успеха все противотуберкулезные препараты временно отменяют. Одним из основных лабораторных критериев в этой ситуации является количество эозинофилов в периферической крови. Длительная высокая эозинофилия (15% и более) независимо от выраженности клинических проявлений подтверждает необходимость отмены лекарств. При тяжелых аллергических реакциях возможно использование преднизолона. Его назначают внутрь в дозе 20 мг по убывающей схеме на 15-30 дней. После исчезновения клинических проявлений побочных реакций противотуберкулезные препараты назначают последовательно один за другим. Таким путем выявляют препарат-аллерген. В последующем его исключают из схемы лечения и заменяют другим препаратом. При возникновении токсических реакций на противотуберкулезные препараты снижают суточную дозу, назначают дробный или прерывистый прием препарата. Большинство нейротоксических побочных реакций, вызванных изониазидом, предупреждают и устраняют назначением пиридоксина (витамин В6). Вводят 2 мл 5% раствора витамина В6 внутримышечно 1 раз в день. При парестезиях и других нейротоксических осложнениях также применяют тиамин (витамин В1). Его назначают также внутримышечно по 2 мл 5% раствора 1 раз в день. Прием витаминов В6 и В1 внутрь значительно менее эффективен. Доза витамина В6 при его назначении внутрь 60-100 мг, витамина В1 50-100 мг. При недостаточной эффективности витамина В1 используют 1-2 мл 1% раствора АТФ внутримышечно ежедневно в течение 3-4 нед. У больных с заболеваниями центральной нервной системы для профилактики нейротоксических реакций, связанных с приемом изониазида, назначают препараты бензодиазепинового ряда - реланиум 2,5-5 мг в день или феназепам 1-2 мг в день. Побочные реакции со стороны печени обычно имеют токсикоаллергический характер. Для устранения слабых и умеренно выраженных реакций (повышение активности трансаминаз до 100 ЕД) и для их профилактики назначают внутрь ноотропил 400-1200 мг в день в сочетании с рибоксином или предукталом 300-600 мг в день, иногда эссенциале форте по 2 капсулы 3 раза в день или гептрал по 400 мг 2-3 раза в день. В большинстве случаев больные удовлетворительно переносят трехкратное повышение активности аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) относительно верхней границы нормы. Однако при выраженных клинических симптомах поражения печени изониазид следует отменить. После ликвидации побочных реакций может быть предпринята попытка возобновить лечение изониазидом, начиная с малой дозы препарата. Аналогичную лечебную тактику применяют при токсических побочных реакциях со стороны печени, вызванных рифампицином или пиразинамидом. При неустранимых побочных реакциях токсического характера на изониазид или рифампицин, но сохранении к ним чувствительности МБТ показана замена препарата его аналогом, а не другим противотуберкулезным препаратом. Изониазид можно заменять фтивазидом, метазидом, а рифампицин - рифабутином. При неустранимых аллергических реакциях замена аналогами не показана и препараты данной группы отменяют. При этом изониазид и рифампицин заменяют 2 резервными препаратами. Появление побочных токсических реакций при лечении стрептомицином или другими аминогликозидами, а также нарушения зрения при лечении этамбутолом требуют немедленной отмены препаратов. Наиболее действенным средством устранения симптомов пеллагры, возникающих при лечении протионамидом, является никотинамид. Его назначают внутрь по 0,025 г 1-2 раза в день. Для профилактики и устранения возможных диспепсических расстройств используют нитрат висмута 0,25 г 3-4 раза в день за 15 мин до еды или викалин 1-2 таблетки 3 раза в день после еды. Для профилактики токсического действия циклосерина целесообразен прием суточной дозы препарата на ночь. Внутрь назначают глутаминовую кислоту по 1,5 г 3 раза в день до еды. Используют также реланиум по 1-2,5 мг или феназепам по 1-2 мг 1-2 раза в день, витамин В6 120 мг 4 раза в день после еды. При токсических побочных реакциях на ПАСК или тиоацетазона от этих препаратов целесообразно отказаться. Перед началом химиотерапии больной должен быть информирован о возможных побочных реакциях. Большинство побочных реакций возникают в первые 2 мес химиотерапии. В последующем вероятность их развития уменьшается. Существующие методы патогенетической терапии. Значение искусственного пневмоторакса и пневмоперитонеума в современных условиях. Механизм действия. Патогенетическая терапия применяется для комплексного лечения пациентов и повышения эффективности лечения за счет применения средств (методов), воздействующих не на возбудителя заболевания (микобактерию туберкулеза), а на состояние различных систем организма пациента. [63, 141]. Патогенетическая терапия включает немедикаментозные и медикаментозные методы и средства [86, 94, 141-158]. Немедикаментозные методы: режим; лечебное питание; воздействие климата и других санаторных факторов; коллапсотерапия; аэрозольтерапия; физиотерапия. Медикаментозные методы (лекарственная терапия): ирригаццонные растворы; нестероидные противовоспалительные и противоревматические препараты; препараты для лечения зуда, в т.ч. антигистаминные и анестетики; ферментные препараты; витамины; лекарственные средства, влияющие на обмен веществ. Обязательным условием назначения любого метода патогенетической терапии является применение его на фоне проводимой специфической химиотерапии. Выбор средства (метода) патогенетической терапии должен быть обоснованным с учетом механизмов патогенеза туберкулеза, применения диагностических методов для оценки имеющихся нарушений, возможного взаимодействия с другими лекарственными средствами (методами), прогноза клинической и фармакоэкономической эффективности. Для выявления и оценки имеющихся нарушений могут применяться различные методы диагностики (клинические, инструментальные, лабораторные) Управляемый коллапс предполагает создание охранительных условий для пораженного органа или его части в виде уменьшения эластического напряжения легкого и частичном сближении стенок каверны, а также способствует возникновению висцеро- висцеральных рефлексов, приводящих к снижению тонуса эластических и гладкомышечных элементов легкого, что способствует рубцеванию деструкции и абацилированию пациента Рекомендуется выполнение искусственного пневмоторакса (ИП): при наличии сформированных каверн без выраженной перикавитарной инфильтрации при инфильтративном, кавернозном и ограниченном диссеминированном туберкулезе легких у пациентов при непереносимости основных химиопрепаратов (ХП), лекарственной устойчивости (ЛУ) МБТ, сопутствующих заболеваниях, ограничивающих проведение адекватной химиотерапии, кровохарканьи. при двустороннем инфильтративном, кавернозном, ограниченном диссеминированном и фиброзно-кавернозном туберкулезе с целью уменьшения остроты и распространенности процесса и подготовки пациента к хирургическому лечению на стороне противоположного легкого (на стороне наименьшего поражения) для закрытия полостей распада в легких [1, 65]. : Искусственный пневмоторакс (ИП) - метод лечения туберкулеза легких, заключающийся во введении через иглу воздуха в грудную клетку между париетальным и висцеральным листками плевры. Искусственный пневмоторакс (ИП) назначается по строго определенным показаниям. Противопоказаниями к ИП являются: Клинические формы: казеозная пневмония; цирротический туберкулез легких; экссудативный и адгезивный плеврит на стороне наложения ИП. Каверны: размерами более 6 см.; расположенные в цирротических участках легкого; примыкающие к плевре; блокированные (противопоказание временное). Общие противопоказания: активный туберкулез бронха на стороне поражения; активное воспаление бронхов любой природы; стеноз бронха 2-3 степени; эмфизема легких; пневмокониоз; дыхательная недостаточность II-III степени; бронхообструктивный синдром; состояние после оперативного вмешательства на стороне каверны; поражение сердечно-сосудистой системы в фазе декомпенсации (ИБС: стенокардия III-IV функционального класса, нарушения сердечного ритма, постинфарктный кардиосклероз, гипертоническая болезнь II-III степени); возраст пациента старше 60 лет. Рекомендуется наложение пневмоперитонеума для повышения эффективности лечения при деструктивных формах туберкулеза при: деструктивных процессах в нижних долях легких независимо от клинической формы; деструктивных процессах в верхних долях легких при противопоказаниях или невозможности проведения ИП; кровохарканьи [1, 65, 135, 136]. Пневмоперитонеум (ПП) - метод лечения туберкулеза легких, заключающийся во введении через иглу воздуха в брюшную полость. При выполнении ПП введенный в брюшную полость газ вызывает висцеро-висцеральный рефлекс, спадение лёгкого, подъём диафрагмы, усиление рёберно-диафрагмального дыхания, повышение лимфотока, улучшение кровообращения, усиление окислительных процессов, артериализацию крови. Противопоказания к ПП: облитерация дренирующего бронха в процессе заживления каверны и образование «блокированной» каверны; генерализованный, в т.ч. милиарный туберкулез; дыхательная недостаточность II-III степени; воспалительные изменения в брюшной полости, грыжи белой линии, паховые, перерастянутый брюшной пресс; активный туберкулез органов малого таза; ИБС, сердечно-сосудистая недостаточность, атеросклероз сосудов; амилоидоз внутренних органов; ранний послеоперационный период на органах брюшной полости. Рекомендуется назначение клапанной бронхоблокации для лечения деструктивых изменений у пациентов с туберкулезом легких (в первую очередь, инфильтративном и фиброзно-кавернозном туберкулезе легких) при: длительно незакрывающейся деструкции при адекватной химиотерапии; состояниях и/или обстоятельствах (непереносимость противотуберкулезных препаратов, МЛУ МБТ, сопутствующих заболеваниях), обусловливающих невозможность проведения адекватной химиотерапии; сопутствующих заболеваниях, повышающих риски неэффективного лечения и/или рецидива туберкулеза Показания и противопоказания.  |
