алканы.. Предельные углеводороды. Алканы
 Скачать 3.19 Mb. Скачать 3.19 Mb.
|
|
ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. АЛКАНЫ. Алканы – это углеводороды, в молекулах которых все атомы углерода находятся в sр3-гибридизации и связаны друг с другом только σ-связями. Алканы (насыщенные алифатические углеводороды, парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой CnH2n+2. Алканы (парафины) – алифатические (нециклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи. Алканы – название предельных углеводородов по международной номенклатуре. Парафины – исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – имеющий мало сродства, малоактивный). Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода. Каждый атом углерода в молекуле алкана связан простыми связями с четырьмя атомами («С» или «Н») и не может присоединить другие атомы. Общая формула алканов – CnH2n+2, где n – число атомов углерода. Простейшие представители алканов: 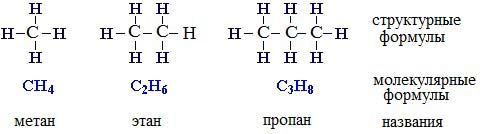  Рисунок 1 Модели молекул При сравнении этих соединений видно, что они отличаются друг от друга на группу -СН2- (метилен). Добавляя к пропану еще одну метиленовую (-СН2-) группу, получим бутан С4Н10, затем алканы С5Н12, С6Н14 и т.д. Строение алкановХимическое строение (порядок соединения атомов в молекулах) простейших алканов – метана, этана и пропана – показывают их структурные формулы. Из этих формул видно, что в алканах имеются два типа химических связей: С–С и С–НСвязь С–С является ковалентной неполярной. Длина связи C–C в предельных углеводородах равна 0,154 нм. Связь С–Н — ковалентная слабополярная, т.к. углерод и водород близки по электроотрицательности (2.5 — для углерода и 2.1 — для водорода). Связи C–Н немного короче. Электронная плотность немного смещена в сторону более электроотрицательного атома углерода. Структурные формулы отражают химическое строение, но не дают представления о пространственном строении молекул, которое существенно влияет на свойства вещества. Пространственное расположение атомных орбиталей углерода зависит от типа его гибридизации. Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации. 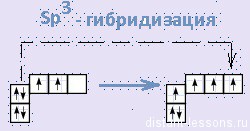 Это означает, что все четыре гибридные орбитали атома углерода одинаковы по форме, энергии и направлены в углы равносторонней треугольной пирамиды – тетраэдра. Углы между орбиталями равны 109028ʹ. Атом углерода в молекуле метана расположен в центре тетраэдра, атомы водорода – в его вершинах. Строение молекулы метана СН4 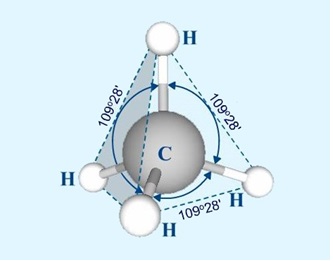  Пространственное строение метана можно показать с помощью объемных (масштабных) и шаростержневых моделей.  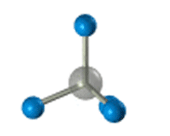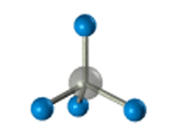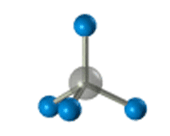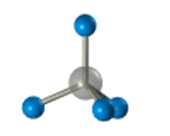 Для записи удобно использовать пространственную (стереохимическую) формулу.  Строение молекулы этана С2Н6 В молекуле следующего гомолога – этана С2Н6 – два тетраэдрических sp3— атома углерода образуют более сложную пространственную конструкцию:    Так как гибридизированные электронные облака атомов углерода направлены к вершинам тетраэдра, то при образовании молекулы алканов, с большим числом атомов углерода, имеют зигзагообразное строение. Строение молекулы пропана С3Н8 – цепь зигзагообразная 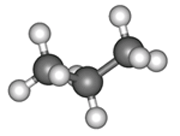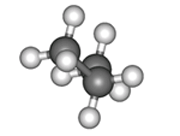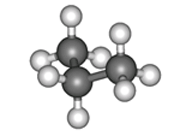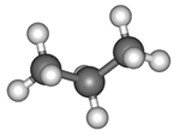 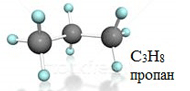  Молекула н-пентана Все связи в молекулах предельных углеводородах одинаковые. Атом углерода образует σ–связь за счет перекрывания гибридных орбиталей с гибридными орбиталями другого атома. Перекрывание осуществляется, таким образом, что область максимальной электронной плотности сосредотачивается в пространстве на прямой, соединяющей ядра атомов. Такое перекрывание оказывается наиболее эффективным, а возникающие при этом σ–связи – наиболее прочными. 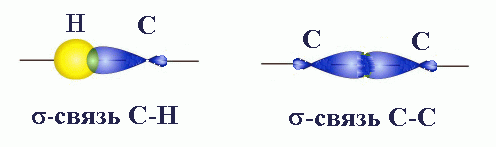 Гомологический ряд алкановГомологический ряд – ряд веществ, расположенных в порядке возрастания их молекулярных масс, сходных по строению, химическим свойствам и отличающихся друг от друга на одну или несколько групп СН2. Гомологи - вещества, принадлежащие к одному классу, сходные по составу, строению и свойствам, но различающиеся на одну или несколько групп СН2. Группу СН2 называют гомологической разностью. Гомологический ряд алканов легко составить, прибавляя каждый раз к предыдущей цепочке группу СН2. Первым членом гомологического ряда алканов является метан СН4. Окончание –ан является характерным для названий предельных углеводородов. Начиная с пятого углеводорода, название образуется из греческого числительного, указывающего число углеродных атомов в молекуле и окончания –ан.  Изомерия алкановИзомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие соединения называются изомерами. 1. Вид изомерии, при которой вещества отличаются друг от друга порядком связи атомов в молекуле, называется структурной изомерией. Строение структурных изомеров отражается структурными формулами. 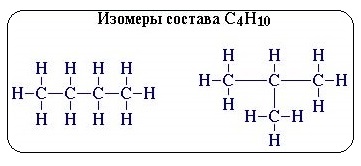 2. Если в молекулах одинакового состава и одинакового химического строения возможно различное взаимное расположение атомов в пространстве, то наблюдается пространственная изомерия (стереоизомерия). В этом случае использование структурных формул недостаточно и следует применять модели молекул или пространственные (стереохимические) формулы. 2.1. Углеводородные цепи молекул алканов могут вращаться вокруг простых связей, принимать различные геометрические формы и переходить друг в друга. Различные геометрические формы молекул, переходящие друг в друга путем поворота вокруг C–C связей, называются конформациями или поворотными изомерами (конформерами), а данный вид изомерии – конформационной (поворотной) изомерией. Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг σ-связей С–С, называют конформациями или поворотными изомерами (конформерами). Характерной особенностью σ-связей является то, что электронная плотность в них распределена симметрично относительно оси, соединяющей ядра связываемых атомов (цилиндрическая или вращательная симметрия). Поэтому вращение атомов вокруг σ-связи не будет приводить к ее разрыву. В результате внутримолекулярного вращения по σ-связям С–С молекулы алканов, начиная с этана С2Н6, могут принимать разные геометрические формы. Поворотные изомеры молекулы представляют собой энергетически неравноценные ее состояния. Их взаимопревращение происходит быстро и постоянно в результате теплового движения. Поэтому поворотные изомеры не удается выделить в индивидуальном виде, но их существование доказано физическими методами. Некоторые конформации более устойчивы (энергетически выгодны) и молекула пребывает в таких состояниях более длительное время. Рассмотрим поворотные изомеры на примере этана Н3С–СН3: 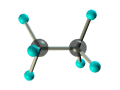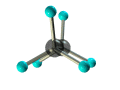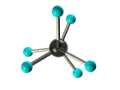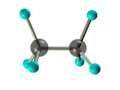 При вращении одной группы СН3 относительно другой возникает множество неодинаковых форм молекулы, среди которых выделяют две характерные конформации (А и Б), отличающиеся поворотом на 60°: 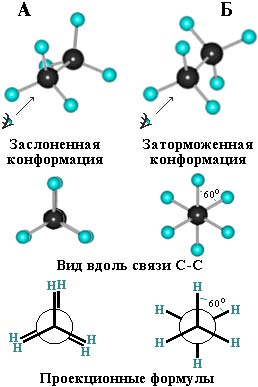 Эти поворотные изомеры этана отличаются расстояниями между атомами водорода, соединенными с разными атомами углерода. В конформации А атомы водорода сближены (заслоняют друг друга), их отталкивание велико, энергия молекулы максимальна. Такая конформация называется «заслоненной», она энергетически невыгодна и молекула переходит в конформацию Б, где расстояния между атомами Н у разных атомов углерода наибольшее и, соответственно, отталкивание минимально. Эта конформация называется «заторможенной», т.к. она энергетически более выгодна и молекула находится в этой форме больше времени. С удлинением углеродной цепи число различимых конформаций увеличивается. Так, вращение по центральной связи в н-бутане 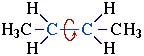 приводит к четырем поворотным изомерам:  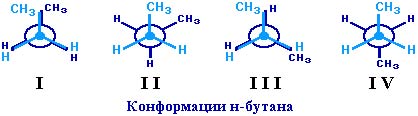 Наиболее устойчивым из них является конформер IV, в котором группы СН3 максимально удалены друг от друга. 2.2. Для предельных углеводородов, начиная с гептана, характерен еще один вид пространственной изомерии, когда два изомера относятся друг к другу как предмет и его зеркальное изображение (подобно тому, как левая рука относится к правой). Такие различия в строении молекул называют зеркальной, или оптической изомерией. Оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение. Если атом углерода в молекуле связан с четырьмя различными атомами или атомными группами, например:  то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами. Изомерия этого вида называется оптической или зеркальной, изомеры – зеркальными изомерами или оптическими антиподами:  Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии. Такие изомеры обладают оптической активностью (один из них вращает плоскость поляризованного света влево, а другой — на такой же угол вправо). Номенклатура алкановВ настоящее время общепринятой является систематическая номенклатура ИЮПАК. Первые четыре углеводорода носят исторически сложившиеся названия: метан, этан, пpопан, бутан, изобутан. Начиная с пятого гомолога названия алканов состоят из корня — греческого числительного и суффикса -ан: пентан, гексан, гептан, октан, нонан, декан и т.д. Для применения номенклатуры ИЮПАК необходимо знать названия и строение определенных фрагментов молекул – органических радикалов. Согласно международной номенклатуре изомеры с разветвленной цепью углеродных атомов следует рассматривать как производные алкана с самой длинной неразветвленной цепью. Правила образования названий разветвленных алканов по международной номенклатуре (ИЮПАК) 1.Найти самую длинную (главную) неразветвленную цепь углеродных атомов. 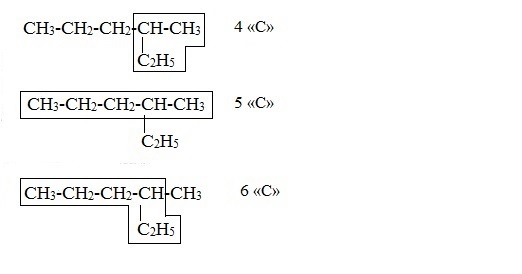 2. Пронумеровать атомы углерода главной цепи. Номер атома углерода, у которого находится заместитель (алкильный радикал), должен быть наименьшим.  3. Указать положение заместителя (номер атома углерода, у которого находится алкильный радикал). 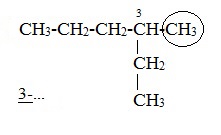 4. Назвать алкильный радикал в соответствии с его положением в цепи. 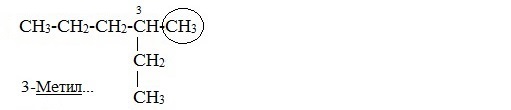 5. Назвать алкан, соответствующий главной цепи.  Если заместителем является галоген (фтор, хлор, бром, йод), то все номенклатурные правила сохраняются.  В молекуле с несколькими одинаковыми заместителями нужно указывать положение каждого заместителя через запятую (2,2-). После номера через дефис указывают количество заместителей (ди - два, три - три, тетра - четыре, пента - пять) и название заместителя (метил, этил, пропил). Далее без пробелов и дефисов название главной цепи. 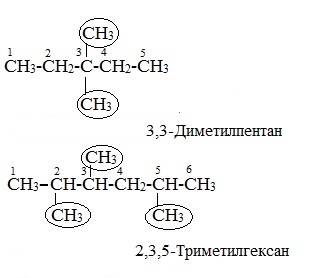 Разные заместители называются в алфавитном порядке. 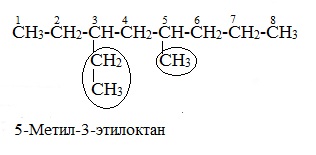 Способы получения аканов Алканы выделяют из природных источников (природный и попутный газ, нефть, каменный уголь). Газообразные алканы получают из природного и попутных нефтяных газов, а твердые алканы — из нефти. Природной смесью твердых высокомолекулярных алканов является горный воск — природный битум. Метан широко распространен в природе. Он является главной составной частью многих горючих газов как природных (80-97%), так и искусственных, выделяющихся при сухой перегонке дерева, торфа, каменного угля, а также при крекинге нефти. Природные газы, особенно попутные газы нефтяных месторождений, помимо метана содержат этан, пропан, бутан и пентан. Метан выделяется со дня болот и из каменноугольных пластов в рудниках, где он образуется при медленном разложении растительных остатков без доступа воздуха. Поэтому метан часто называют болотным или рудничным газом. В промышленности 1. Получение алканов из природных источников (нефть, природный газ) 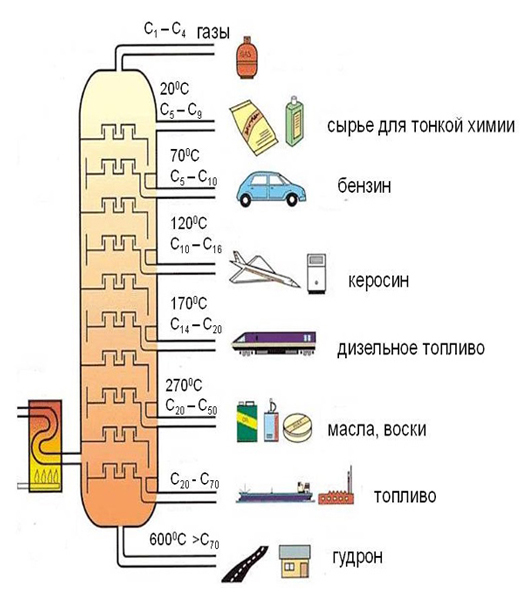 2. Синтезом на основе водяного газа из оксида углерода (II) и водорода можно получить метан: 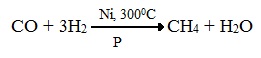 3. Синтезом из водяного газа (СО+Н2) получают смесь алканов: 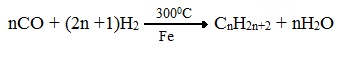 В лаборатории 1. Метан можно получить синтезом из простых веществ при нагревании, повышенном давлении в присутствии катализатора (Ni): 2. Гидролиз карбида алюминия (получение метана) 3. Взаимодействие карбида алюминия с сильными кислотами  4. Сплавление солей уксусной кислоты со щелочами (реакция Дюма)  5. Каталитическое гидрирование (+Н2) непредельных углеводородов  6. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца) Происходит димеризация углеродной цепи исходного галогеналкана, образуется алкан с четным числом атомов углерода в цепи:  Если в реакции участвуют разные галогеналканы, то образуется смесь алканов: 7. Электролиз растворов солей карбоновых кислот (реакция Кольбе)  Химические свойства алканов Члены гомологического ряда алканов имеют общие химические свойства. В обычных условиях алканы химически инертны. Они устойчивы к действию многих реагентов: не взаимодействуют с концентрированной серной и азотной кислотами, с концентрированными и расплавленными щелочами, не окисляются сильными окислителями – КМnО4 и т.п Химическая устойчивость алканов объясняется высокой прочностью σ–связей С ─ С и С ─ Н, а также их неполярностью. Неполярные связи С ─ С и С ─ Н в алканах не склонны к ионному разрыву, но способны расщепляться гомолитически под действием активных свободных радикалов. Поэтому для алканов характерны радикальные реакции (реакции замещения), в результате которых получаются соединения, где атомы водорода замещены на другие атомы или группы атомов. Алканы вступают в реакции, протекающие по свободно-радикальному (цепному) механизму и протекают обычно на свету или при нагревании. По этому механизму легче всего замещаются атомы водорода у третичных, затем вторичных и первичных атомов углерода. При хлорировании эта закономерность не соблюдается при T>400˚C. Алканы относятся к углеводородам, в которых отсутствуют кратные связи. Из-за предельности алканов реакции присоединения для них нехарактерны. Реакции замещения (разрыв связей С ─ Н)1. Галогенирование (замещение атома водорода атомом галогена — F, Cl, Br с образованием галогеналкана). Реакция галогенирования алканов протекает по радикальному цепному механизму, т.е. как цепь последовательных превращений с участием свободно-радикальных частиц. Теорию цепных реакций разработал советский ученый, один из основоположников химической физики, академик Н.Н. Семенов (1896—1986), за что в 1956 г. был награжден Нобелевской премией. Скорость реакции зависит от активности галогенов, которая уменьшается с увеличением радиуса атома. Алканы очень активно реагируют с фтором, реакция алканов с его участием сопровождается взрывом и окислением до СF4. Реакции хлорирования и бромирования протекают под действием света (фотохимическая цепная реакция) или при 300–400оC. Иодирование проходит обратимо, поэтому требуется окислитель для удаления НI из реакции. Низшие алканы (СН4, С2Н6, С3Н8) можно прохлорировать полностью. В молекуле метана атомы хлора могут заместить от одного до четырех атомов водорода в зависимости от соотношения реагентов Хлорирование метана: (hv — формула кванта света) 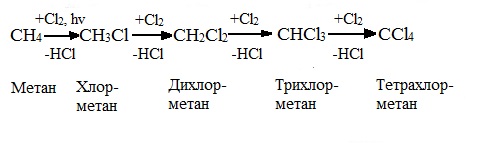 Тривиальное название трихлорметана – хлороформ. Механизм реакцииРеакция осуществляется в три стадии: А) Инициирование (зарождение цепи) – гомолитическое расщепление молекулы Сl2 с образованием свободных радикалов хлора:  Свободные радикалы – это атомы или группы атомов с неспаренными электронами (•Сl, •Н, •СН3…) Б) Развитие цепи (взаимодействие радикала хлора с молекулой алкана, метильного радикала с новой молекулой хлора и т.д.): 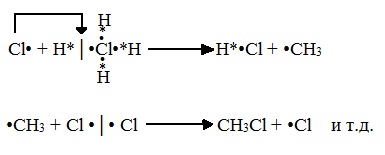 В) Обрыв цепи (происходит при соединении двух радикалов друг с другом):  Скорость реакции замещения водорода на атом галогена у галогеналканов выше, чем у соответствующего алкана, это связано с взаимным влиянием атомов в молекуле:  Электронная плотность связи С – Cl смещена к более электроотрицательному атому хлора, в результате этого на нем образуется частичный отрицательный заряд, а на атоме углерода – частичный положительный заряд. На атоме углерода в метильной группе (-СН3) создаётся недостаток электронной плотности, поэтому он оттягивает на себя электронную плотность от соседних атомов водорода, в результате этого связи С – Н становятся менее прочными и атомы водорода легче замещаются на атомы хлора. При увеличении углеводородного радикала наиболее подвижными остаются атомы водорода у атома углерода ближайшего к заместителю: Алканы обесцвечивают раствор брома при нагревании, вступая в реакцию радикального замещения. 2.Нитрование (замещение атома водорода нитрогруппой – NO2 с образованием нитроалканов R-NO2). Нитрующий реагент – разбавленная азотная кислота HNO3 (НО─NО2). Нитрование разбавленной азотной кислотой при t = 1400С и при повышенном или нормальном давлении - реакция М.И.Коновалова. В результате реакции образуется смесь изомерных нитросоединений. Наиболее легко замещаются атомы водорода у третичного атома углерода, труднее – у вторичного, наиболее трудно – у первичного:  3.Сульфирование (замещение атомов водорода сульфогруппой SO3Н с образованием алкансульфокислот RSO3Н). Сульфирующий реагент – серная кислота Н2SO4 (НО─SO3Н). Сульфирование алканов происходит при действии очень концентрированной Н2SO4 при небольшом нагревании. Наиболее легко замещается атом водорода у третичного атома углерода: 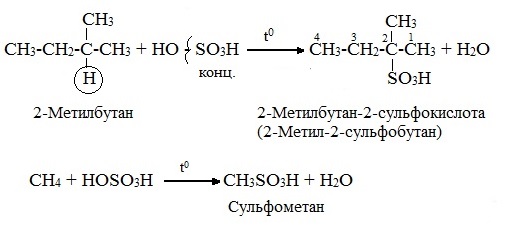 Реакции окисленияАлканы – соединения с низкими степенями окисления углерода и в зависимости от условий реакции они могут окисляться с образованием различных соединений. 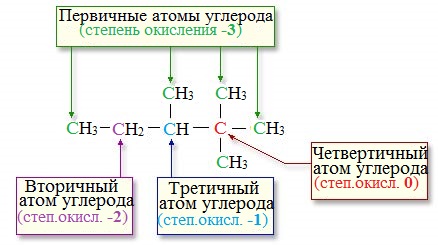 При обычных условиях алканы устойчивы к действию сильных окислителей (КМnO4, К2Сr2О7). 1. Горение (окисление кислородом воздуха при высоких температурах) А) Полное окисление (избыток О2) При избытке кислорода происходит полное окисление алканов до СО2, где углерод имеет высшую степень окисления +4, и воды. Горение углеводородов приводит к разрыву всех связей С–С и С–Н и сопровождается выделением большого количества тепла (экзотермическая реакция). Низшие гомологи (метан, этан, пропан, бутан) образуют с воздухом взрывоопасные смеси, что необходимо учитывать при их использовании. С увеличением молекулярной массы алканы загораются труднее. Процесс горения углеводородов широко используется для получения энергии (в двигателях внутреннего сгорания, в тепловых электростанциях и т.п.). Общий вид реакции горения алканов: 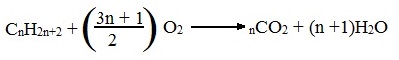 Б) Неполное окисление (недостаток О2) При горении высших алканов ((n >>1)) при недостатке кислорода образуются продукты частичного окисления: угарный газ СО (степень окисления углерода +2), сажа (мелкодисперсный углерод, со степенью окисления 0). Поэтому высшие алканы горят на воздухе коптящим пламенем, выделяя токсичный угарный газ, представляющий опасность для человека. Горение метана при недостатке кислорода происходит по уравнениям:  Последняя реакция используется в промышленности для получения сажи из природного газа, содержащего 80-97% метана. 2. Каталитическое окисление Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов. Например, при неполном окислении бутана происходит разрыв связи (С2–С3) и получается две молекулы уксусной кислоты: Этим способом в промышленности получают уксусную кислоту. При мягком окислении метана кислородом воздуха в присутствии катализаторов могут быть получены метиловый спирт, формальдегид и муравьиная кислота. 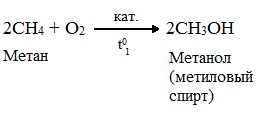 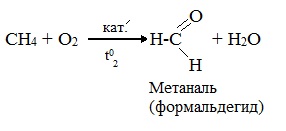 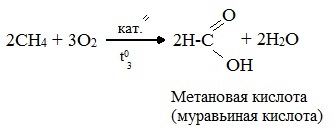 Высшие алканы (n>25) под действием кислорода воздуха в жидкой фазе в присутствии солей марганца превращаются в смесь карбоновых кислот со средней длиной цепи С12–С18, которые используются для получения моющих средств и поверхностно-активных веществ. Физические свойства алкановВ обычных условиях первые четыре члена гомологического ряда алканов – газы, углеводороды состава от C5Н12 до C15Н32 – жидкости, а начиная с C16Н34 – твердые вещества. Газообразные и твердые алканы не имеют запаха, жидкие алканы обладают характерным «бензиновым» запахом. Температуры плавления и кипения алканов, их плотности увеличиваются в гомологическом ряду с ростом молекулярной массы.  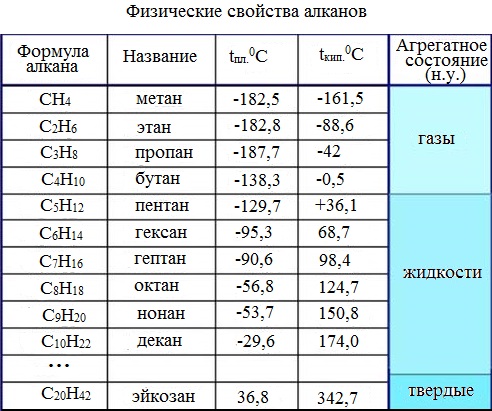 Предельные углеводороды — соединения неполярные. Они легче воды и практически нерастворимы в ней, однако, они способны растворяться в большинстве органических растворителей, в том числе и друг в друге. Жидкие алканы сами являются хорошими растворителями для многих органических веществ. Метан и этан, а также высшие алканы не имеют запаха. Алканы — горючие вещества. Метан горит бесцветным пламенем. Применение алкановПредельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека. Газообразные алканы используются в качестве ценного топлива.Жидкие алканы – это бензин, керосин, жидкость для разжига костров. Из твердых алканов делают свечи. Метан – является основным компонентом природных и попутных газов (60-99%). В состав природных газов входят пропан и бутан. Благодаря большой теплотворной способности метан в больших количествах расходуется в быту и в промышленности. Именно он горит в кухонных плитах и сжигается на теплоэлектростанциях для производства электроэнергии. В смеси с воздухом метан взровоопасен. Смесь пропана и бутана используется в качестве бытового топлива. Пропан и бутан при повышении давления сжижаются, поэтому пропаном заправляют балоны для тушения пожаров. Пропан-бутановой смесью заправляют зажигалки. 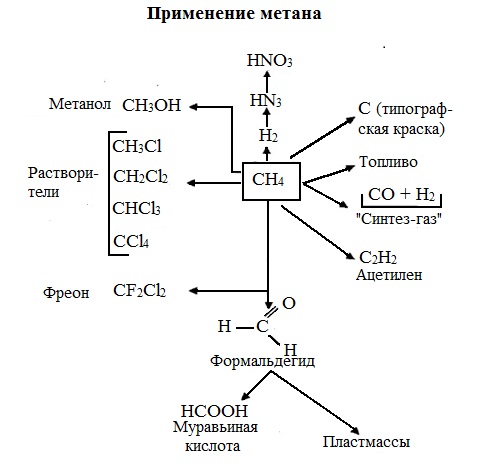 Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей. Большое промышленное значение имеет окисление высших предельных углеводородов – парафинов с числом углеродных атомов 20-25. Этим путем получают синтетические жирные кислоты с различной длиной цепи, которые используются для производства мыл, различных моющих средств, смазочных материалов, лаков и эмалей. Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода до 15) — пpозpачная жидкость без запаха и вкуса, используется в медицине, паpфюмеpии и косметике. Вазелин (смесь жидких и твеpдых пpедельных углеводоpодов с числом углеpодных атомов до 25) пpименяется для пpиготовления мазей, используемых в медицине. Паpафин (смесь твеpдых углеводоpодов С19-С35) — белая твеpдая масса без запаха и вкуса (tпл= 50-70°C) — пpименяется для изготовления свечей, пpопитки спичек и упаковочной бумаги, для тепловых пpоцедуp в медицине и т.д. В современной нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Нормальные предельные углеводороды средней молекулярной массы используются как питательный субстрат в микробиологическом синтезе белка из нефти. Большое значение имеют галогенопроизводные алканов, которые используются как растворители, хладоагенты и сырье для дальнейших синтезов. |
