Использование_термогравиметрического_метода_анализа_для_определения. Использование_термогравиметрического_метода_анализа_для_определе. Реферат. 3 Введение. 4 Общая часть. 6 Сульфаниламиды и их фармакологическое действие. 6
 Скачать 0.9 Mb. Скачать 0.9 Mb.
|
1 2 СОДЕРЖАНИЕ Реферат. 3 Введение. 4 Общая часть. 6 Сульфаниламиды и их фармакологическое действие. 6 Физико-химические свойства сульфаниламидов. 7 Фармакологические параметры сульфаниламидов. 8 Лекарственные препараты, содержащие сульфаниламиды. 10 Испытание на подлинность сульфаниламидов. 11 Методы количественного определения сульфаниламидов. 14 Специальная часть. 16 Термогравиметрический метод анализа. 16 Методика ТГА. 17 Оценка качества сульфаниламида методом термогравиметрического анализа. 18 Заключение. 32 Список используемой литературы. 33 Реферат Курсовая работа включает 33 страницы, 7 рисунков, 5 литературных Ключевые слова: СУЛЬФАНИЛАМИДЫ, ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА СУЛЬФАНИЛАМИДОВ, ТЕРМОГРАВИМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА. Тема работы: «Использование термогравиметрического метода анализа для определения качества сульфаниламидных препаратов». Цель работы: Изучить термогравиметрический метод анализа для определения качества сульфаниламидных препаратов. Задачи работы: Рассмотреть свойства сульфаниламидов. Описать методы количественного определения сульфаниламидов. Описать термогравиметрический метод анализа для сульфаниламидных препаратов. В специальной части представлены некоторые методики определения сульфаниламидов лекарственном растительном сырье, в частности, определение сульфаниламидов методом термогравиметричеекого анализа. Приведены результаты экспериментов и сделаны выводы по оптимальной методике анализа и выращивания лекарственного сырья. Введение Проблема обеспечения качества лекарственных средств сохраняет свою актуальность как на национальном, так и на международном уровне. Это обусловлено расширением их номенклатуры в первую очередь за счет увеличения воспроизведенных лекарственных средств, вовлечением в сферу обращения наряду с лекарственными препаратами фармацевтических субстанций. В условиях рыночного развития экономики страны в производство лекарственных средств включаются предприятия, не занимавшиеся ранее фармацевтическим производством, и использующие различные технологичные схемы получения лекарственных средств. Многообразие технологических процессов получения как субстанций, так и лекарственных препаратов на различных заводах привело к существованию на фармацевтическом рынке лекарственных средств одного наименования, но изготовленных по разным технологиям и вследствие этого различающихся по наличию или отсутствию полиморфных форм, сольватов и/или кристаллогидратов, что влияет на их биодоступность и ряд технологических характеристик. Современные требования к качеству лекарственных средств характеризуются тенденцией к получению новых или дополнительных данных о свойствах и химических превращениях лекарственных веществ в составе лекарственных форм с помощью таких методов, которые еще не получили широкого распространения в фармацевтическом анализе и контроле процесса производства. К таким методам относятся ИК- спектроскопия в вариантах нарушенного полного внутреннего отражения (HПBO) и ближней инфракрасной спектроскопии (БИК), дифференциальная сканирующая калориметрия (ДСК) и термогравиметрический анализ (ТГА). Я решила проверить качество с помощью ТГА. Общая часть Сульфаниламиды и их фармакологическое действие Сульфаниламиды (лат. sulfanilamidum) это гpyппa химических Фармакологическое действие. Сульфаниламиды действуют бактериостатически, то есть обладают химиотерапевтической активностью при инфекциях, вызванных грамположительными и грамотрицательными бактериями, некоторыми простейшими (возбудители малярии токсоплазмоза), хламидиями (при трахоме, паратрахоме). Их действие связано главным образом с нарушением образования микроорганизмами необходимых для их развития ростовых факторов - фолиевой и дигидрофолиевой кислот и других веществ, в молекулу которых входит пара-аминобензойная кислота. Механизм действия связан со структурным сходством сульфаниламидного фрагмента с пара- аминобензойной кислотой (ПАБК) - субстрата фермента дигидроптероатсинтетазы, синтезирующим дигидроптероевую кислоту, что ведёт к конкурентному угнетению дигидроптероатсинтетазы. Это, в свою очередь, приводит к нарушению синтеза из дигидроптероевой дигидрофолиевой, а затем тетрагидрофолиевой кислоты и в результате к нарушению синтеза нуклеиновых кислот у бактерий. Физико-химические свойства сульфаниламидов К лекарственным средствам, производным пара- аминобензолсульфониламидов, относятся препараты, обладающие различным фармакологическим действием: антибактериальным, антидиабетическим, диуретическим, антисептическим. Рассмотрим свойства антибактериальных производных сульфаниламидов. Структурной единицей сульфаниламидов является амид п- аминобензол-сульфоновой (сульфаниловой) кислоты (рис.1): О  л-w беюолгутфоіоzвR imriioщ л-w беюолгутфоіоzвR imriioщH,N О  S—NHj Аюід сулфаюшовэй кислоты S—NHj Аюід сулфаюшовэй кислотыСульфаниламид — белый кристаллический порошок, без запаха. Мало растворим в воде и спирте, хорошо растворим в кипящей воде и в растворах щелочей. Стрептоци.д растворимый — белый кристаллический порошок, без запаха. Хорошо растворим в воде. Практически не растворим в органических растворителях. Сульфацетамид натрия — легко растворим в воде, практически нерастворим в спирте. Водный раствор (1:20) имеет pH между 8,0 и 9,5. Фармакологические параметры сульфаниламидов. Имеющиеся сульфаниламидные средства различаются по фармакологическим параметрам. Стрептоцид, норсульфазол, сульфазин, сульфадимезин, этазол, сульфапиридазин, сульфадиметоксин и др. относительно легко всасываются и быстро накапливаются в крови и органах в бактериостатических концентрациях, проникают через гистогематические барьеры (гематоэнцефалический, плацентарный и др.); они находят применение при лечении различных инфекционных заболеваний. Другие препараты, такие как фталазол, фтазин, сульгин, трудно всасываются, относительно долго находятся в кишечнике в высоких концентрациях и выделяются преимущественно с калом. Поэтому они применяются главным образом при инфекционных заболеваниях желудочно-кишечного тракта. Уросульфан выделяется в значительном количестве почками; он применяется преимущественно при инфекциях мочевых путей. По времени выделения из организма сульфаниламиды можно разделить на 4 группы: препараты короткого действия (стрептоцид, норсульфазол, этазол, сульфадимезин и др.); среднего действия (сульфазин и др.); длительного действия (сульфапиридазин, сульфамонометоксин, сульфадиметоксин и др.); сверхдлительного действия (сульфален и др.). Препараты, медленно выделяющиеся из организма, называют депо- сульфаниламиды. Их медленное выведение связано в значительной мере со способностью обратно всасываться (реабсорбироваться) в почечных канальцах после фильтрации клубочками. Всасывание и скорость выведения из организма в значительной мере определяют величину дозы и частоту приёма препаратов. Максимальная концентрация в крови препаратов короткого действия понижается на 50% обычно менее чем за 8 ч, а выделение 50% их с мочой происходит менее чем за 16 ч. Снижение максимальной концентрации в крови на 50% препаратов среднего и длительного действия происходит соответственно через 8 - 16 и 24 - 48 ч, выделение 50% с мочой - через 16 - 24 и 24 - 56 ч, что дает возможность назначать эти препараты реже и в меньших дозах. Ещё медленнее выделяются препараты сверхдлительного действия: их максимальная концентрация в крови сохраняется до 7 дней. Сульфаниламидные препараты можно при необходимости применять в разных соиетаниях. Плохо всасывающиеся препараты можно назначать одновременно с хорошо всасывающимися. Можно комбинировать сульфаниламиды с антибиотиками. Лекарственные препараты, содержащие сульфаниламиды Сульфаниламидные препараты: Сульфаниламид (стрептоцид) — практически не используется сегодня ввиду низкой эффективности и большой токсичности; Сульфадимидин (сульфадимезин) — менее токсичный препарат, однако также не отличается высокой активностью; Сульфакарбамид (уросульфан) — ранее широко применялся при лечении инфекций мочеполовой системы; Сульфадиазин (сульфазин) — более активный, чем другие сульфаниламиды, создаёт высокие концентрации в крови; Сульфаметоксазол — хорошо проникает в различные органы и ткани; Сульфадиметоксин — средство длительного действия; Сульфамонометоксин — относительно малотоксичен; Сульфадоксин — используется для лечения малярии в комбинации с антиметаболитом пириметамином; Сульфаметоксипиридазин — применяется при лечении OP3, пневмании, бронхита и д.р.; Сульфален — препарат сверх длительного действия; 11.Сульфагуанидин (сульгин) — эффективен при лечении кишечных инфекций; Фталлилсульфатиазол (фталазол) — концентрации в просвете кишечника; создаёт высокие Сульфадиазин серебра (дермазин) — средство для местного Сульфасалазин кишечное противоспалительное и антиревматическое средство; Испытание на подлинность сульфаниламидов Сульфаниламиды — полифункциональные соединения, реакционная способность которых определяется первичной ароматической аминогруппой и сульфаниламидной группой в пара-положении. Основные свойства сульфаниламидов обусловлены ароматической аминогруппой и проявляются при растворении сульфаниламидов в кислотах с образованием солей. Кислотные своиства обусловлены присутствием группы —S02NH — (NН-кислоты). Поэтому практически все сульфаниламиды хорошо растворимы в щелочах и могут быть получены в виде натриевых солей (норсульфазол-натрий, сульфацил-натрий). Однако кислотные свойства выражены по-разному: для стрептоцида pKa = 10.4, сульфацила pKa — 5. Натриевые соля сульфаниламидов хорошо растворимы в воде. При этом вследствие гидролиза их водные растворы имеют щелочную реакцию. При оценке качества ЛС — растворов натриевых солей сульфаниламидов — определяют pH. Повышенная щелочность может быть связана как с нарушением условий, так и с гидролизом солей. Например, в препарате сульфацил-натрия требуемое значение щелочности должно находиться в пределах pH 7.5 — 8.3. Сульфаниламиды, проявляющие кислотные свойства, не растворимы в воде, но растворимы в растворах щелочей. Кислотные свойства  сульфаниламидов используются при определении подлинности и количественном определении (фталазол) по реакциям с солями металлов сульфаниламидов используются при определении подлинности и количественном определении (фталазол) по реакциям с солями металлов(CuS04. CoCl2, AgN0з). Чаще всего используют реакцию с CuS04. Определение проводят в присутствии щелочи, которую добавляют в строго эквивалентном количестве (во избежание образования гидроксида меди). Норсульфазол дает грязно-фиолетовую, сульфадимезин — зеленую, переходящую в бурую; этазол — травянисто-зеленую, переходящую в черную, а сульфацил натрия образует голубой осадок изменяющийся во времени по интенсивности. Стрептоцид вследствие слабых кислотных свойств устойчивых комплексов с солями тяжелых металлов не образует. Реакция гидролитического расщепления. Гидролиз сульфаниламидов протекает по сульфамидной гpyппe. При гидролизе фталазола происходит образование малорастворимого 2-аминотиазола, по температуре плавления которого определяют подлинность препарата. Реакции окисления. Сульфаниламиды при окислении образуют окрашенные соединения. Окисление может происходить под действием кислорода воздуха, особенно в растворах. Например, появление желтой окраски раствора сульфацил-натрия свидетельствует об окислении препарата. Степень окисления препаратов может быть оценена по эталонам цветности. На способности окисляться основана реакция пиролиза сульфаниламидов, т.е. термическое разложение на воздухе. При этом кристаллические сульфаниламиды при нагревании образуют окрашенные плавы. При пиролизе стрептоцида образуется плав фиолетово-синего цвета с выделением аммиака; нор-сульфазол дает плав темно-бурого цвета с запахом сероводорода. Общие реакции подлинности. На CBoбoДнyю aMинoгpУппУ: Диазотирование - азосочетание:  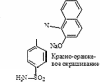 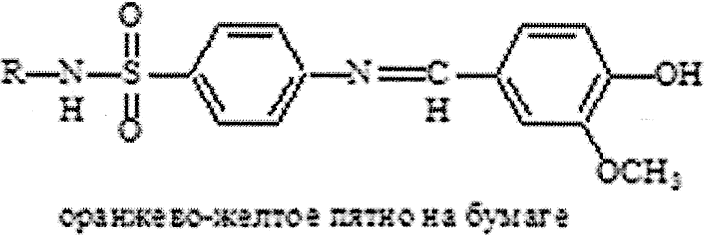 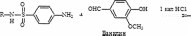 С Br , I2 (выпадение осадка): 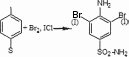 На сульфогруппу. Мокрая минерализация: 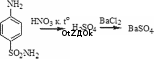 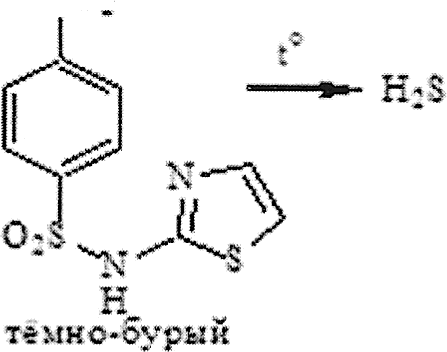 Наличие у сульфаниламида кислотных свойств позволяет в случае необходимости получать натриевое производное, а затем проводить реакцию с сульфатом меди: 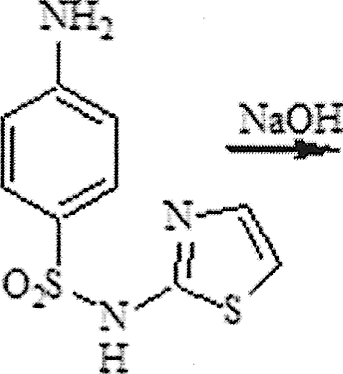  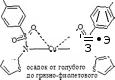 На азо-группу (происходит обесцвечивание):  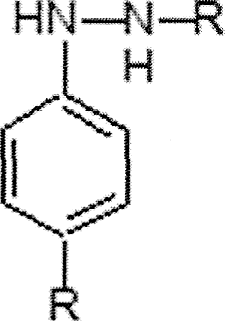 Методы количественного определение сульфаниламидов Современные требования к качеству лекарственных средств характеризуются тенденцией к получению новых или дополнительных данных о свойствах и химических превращениях лекарственных веществ в составе лекарственных форм с помощью таких методов, которые еще не получили широкого распространения в фармацевтическом анализе и контроле процесса производства. К таким методам относятся ИК- спектроскопия в вариантах нарушенного полного внутреннего отражения (HПBO) и ближней инфракрасной спектроскопии (БИК), дифференциальная сканирующая калориметрия (ДСК) и термогравиметрический анализ (ТГА). Метод HПBO, в отличие от общепринятого варианта ИК- спектроскопии пропускания в дисках калия бромида или суспензии в масле, не требует специальной пробоподготовки образца и может быть использован в качестве экспресс-метода в испытаниях на подлинность лекарственных средств. В последнее время возрос интерес к ближней области ИК- спектроскопии (БИК), но ее место в системе контроля качества лекарственных средств до конца не определено. Термоаналитические методы анализа (ДСК и ТГА) находят практическое применение в анализе полиморфных форм веществ, для выявления различий в технологии получения субстанций и определения полиморфных форм веществ или примесей в лекарственных формах. Таким образом, обоснование применения данных методов в системе контроля качества и производства лекарственных средств является актуальным и своевременным. Специальная часть Термогравиметрический метод анализа Термогравиметрия или термогравиметрический анализ (ТГ) метод термического анализа, при котором регистрируется изменение массы образца в зависимости от температуры. Этот метод анализа заключается в наблюдении массы исследуемой навески вещества при изменении её температуры. Результатом анализа являются ТГ-кривые — зависимости массы навески (или изменения массы навески) от температуры или времени. Для интерпретация результатов ТГ- анализа необходима обработка ТГ-кривых. В частности, производная от ТГ- сигнала (скорость изменения массы), представляемая кривой ДТГ, позволяет установить момент времени или температуру, при которой изменение веса происходит наиболее быстро. ТГ-анализ широко используется в исследовательской практике для определения температуры деградации полимеров, влажности материалов, доли органических и неорганических компонентов, входящих в состав исследуемого вещества, точки разложения взрывчатых веществ и cyxoгo остатка растворенных веществ. Метод также пригоден для определения скорости коррозии при высоких температурах. При синхронном ТГ-ДТА/ДСК анализе одновременно измеряется изменение теплового потока и массы образца как функция от температуры или времени, обычно при этом используется контролируемая атмосфера. Такой синхронный анализ не только увеличивает производительность измерений, но и упрощает интерпретацию результатов, благодаря возможности отделить эндо- и экзотермические процессы, не сопровождающиеся изменением массы (например, фазовые переходы) от тех, при которых происходит изменение массы (например, деградация). 2.1.1 Методика ТГА Термоанализатор состоит из высокоточных весов с тиглями (как правило, платиновыми), которые размещаются в камере небольшой электропечи. В непосредственной близости от образца, например, под донышком тигля, находится контрольная термопара, с высокой точностью измеряющая температуру. Камера печи может заполняться инертным газом для предотвращения окисления или иных нежелательных реакций. Для управления измеряющей аппаратурой и снятия показаний используется компьютер. В процессе анализа температура поднимается с постоянной скоростью, и записывается изменение массы в зависимости от температуры. Верхний предел температуры ограничен только возможностями прибора, и может достигать 1500 °С и более. При этом, благодаря хорошей теплоизоляции печи температура на её внешней поверхности невысока и не вызывает ожога. В методе ТГ-анализа высокое разрешение достигается за счёт наличия петли обратной связи между весом образца и его температурой. Нагрев замедляется по мере изменения веса образца, и, таким образом, температуру, при которой изменяется вес можно установить с большой точностью. Многие современные термоанализаторы позволяют подключить к выходному штуцеру печи инфракрасный спектрофотометр для непосредственного анализа химического состава газа. Оценка качества термогравиметрического анализа. сульфаниламида методом Объекты исследования: стрептоцид, стрептоцид растворимый, сульфацил-натрий, сульгин, норсульфазол, норсульфазол-натрий, фталазол, этазол, сульфален, сульфадимезин, сульфадимезин-натрий, сульфадиметоксин и сульфаметоксазол. Общее количество серий образцов составило 167, из них 117 серий — субстанции и 50 серий — промышленные лекарственные формы (таблетки, порошки, мазь, глазные капли). В работе использовались образцы лекарственных средств, отвечающие требованиям действующей нормативной документации (ФСП или НД). Исследование термическими методами проводилось на приборах с модулями DSC822e и TGAl фирмы «Mettler Tolledo» в диапазоне температур от 0 до 500 °С, с использованием системы термического анализа STARe (2005 г). Работа проводилась согласно следующей схеме: вначале исследовали обр ец при стандартном режиме нагревания (от 30 до 300 °С со скоростью 5 °С/мин). Появление пиков на кривой ДСК свидетельствовало об изменении энтальпии, связанных с фазовым переходом вещества. Для установления однородности пиков нагревание проводили со скоростью 1 и 100 °С/мин. Термическую устойчивость пиков изучали нагреванием от 30 °С до температуры максимума пика, последующем охлаждением образца до 30°C и повторным нагреванием до 300 °С (скорость нагревания была постоянной — 5 °С/мин). Исследование соединения термогравиметрическим методом (ТГА) дало дополнительную информацию о возможной природе отмеченных пиков. В результате проведенного исследования установлено, что пик на термограммах субстанции и таблеток стрептоцида с максимумом при температуре около 164.0 °С является фазовым переходом вещества из кристаллической формы в жидкую. Процесс плавления стрептоцида является обратимым и после плавления вещество восстанавливает свою 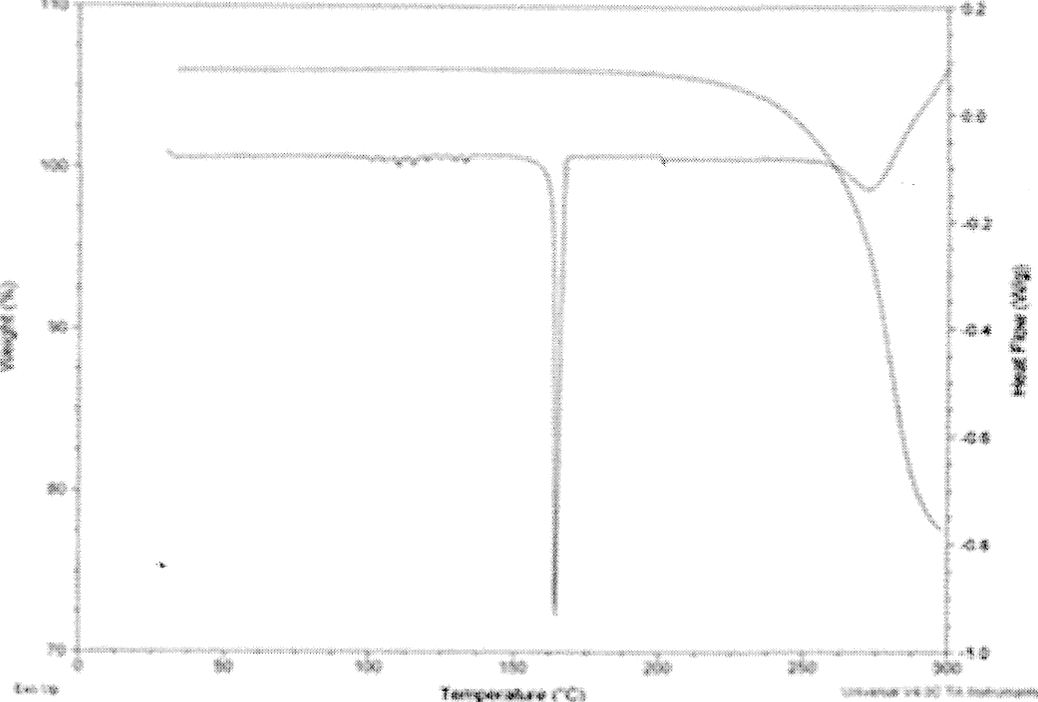 кристаллическую структуру. Кроме данного пика на термограммах обнаружены низкоинтенсивные пики, свидетельствующие о присутствии в стрептоциде метастабильных полиморфных форм, которые после плавления переходят в основную форму. Их присутствие подтверждено плавлением образца со скоростью нагревания 100 °С/мин (рис. 1). Примесь полиморфной формы была обнаружена также на термограммах таблеток стрептоцида. Термограммы субстанциистрептоцида растворимого различных серий и заводов-изготовителей имеют различия в области фазового перехода вещества, что возможно, связано с разрушением структуры. кристаллическую структуру. Кроме данного пика на термограммах обнаружены низкоинтенсивные пики, свидетельствующие о присутствии в стрептоциде метастабильных полиморфных форм, которые после плавления переходят в основную форму. Их присутствие подтверждено плавлением образца со скоростью нагревания 100 °С/мин (рис. 1). Примесь полиморфной формы была обнаружена также на термограммах таблеток стрептоцида. Термограммы субстанциистрептоцида растворимого различных серий и заводов-изготовителей имеют различия в области фазового перехода вещества, что возможно, связано с разрушением структуры.а)   I  B) B)137Œ’C    152.56 C 152.56 C    °С/мин (г, д); термостабильность (в); термограммы ДСК таблеток стрептоцида (е). На термограммах ДСК всех образцов субстанции сульфацил-натрия четко видны два эндотермических пика с разной интенсивностью. По характеру термограмм ДСК исследуемые образцы сульфацил-натрия были разделены на две группы. На термограммах образцов первой группы между указанными пиками присутствует широкий эндотермический пик, а на термограммах второй группы — многочисленные низкоинтенсивные пики. Форма пиков и их поведение при различных режимах нагревания позволяют предположить, что первый пик (144,0 °С) на термограммах сульфацил-натрия является плавлением кристаллогидратной формы, второй — удалением растворителя (179,8 °С), третий пик (266,7 °С) — фазовым переходом кристаллической формы сульфацил-натрия, которая плавится с аморфизацией. Микроскопическое исследование субстанций сульфацил— натрия выявило различия по форме и размеру кристаллов между исследуемыми образцами (рис. 2).     168.57”C 168.57”Ci ł 26ł.45“C 264 O2*C 143.10”C  B) B) ” 22   е) е)Из термограммы сульгина следует, что анализируемый образец содержит несколько полиморфных форм, одна из которых является кристаллогидратом и/или сольватом, две другие — собственно полиморфными формами. Установлено, что температура плавления сульгина в таблетках и субстанциях практически совпадает (рис. 3). 1 2 |
