невра 1. 1. Анатомия сосудов головного мозга. Виллизиев круг. Кровоснабжение и отток. Бассейны. Анатомия кровоснабжения головного мозга
 Скачать 0.82 Mb. Скачать 0.82 Mb.
|
1 2 1.Анатомия сосудов головного мозга. Виллизиев круг. Кровоснабжение и отток. Бассейны. Анатомия кровоснабжения головного мозга. Мозг снабжается кровью 4 крупными сосудами, являющимися непос-редственными или опосредованными ветвями дуги аорты — 2 внутренними сонными и 2 позвоночными артериями (рис. 1). Внутренняя сонная артерия (ВСА) (a. carotis interna) является самой крупной ветвью общей сонной арте-рии (a. carotis communis). Она возникает при делении последней на уровне поперечных отростков СIII—СIV. В самом начале ВСА имеется ее расширение (sinus caroticus). Здесь же в ее стенке располагается небольшое утолщение — сонный клубок (glomus caroticus). В нем находятся специальные «гломусные клетки», дендриты которых имеют рецепторные аппараты — баро- и хемо-рецепторы. Правая общая сонная артерия (ОСА) берет начало от плечеголовного ствола (truncus brachiocephalicus), отходящего от аорты. Левая общая сонная артерия отходит непосредственно от дуги аорты. Позвоночная артерия (ПА) (a.vertebralis) является ветвью подключичной артерии (a. subclavia). Правая подключичная артерия, как и правая ОСА, отходит от плечеголовного ство-ла, а левая — от дуги аорты. 2/3 всего количества крови, поступающей в мозг человека, доставляется ВСА (каротидными) артериями, 1/3 — позвоночными (вертебральными). Первые из них образуют каротидную (КС), а вторые — вертебрально-базилярную (ВБС) системы кровоснабжения мозга (рис. 1). ВСА проходит через каротидное отверстие (foramen caroticus) в основании черепа в одноименный канал (canalis caroticus) в пирамиде височной кости. Выйдя из этого канала в полость черепа, ВСА проникает в пещеристую ве-нозную пазуху, где образует S-образный изгиб, так называемый сифон, обычно состоящий из 2 колен. В полости черепа от внутренней сонной арте-рии отходит глазная артерия (arteria ophtalmica). После этого ВСА проходит через твердую мозговую оболочку, попадает в субарахноидальное простран-ство и уже здесь, оказавшись вблизи от турецкого седла, отдает ветви: перед-нюю ворсинчатую артерию (a. choroidea anterior) и заднюю соединительную артерию (a. communicans posterior). После этого ВСА делится на две конечные ветви: переднюю мозговую артерию (ПМА) (a. cerebri anterior) и среднюю мозговую артерию (СМА) (a. cerebri media) (рис. 1). Позвоночные артерии (ПА) на шее проходят через костный канал, образо-ванный отверстиями поперечных отростков VI—II шейных позвонков. Вый-дя из отверстия поперечного отростка позвонка СII, ПА делает изгиб, пово-рачивая кнаружи, а затем вверх, проходит сквозь отверстие поперечного от-ростка атланта и через большое затылочное отверстие проникает в полость черепа. Субокципитальная часть ПА образует извитость, которая при пово-ротах и сгибаниях головы предотвращает ее резкое растяжение. Прободая ат-лантозатылочную мембрану (membrana atlanto-occipitalis) и твердую мозго-вую оболочку, обе ПА, сближаясь, подходят к нижней поверхности продол-говатого мозга. На его границе с мостом они соединяются, образуя базиляр-ную артерию (a. basilaris). От ПА уже в полости черепа отходят ветви, кото-рые, соединяясь, образуют переднюю спинномозговую артерию (a. spinalis anterior). Кроме того, от ПА до места их слияния отходят менингеальные ветви и нижняя задняя мозговая артерия (a. cerebelli inferior posterior), участ-вующие в снабжении кровью продолговатого мозга и мозжечка. Базилярная артерия на границе моста со средним мозгом делится на две задние мозговые артерии (ЗМА). От базилярной артерии и задних мозговых артерий отходят: передняя нижняя мозжечковая артерия (a. cerebelli inferior anterior) и отходящая от нее ветвь внутреннего слухового прохода (a. labyrin-thi), верхняя мозжечковая артерия (a. cerebelli anterior). Артериальный круг большого мозга (circulus arteriosis cerebri), или Вилли-зиев круг, является наиболее постоянным и важным связующим звеном между КС и ВБС кровоснабжения мозга. Этот круг составляют дистальные фрагменты обеих ВСА, проксимальные участки обеих СМА ПМА, передней соединительной артерии, а также фрагменты ЗМА и задние соединительные артерии. Отступления от этой схемы построения артериального круга большого мозга возможны в 50—80% случаев (Беленькая P.M., 1979). Парные ПМА, СМА, ЗМА, передняя ворсинчатая артерия и их многочисленные ветви обеспечивают кровоснабжение промежуточного мозга и больших полушарий Передние мозговые артерии дистальнее передней соединительной артерией огибает мозолистое тело и образует большую дугу на медиальной поверхности полушария. Затем артерия направляется вверх и заканчивается в задних отделах теменно-затылочной борозды. По пути следования от нее отходят ветви, основными из которых являются переднемедиальные центральные, короткая и длинная центральные, переднемедиальные центральные, перикаллезная, медиальная лобно-базальная, мозолисто-краевая, парацентральная, предклинная и теменно-затылочная артерии. Ветви ПМА снабжают кровью большую часть медиобазальных структур большого полушария, его верхний медиальный край и парасагиттальную часть передних отделов его конвекситальной поверхности, головки хвостато-го ядра, передней части скорлупы, части бледного шара, белого вещества медиобазальной части полушария, расположенной впереди от хиазмы. ПМА анастомозирует со СМА и ЗМА. Средняя мозговая артерия (a. cerebri media) — самая крупная из артерий мозга. В ней выделяют клиновидную, островковую и конечную (корковую) части. От клиновидной части отходят переднелатеральные таламостриарные артерии. От островковой — островковые артерии, латеральная лобно-глазничная ветвь, возможно, передняя ворсинчатая артерия (у многих эта артерия отходит непосредственно от ствола ВСА), промежуточная височная артерия, задняя височная артерия. От конечной части отходят артерии центральной борозды, прецентральной борозды, постцентральной борозды, передняя и задняя теменные артерии, артерия угловой извилины. Глубокие ветви СМА, отходящие от ее проксимального участка на основании мозга, снабжают кровью переднюю часть заднего бедра внутренней капсулы, часть хвостатого ядра, скорлупу, часть таламуса, наружную часть бледного шара. Одну из глубоких ветвей средней мозговой артерии Шарко называл arteria gemorragica, считая, что она часто является источником внутримозговых кровоизлияний. Задняя мозговая артерия (a. cerebri posteror) огибает ножку мозга и идет к наружному коленчатому телу. Далее направляется через отверстие намета мозжечка к височной доле, проходит по внутреннему краю ее нижней по-верхности и достигает полюса затылочной доли. Основные ветви задней мозговой артерии — заднемедиальные центральные артерии, таламические ветви, медиальные задние ворсинчатые ветви, ножковые ветви, латеральная и медиальная затылочные артерии, шпорная ветвь, направляющаяся к корковому полю 17, по Бродману (к корковому концу зрительного анализатора). Небольшая часть этого поля получает кровь из СМА, чем и объясняется сохранность макулярного зрения при гомонимной гемианопсии, обусловленной окклюзией ЗМА. В месте прохождения ЗМА через тенториальное отверстие может сдавливаться при вклинении височной доли. В глубину полушария уходят 3 ветви ЗМА: таламоперфорирующая, премаммилярная и таламоколенчатая. Они снабжают кровью задненижнюю часть зрительного бугра и гипоталамической области, утолщение мозолистого тела, зрительный венец и льюисово тело. Самая крупная из этих ветвей — задняя ворсинчатая артерия, которая кончается в сосудистом сплетении III мозгового желудочка. 2.Каротидный бассейн. Топографическое расположение. Важность бассейна. Близость к сосудам и нервам. 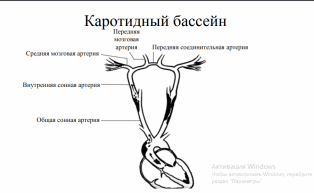 Сонные артерии формируют каротидный бассейн. Они берут своё начало в грудной полости: правая от плечеголовного ствола (лат. truncus brachiocephalicus), левая — от дуги аорты (лат. arcus aortae). Сонные артерии обеспечивают около 70-85 % притока крови к мозгу. Система каротидного бассейна в своем начальном отрезке представлена общими сонными артериями. Правая общая сонная артерия является ветвью плечеголовного ствола, левая — непосредственно отходит от аорты. На уровне верхнего края щитовидного хряща общая сонная артерия разветвляется на наружную и внутреннюю сонные артерии (см. рис. 11.1 на цветной вклейке). Затем через foramen caroticum внутренняя сонная артерия (ВСА) входит в canalis caroticum пирамиды височной кости. После того как артерия выходит из канала, она проходит по передней стороне тела крыловидной кости, вступает в sinus cavernosus твердой мозговой оболочки и доходит до места под передним продырявленным веществом, где делится па конечные ветви. В составе ВСА топографически выделяют 5 отделов: шейный, каменистый, кавернозный, клиноидный и супраклиноидный (см. рис. 11.1). Указанные отделы подразделяются на сегменты, начало нумерации которых начинается от развилки ВСА. Система каротидного бассейна в своем начальном отрезке представлена общими сонными артериями. Правая общая сонная артерия является ветвью плечеголовного ствола, левая — непосредственно отходит от аорты. На уровне верхнего края щитовидного хряща общая сонная артерия разветвляется на наружную и внутреннюю сонные артерии (см. рис. 11.1 на цветной вклейке). Затем через foramen caroticum внутренняя сонная артерия (ВСА) входит в canalis caroticum пирамиды височной кости. После того как артерия выходит из канала, она проходит по передней стороне тела крыловидной кости, вступает в sinus cavernosus твердой мозговой оболочки и доходит до места под передним продырявленным веществом, где делится па конечные ветви. В составе ВСА топографически выделяют 5 отделов: шейный, каменистый, кавернозный, клиноидный и супраклиноидный (см. рис. 11.1). Указанные отделы подразделяются на сегменты, начало нумерации которых начинается от развилки ВСА. атеросклероз; сахарный диабет; гипертонический синдром; нарушение обмена веществ; нарушение свертываемости крови; склонность к кровотечениям; сердечнососудистые патологии; инфекционные болезни; шейный остеохондроз и пр. Нарушение работы сосудов каротидного бассейна редко проходит незамеченным. У человека, в организме которого возникли серьезные проблемы с сосудами, снабжающими кровью мозг, появятся следующие симптомы: нарушение мозговой деятельности; ухудшение зрения; потеря памяти; невнятная речь; нарушение ориентации в пространстве; головокружение, головные боли; онемение или тремор конечностей; тошнота и приступы рвоты; нарушение двигательных функций. 3. ПМА (передняя мозговая артерия), ветви. Топографическое расположение. Важность бассейна. Близость к другим сосудам и нервам. Передние мозговые артерии дистальнее передней соединительной артерией огибает мозолистое тело и образует большую дугу на медиальной поверхности полушария. Затем артерия направляется вверх и заканчивается в задних отделах теменно-затылочной борозды. По пути следования от нее отходят ветви, основными из которых являются переднемедиальные центральные, короткая и длинная центральные, переднемедиальные центральные, перикаллезная, медиальная лобно-базальная, мозолисто-краевая, парацентральная, предклинная и теменно-затылочная артерии. Ветви ПМА снабжают кровью большую часть медиобазальных структур большого полушария, его верхний медиальный край и парасагиттальную часть передних отделов его конвекситальной поверхности, головки хвостатого ядра, передней части скорлупы, части бледного шара, белого вещества медиобазальной части полушария, расположенной впереди от хиазмы. ПМА анастомозирует со СМА и ЗМА. Важность бассейна: Изолированный инфаркт зоны кровоснабжения ПМА наблюдается сравнительно редко по сравнению с «вазоспазмом». Отчасти это происходит из-за того, что при закупорке проксимального участка ПМА дистальные её отделы будут снабжаться из другой ПМА через ПСоедин.А. Двусторонний инфаркт в зоне кровоснабжения ПМА всегда требует поиска недавно разорвавшейся аневризмы, хотя он также встречается, когда обе ПМА питаются из одной сонной артерии через ПСоед.А или из-за перекреста дистальных ветвей в продольной щели головного мозга. Большинство случаев инфаркта в территории ПМА возникают или из-за кардиогенной эмболии, или вследствие артерио-артериальной эмболии из закупоренной или стенозированной ВнутрСонА 4. СМА (средняя мозговая артерия), ветви. Топографическое расположение. Важность бассейна. Близость к другим сосудам и нервам. Средняя мозговая артерия (a. cerebri media) — самая крупная ветвь внутренней сонной артерией .Уходит в латеральную сторону,в глубокую латеральную борозду ,следует по поверхности островковой доли и делится на свои конечные ветви .В ней выделяют клиновидную, островковую и конечную (корковую) части. От клиновидной части отходят переднелатеральные таламостриарные артерии. От островковой — островковые артерии, латеральная лобно-глазничная ветвь, промежуточная височная артерия, задняя височная артерия. От конечной части отходят артерии цен-тральной борозды, прецентральной борозды, постцентральной борозды, передняя и задняя теменные артерии, артерия угловой извилины. Глубокие ветви СМА, отходящие от ее проксимального участка на основании мозга, снабжают кровью переднюю часть заднего бедра внутренней капсулы, часть хвостатого ядра, скорлупу, часть таламуса, наружную часть бледного шара. Одну из глубоких ветвей средней мозговой артерии Шарко называл arteria gemorragica, считая, что она часто является источником внутримозговых кровоизлияний. Важность бассейна: Окклюзия ствола СМА почти всегда вызывает появление неврологических симптомов. В большинстве случаев окклюзия наступает в проксимальном участке ствола и, следовательно, развивается ишемия как поверхностных, так и глубоких зон кровоснабжения СМА. Обычно это проявляется гемиплегией и гемианестезией на противоположной стороне, гемианопсией и расстройством соответствующих высших корковых функций (т.е. дисфазией, если процесс развивается в доминантном полушарии). Однако часто наблюдается развитие и корковой ишемии, но без инфаркта и, следовательно, клинические признаки могут быть весьма схожими. Если закупорен более дистальный участок ствола и нет ишемии в зоне кровоснабжения СМА, то функция ноги может быть относительно сохранена, потому что большинство волокон для ноги берут начало в тех корковых полях, которые обычно снабжаются из ПСА. Вертебробазилярный бассейн. Топографическое расположение. Важность бассейна. Близость к сосудам и нервам. Вертебро-базилярный бассейн формируется двумя позвоночными артериями, берущими начало от подключичных артерий и их ветвями (базилярной, задними мозговыми и мозжечковыми артериями. Артерии вертебробазилярного бассейна осуществляют кровоснабжения около 15-25% головного мозга. Позвоночные артерии (ПА) на шее проходят через костный канал, образованный отверстиями поперечных отростков VI—II шейных позвонков. Выйдя из отверстия поперечного отростка позвонка СII, ПА делает изгиб, поворачивая кнаружи, а затем вверх, проходит сквозь отверстие поперечного отростка атланта и через большое затылочное отверстие проникает в полость черепа. Субокципитальная часть ПА образует извитость, которая при поворотах и сгибаниях головы предотвращает ее резкое растяжение. Прободая атлантозатылочную мембрану (membranaatlanto-occipitalis) и твердую мозговую оболочку, обе ПА, сближаясь, подходят к нижней поверхности продолговатого мозга. На его границе с мостом они соединяются, образуя базилярную артерию (a. basilaris). От ПА уже в полости черепа отходят ветви, которые, соединяясь, образуют переднюю спинномозговую артерию (a. spinalisanterior). Кроме того, от ПА до места их слияния отходят менингеальные ветви и нижняя задняя мозговая артерия (a. cerebelliinferiorposterior), участвующие в снабжении кровью продолговатого мозга и мозжечка. Базилярная артерия на границе моста со средним мозгом делится на две задние мозговые артерии (ЗМА). От базилярной артерии и задних мозговых артерий отходят: передняя нижняя мозжечковая артерия (a. cerebelliinferioranterior) и отходящая от нее ветвь внутреннего слухового прохода (a. labyrinthi), верхняя мозжечковая артерия (a. cerebellianterior). Этот бассейн является общим для обеих позвоночных артерий и поэтому нарушение кровообращения только по одной позвоночной артерии может вызвать симптомы из всей территории вертебробазилярного бассейна мозга. Слуховые центры и нервы, вестибулярные ядра, нижние части мозжечка кровоснабжаются позвоночной артерией той же самой стороны еще до слияния их в основную артерию. Потому звон или шум в ушах, понижение или потеря слуха характерны для уха на той же самой стороне, как и поврежденная позвоночная артерия. ЗМА (задняя мозговая артерия), ветви. Топографическое расположение. Важность бассейна. Близость к другим сосудам и нервам. Задняя мозговая артерия (a. cerebriposteror) огибает ножку мозга и идет к наружному коленчатому телу. Далее направляется через отверстие намета мозжечка к височной доле, проходит по внутреннему краю ее нижней поверхности и достигает полюса затылочной доли. Сосуд условно подразделяется на три части, которые еще называют сегментами задней мозговой артерии. предкоммуникационная часть; посткоммуникационная часть; конечная, или корковая, часть. Предкомуникационная часть (P1 сегмент задней мозговой артерии) - это участок сосуда, расположенный до места впадения в него задней соединительной артерии. От нее отходят такие ветви, как медиальная задняя хориоидальная, парамедианная мезэнцефалическая, а также задняя таламоперфорирующая артерии. Они несут кровь ядрам таламуса и коленчатому телу (медиальной его части). Посткоммуникационная часть (P2 сегмент) - это участок, размещенный после впадения в сосуд задней соединительной артерии. От него отходят следующие ветви задней мозговой артерии: таламогеникулятная, педункулярные перфорантные и латеральная задняя хориоидальная артерии. Они также снабжают кровью коленчатое тело, но срединную его часть. Кроме того, эти сосуды несут кислород и питательные вещества к части среднего мозга, ядрам и подушке таламуса, боковой стенке первого и второго желудочков. Конечная часть (P3 и P4 сегменты) несет кровь к коре головного мозга. Она дает переднюю и заднюю височные, шпорную и теменно-височные ветви. В большинстве случаев кровь от конечного сегмента поступает к отделам коры до сильвиевой борозды. Основные ветви задней мозговой артерии — заднемедиальные центральные артерии, таламические ветви, медиальные задние ворсинчатые ветви, ножковые ветви, латеральная и медиальная затылочные артерии, шпорная ветвь, направляющаяся к корковому полю 17, по Бродману (к корковому концу зрительного анализатора). Небольшая часть этого поля получает кровь из СМА, чем и объясняется сохранность макулярного зрения при гомонимной гемианопсии, обусловленной окклюзией ЗМА. В месте прохождения ЗМА через тенториальное отверстие может сдавливаться при вклинении височной доли. В глубину полушария уходят 3 ветви ЗМА: таламоперфорирующая, премаммилярная и таламоколенчатая. Они снабжают кровью задненижнюю часть зрительного бугра и гипоталамической области, утолщение мозолистого тела, зрительный венец и льюисово тело. Самая крупная из этих ветвей — задняя ворсинчатая артерия, которая кончается в сосудистом сплетении III мозгового желудочка. Важность в том, что клинические проявления нарушения тока крови в ЗМА зависят от локализации повреждения. Это могут быть симптомы поражения среднего мозга, таламуса, затылочной и теменной области коры головного мозга. 7. Анатомия и физиология мозгового кровообращения. Особенности мозгового кровотока у здорового человека. Энергетический метаболизм головного мозга. 8. Механизмы регуляции (общие и местные) и саморегуляции. Феномен Остроумова-Бейлиса. Феномен «обкрадывания» и обратного «обкрадывания». Клиническое значение. Физиология мозгового кровообращения. Важной особенностью мозгового кровообращения является его определенная автономность, регуляция которого осуществляется через сложную систему, в которую входят следующие компоненты: Мышечная системы сосудистой стенки (эффект Остроумова-Бейлисса); Состояние метаболизма мозговой ткани; Напряжение кислорода (O2); Напряжение углекислого газа (СО2); Состояние кислотно-основного состояния и рН ткани мозга, количество молочной и пировиноградной кислоты; Нервная регуляция; Анатомические особенности сосудов головного мозга. Осуществление регуляции мозгового кровотока за счет колебаний внутрисосудистого давления происходит за счет его прямого влияния на тонус гладких мышц мозговых артерий. Реакция мышечных клеток па изменения внутрисосудистого давления, впервые описанная А. Остроумовым (1876), а затем детально изученная Bayliss (1902, 1923), выражается в вазоконстрикции при повышении артериального давления и вазодилатации в случаях его падения. Механизм этой реакции считается миогенным, так как сокращение гладких мышц сосудов возникает при растяжении их стенки, даже если для этого берется изолированный сегмент артерии. Таким образом, при повышении уровня общего артериального давления происходит сужение сосудов мозга, при снижении — их расширение. Феномен саморегуляции мозгового кровотока осуществляется в определенных границах при колебаниях общего артериального давления между 60 и 180 мм рт. ст. (табл. 1). 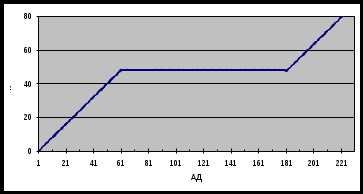 Табл.1: Схема взаимоотношений между мозговым кровотоком и артериальным давлением (по Lassen, 1959). МК – мозговой кровоток в миллилитрах на 100 г в 1 мин; АД – артериальное давление в миллиметрах ртутного столба. Саморегуляторный ответ сосудов мозга, в основе которого лежит эффект Остроумова — Бейлисса, длится очень короткое время, не более чем 30 с. Затем начинает проявляться влияние сдвигов метаболизма ткани мозга. В последние годы в связи с исследованием влияния внутричерепного давления на мозговой кровоток и его саморегуляцию специальному обсуждению подвергаются представления о так называемом перфузионном мозговом давлении. Под перфузионным мозговым давлением понимается разность между средним артериальным давлением и внутричерепным давлением. Для сохранения саморегуляции мозгового кровотока и отсутствия его редукции при повышении внутричерепного давления необходимо, чтобы перфузионное мозговое давление не снижалось ниже 40 мм. рт. ст. Определенное влияние на мозговой гемодинамики оказывают метаболические сдвиги ткани мозга. При снижении содержания в артериальной крови кислорода ниже 60-50% от исходной величины возникает расширение мозговых сосудов. В ответ на гипероксию мозговые сосуды суживаются и мозговой кровоток заметно снижается. Углекислота оказывает обратное влияние на тонус сосудов мозга и мозговой кровоток. Уменьшение содержания углекислоты в артериальной крови и ткани мозга вызывает сосудосуживающий эффект и снижение мозгового кровотока. Гиперкапния и накопление углекислоты в ткани мозга являются одним из самых сильных сосудорасширяющих факторов, увеличивающих мозговой кровоток. Влияние разных концентраций углекислоты во вдыхаемом воздухе и в артериальной крови на тонус сосудов мозга и мозговой кровоток весьма вариабельно. Например, при ингаляции 5% смеси углекислого газа мозговой кровоток может увеличиваться на 50% . Влияние кислотно-основного состояния можно рассмотреть на примере данных работ М. Е. Маршака (1965) и других, при активизации нервных клеток, вызванной пробуждением, освещением в темной комнате, при стрихнинизации коры мозга увеличивается потребление кислорода и глюкозы, в связи с чем падает рО2, возрастает продукция рСО2 и лактата, снижается количество АТФ и креатинфосфата, а количество неорганического фосфата увеличивается. Вслед за указанными сдвигами в исследуемой части мозга падает тонус артерий, они расширяются, и мозговой кровоток возрастает. В результате компенсируется недостаток кислорода и удаляется избыточное количество углекислоты и других продуктов метаболизма. Обратные явления наблюдаются при наркозе, когда угнетается дыхание ткани мозга, снижается количество образующейся молочной кислоты и углекислоты, повышается содержание АТФ и креатинфосфата, а количество неорганического фосфата снижается. После нормализации метаболизма мозговой кровоток начинает возвращаться к исходному уровню. Велика роль в регуляции мозгового кровообращения принадлежит рефлексогенным влияниям артериальной синокаротидной зоны и возбуждению симпатической нервной системы, которые вызывают рефлекторный спазм крупных и средних артериальных стволов как на поверхности, так и внутри мозгового вещества. Анатомические особенности представлены в виде физиологических приспособлений, регулирующих величину и скорость пульсовых артериальных волн. Удар пульсовой волны амортизируется благодаря изгибам крупных (внутренних сонных, позвоночных) артерий, сложному строению артериальной сети, наличию анастомозов, особенностям хода артерий, снабжающих кровью подкорковые узлы, а также отхождению от артерий мягкой мозговой оболочки ветвей, идущих радиально в мозг и питающих его поверхностные структуры, в том числе кору и прилежащее к ней белое вещество. Повреждения и отек мозга, нарушение кровоснабжения вследствие патологии сосудистой системы ограничивают возможности саморегуляции мозгового кровотока следующим образом: Сосудорасширяющие влияния приводят к увеличению притока крови только в здоровые области мозга, тем самым анемизируя патологический очаг – синдром внутримозгового обкрадывания; Сосудосуживающие влияния, уменьшая кровоснабжение здоровых тканей, перераспределяют кровоток в пользу очага повреждения – извращенный синдром внутримозгового «обкрадывания» (синдром Робин-Гуда); При прекращении кровотока в проксимальных отделах дуги аорты дистальнее отхождения левой общей сонной артерии, но проксимальнее отхождения левой позвоночной артерии может возникать «подключичный феномен обкрадывания», когда левая позвоночная артерия играет роль коллатерали для левой руки Энергетический метаболизм головного мозга. Мозговая ткань беспрерывно активно функционирует, а ее потребность в кислороде больше, чем у других тканей и органов. Масса мозга составляет приблизительно 2% массы тела — 1350—1450 г. За минуту через мозг проходит около 800 мл крови, что составляет 15—20% сердечного выброса, при этом в мозге нет запасов кислорода и единственного субстрата, необходимого для выработки энергии, — глюкозы. Потому необходимо постоянное поступление глюкозы в количестве 75—100 мг/мин или 125 г/сут. В метаболических процессах в мозговой ткани, направленных на выработку энергии, преобладающим (90%) является аэробный гликолиз, в цикле которого образуется 36 молекул АТФ. Тогда как за счет анаэробного гликолиза обеспечивается 10% энергетических процессов, синтезирующего только 2 молекулы АТФ. Постоянное обеспечение мозга АТФ требуется для поддержания целостности и функциональной активности его ткани, в частности сохранения необходимого соотношения главных внутриклеточных катионов — ионов калия (К+) и основных внеклеточных катионов — ионов натрия (Na+) и кальция (Са2+). Кровь, поступающая в мозг и содержащая нужное количество глюкозы, для обеспечения аэробных метаболических процессов должна быть и достаточно оксигенированной. Общий мозговой кровоток у здорового человека составляет 50—55 мл на 100 г мозговой ткани в 1 мин (от 45 до 75 мл). В таком случае в мозг попадает около 20% поступающего в организм кислорода. Общее потребление мозгом кислорода, т.е. скорость церебрального метаболизма кислорода, составляет 3,3—3,5мл/100 г/мин. Таким образом, головной мозг в минуту потребляет около 45 мл кислорода. Для обеспечения достаточного кровотока в мозге и полноценного снабжения его необходимыми ингредиентами должны быть в норме общее кровообращение, состав крови, ее насыщенность кислородом и многие другие факторы которые будут рассмотрены в соответствующих разделах. Феномен обкрадывания 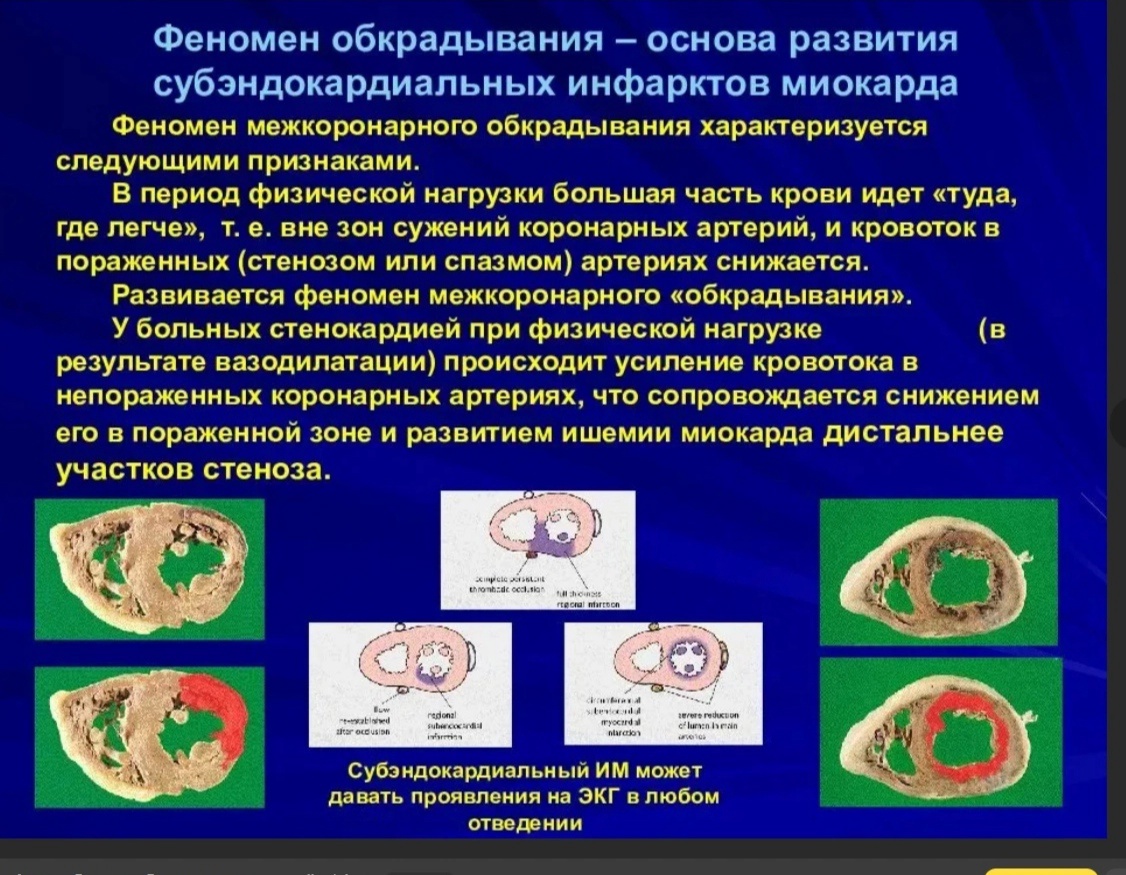 9. Отток крови (венозная система). Механизм. Причины нарушения оттока крови. Венозная система ГМ служит не только для оттока венозной крови, но и для всасывания ликвора. Резорбция ликвора осуществляется через пахионовы грануляции в венозные синусы ГМ, а значит, от нормального состояния и функционирования венозной системы напрямую зависят внутричерепное давление и вероятность развития отека ГМ. В венозной системе ГМ выделяют несколько уровней: поверхностные и глубокие вены; синусы твердой мозговой оболочки; вены-выпускники; сплетения основания черепа. Благодаря сильно развитой системе анастомозов к ней относятся также вены свода черепа и лица, вены позвоночника.Через поверхностные мозговые вены кровь отводится от коры и тех отделов белого вещества, которые расположены на небольшом расстоянии от нее. Большая часть этих вен проходит через мягкую и твердую мозговые оболочки и впадает в крупные вены или синусы: поперечные, пещеристые, сфенопариетальные, каменистые, верхний сагиттальный, базальное сплетение. Большое значение имеют межвенозные и межсинусные анастомозы на поверхности полушарий мозга. По системе глубоких мозговых вен осуществляется отток крови от глубокорасположенных структур ГМ. С анатомической точки зрения в этой системе различают короткие и длинные вены. По коротким венам кровь оттекает от ядерных образований мозга и узких прослоек белого вещества (внутренней капсулы), по длинным – от глубокорасположенных участков белого вещества истриатума. Главным коллектором вен данной системы является большая мозговая вена Галена. По ней венозная кровь оттекает в прямой синус. Некоторые глубокие вены топографоанатомически соотносятся с мозговыми артериями. На основании черепа вены образуют круг Розенталя, аналогичный артериальному кругу Виллизия. Глубокая средняя мозговая вена соотносится со средней мозговой артерией. Глубокие мозговые вены связаны анастомозами с другими отделами интракраниального венозного русла. Это имеет большое значение для компенсации венозного оттока при развитии патологических процессов, приводящих к нарушению проходимости вен. Синусы твердой мозговой оболочки представляют собой коллекторы для венозной крови мозга и его оболочек. В них впадают вены мозга и диплоические вены черепа. В устье вен располагаются полулунные створки, выполняющие функцию клапанов. Они могут изменять направление тока крови, закрывая венозные устья, и предохраняют синусы от переполнения кровью. Ту же функцию осуществляют трабекулы – эластические перекладины, перекинутые от одной стенки синуса к другой. Диплоические вены находятся во внутренних каналах свода черепа. Они обеспечивают дренаж крови из костной ткани, и в них отсутствуют клапаны. Эти вены сообщаются с венами мягких тканей черепа, мозговыми венозными синусами, менингеальными венами. Отток крови направлен к основанию черепа, в синусы и среднюю оболочечную вену. Венывыпускники (венозные эмиссарии) проходят внутри костей свода и основания черепа, соединяя диплоические вены с венозными синусами и венами мягких тканей головы. Вены свода черепа и лица также участвуют в обеспечении интракраниального венозного оттока. Выявлены анастомозы этих вен с диплоическими венами и выпускниками. Большая часть этих анастомозов находится в области сосцевидно-теменного костного шва основания сосцевидного отростка височной кости и в парасагиттальной зоне. избыточное кровенаполнение сосудов головного мозга устраняется путем ослабления притока крови в его сосудистую систему вследствие констрикции всей системы магистральных артерий. В таких случаях регуляция происходит также рефлекторно. Рефлексы посылаются с механорецепторов венозной системы, мелких артерий и оболочек мозга (вено-вазальный рефлекс). Причины в физиологических условиях: при натуживании, во время затяжного кашля, при физическом напряжении, пении, игре на духовых инструментах, родах, крике, нахмуривании бровей, нагибании головы (например, во время физкультурных упражнений – при положении тела вверх ногами), в положении лежа без подушки под головой, при сдавлении шеи тесным воротничком и т.д. Затруднение венозного оттока из полости черепа наблюдается также при целом ряде соматических заболеваний [сердечная и сердечно-легочная недостаточность; сдавление внечерепных вен; опухоли головного мозга, его оболочек, черепа, арахноидиты; черепно-мозговая травма; тромбозы вен и синусов; инфекционно-токсические поражения вен; церебральные тромбофлебиты; сдавление вен при краниостенозе, водянке мозга; асфиксия новорожденных и взрослых, повешение; венозная и артериовенозная гипертония; затруднение/ прекращение носового дыхания. Венозная энцефалопатия может быть также обусловлена классическими причинами цереброваскулярной патологии: артериальной гипертензией (АГ), атеросклерозом, курением, сахарным диабетом, употреблением гормональных препаратов (эстрогенов), злоупотреблением алкоголем и наркотическими веществами, синдромом апноэ, использованием нитратов и некоторых вазодилататоров. 10)Гемодинамические кризы (1-8). Причины, к какому варианту инсульта это приводит. Гемодинамические кризы могут быть вызваны стрессом, изменениями климатических факторов, нарушениями режима или характера питания и другими факторами дестабилизации. Клинические данные, анамнез и современные методы исследования дают возможность выделять и идентифицировать: восемь вариантов гемодинамических кризов: гипертонический, гипотонический, аритмический, коронарный, ангиодистонический, гемореологический, нейроэндокринный, обтурационный. Гипертонический криз может быть спровоцирован стрессом, употреблением алкоголя, отменой приема лекарств. В зависимости от сократительной функции сердца и состояния сосудов мозга гипертонический криз может привести к развитию лакунарного, гемодинамического ишемического инсульта (ИИ) [7-9]. Снижение сократительной способности миокарда (фракции выброса и минутного объема крови) у пациентов с артериальной гипертензией позволяет предполагать развитие лакунарного или крупноочагового гемодинамического инфаркта мозга. Коронарный криз – Коронарный криз – одна из частых, но не всегда диагностируемых причин декомпенсации мозгового кровообращения. Не только стенокардия, но и безболевая ишемия миокарда способны привести к снижению эффективной работы сердца. Кроме того, коронарная недостаточность часто сопровождается кратковременными нарушениями ритма сердца (желудочковой экстрасистолией, фибрилляцией предсердий). Коронарный атеросклероз, проявляющийся стенокардией или безболевой ишемией миокарда, как правило, сочетается со стенозами брахиоцефальных артерий. Кратковременное снижение ударного объема крови не может быть компенсировано патологически измененной артериальной системой мозга.одна из частых, но не всегда диагностируемых причин декомпенсации мозгового кровообращения. Не только стенокардия, но и безболевая ишемия миокарда способны привести к снижению эффективной работы сердца. Коронарный криз обычно приводит к развитию гемодинамического или кардиоэмболического инсульта Гипотонический криз развивается на фоне абсолютной и относительной гипотонии, атеросклеротические изменения в брахиоцефальных артериях Паркинсонизм неадекватное применение антигипертензивных средств (21%). Интоксикации инфекции Приводит к: Гипотонические кризы приводят к гемодинамическим инсультам с мультифокальными мелкоочаговыми повреждениями мозга. Аритмический криз (пароксизмальные формы нарушений ритма сердца) – одна из самых частых причин ОНМК. Пароксизм мерцательной аритмии снижает минутный объем крови на 20 – 25%, что составляет патофизиологическую основу для ишемии мозга. Фибрилляция предсердий создает условия для образования тромбов в полостях сердца. Известно, что синдром слабости синусового узла встречается значительно чаще у пациентов с инсультами не установленной этиологии. Аритмический криз является основной причиной кардиоэмболического инсульта. Ангиодистонический криз обычно сопутствует вертеброгенным нарушениям сосудистого тонуса (синдром позвоночной артерии). Эпизоды недостаточности кровообращения в вертебрально-базилярной системе. Приступ мигрени-тяжелые формы мигрени предполагают возможность очаговых повреждений мозга (мигренозный инсульт). приводит к преходящим нарушениям мозгового кровообращения, реже – к развитию гемодинамического ишемического инсульта с мелкоочаговыми повреждениями мозга. Нейроэндокринный криз – всегда следствие гормональной дисфункции или нарушений нейрогенной регуляции. Нейроэндокринные кризы можно наблюдать у женщин в период климакса, у больных с тиреотоксикозом. Наиболее демонстративны их проявления у больных с нейроэндокринными опухолями. В этом случае патофизиологической основой повреждения сердечно-сосудистой системы является массивный выброс в кровь катехоламинов, который помимо выраженных гемодинамических эффектов и приводит к повреждению миокарда и сосудистой стенки. Нейроэндокринные кризы приводят к развитию гемодинамических и атеротромботических ИИ Гемореологический криз – одна из наиболее частых причин декомпенсации мозгового кровообращения. Гиперкоагуляция, гипервискозность крови служат основой для системных нарушений микроциркуляции. При определенных условиях (гипертермия, обезвоживание, интоксикация, стресс) системные расстройства регионального кровообращения могут привести к блокаде микроциркуляции. Микроциркуляторный блок создает условия для ишемии стандартных органов-мишеней: мозг, сердце, почки. Артериальная гипертензия в таких случаях носит симптоматический характер и лишь увеличивает нагрузку на миокард. Гемореологический криз осложняется ОНМК по типу гемореологической микроокклюзии (гемореологический инсульт), гемодинамическим или атеротромботическим инсультом.. Обтурационный криз предполагает острую закупорку артерии среднего или крупного калибра тромбом или фрагментом распадающейся атеросклеротической бляшки. Расслаивание стенки артериального ствола также может стать причиной обтурации. Закупорка крупной артерии обычно возникает в местах наиболее выраженных артеросклеротических изменений вследствие «активации» бляшек или тромботических осложнений. В результате обтурационного криза развиваются тяжелые крупноочаговые ишемические повреждения мозга, протекающие по типу атеротромботического инсульта. 11. Ишемическая «полутень» - развитие ишемического очага. Схема с пояснением. Ишемический инсульт - ключевым моментом патогенеза является локальная ишемия мозга (местное малокровие мозговой ткани), развивающаяся при снижении церебральной перфузии ниже 18 - 22 мл на 100г/мин (при норме в 50-60 мл на 100г/мин), что является функциональным порогом (в частности, при показателях ниже которого, ЭЭГ в соответственной зоне мозга становится плоской). Уровень перфузии менее 8 -10 мл на 100 г мозговой ткани в минуту является порогом развития необратимых изменений - порогом инфаркта. Также необходимо осветить следующие моменты патогенеза инфаркта мозга: 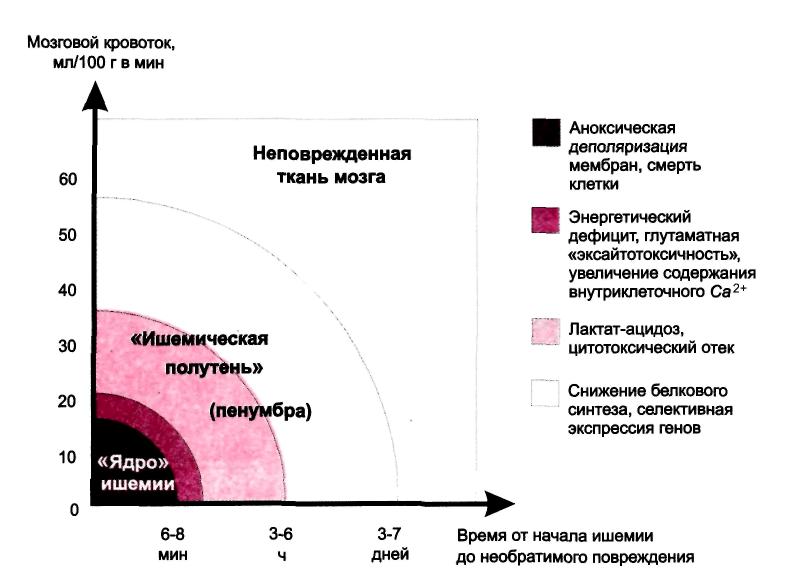 Рис. 5. Формирование инфаркта мозга на фоне снижения церебрального кровотока.  Рис. 6. Ишемизированная область головного мозга. Пенумбра. Терапевтическое окно - при длительности гипоперфузии более 6 – 8 мин в зоне порога инфаркта образуется некроз мозговой ткани - инфаркт мозга, а в области функционального порога формируется зона «ишемической полутени» (или ишемической пенумбры), кровоснабжение в которой выше критического порога необратимых изменений (8 - 10 мл на 100г/мин), но ниже функционального порога, и нервные клетки в которых в течение определенного срока сохраняют жизнеспособность. Эта зона может трансформироваться в инфаркт (зону некроза ткани мозга) в результате вторичных нейрональных повреждений или остаться неповрежденной в случае восстановления кровотока (реперфузии). В основном формирование инфаркта мозга в области пенумбры происходит в течение 3-6 часов. Этот промежуток времени получил название «терапевтического окна», т.е. 3-6 часов от начала инсульта являются промежутком времени, в течение которого можно оказать лечебное воздействие на клетки зоны «ишемической полутени» и предотвратить развитие некроза. 12. Развитие геморрагического инсульта (разрыв (причины)), геморрагическое пропитывание. Геморрагический инсульт - вследствие хронической артериальной гипертензии происходит развитие липогиалиноза, фибриноидного некроза в стенках мелких перфорирующих артерий мозга (корково-медуллярные, лентикулостриарные ветви) с формированием так называемых микроаневризм Шарко-Бушара. (Шарко–Бушара аневризмы чаще всего располагаются в лентикулостриарных сосудах базальных ганглиев, связанных с хронической гипертонией. Шарко–Бушара аневризм являются частой причиной кровоизлияния в мозг.) Далее, как правило, на фоне и в результате резкого повышения АД, наблюдается разрыв измененной артерии или микроаневризмы с последующим формированием тромба и развитием кровоизлияния непосредственно в паренхиму головного мозга по типу гематомы (85% случаев) или геморрагического пропитывания вещества мозга. Средний объем гематом в полушариях большого мозга 60 - 80 мл, полушариях мозжечка 30 - 50 мл. Далее происходит расслоение мозговой ткани гематомой, окруженной узкой зоной некроза мозга в месте кровоизлияния. Развивается цитотоксический и вазогенный отек головного мозга (Вазогенный отек мозга является отеком головного мозга, при котором имеется повреждение гематоэнцефалического барьера), ишемия перифокальной зоны вследствие сдавления ткани мозга, и/или вторичная ишемия за счет сдавления артерий. Возможно развитие прорыва крови в желудочковую систему мозга, острой обструктивной гидроцефалии, дислокации и вклинения головного мозга. Нередко кровь попадает в подпаутинное пространство и желудочки головного мозга. По данным КТ исследований до 26% гематом продолжают нарастать в размерах в течение ближайшего часа от начала инсульта, а 12% гематом - в течение 20 ч. Это может быть связано как с сохраняющейся артериальной гипертензией, так и с локальным коагуляционным дефицитом. В периоде регресса кровоизлияния происходит резорбция крови с образованием кисты в течение недель и месяцев. Значительно реже, чем кровоизлияния вследствие разрыва артерии или аневризмы, встречаются диапедезные кровоизлияния вследствие ишемии и повышения проницаемости сосудистой стенки, например, при заболеваниях крови, сепсисе, антитромболитической, фибринолитической терапии, морфологически проявляющиеся небольшими гематомами или геморрагическим пропитыванием вещества мозга. В эту же группу может быть отнесена геморрагическая трансформация ишемического инсульта. Геморрагическая трансформация - вариант геморрагической трансформации инфаркта мозга в 90 – 95% случаев связан с кардиогенной эмболией. Ключевым моментом является фибринолиз эмбола, приводящий к реперфузия ткани мозга в зоне инфаркта с восстановлением кровотока по пораженным ишемией артериям и капиллярам, и последующим развитием диапедезных кровоизлияний в зоне инфаркта — геморрагического инфаркта. 13. Влияние сосудорасширяющих и сосудосуживающих препаратов на свежий очаг ишемии. СосудорасширяющиеВ тех случаях, когда недостаточное кровоснабжение спровоцировано спазмом сосудов, образованием тромбов наиболее эффективны сосудорасширяющие препараты. Они расширяют артериолы мозга, облегчают поступление крови вместе с кислородом и питательными компонентами к мозгу, усиливают кровоток, препятствуют склеиванию тромбоцитов при образовании тромбов. Сосудорасширяющие препараты имеют существенный недостаток: действуют неизбирательно, таким образом происходит расширение не только артерий головного мозга, но и остальных сосудов. Это может стать причиной стойкого снижения артериального давления, что особенно неблагоприятно для людей пожилого возраста с атеросклерозом. У пациентов, принимающих сосудорасширяющие средства на фоне остеохондроза, возникает угроза ишемических инсультов, появляются признаки гипотонии в виде головокружения, нарушения зрения, шаткости походки, обмороков. Сосудосуживающие препараты усугубляют очаг ишемии и препятствуют коллатеральному току крови (это не точно) но похоже на правду 14. Классификация ОНМК. Начальные проявления недостаточности мозгового кровообращения (НПНМК), признаки. Преходящие нарушения мозгового кровообращения (ПНМК). ТИА, ГЦК.  Характер нарушения мозгового кровообращения: A. Начальные проявления недостаточности кровоснабжения головного мозга: 1. Начальные проявления недостаточности кровоснабжения головного мозга (НПНКГМ) Б. Преходящие нарушения мозгового кровообращения (регресс симптоматики в течение 24 часов): 1. Транзиторные ишемические атаки 2. Гипертензивные церебральные кризы: 2.0. Общемозговые 2.1. С очаговыми нарушениями Инсульт: 1. Субарахноидальное нетравматическое кровоизлияние: 2. Геморрагический инсульт - нетравматическое кровоизлияние: 3. Другие и неуточненные внутричерепные кровоизлияния: 3.0. Нетравматическое экстрадуральное кровоизлияние 3.1. Нетравматическое острое субдуральное кровоизлияние 3.2. Неуточненные внутричерепные кровоизлияния 4. Ишемический инсульт (инфаркт): 4.0. Церебральный ишемический инсульт: 4.0.0. При поражении прецеребральных магистральных артерий 4.0.1. При поражении церебральных артерий 4.0.2. При эмболии церебральных артерий 4.1 Спинальный ишемический инсульт: 5. Инсульт с восстановимым неврологическим дефицитом - малый инсульт Недостаточно уточненные острые нарушения мозгового кровообращения 6. Последствия раннего (более 1 года) перенесенного инсульта Начальные проявления недостаточности кровоснабжения мозга (нпнкм). Согласно существующей классификации, их относят к ранним проявлением ишемического поражения мозга. Это компенсированная стадия сосудистой патологии мозга, клинически манифестирующая лишь при повышенной потребности мозга в притоке крови (напряженная умственная работа, особенно в условиях гипоксии, выраженное утомление). Диагностика НПНКМ на первом этапе базируется на 5 основных жалобах: 1) головная боль; 2) головокружение; 3) шум в голове; 4) ухудшение памяти; 5) снижение работоспособности. Наличие двух и более жалоб, повторяющихся не реже 1 раза в неделю на протяжении последних 3 месяцев является диагностическим критерием НПНКМ. Наиболее частые этиологические факторы НПНКМ - атеросклероз, артериальная гипертензия, вегетативно-сосудистая дистония (церебральная ангиодистония, приводящие к ухудшению центральной и церебральной гемодинамики. Клинический паттерн заболевания мало специфичен и напоминает “неврастенический” синдром: ухудшение памяти, снижение работоспособности, раздражительность, головные боли, головокружение, расстройства сна, неуверенность и тревожность, признаки вегетативно-сосудистой лабильности. Могут обнаруживаться отдельные органические микросимптомы. Психологическое тестирование позволяет фиксировать некоторую замедленность при выполнении проб и заданий, эмоциональную напряженность, тревогу, трудность интерперсональных отношений. Динамика заболевания достаточно стереотипна: у большинства больных с НПНКМ постепенно формируется картина сосудистой энцефалопатии, а у части последних развивается мозговой инсульт. У определенного числа лиц на протяжении десятков лет регистрируется стационарный вариант течения. Для верификации сосудистой природы клинико-неврологического симптомокомплекса широко используются подробное неврологическое и соматическое исследования, аппаратные и лабораторные методы. 1 2 |
