ответы к экзамену биотехнология. 1. Биотехнология как межотраслевая область научнотехнического прогресса и раздел практических знаний 1917 г был введён термин биотехнология
 Скачать 340.74 Kb. Скачать 340.74 Kb.
|
|
44. Требования, предъявляемые к продуцентам · штаммы не должны продуцировать антибиотики и токсичные вещества,не должны быть родственны штаммам,образующихтоксины. · Легкая очистка энзимов от культуральной среды · Высокий выход энзима за короткое время · Желательно образование энзима экспресивно-легче выделить Высокое содержание белка,слабый запах,мягкий вкус одноклеточного протеина в сочетании с лёгкостью хранения придают существенную ценность этому продукту питания. Организм –продуцент должен быть непатогенени нетоксичен,а его продукты метаболизмам безвредными,строгий санитарный режим и различные процедуры контроля качества должны постоянно осуществляться в течении всего биотехнологического процесса в целях предотвращения порчи продукта,а также загрязнения его потогенными или токсигенными микроорганизмами. 45.Иммобилизованные энзимы и преимущества их применение в биотехнологии Иммобилизация представляет собой включение фермента в такую среду, в которой для него доступной оказывается лишь ограниченная часть общего объема. На практике для иммобилизации ферментов используют рутинные физические и химические методы. Все существующие методы физической иммобилизации (т. е. иммобилизации, при которой фермент не соединяется с носителем ковалентными связями) могут быть подразделены на четыре основные группы: · адсорбция на поверхности нерастворимого носителя (или как иногда говорят матрикса); · включение в поры геля; · пространственное разделение фермента от остальной части реакционной смеси с помощью полупроницаемой мембраны; · введение фермента а двухфазную реакционную среду, в которой он растворим, но может находиться только в одной из фаз. Эффективность ферментативных процессов, используемых в самых раз-личных областях человеческой деятельности, удалось увеличить с помощью иммобилизации ферментов. Иммобилизованные ферменты обладают несколькими преимуществами над своими растворимыми аналогами: 1) могут быть отделены от продукта и использованы повторно, что снижает стоимость процесса; 2) характеризуются повышенной стабильностью и длительным со-хранением активности; 3) пригодны для непрерывных процессов, которые, в свою очередь, облегчают контроль за качеством и снижают стоимость труда; 4) время реакции может быть уменьшено за счет создания более высокого соотношения ферментов и субстратов; 5) возможностью создания мультиферментных систем. Однако применение ферментов ограничено из-за их низкой стабильности, способности катализировать только одну единственную реакцию, высокой стоимости чистых препаратов. Кроме того, для практических целей могут использоваться только те ферменты, для которых не требуется регенерации кофакторов. Поэтому в настоящее время наряду с иммобилизацией ферментов внимание исследователей все больше привлекает иммобилизация клеток и органелл. Живая клетка в отличие от фермента представляет собой готовый биотехнологический реактор, в котором реализуются не только процессы, приводящие к образованию конечного продукта, но и многие другие, способствующие поддержанию каталитической эффективности системы на высоком уровне (например, регенерация кофакторов). Поскольку ферменты функционируют в нативном окружении, их денатурация в процессе работы сводится к минимуму. Это расширяет число применяемых ферментов и позволяет осуществлять как процессы синтеза, так и процессы деградации. Иммобилизованные клетки идеально подходят для использования в реакторах с перемешиванием, через которые пропускают субстрат. Преимуществом таких реакторов является возможность их многократного использования и получения продукта, свободного от фермента. Конечно, использование иммобилизованных клеток не лишено недостатков. Например, клеточная стенка или плазматическая мембрана могут препятствовать проникновению субстрата к ферменту или диффузии продукта из клетки. Кроме того, возникает необходимость поддержания целостности клеток и удержания их в той фазе роста, в которой синтезируются требуемые ферменты. Наконец, из-за большого числа присутствующих в клетке ферментов (что в ряде случаев рассматривается как достоинство)возможно протекание нежелательных побочных реакций. Для иммобилизации клеток используется множество способов (сорбция инертными и ионообменными носителями, ковалентное связывание с полимерным носителем, включение в гель) и носителей разных типов (природные и синтетические полимеры и неорганические вещества). Включение живых клеток требует мягких условий иммобилизации, носитель при этом должен представлять собой систему открытых пор с хорошими условиями для газообмена. Следует принимать во внимание и возможное вредное влияние на жизнеспособность клеток сшивающих агентов. Наибольшее распространение получило включение клеток в полиакриламидный гель и гель альгината кальция. Альгинат – основной структурный полисахарид бурых морских водо-рослей. В присутствии моновалентных катионов полисахарид образует вязкий раствор, тогда как в присутствии двухвалентных катионов, особенно кальция, наблюдается образование геля. Поскольку гель образуется в мягких условиях, в нем можно иммобилизовать живые клетки. Во-первых, чистые препараты ферментов неустойчивы при длительном хранении, а также при разного рода воздействиях, особенно тепловых. Во-вторых, в виду сложности отделения ферментов от различных реагентов смеси многократное их использование весьма затруднено. Однако принципиально новые перспективы открылись перед прикладной энзимологией с разработкой принципов создания иммобилизованных ферментов. Иммобилизованные ферментные препараты обладают рядом существенных преимуществ при использовании в прикладных (промышленных целях) производствах по сравнению с чистыми препаратами. Гетерогенный (иммобилизованный) катализатор легко отделить от реакционной среды, что обусловливает: · возможность остановки реакции в любой нужный момент; · повторное использование катализатора; · получение конечного продукта, не загрязненного ферментом. Последний момент весьма важен при производстве пищевых и медицинских продуктов. Применение иммобилизованного катализатора позволяет проводить ферментный процесс непрерывно и регулировать скорость реакции, а также изменять количество получаемого продукта в соответствии с изменениями скорости протока реакционной смеси. Иммобилизация или некоторая модификация фермента может обусловить изменения и некоторых его свойств (специфичность взаимодействия с субстратом; зависимость каталитической активности от рН, ионного состава и других параметров среды, а также его стабильность по отношению к различного рода денатурирующим воздействиям). Иммобилизация ферментов дает возможность регулировать их каталитическую активность за счет изменения свойств носителя. 46. Носители, используемые для иммобилизации энзимов природные и синтетические органические носители 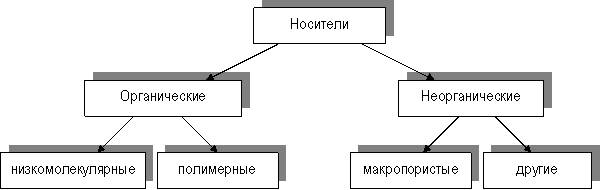 Органические полимерные носители Используемые в настоящее время органические носители можно разделить на два класса: 1 – природные полимеры, 2 – синтетические полимерные носители. Первые, в свою очередь, подразделяются на группы в соответствии с их биохимической классификацией: полисахаридные, белковые и липидные носители. Синтетические полимеры также могут быть подразделены на несколько групп: полиметиленовые, полиамидные и полиэфирные носители. Помимо вышеупоминавшихся требований, к рассматриваемым носителям предъявляются дополнительные, обусловленные методом иммобилизации, свойствами иммобилизуемого фермента, а также способом дальнейшего использования получаемого препарата: • при ковалентной иммобилизации носитель должен связываться только с теми функциональными группами на молекуле фермента, которые не являются ответственными за катализ; • носители не должны оказывать ингибирующего действия на фермент. Применение природных полимеров в качестве носителей аргументируется их доступностью и наличием свободных функциональных групп, легко вступающих в разнообразные химические реакции, а также их высокой гидрофильностью. К недостаткам следует отнести неустойчивость к воздействию некоторых микроорганизмов и относительно высокую стоимость многих из них. Полисахариды Наиболее часто для иммобилизации ферментов используют целлюлозу, декстран, агарозу и их производные. Целлюлоза отличается высокой степенью гидрофильности и наличием большого числа гидроксильных групп, что обусловливает ее легкое модифицирование путем введения различных заместителей. Для увеличения механической прочности целлюлозу гранулируют, что делает ее относительно дешевым и удобным для иммобилизации различных ферментов носителем. Гранулированная целлюлоза легко превращается в различные ионообменные производные. Однако она неустойчива к действию сильных кислот, щелочей и некоторых окислителей, что ограничивает области ее применения. Хитин – природный аминополисахарид, напоминающий некоторым образом целлюлозу и является компонентом наружного скелета ракообразных, насекомых, а также входит в состав оболочек некоторых грибов. Являясь отходом промышленной переработки креветок и крабов, данное соединение имеется в достаточно больших количествах при относительно низкой стоимости. Хитин обладает пористой структурой, не растворяется в воде, разбавленных кислотах и щелочах, а также в органических растворителях. Путем обработки щелочами хитин превращается в хитозан, который в качестве носителя дает хорошие результаты, поскольку препараты иммобилизованных ферментов, приготовленные с помощью хитозана, обладают высокой каталитической активностью и устойчивы к микробному воздействию. Декстран – разветвленный полисахарид бактериального происхождения, содержащий остатки глюкозы. Приготовленные на его основе гели выпускаются различными зарубежными фирмами и широко используются в различного рода работах. Гели, приготовленные на основе декстрана, отличаются высокой стойкостью по отношению к различным химическим веществам, что делает их весьма широко используемыми в различного рода исследованиях и на производстве. К группе декстранов может быть отнесен и крахмал, представляющий собой смесь полисахаридов, основным компонентом которой является амилоза и амилопектин. Посредством определенных химических обработок из крахмала получен новый носитель – губчатый крахмал, обладающий повышенной устойчивостью к ферментам, гидролизующим полисахариды. Агароза – широко используется в качестве носителя для иммобилизации ферментов, однако стоимость ее довольно высока, что заставляет разрабатывать различные ее модификации с целью получения легко регенерируемых форм, которые в результате этого могли бы использоваться повторно. Агар – природный полисахарид, выделяемый из клеточных стенок некоторых морских водорослей. Точный состав его не известен, но установлено, что он содержит, по крайней мере, два полисахарида: агарозу и агаропектин. Преимуществом агара является его низкая стоимость и нетоксичность. Некоторые производные агара отличаются высокой механической прочностью и устойчивостью в щелочной среде, что явилось основанием рассматривать данный носитель почти идеальным. Другими полисахаридами, получаемыми из морских водорослей, являются альгиновые кислоты и их соли, которые после некоторой модификации применяются для иммобилизации ферментов, клеток и клеточных органелл. Гепарин – кислый полисахарид, успешно применяемый для получения водорастворимых препаратов иммобилизованных ферментов, используемых в медицине. Синтетические полимерные носители Огромное разнообразие синтетических полимеров обеспечивает их широкое использование в качестве носителей для иммобилизации ферментов. Синтетические полимеры используются для иммобилизации ферментов различными способами, а также для получения гелей и микрокапсул. Полимеры на основе стирола Полимеры этого типа являются основой для изготовления ионообменных материалов, а также для изготовления микропористых и макропористых материалов, используемых в сорбционной иммобилизации. Полимеры на основе производных акриловой кислоты Одним из производных акриловой кислоты, широко применяемым в качестве носителя, является акриламид. Весьма широко применяется метод иммобилизации ферментов и клеток путем включения их в полиакриламидный гель (ПААГ). Полиамидные носители Это группа различных полимеров с повторяющейся амидной группировкой. Главным достоинством носителей этого типа является то, что они могут быть созданы в различной физической форме: в виде гранул, порошков, волокон, мембран, трубок и т. п. Широкое применение таких носителей, особенно для медицинских целей, обусловлено и биологической инертностью, и стойкостью к воздействию биологических факторов. 47. Типы неорганических носителей Носители 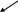    Органические Неорганические Органические НеорганическиеНизкомолекулярные Полимерные Макропористые другие Неорганические носители созданы из стекла, глины, керамики, графитовой сажи, силикагеля, а также силохромы, оксидов металлов. Их можно подвергать химической модификации, для чего носители покрывают пленкой оксидов алюминия, титана, гафния, циркония или обрабатывают органическими полимерами. Преимущества использования неорганических носителей: - легкость их регенерации - неорганическим носителям можно придать любую форму и получать их с любой степенью пористости. Достоинства микропористых кремнеземов: 1)отнести механическую прочность, 2)химическую инертность по отношению ко многим растворителям, 3)наличие жесткого скелета с заданным размером пор, 4)устойчивость к микроорганизмам. Недостатками кремнеземов 1)их использование в ограниченном диапазоне рН, 2)явление неспецифической сорбции на их поверхности, хотя последнее может быть устранено различными модифицирующими воздействиями. 3)стоимость кремнеземных носителей относительно высока, и модификация еще больше повышает цену, поэтому внедрение их в промышленность существенно ограничено. Более пригодными для промышленного использования могут оказаться природные алюмосиликаты - глины, а также пористая керамика, в состав которой, помимо алюмосиликатов, входят окислы титана, циркония или другие добавки. Следует также упомянуть такие широко распространенные носители, как уголь и графитированная сажа. Весьма перспективными носителями являются приготавливаемые на основе металлов и их оксидов, которые характеризуются: высокой механической прочностью, относительной дешевизной, стабильностью и хорошими гидродинамическими свойствами. Таким образом, к настоящему времени создано огромное число разнообразных носителей для иммобилизации ферментов. Однако для каждого индивидуального фермента, используемого в конкретном технологическом процессе, необходимо подбирать оптимальные варианты, как носителя, так и условий и способов иммобилизации. 48. Способы иммобилизации энзимов: адсорбция, включение в гели и полупроницаемые мембраны; химические методы иммобилизации ферментов Существуют два принципиально различных метода иммобилизации ферментов: без возникновения ковалентных связей между ферментом и носителем (физические методы иммобилизации) и с образованием ковалентной связи между ними (химические методы иммобилизации). При ковалентной иммобилизации носитель должен связываться только с группами, отвечающими за катализ; носитель не должен оказывать ингибирующее действие на энзим. К недостаткам адсорбционного метода следует отнести невысокую прочность связывания фермента с носителем. При изменении условий иммобилизации могут происходить десорбция фермента, его потеря и загрязнение продуктов реакции. Существенно повысить прочность связывания фермента с носителем может предварительная его модификация (обработка ионами металлов, полифункциональными агентами — полимерами, белками, гидрофобными соединениями, монослоем липида и пр.). Иммобилизация ферментов путем включения в гель. Иммобилизацию ферментов в геле осуществляют двумя способами. В первом случае фермент вводят в водный раствор мономера, а затем проводят полимеризацию, в результате которой возникает пространственная структура полимерного геля с включенными в его ячейки молекулами фермента. Во втором случае фермент вносят в раствор уже готового полимера, который впоследствии переводят в гелеобразное состояние. Иммобилизация ферментов в гелях обеспечивает равномерное распределение энзима в объеме носителя. Большинство гелевых матриц обладает высокой механической, химической, тепловой и биологической стойкостью и обеспечивает возможность многократного использования фермента, включенного в его структуру. Однако метод непригоден для иммобилизации ферментов, действующих на водонерастворимые субстраты. Иммобилизация ферментов в полупроницаемые структуры. Сущность этого способа заключается в отделении водного раствора фермента от водного раствора субстрата с помощью полупроницаемой мембраны, пропускающей низкомолекулярные молекулы субстратов и кофакторов, но задерживающей большие молекулы фермента. Разработано несколько модификаций этого метода, из которых интерес представляет микрокапсулирование и включение ферментов в липосомы. Первый способ предложен Т.Чангом в 1964 г. и состоит в том, что водный раствор фермента включается внутрь замкнутой микрокапсулы, стенки которой образованы полупроницаемым полимером. Достоинства метода микрокапсулирования — простота, уни-версальность, возможность многократного использования натив ного фермента (фермент может быть отделен от непрореагировавшего субстрата и продуктов реакции процедурой простого фильтрования). Близким к инкапсулированию методом иммобилизации можно считать включение водных растворов ферментов в липосомы. Для получения липосом из растворов липида (чаще всего лецитина) упаривают органический растворитель. Ферменты, иммобилизованные путем включения в структур липосом, используют преимущественно в медицинских и научных целях. Химические методы иммобилизации ферментов. Иммобилизация ферментов путем образования новых ковалентных связей между ферментом и носителем — наиболее массовый способ получений промышленных биокатализаторов. В отличие от физических методов этот способ иммобилизации обеспечивает прочную и необратимую связь фермента с носителем и часто сопровождается стабилизацией молекулы энзима. Однако расположение фермента относительно носителя на расстоянии одной ковалентной связи создает стерические трудности в осуществлении каталитического процесса. Фермент отделяют от носителя с помощью вставки (сшивка, спейсер), в роли которой чаще всего выступают бифункциональные и полифункциональные агенты (бромциан, гидразин, сульфурилхлорид, глутаровый диальдегид и др. Принципиально важно, чтобы в иммобилизации фермента участвовали функциональные группы, не существенные для его каталитической функции. 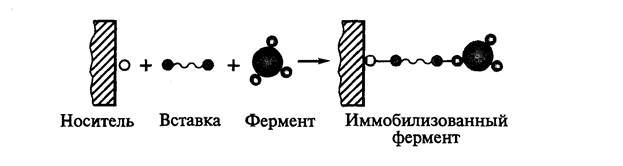 |
