Физика Теория. 1. Электромагнитная природа света. Сложение колебаний, понятие о когерентности. Интерференция световых волн. Расчет интерференционной картины от двух источников.
 Скачать 1.17 Mb. Скачать 1.17 Mb.
|
|
Фотоэффект. Гипотеза Планка, решившая задачу теплового излучения черного тела, получила подтверждение и дальнейшее развитие при объяснении фотоэффекта – явление, открытие которого сыграло важную теорию в становлении квантовой теории. Различают фотоэффект внешний, внутренний и вентильный. Внешним фотоэффектом называется испускание электронов в-вом под действием электромагнитного излучения (света). Он наблюдается в твердых телах (металлах, полупроводниках, диэлектриках), а так же в газах на отдельных атомах и молекулах. Внутренний фотоэффект – это вызванные электромагнитным излучением переходы электронов внутри полупроводника или диэлектрика из связанных состояний в свободные без вылета наружу. В р- тате концентрация носителей тока внутри тела увеличивается, что приводит к возникновению фотопроводимости (повышению электропроводности полупроводника или диэлектрика при его освещении) или возникновению ЭДС. Вентильный фотоэффект – возникновение ЭДС (фото-ЭДС) при освещении контакта двух разных полупроводников или полупроводника и металла (при отсутствии внешнего электрического поля). При помощи вентильного фотоэффекта можно напрямую преобразовывать солнечную энергию в электрическую. Уравнение Эйнштейна для внешнего фотоэффекта: Энергия падающего фотона расходуется на совершение работы выхода из металла и на сообщение фотоэлектрону кинетической энергии  . По закону сохранения энергии, . По закону сохранения энергии,  . .
В эффекте Комптона наиболее полно проявляются корпускулярные свойства света. Исследуя рассеяние монохроматического рентгеновского излучения в-вами с легкими атомами Комптон обнаружил, что в составе рассеянного излучения на ряду с излучением первоначальной длины волны наблюдается также излучение более длинных волн. Опыты показали, что разность Δλ = λ’ −λ не зависит от длины волны λ падающего излучения и природы рассеивающего в-ва, а определяется только величиной угла рассеивания  ,где ,где  –длина волны рассеянного излучения, –длина волны рассеянного излучения,  - комптоновская длина волны (при рассеяние фотона на электроне - комптоновская длина волны (при рассеяние фотона на электроне  = 2,426нм ). Эффектом Комптона наз-ся упругое рассеяние коротковолнового излучения (рентгеновского и γ -излучений) на свободных (или слабосвязанных) электронах в-ва, сопровождающееся увеличением длины волны. Если считать, как это делает квантовая теория, что излучение имеет корпускулярную природу, т.е. представляет собой поток фотонов, то эффект Комптона – р-тат упругого столкновения рентгеновских фотонов со свободными электронами в-ва (для легких атомов электроны слабо связаны с ядрами атомов, поэтому их можно считать свободными). В процессе этого столкновения фотон передает часть своих энергии и импульса в соответствии с законами их сохранения. = 2,426нм ). Эффектом Комптона наз-ся упругое рассеяние коротковолнового излучения (рентгеновского и γ -излучений) на свободных (или слабосвязанных) электронах в-ва, сопровождающееся увеличением длины волны. Если считать, как это делает квантовая теория, что излучение имеет корпускулярную природу, т.е. представляет собой поток фотонов, то эффект Комптона – р-тат упругого столкновения рентгеновских фотонов со свободными электронами в-ва (для легких атомов электроны слабо связаны с ядрами атомов, поэтому их можно считать свободными). В процессе этого столкновения фотон передает часть своих энергии и импульса в соответствии с законами их сохранения.Эффект Комптона не может наблюдаться в видимой области спектра, поскольку энергия фотона видимого света сравнима с энергией связи электрона с атомом, при этом даже внешний электрон нельзя считать свободным. Эф. К. наблюдается не только в эл-тронах, но и на заряженных частицах, например протонах, однако из-за большой массы протона его отдача «просматривается» лишь при рассеянии фотонов очень высоких энергий. Как эф. К. так и фотоэффект на основе квантовых представлений обусловлены взаимодействием фотонов с электронами. В первом случае фотон рассеивается, во втором – поглощается. Рассеивание происходит при взаимодействии фотона со свободным электроном, а фотоэффект со связанными электронами. При столкновении фотона, так как это находится в противоречии с законами сохранения импульса и энергии. Поэтому при взаимодействии фотонов со свободными электронами может наблюдаться только их рассеяние, т.е. эффект Комптона.
Если фотон обладает импульсом, то свет, падающий на тело, должен оказывать на него давление. С точки зрения квантовой теории, давление света на пов-ть обусловлено тем, что каждый фотон при соударении с пов-тью передает ей свой импульс. Рассчитаем с точки зрения квантовой теории световое давление, оказываемое на пов-ть тела потоком монохроматического излучения (частота ν), падающего перпендикулярно пов-ти. Если в единицу времени на единицу площади пов-ти тела падает N фотонов, то при коэффициенте отражения ρ света от пов-ти тела отразится ρN фотонов, а (1− ρ )N - поглотится. Каждый поглощенный фотон передает пов-ти импульс  , а каждый отраженный - 2 , а каждый отраженный - 2  =2hν / c (при отражении импульс фотона изменяется на =2hν / c (при отражении импульс фотона изменяется на  ). Давление света на пов-ть равно импульсу, который передают пов-ти в 1 с N фотонов: ). Давление света на пов-ть равно импульсу, который передают пов-ти в 1 с N фотонов:  есть энергия всех фотонов, падающих на единицу пов-ти в единицу времени, т.е. энергетическая освещенность пов-ти, а есть энергия всех фотонов, падающих на единицу пов-ти в единицу времени, т.е. энергетическая освещенность пов-ти, а  /c =ω - объемная плотность энергии излучения. Поэтому давление производимое светом при нормальном падении на пов-ть, /c =ω - объемная плотность энергии излучения. Поэтому давление производимое светом при нормальном падении на пов-ть,  . .6. Атомные спектры. Сериальные формулы. Опыт Резерфорда. Постулаты Бора. Опыт Франка-Герца. Элементарная теория атома водорода. Значение теории Бора. Рентгеновские характеристические спектры. Закон Мозли.
Исследования спектров излучения разреженных газов (т.е. спектров излучения отдельных атомов) показали, что каждому газу присущ вполне определенный линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий. Самым изученным явл-ся спектр наиболее простого атома – атома водорода. Бальмер (1825-1898) подобрал эмпирическую ф-лу описывающую все известные в то время спектральные линии атома водорода и видимой области спектра  ,(n = 3, 4, …) где R'– постоянная Ридберга. Так как ν = с /λ , то ф-ла может быть переписана для частот: ,(n = 3, 4, …) где R'– постоянная Ридберга. Так как ν = с /λ , то ф-ла может быть переписана для частот:  , где R = R'c - так же постоянная Ридберга. Из полученных выражений вытекает, что спектральные линии отличающиеся различными значениями n, образуют группу или серию линий, называемую серией Бальмера. С увеличением n линии серии сближаются; значение n = ∞ определяет границу серии, к которой со стороны больших частот примыкает сплошной спектр. В дальнейшем в спектре атома водорода было обнаружено еще несколько серий. , где R = R'c - так же постоянная Ридберга. Из полученных выражений вытекает, что спектральные линии отличающиеся различными значениями n, образуют группу или серию линий, называемую серией Бальмера. С увеличением n линии серии сближаются; значение n = ∞ определяет границу серии, к которой со стороны больших частот примыкает сплошной спектр. В дальнейшем в спектре атома водорода было обнаружено еще несколько серий. В ультрафиолетовой области спектра находится серия Лаймана:  В инфракрасной области были обнаружены: серия Пашена:  серия Брэкета:  серия Пфунда:  серия Хэмфи:  Все приведенные выше серии в спектре атома водорода могут быть описаны одной ф-лой, называемой обобщенной ф-лой Бальмера:  , где m – имеет в каждой данной серии постоянное значение, m = 1, 2, 3, 4, 5, 6 (определяет серию), n – принимает целочисленные значения, начиная с m+1 (определяет отдельные линии этой серии). , где m – имеет в каждой данной серии постоянное значение, m = 1, 2, 3, 4, 5, 6 (определяет серию), n – принимает целочисленные значения, начиная с m+1 (определяет отдельные линии этой серии).
В развитии представлений о строении атома велико значение опытов Резерфорда по рассеянию α -частиц в в-ве. Альфа частицы возникают при радиоактивных превращениях; они являются положительными заряженными частицами с зарядом 2е и массой, примерно в 7300 раз большей массы эл-трона. Пучки α -частиц обладают высокой монохроматичностью (для данного превращения имеют практически одну и ту же скорость (порядка 10^7 м/с)). Резерфорд, исследуя прохождение α-частиц в в-ве (через золотую фольгу толщиной примерно 1 мкм), показал, что основная их часть испытывает незначительные отклонения, но некоторые α-частицы (примерно одна из 20000) резко отклоняются от первоначального направления (углы отклонения достигали даже180° ). Т.к. электроны не могут существенно изменить движение столь тяжелых и быстрых частиц, как α-частицы, то Резерфордом был сделан вывод, что значительное отклонение α-частиц обусловлено их взаимодействием с положительным зарядом большой массы. Однако значительное отклонение испытывают лишь немногие α -частицы; следовательно, лишь некоторые из них проходят вблизи данного положительного заряда. Это, в свою очередь означает, что положительный заряд атома сосредоточен в объеме, очень малом по сравнению с объемом атома. На основании своих опытов Резерфорд предложил ядерную модель атома. Согласно этой модели, вокруг положи порядковый номер эл-та в системе Менделеева, е -элементарный заряд), размер 10^(−15) −10^(−14) м и массу , практически равную массе атома, в области с линейными размерами порядка 10^(−10) м по замкнутым орбитам движутся электроны, образую электронную оболочку атома. Так атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т.е. вокруг ядра должно вращаться Z электронов.
Первая попытка построить качественно новую – квантовую -- теорию атома была предпринята Бором. Он поставил перед собой цель связать в единое целое эмпирические закономерности линейчатых спектров, ядерную модель атома Резерфорда (Согласно этой модели, вокруг положительного ядра, имеющего заряд Ze (Z – порядковый номер эл-та в системе Менделеева, е – элементарный заряд), размер 10^(−15) −10^(−14) м и массу , практически равную массе атома, в области с линейными размерами порядка 10^(−10 м) по замкнутым орбитам движутся электроны, образую электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен cуммарному заряду электронов, т.е. вокруг ядра должно вращаться Z электронов) и квантовый характер излучения и поглощения света. Два постулата: Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн. В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантовые значения момента импульса, удовлетворяющие условию  (n=1,2,3,…), где (n=1,2,3,…), где 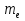 -масса эл-трона, v – его скорость по n-ой орбите радиуса -масса эл-трона, v – его скорость по n-ой орбите радиуса  , ,  = h / 2π . = h / 2π .Второй постулат (правило частот): при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией  , равной разности энергий соответствующих стационарных состояний ( , равной разности энергий соответствующих стационарных состояний (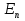 и и  -- соответственно энергии стационарных состояний атома до и после излучения (поглощения)). При -- соответственно энергии стационарных состояний атома до и после излучения (поглощения)). При  < <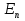 происходит излучение фотона (переход атома из состояния с большей энергией в состояние с меньшей, т.е. переход электрона с более удаленной от ядра орбиты на близлежащую), при происходит излучение фотона (переход атома из состояния с большей энергией в состояние с меньшей, т.е. переход электрона с более удаленной от ядра орбиты на близлежащую), при  > >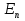 – его поглощение (переход атома в состояние с большей энергией, т.е. переход электрона на более удаленную от ядра орбиту). Набор всевозможных дискретных частот ν=( – его поглощение (переход атома в состояние с большей энергией, т.е. переход электрона на более удаленную от ядра орбиту). Набор всевозможных дискретных частот ν=(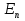 − − )/h квантовых переходов и определяет линейчатый спектр атома. )/h квантовых переходов и определяет линейчатый спектр атома.
Изучая методом задерживающего потенциала столкновения электронов с атомами газов, экспериментально было доказано, что значения энергии атомов дискретны. Принципиальная схема их установки приведена на рис. Вакуумная трубка, заполненная парами ртути (давление приблизительно равно 13 Па), содержала катод (К), две сетки (  и и  ) и анод (А). Электроны, эмитируемые катодом, ускорялись разностью потенциалов, приложенной между катодом и сеткой ) и анод (А). Электроны, эмитируемые катодом, ускорялись разностью потенциалов, приложенной между катодом и сеткой  . Между сеткой . Между сеткой  и анодом приложен небольшой (примерно 0.5 В) задерживающий потенциал. Электроны, ускоренные в области 1, попадают в область 2 между сетками, где испытывают соударения с атомами паров ртути. Электроны, которые после соударений имеют достаточную энергию для преодоления задерживающего потенциала в области 3, достигают анода. При неупругих соударениях электронов с атомами ртути последние могут возбуждаться. Согласно боровской теории, каждый из атомов ртути может получить лишь вполне определенную энергию, переходя при этом в одно из возбужденных состояний. Из опыта следует, что при увеличении ускоряющего потенциала вплоть до 5 В анодный ток возрастает монотонно, его значение проходит через максимум, затем резко уменьшается и возрастает вновь. и анодом приложен небольшой (примерно 0.5 В) задерживающий потенциал. Электроны, ускоренные в области 1, попадают в область 2 между сетками, где испытывают соударения с атомами паров ртути. Электроны, которые после соударений имеют достаточную энергию для преодоления задерживающего потенциала в области 3, достигают анода. При неупругих соударениях электронов с атомами ртути последние могут возбуждаться. Согласно боровской теории, каждый из атомов ртути может получить лишь вполне определенную энергию, переходя при этом в одно из возбужденных состояний. Из опыта следует, что при увеличении ускоряющего потенциала вплоть до 5 В анодный ток возрастает монотонно, его значение проходит через максимум, затем резко уменьшается и возрастает вновь.
7. Длина волны де Бройля. Опытное обоснование волнового дуализма. Соотношение неопределенностей Гейзенберга. Волновая функция и ее статистический смысл. Уравнение Шредингера. Собственные функции и собственные значения. Стационарное уравнение Шредингера. Квантомеханическое представление свободно движущейся частицы. Квантомеханическое описание частицы в бесконечно глубокой прямоугольной потенциальной яме.
Французский ученый Луи де Бройль (1892—1987), осознавая существующую в природе симметрию и развивая представления о двойственной корпускулярно-волновой природе света, выдвинул в 1923 г. гипотезу об универсальности корпускулярно-волнового дуализма. Де Бройль утверждал, что не только фотоны, но и электроны и любые другие частицы материи наряду с корпускулярными обладают так- же волновыми свойствами. Итак, согласно де Бройлю, с каждым микрообъектом связываются, с одной стороны, корпускулярные характеристики — энергия Е и импульс р, а с другой — волновые характеристики — частота v и длина волны К. Количественные соотношения, связывающие корпускулярные и волновые свойства частиц, такие же, как для фотонов:  Таким образом, любой частице, обладающей импульсом, сопоставляют волновой процесс с длиной волны, определяемой по формуле де Бройля: Таким образом, любой частице, обладающей импульсом, сопоставляют волновой процесс с длиной волны, определяемой по формуле де Бройля:  Это соотношение справедливо для любой частицы с импульсом р. Это соотношение справедливо для любой частицы с импульсом р.
Вскоре гипотеза де Бройля была подтверждена экспериментально. В 1927 г. американские физик и К. Дэвиссо н (1881 — 1958) и Л. Джермер (1896 — 1971) обнаружили, что пучок электронов, рассеивающийся от естественной дифракционной решетки — кристалла никеля, дает отчетливую дифракционную картину. Дифракционные максимумы соответствовали формуле Вульфа — Брэггов (182.1), а брэгговская длина волны оказалась в точности равной длине волны, вычисленной по формуле. В дальнейшем формула де Бройля была подтверждена опытами П. С. Тартаковского и Г. Томсона, наблюдавших дифракционную картину при прохождении пучка быстрых электронов (энергия «50 кэВ) через металлическую фольгу (толщиной ж 1 мкм). Так как дифракционная картина исследовалась для потока электронов, то необходимо было доказать, что волновые свойства присущи не только потоку большой совокупности электронов, но и каждому электрону в отдельности. Это удалось экспериментально подтвердить в 1948 г. советскому физику В. А. Фабриканту (р. 1907). Он показал, что даже в случае столь слабого электронного пучка, когда каждый электрон проходит через прибор независимо от других (промежуток времени между двумя электронами в 10^4 раз больше времени прохождения электроном прибора), возникающая при длительной экспозиции дифракционная картина не отличается от дифракционных картин, получаемых при короткой экспозиции для потоков электронов, в десятки миллионов раз более интенсивных. Следовательно, волновые свойства частиц не являются свойством их коллектива, а присущи каждой частице в отдельности. Впоследствии дифракционные явления обнаружили также для нейтронов, протонов, атомных и молекулярных пучков. Это окончательно послужило доказательством наличия волновых свойств микрочастиц и позволило описывать движение микрочастиц в виде волнового процесса, характеризующегося определенной длиной волны, рассчитываемой по формуле де Бройля. Открытие волновых cвойств микрочастиц привело к появлению и развитию новых методов исследования структуры веществ, таких, как электронография и нейтронография, а также к возникновению новой отрасли науки — электронной оптики. |
