ответы. биохимия.. 1 Классификация и строение углеводов. Функции углеводов различных классов
 Скачать 468 Kb. Скачать 468 Kb.
|
Механизмы действияОкисление углеводородов, спиртов, кислот, жиров и других веществ свободным кислородом представляет собой цепной процесс. Цепные реакции превращений осуществляются с участием активных свободных радикалов — перекисных (RO2*), алкоксильных (RO*), алкильных (R*), а также активных форм кислорода (супероксид анион, синглетный кислород). Для цепных разветвлённых реакций окисления характерно увеличение скорости в ходе превращения (автокатализ). Это связано с образованием свободных радикалов при распаде промежуточных продуктов — гидроперекисей и др. Механизм действия наиболее распространённых антиоксидантов (ароматические амины, фенолы, нафтолы и др.) состоит в обрыве реакционных цепей: молекулы антиоксиданта взаимодействуют с активными радикалами с образованием малоактивных радикалов. Окисление замедляется также в присутствии веществ, разрушающих гидроперекиси (диалкилсульфиды и др.). В этом случае падает скорость образования свободных радикалов. Даже в небольшом количестве (0,01—0,001 %) антиоксиданты уменьшают скорость окисления, поэтому в течение некоторого периода времени (период торможения, индукции) продукты окисления не обнаруживаются. В практике торможения окислительных процессов большое значение имеет явление синергизма — взаимного усиления эффективности антиоксидантов в смеси, либо в присутствии других веществ. 48. антиоксидантные системы клетки и их биологическая роль В ходе жизнедеятельности организма образуются свободные радикалы - промежуточные продукты обмена, которые благодаря наличию неспаренного электрона обладают чрезвычайно высокой реакционноспособностью и могут вносить «хаос и беспорядок» в тонко налаженную биохимическую машинуАнтиоксиданты— ингибиторы окисления, природные или синтетические вещества, способные замедлять окисление.Механизм действия наиболее распространённых антиоксидантов (ароматические амины, фенолы, нафтолы и др.) состоит в обрыве реакционных цепей: молекулы антиоксиданта взаимодействуют с активными радикалами с образованием малоактивных радикалов. Окисление замедляется также в присутствии веществ, разрушающих гидроперекиси. В этом случае падает скорость образования свободных радикалов. 49. Биохимические механизмы окислительного декарбоксилирования пирувата Пировиноградная кислота (пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробных условиях она восстанавливается до молочной кислоты. В аэробных условиях пируват с импортом с ионами Н+, движущимися по протонному градиенту, проникает в митохондрии. Здесь происходит его превращение до уксусной кислоты, переносчиком которй служит коэнзим А. Суммарное уравнение отражает окислительной декарбоксилирование пирувата, восстановление НАД до НАДН и образования ацетил-SKoA. 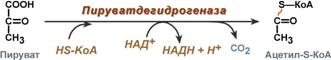 Превращение состоит из 5 последовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса-3фермента и 5 коферментов: -пируватдегидрогеназа, ее кофермент-тиаминдифосфат; -дигидролипоат-ацетилтрансфераза, ее кофермент-липоевая кислота; -дигидролипоат-дегидрогеназа, кофермент ФАД. Помимо этих коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД. Суть первых трех реакций сводится к декарбоксилированию пирувата: 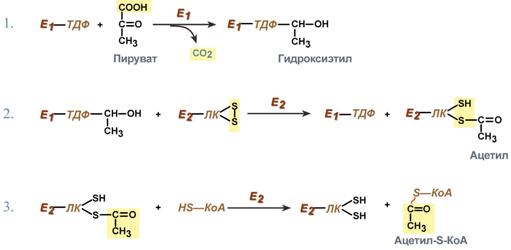 50. механизм реакций и биологическая роль цикла кребса Это цепь из 8 посл-ых р-ций , связ с циклическим окис-ем ацетил-КоА.Начинается с конденсации ацетил-S-КоА с ОА и образ-м цитрата. Затем цитрат изомеризуется Оксалоацетат – цитрат – изоцитрат – альфа-кетаглутерат – сукцинил КоА – сукцинат – фурамат – малат. На выходе 12 АТФ. Цикл трикарбоновых кислот (цикл Кребса, цитратный цикл) — центральная часть общего пути катаболизма, циклический биохимический аэробный процесс, в ходе которого происходит превращение двух- и трёхуглеродных соединений, образующихся как промежуточные продукты в живых организмах при распаде углеводов, жиров и белков, до CO2. При этом освобождённый водород направляется в цепь тканевого дыхания, где в дальнейшем окисляется до воды, принимая непосредственное участие в синтезе универсального источника энергии — АТФ. Цикл Кребса — это ключевой этап дыхания всех клеток, использующих кислород, центр пересечения множества метаболических путей в организме. В процессе цикла используются три молекулы воды, выделяются две молекулы СО2 и четыре пары атомов водорода, которые восстанавливают соответствующие коферменты (ФАД - флавинадениндинуклеотид и НАД). Суммарно реакция цикла может быть выражена следующим уравнением: ацетил-КоА + ЗН2О + ЗНАД+ + ФАД + АДФ + Н3РО4 > КоА + 2СО2 + ЗНАД * Н + Н* + ФАД * Н2 + АТФ. Таким образом, в результате распада одной молекулы пировиноградной кислоты в аэробной фазе (декарбоксилирование ПВК и цикла Кребса) выделяется ЗСО2, 4НАД * Н + Н+, ФАД * Н2. Суммарно реакцию гликолиза, окислительного декарбоксилирования и цикла Кребса можно записать в следующем виде: С6Н,2Об + 6Н20 + 10НАД + 2ФАД > 6СО2 + 4АТФ + 10НАД * Н + Н+ + 2ФАД * Н2. У эукариот все реакции цикла Кребса протекают внутри митохондрий, причём катализирующие их ферменты, кроме одного, находятся в свободном состоянии в митохондриальном матриксе, исключение составляет сукцинатдегидрогеназа, которая локализуется на внутренней митохондриальной мембране, встраиваясь в липидный бислой. У прокариот реакции цикла протекают в цитоплазме. 51. Биосинтез гликогена Гликоген - основная форма депонирования глюкозы в клетках животных. У растений эту же функцию выполняет крахмал. В структурном отношении гликоген, как и крахмал, представляет собой разветвленный полимер из глюкозы. Однако гликоген более разветвлен и компактен. Ветвление обеспечивает быстрое освобождение при распаде гликогена большого количества концевых мономеров. Синтез и распад гликогена не являются обращением друг в друга, эти процессы происходят разными путями. Биосинтез гликогена. Гликоген синтезируется в период пищеварения (в течение 1-2 ч после приема углеводной пищи). Гликогенез особенно интенсивно протекает в печени и скелетных мышцах. В начальных реакциях образуется UDF-глюкоза (реакция 3), которая является активированной формой глюкозы, непосредственно включающейся в реакцию полимеризации (реакция 4). Эта последняя реакция катализируется гликогенсинтазой, которая присоединяет глюкозу к олигосахариду или к уже имеющейся в клетке молекуле гликогена, наращивая цепь новыми мономерами. Для подготовки и включения в растущую полисахаридную цепь требуется энергия 1 моль АТР и 1 моль UTP. Ветвление полисахаридной цепи происходит при участии фермента амило - -1,4--1,6-гликозил-трансферазы путем разрыва одной -1,4-связи и переноса олигосахаридного остатка от конца растущей цепи к ее середине с образованием в этом месте -1,6-гликозидной связи. Молекула гликогена содержит до 1 млн остатков глюкозы, следовательно, на синтез расходуется значительное количество энергии. Необходимость превращения глюкозы в гликоген связана с тем, что накопление значительного количества глюкозы в клетке привело бы к повышению осмотического давления, так как глюкоза хорошо растворимое вещество. Напротив, гликоген содержится в клетке в виде гранул, и мало растворим. Распад гликогена - гликогенолиз - происходит в период между приемами пищи. Распад гликогена. Освобождение глюкозы в виде глюкозо-1-фосфата (реакция 5) происходит в результате фосфоролиза, катализируемого фосфорилазой. Фермент отщепляет концевые остатки один за другим, укорачивая цепи гликогена. Однако этот фермент расщепляет только -1,4 гликозидные связи. Связи в точке ветвления гидролизуются ферментом амило--1,6-гликозидазой, который отщепляет мономер глюкозы в свободном виде. 52. Гликолиз и его биологическое значение - ферментативный процесс последовательного расщепления глюкозы в клетках, сопровождающийся синтезом АТФ. Гликолиз при аэробных условиях образов – пирувата, в анаэробных - лактата. Гликолиз является основным путём катаболизма глюкозы в организме животных. Имеет большое значение для мышеч клеток, растущ тканей (опух) , т.к обеспечивает накопление энергии в отсутсвие кислорода. Состоит из 10 последовательных реакций. Глюкоза - глюкоза-6-фосфат – фруктоза-6-фосфат – фруктоза-1,6-бифосфат – дегидроксиацетон фасфат + глицеральдегид-3-фасфат – 1,3-дифосфоглицерат – 3 фосфоглицерат – 2 фосфоглицерат – фосфоенол пируват – пируват. Биологическое значение процесса гликолиза заключается прежде всего в образовании богатых энергией фосфорных соединений. На первых стадиях гликолиза затрачиваются 2 молекулы АТФ (гексокиназная и фосфофрукто-киназная реакции). На последующих образуются 4 молекулы АТФ (фосфоглицераткиназная и пируваткиназная реакции). Таким образом, энергетическая эффективность гликолиза в анаэробных условиях составляет 2 молекулы АТФ на одну молекулу глюкозы. Большинство реакций обратимо, за исключением трех (реакций 1, 3, 10); все метаболиты находятся в фосфорилированной форме; источником фосфатной группы в реакциях фосфорилирования являются АТФ (реакции 1, 3) или неорганический фосфат (реакция 6); регенерация NAD+, являющаяся необходимым условием протекания гликолиза, происходит при аэробном гликолизе посредством дыхательной цепи. В этом случае водород транспортируется в митохондрии с помощью челночного механизма при участии переносчиков. Это происходит потому, что мембрана митоходрий непроницаема для протонов. При анаэробном гликолизе регенерации NAD+ осуществляется независимо от дыхательной цепи. В этом случае акцептором водорода от NADH является пируват, который восстанавливается в лактат; образование АТФ при гликолизе может идти двумя путями: либо субстратным фосфорилированием, когда для фосфорилирования AДФ используется энергия макроэргической связи субстрата (реакции 7, 9), либо путем окислительного фосфорилирования AДФ, сопряженного с дыхательной цепью (реакция 6). 53. Глюконеогенез и его биологическая роль — процесс образования в печени и отчасти в корковом веществе почек (около 10 %) молекул глюкозы из молекул других органических соединений — источников энергии, например свободных аминокислот, молочной кислоты, глицерина. Стадии глюконеогенеза повторяют стадии гликолиза в обратном направлении и катализируются теми же ферментами за исключением 4 реакций: 1. Превращение пирувата в оксалоацетат (фермент пируваткарбоксилаза) 2. Превращение оксалоацетата в фосфоенолпируват (фермент фосфоенолпируваткарбоксикиназа) 3. Превращение фруктозо-1,6-дифосфата в фруктозо-6-фосфат (фермент фруктозо-1,6-дифосфатаза) 4. Превращение глюкозо-6-фосфата в глюкозу (фермент глюкозо-6-фосфатаза) Суммарное уравнение глюконеогенеза: 2 CH3COCOOH + 4ATP + 2GTP + 2NADH.H+ + 6 H2O = C6H12O6 + 2NAD + 4ADP + 2GDP + 6Pn При голодании в организме человека активно используются запасы питательных веществ (гликоген, жирные кислоты). Они расщепляются до аминокислот, кетокислот и других неуглеводных соединений. Большая часть этих соединений не выводится из организма, а подвергаются реутилизации. Вещества транспортируются кровью в печень из других тканей, и используются в глюконеогенезе для синтеза глюкозы — основного источника энергии в организме. Таким образом при истощении запасов организма, глюконеогенез является основным поставщиком энергетических субстратов. 54. Пентозофосфатный путь окисления углеводов - механизм с помощью кот шестиуглеродная глюкоза превращается в углеводы с 5 углеродными атомами, по ходу обеспеч образование восстан формы кофермента NADPH. В определен условиях через этот путь глюкоза может окисляться до пирувата, а затем – до СО2 и воды. Значение этого пути в обмене веществ велико. Он поставляет восстановленный НАДФН, необходимый для биосинтеза жирных кислот, холестерина и т.д. За счет пентозофосфатного цикла примерно на 50% покрывается потребность организма в НАДФН. Другая функция пентозофосфатного цикла заключается в том, что он поставляет пентозофосфаты для синтеза нуклеиновых кислот и многих коферментов. Основными потребит NADPH, полученных в ППФ, явл-ся клетки печени,жировой ткани, коры надпочечников , молоч желез - все клетки где актив происходят процессы биосинтеза жиров и стероидов. Очень богаты ферментами ПФП эритроциты,где оч необходим NADPH(р-ция вост-я глютатиона) Может реализоваться двумя способами – окислительным и неокислительным. Все р-ции ПФП осущ-ся в цитоплазме. 55. Особенности углеводного обмена у жвачных животных. Пути синтеза глюкозы у жвачных животных В ротовой полости переваривание сахаров не происходит из за отсутствия ферментов. В рубце происходит 50% перевар сахаров. Ферменты вырабатываются микрофлорой рубца(мальтоза,сахароза,целлюлоза). Образовавшиеся в результате ферментативного гидролиза поли- и дисахаридов моносахара под действием бактерий рубца подвергаются процессам брожения (глюкоза далее распад до ЛЖК(уксусн ,молочн,пропионовой,масляной кислот, кот затем всасыв в кровь) ЛЖК всасыв в стенки сетки и книжки и идут на энергетические нужды организма.) В сычуге – отсутствуют ферменты – нет переваривания углеводов. В тонком отделе идет перевар остатков сахаров как у моногастричных жив. Целлюлоза - целлобиаза – 2бета-В-глюкозы. Для жвачных животных основными источниками углеводов является клетчатка. В рубце у них при расщеплении клетчатки образуется глюкоза. Одна часть ее всасывается в кровь, другая — служит пищей для микробов и подвергается дальнейшему распаду с образованием летучих жирных кислот: уксусной, масляной, пропионовой. Всосавшиеся из пищеварительного тракта углеводы через воротную вену поступают в печень, где из них образуется гликоген. Здесь он депонируется и является резервным источником образования глюкозы. Остальная часть глюкозы из печени поступает в большой круг кровообращения и далее в органы и ткани как энергетический материал. Неиспользованная часть глюкозы превращается триглицерин (в жировом депо). У жвачных животных уровень глюкозы в крови низкий (40–60 мг %) и мало зависит от содержания углеводов в корме. При избытке белка, жира в рационе и нарушении углеводно-жирового обмена у высокопродуктивных животных возникает заболевание кетоз. Оно характеризуется повышенным образованием и выведением кетоновых тел. При этом у животных нарушается пищеварение, обмен веществ, снижается продуктивность. Особенностью углеводного обмена у молодняка жвачных также является высокое содержание глюкозы (100–120 мг %) в крови. С возрастом концентрация постепенно снижается. 56. Роль летучих жирных кислот в метаболизме жвачных животных Давно известно, что значительная часть питательных веществ корма переваривается у жвачных в преджелудках за счет симбиотической микрофлоры. Здесь переваривается 80-95% крахмала и растворимых углеводов рациона, 60-70% клетчатки, 40-80% белков. В преджелудках также происходят процессы превращения липидов, нитратов и других веществ, синтез микробного белка и аминокислот. Летучие жирные кислоты, образующиеся в процессе микробной ферментации корма, всасываясь через эпителий преджелудков, служат источником энергии для организма животного, а также предшественниками компонентов молока. Правильное течение процессов в преджелудках - залог нормального обмена веществ. Регуляция состава микрофлоры. ЛЖК обладают известной антибактериальной активностью. Благодаря этому они могут служить важным фактором в поддержании баланса микробной экосистемы. Они могут как препятствовать колонизации кишечника патогенными микроорганизмами, например, сальмонеллами, так и служить промоторами роста некоторых анаэробных бактерий. Поддержание водно-электролитного баланса в просвете кишки. Вместе с ЛЖК всасываются ионы натрия, калия, хлора и воды. От всасывания ЛЖК зависит содержание карбонатов в просвете кишечника и рН кишечного содержимого. Поддержание энергообмена. У жвачных животных ЛЖК обеспечивают почти 70% энергопотребности организма. Особенно велика роль кислот с четным числом атомов углерода - уксусной, масляной и капроновой кислот. Питание и рост кишечного эпителия. ЛЖК, особенно масляная кислота, являются основным источником питания колоноцитов, обеспечивая их энергией почти на 70%. ЛЖК стимулируют пролиферацию кишечного эпителия. Их отсутствие в просвете кишки или нарушение утилизации колоноцитами приводит к развитию язвенного колита и других воспалительных заболеваний кишечника. Антиканцерогенное действие. Масляная кислота действует на многие клеточные регуляторы, участвующие в дифференцировке эпителия толстого кишечника. Многочисленные исследования показали защитную роль масляной кислоты в отношении появления и роста раковой опухоли толстого кишечника. У ЛЖК обнаружено еще много других способностей, которые до конца не осмысленны. Например, регулировать гликогенез и кетонообразование в печени, расслаблять гладкую мускулатуру кишечника, влиять на экспрессию различных генов в колоноцитах. 57. строение клеточных мембран и их функции Мемб- актив молек комплекс с высокоизбирательными свойствами, обеспеч обмен веществ и энергии с окружающей средой. Сост из белков и липидов. 3типа липидов: -фосфолипиды, гликолипиды, холестерин. Фосфолипидный слой - бислой с гидрофобными головками и гидрофил хвостами. И еще присутсвуют микротрубочки Функции: -1)барьерная – обеспечивает регул-ый,избирательный, пассив и актив обмен веществ с окруж средой. -2) транспортная – транспорт веществ в клетку и из клетки; доставка питат веществ, удаление конеч продуктов обмена. -3) матричная – обеспеч взаиморасп и ориентацию мемб белков. -4) механическая – обеспечив автономность клетки. -5) энергетическая -6) рецепторная –как белки рецепторы восприн те или иные сигналы . -7) ферментативная – белки-ферменты. |
