Зачёт клин патфиз. Patfiz_zachet переделанный. 1. Понятие о клинической патофизиологии, ее задачи и перспективы
 Скачать 5.74 Mb. Скачать 5.74 Mb.
|
|
56.Осложнения и исходы стенокардии. 1.переход из стабильной стенокардии в нестабильную. 2.острый инфаркт миокарда. 3.нарушение ритма сердца(аритмия). 4.остановка сердца. 57.Ишемия миокарда. Этиология. Механизм повреждения сердца при ишемии. Ишемия миокарда — состояние, при котором нарушается кровообращение в мышце сердца, вследствие чего возникает несоответствие между потребностями миокарда в крови и в первую очередь в кислороде, с одной стороны, и уровнем коронарного кровотока и количеством поступающего с кровью кислорода в данный момент, с другой. Нарушение баланса между реальным коронарным кровотоком и по-требностями миокарда в кислороде может быть обусловлено: 1) причинами внутри сосуда: – атеросклеротическим сужением просвета венечных артерий; – тромбозом и тромбоэмболией венечных артерий; – спазмом венечных артерий; 2) причинами вне сосуда: – тахикардией; – гипертрофией миокарда; – артериальной гипертензией. Ишемия миокарда может быть результатом либо повышения потребно-сти миокарда в кислороде (физическая или психическая перегрузка, спонтан-ные изменения частоты сердечного ритма или АД), либо снижения доставки кислорода (спазм коронарной артерии, закупорка артерии тромбоцитами, парциальный тромбоз). Нарушение функции эндотелия играет роль в изме-нении порога развития ишемии, нарушение высвобождения оксида азота (главный фактор расслабления эндотелия) может способствовать беспрепят-ственному развитию вазоконстрикции и облегчать адгезию тромбоцитов. Повышение потребности миокарда в кислороде является преобладаю-щим механизмом ишемии, атеросклеротическое поражение коронарных ар-терий — основным этиологическим фактором. Механизм (Таб 6)  58.Острый инфаркт миокарда. Этиология.(Таб 8) Основными патогенетическими факторами ИМ являются: – коронарный атеросклероз; – тромбоз; – спазм коронарной артерии. 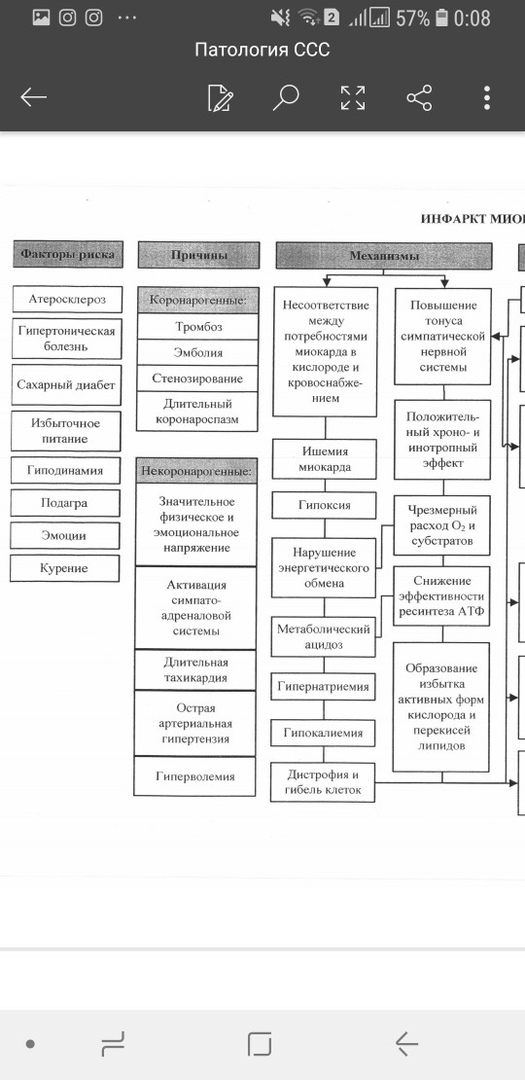 59.Острый инфаркт миокарда. Патогенез. 62.Перечислить и объяснить патогенез основных проявлений инфаркта миокарда. Стадии патогенеза ИМ следующие: 1) ишемия; 2) повреждение (некробиоз); 3) некроз; 4) рубцевание.  60.Дать патофизиологическое объяснение ЭКГ признаков ишемии и инфаркта миокарда, ишемического и реперфузионного повреждения миокарда.(Таб 11) 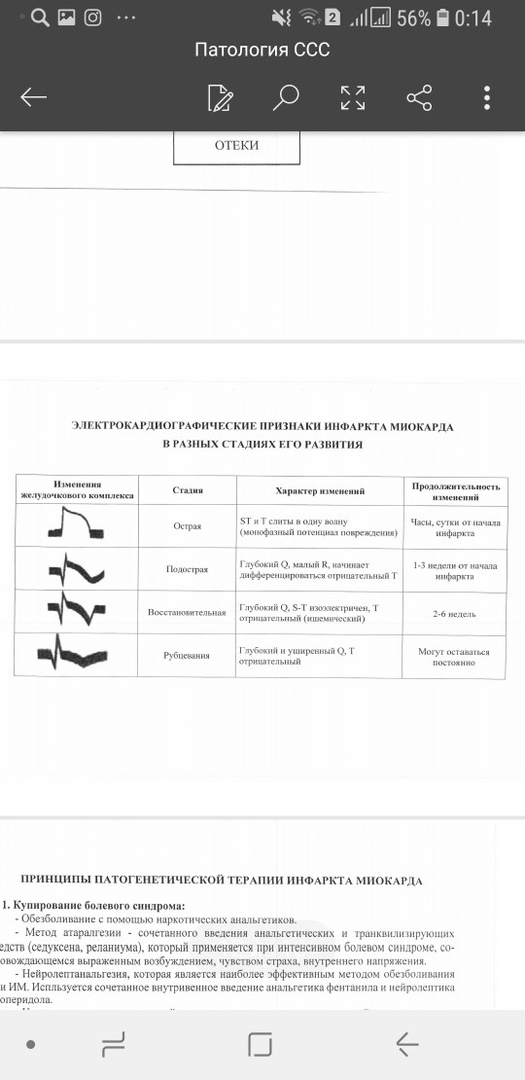 61.Охарактеризовать метаболические, электрогенные, сократительные нарушения миокарда при инфаркте миокарда. 63.Осложнения и исходы инфаркта миокарда.(Таб 8) 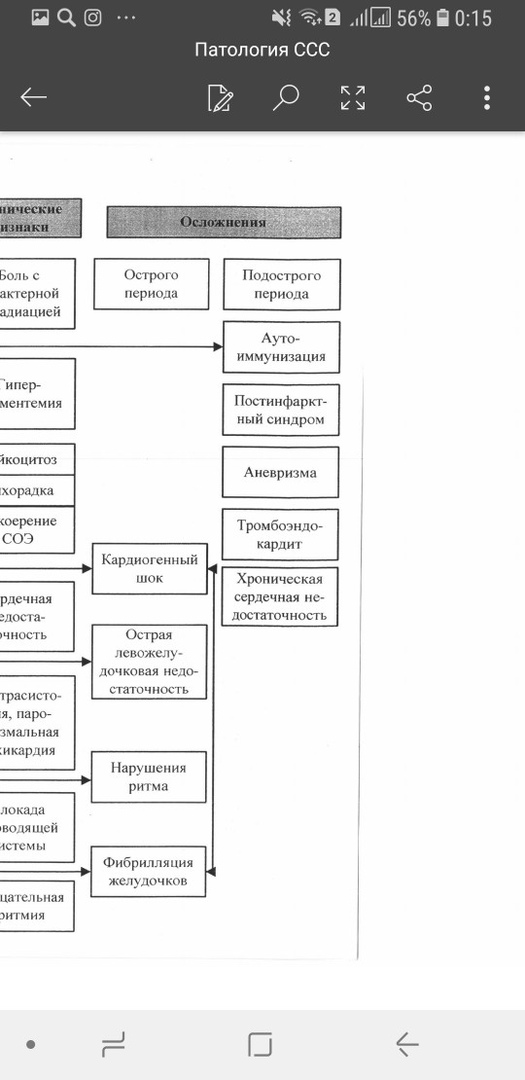 64.Острый инфаркт миокарда. Принципы патогенетической терапии.(Таб 3)  65.Гипертрофии миокарда. Этиология. Виды. Стадии. Патогенез. Исход. (Патогенез Таб 10) 66.Механизмы кардиотоксического действия катехоламинов в миокарде. 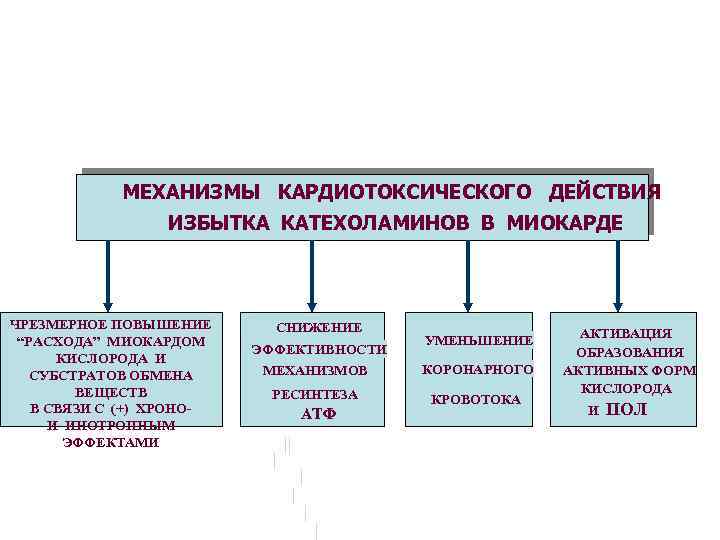 67.Коронарная недостаточность. Основным механизмы повреждения.(Таб 2?)  68.Реперфузионное повреждение миокарда этиология, патогенез, исходы. Наиболее распространённые формы коронарной недостаточности — стенокардии различного течения — характеризуются спонтанной или вызванной медикаментозно сменой более или менее длительного периода ишемии миокарда периодом возобновления коронарного кровотока — реперфузией. Основными механизмами дополнительного — реперфузионного — повреждения клеток миокарда являются: - усугубление нарушения энергетического обеспечения клеток реперфузируемого миокарда на этапах ресинтеза, транспорта, утилизации энергии АТФ (см. рис. 23–9). Это характеризуется: - снижением эффективности ресинтеза АТФ. Причинами дополнительного – реперфузионного – подавления рефосфорилирования АДФ является: ипергидратация, набухание и разрушение митохондрий в реперфузируемом миокарде (результат осмотического отёка органелл, перерастяжения и разрыва их мембран в связи с избыточным накоплением в них Ca2+ и жидкости), разобщающий эффект избытка Ca2+; выход АДФ, АМФ и других пуриновых соединений из митохондрий кардиомиоцитов в межклеточную жидкость; - нарушением механизма транспорта энергии АТФ в клетках миокарда; - снижением эффективности механизмов утилизации энергии АТФ; - нарастание степени повреждения мембран и ферментов клеток и миокарда (см. рис. 23–11). Причины этого: реперфузионная (кислородзависимая) интенсификации липопероксидного процесса, кальциевая активация протеаз, липаз, фосфолипаз и других гидролаз, а также осмотическое набухание и разрыв мембран клеток миокарда и их органелл; - потенцирование дисбаланса ионов и жидкости в кардиомиоцитах (см. рис. 23–12). Причинами этого считают реперфузионные расстройства процессов энергообеспечения и повреждение мембран и ферментов. В результате в клетках миокарда накапливается избыток Na+ и Ca2+ и как следствие — жидкости; - снижение эффективности регуляторных (нервных, гуморальных) воздействий на клетки миокарда (в норме способствующих интеграции и нормализации внутриклеточных процессов); - нарастание выраженности гормоно нейромедиаторной диссоциации катехоламинов. Эффективная профилактика и терапия постишемических реперфузионных состояний позволяет: - предотвратить развитие инфаркта миокарда или значительно уменьшить объём поражённого участка миокарда; - стимулировать процессы репарации в сердечной мышце; - нормализовать сократительную функцию сердца; - восстановить оптимальные параметры кровообращения в организме |
