|
Зачёт клин патфиз. Patfiz_zachet переделанный. 1. Понятие о клинической патофизиологии, ее задачи и перспективы
30.«ДВС - синдром». Определение. Перечислить стадии.
ДВС-синдром (тромбогеморрагический синдром) - неспецифический патологический процесс, связанный с поступлением в кровь активаторов ее свертывания и агрегации тромбоцитов, образованием тромбина, активацией и последующим истощением плазменных ферментных систем (свертывающей, калликреин-кининовой, фибринолитической и др.), образованием в крови множественных микросгустков и агрегатов клеток, блокирующих микроциркуляцию в органах.
Стадии:1)Гиперкоагуляции
2)Разнонаправленных изменений – переходная (коагулопатия потребления)
3)Гипокоагуляции
4)Исход
31.ДВС-синдром. Причины и условия возникновения. (таб 4)

32.ДВС-синдром. Патогенез 1 стадии.
1 стадия - гиперкоагуляторная. характеризующаяся:
-активацией свертывания крови;
-внутрисосудистой агрегацией клеток;
-активацией других плазменных систем крови
(калликреин-кининовой, системы комплемента);
-блокадой микроциркуляции в органах.
33.ДВС-синдром. Патогенез 2 стадии.
2 стадия - коагулопатия потребления. Происходит:
-уменьшение количества тромбоцитов;
-блокада оставшихся тромбоцитов ПДФ;
-снижение содержания фибриногена;
-расход других факторов регуляции агрегантного состояния крови);
-гипокоагуляция.
34.ДВС-синдром. Патогенез 3 стадии.
3 стадия - гипокоагуляция и активация фибринолиза. Ее проявления:
-восстановление проходимости сосудов микроциркуляторного русла
(лизис микротромбов);
-при генерализации фибринолиза - повреждение факторов свертывания
и фибриногена;
-дефибринация (фибриноген коагуляционными методами не выявляется),
образование РФМК;
-геморрагический синдром.
35.ДВС-синдром. Основные проявления по стадиям.(Таб 2)

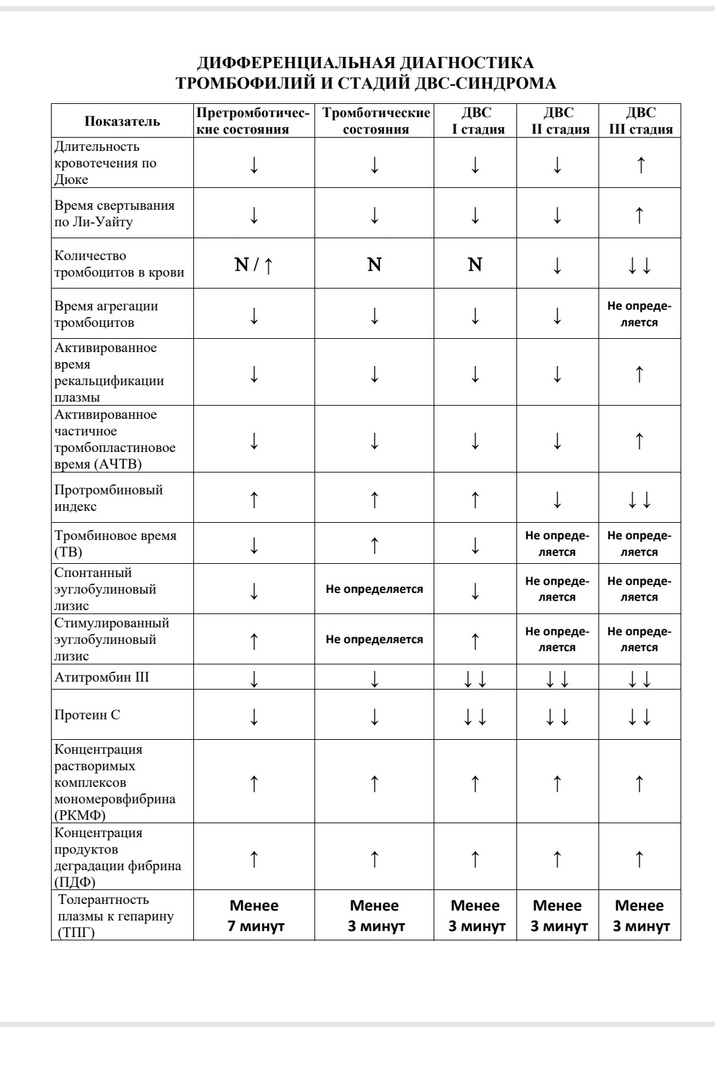
36.ДВС-синдром. Дать характеристику гемостазиограммы при 1 стадии.(Таб 6)
37.ДВС-синдром. Дать характеристику гемостазиограммы при 2 стадии.(Таб 6)
38.ДВС-синдром. Дать характеристику гемостазиограммы при 3 стадии (Таб 6)
39.ДВС - синдром. Основные принципы терапии по стадиям. (Таб 7)

40.Охарактеризовать уравнение (закон) Старлинга в патогенезе развития различных видов отека.
Согласно классической теории Э. Старлинга (1896), нарушение обмена воды между капиллярами и тканями определяется следующими факторами: 1) гидростатическим давлением крови в капиллярах и давлением межтканевой жидкости; 2) коллоидноосмотическим давлением плазмы крови и тканевой жидкости; 3) проницаемостью капиллярной стенки.
Кровь движется в капиллярах с определенной скоростью и под определенным давлением (рис. 12-45), в результате чего создаются гидростатические силы, стремящиеся вывести воду из капилляров в интерстициальное пространство. Эффект гидростатических сил будет тем больше, чем выше кровяное давление и чем меньше величина давления тканевой жидкости. Гидростатическое давление крови в артериальном конце капилляра кожи человека составляет 30-32 мм рт.ст., а в венозном конце - 8-10 мм рт.ст.
Установлено, что давление тканевой жидкости является величиной отрицательной. Она на 6-7 мм рт.ст. ниже величины атмосферного давления и, следовательно, обладая присасывающим эффектом действия, способствует переходу воды из сосудов в межтканевое пространство.
Таким образом, в артериальном конце капилляров создается эффективное гидростатическое давление (ЭГД) - разность между гидростатическим давлением крови и гидростатическим давлением межклеточной жидкости, равное
36 мм рт.ст. (30 - (-6)). В венозном конце капилляра величина ЭГД соответствует 14 мм рт.ст.
(8 - (-6)).
Удерживают воду в сосудах белки, концентрация которых в плазме крови (60-80 г/л) создает коллоидно-осмотическое давление, равное 25-28 мм рт.ст. Определенное количество белков содержится в межтканевых жидкостях. Коллоидно-осмотическое
Обмен жидкости между различными частями капилляра и тканью (по Э. Старлингу): pa - нормальный перепад гидростатического давления между артериальным (30 мм рт.ст.) и венозным (8 мм рт.ст.) концом капилляра; bc - нормальная величина онкотического давления крови (28 мм рт.ст.). Влево от точки A (участок Ab) происходит выход жидкости из капилляра в окружающие ткани, вправо от точки А (участок Ac) происходит ток жидкости из ткани в капилляр (А1 - точка равновесия). При повышении гидростатического давления (p'a') или снижении онкотического давления (b'c') точка A смещается в положение А1 и А2. В этих случаях переход жидкости из ткани в капилляр затрудняется и возникает отек
давление интерстициальной жидкости для большинства тканей составляет
5 мм рт.ст. Белки плазмы крови удерживают воду в сосудах, белки тканевой жидкости - в тканях. Эффективная онкотическая всасывающая сила (ЭОВС) - разность между величиной коллоидно-осмотического давления крови и межтканевой жидкости. Она составляет
23 мм рт. ст. (28-5). Если эта сила превышает величину эффективного гидростатического давления, то жидкость будет перемещаться из интерстициального пространства в сосуды. Если ЭОВС меньше ЭГД, обеспечивается процесс ультрафильтрации жидкости из сосуда в ткань. При выравнивании величин ЭОВС и ЭГД возникает точка равновесия А (см. рис. 12-45).
В артериальном конце капилляров (ЭГД = 36 мм рт.ст., а ЭОВС = 23 мм рт.ст.) сила фильтрации преобладает над эффективной онкотической всасывающей силой на 13 мм рт.ст. (36-23). В точке равновесия А эти силы выравниваются и составляют 23 мм рт.ст. В венозном конце капилляра ЭОВС превосходит эффективное гидростатическое давление на 9 мм рт.ст. (14 - 23 = -9), что определяет переход жидкости из межклеточного пространства в сосуд.
По Э. Старлингу, имеет место равновесие: количество жидкости, покидающей сосуд в артериальной части капилляра, должно быть равно количеству жидкости, возвращающейся в сосуд в венозном конце капилляра. Как показывают расчеты, такого равновесия не происходит: сила фильтрации в артериальном конце капилляра равна 13 мм рт.ст., а всасывающая сила в венозном конце капилляра -9 мм рт.ст. Это должно приводить к тому, что в каждую единицу времени через артериальную часть капилляра в окружающие ткани жидкости выходит больше, чем возвращается обратно. Так оно и происходит - за сутки из кровяного русла в межклеточное пространство переходит около 20 л жидкости, а обратно через сосудистую стенку возвращается только 17 л. Три литра транспортируется в общий кровоток через лимфатическую систему. Это довольно существенный механизм возврата жидкости в кровяное русло, при повреждении которого могут возникать так называемые лимфатические отеки.
41.Дать классификацию отека легкого.(Таб 6)
С учетом пусковых механизмов выделяют кардиогенный (сердечный), некардиогенный (респираторный дистресс-синдром) и смешанный отек легких. Термином некардиогенный отек легких объединяются различные случаи, не связанные с сердечно-сосудистыми заболеваниями: нефрогенный, токсический, аллергический, неврогенный и другие формы отека легких.
По варианту течения различают следующие виды отека легких:
молниеносный – развивается бурно, в течение нескольких минут; всегда заканчиваясь летальным исходом
острый – нарастает быстро, до 4-х часов; даже при немедленно начатых реанимационных мероприятиях не всегда удается избежать летального исхода. Острый отек легких обычно развивается при инфаркте миокарда, ЧМТ, анафилаксии и т. д.
подострый – имеет волнообразное течение; симптомы развиваются постепенно, то нарастая, то стихая. Такой вариант течения отека легких наблюдается при эндогенной интоксикации различного генеза (уремии, печеночной недостаточности и др.)
затяжной – развивается в период от 12 часов до нескольких суток; может протекать стерто, без характерных клинических признаков. Затяжной отек легких встречается при хронических заболеваниях легких, хронической сердечной недостаточности.
В зависимости от причин, вызвавших развитие отека легких, различают следующие его виды: 1) кардиогенный (при болезнях сердца и сосудов); 2) обусловленный парентеральным введением большого количества кровезаменителей; 3) воспалительный (при бактериальных, вирусных поражениях легких); 4) вызванный эндогенными токсическими воздействиями (при уремии, печеночной недостаточности) и экзогенными поражениями легких (вдыхание паров кислот, отравляющих веществ); 5) аллергический (например, при сывороточной болезни и других аллергических заболеваниях).
42.Охарактеризовать интерстициальный и альвеолярный отек легких.
Переход жидкости через первый барьер приводит к тому, что жидкость накапливается в интерстициальных пространствах и формируется интерстициальный отек. Когда в интерстиций поступает большое количество жидкости и поврежден альвеолярный эпителий, то жидкость проходит через второй барьер, заполняет альвеолы и формируется альвеолярный отек.
Больные с легочным отеком могут просыпаться ночью с тяжелой одышкой (пароксизмальное ночное диспноэ). При альвеолярном отеке определяются влажные хрипы и пенистая, жидкая, с кровью мокрота. При интерстициальном отеке хрипов нет. Степень гипоксемии зависит от тяжести клинического синдрома. При интерстициальном отеке более характерна гипокапния в связи с гипервентиляцией легких. В тяжелых случаях развивается гиперкапния.
43.Кардиогенный отек легких. Этиология, патогенез, проявления, исходы.
Кардиогенный отек - это патологическое состояние, которое характеризуется перфузией жидкости из легочных сосудов в интерстициальное пространство и альвеолы.

44.Нейрогенный отек легких. Этиология, патогенез, проявления, исходы.

Нейрогенный отек легких(НЕОЛ) возникает вследствие увеличения количества жидкости в интерстициальной ткани, а также ее пропитывания на поверхность альвеол. Отек обычно развивается очень быстро после повреждения центральных структур головного мозга. Эти клинические проявления трактуются, как острый респираторный дистресс-синдром, хотя патофизиологические механизмы и прогноз значительно отличаются от некардиогенного отека легких.
НЕОЛ развивается у лиц с травмами головы, когда пораженные поступают в госпитали с травмой головы. В мирное время это проблема пострадавших в транспортных авариях. При аускультации легких выявляются влажные хрипы, которые выслушиваются как в верхних, так и в нижних отделах легких. При рентгенографии выявляются застойные признаки в легких, при этом размеры сердца не изменены. Гемодинамические параметры, такие как артериальное давление, давление заклинивания, сердечный выброс – в пределах физиологической нормы. Эти признаки являются важными в проведении дифференциальной диагностики между различными формами отека легких.
Нейрогенный отек легких является довольно редким видом некардиогенного отека легких. При данной патологии вследствие нарушения иннервации сосудов дыхательной системы происходит значительный спазм вен. В дальнейшем это приводит к повышению гидростатического давления крови внутри капилляров (мельчайшие сосуды, которые участвуют вместе с альвеолами в процессе газообмена). Как следствие жидкая часть крови выходит из кровяного русла в межклеточное пространство легких, а затем попадает и в сами альвеолы (происходит отек легких).
Нейрогенные отеки. При некоторых видах отеков роль нервной системы выступает наиболее ярко и непосредственно, так как нервная система обеспечивает трофику сосудистой стенки и обменных процессов в тканях. Такие отеки называют нейрогенными. В их происхождении важную роль играют повышение проницаемости сосудистых стенок и нарушение обмена веществ в тканях с развитием метаболического ацидоза. Так, например, развиваются отеки конечностей при сирингомиелии (образование полостей в сером веществе спинного мозга) и сухотке спинного мозга (поражение задних рогов и столбов спинного мозга). Невралгия тройничного нерва нередко сопровождается развитием отека лица. К нейрогенным относятся отеки кожи при истерии, контузионные отеки и др.
45.Перечислить основные принципы терапии и профилактики отека легких.
Срочная медицинская помощь при отеке легких
Терапевтические мероприятия
|
Механизм действия
|
Прием наркотических обезболивающих медикаментов (морфин).
Морфин следует вводить по 10 миллиграмм внутривенно дробно.
|
Данные медикаменты способствуют устранению одышки и снимают психоэмоциональный стресс (уменьшают выработку адреналина и норадреналина).
Также морфин приводит к умеренному расширению вен, что приводит к уменьшению выраженности клинических симптомов отека легких.
|
Оксигенотерапия (ингаляция кислорода) с парами этилового спирта со скоростью 3 – 6 литров в минуту.
|
В значительной степени снижает гипоксию (кислородное голодание). Гипоксия крайне неблагоприятно воздействует на сосуды легких, увеличивая их проницаемость, а также увеличивая застой в малом круге кровообращения (сосуды, которые участвую в переносе крови от сердца к легким и наоборот).
Оксигенотерапия является одним из самых важных мероприятий и назначается при любом виде отека легких (при кардиогенном и некардиогенном).
|
Прием нитратов (нитроглицерин) внутрь по 1 – 2 таблетки через 3 – 5 минут.
Также возможно внутривенное введение до 25 мкг болюсно (быстрое введение всего содержимого шприца), а затем капельное введение с увеличением дозы.
|
Нитраты в определенной степени уменьшают застой венозной крови в легких, за счет расширения стенок вен. В больших дозах нитраты способны расширять и коронарные сосуды, питающие сердце.
Также данные лекарственные средства уменьшают нагрузку на миокард (мышечный слой) левого желудочка.
Необходимо заметить, что использование нитратов необходимо лишь в том случае, когда отек легких был вызван инфарктом миокарда (наиболее частая причина отека легких) и строго запрещено при гипертонической кардиомиопатии (утолщение мышечного слоя левого желудочка).
|
Прием мочегонных препаратов (фуросемид).
Медикамент вводят внутривенно в разовой дозе 40 миллиграмм.
В дальнейшем фуросемид можно ввести повторно.
|
Мочегонные медикаменты (диуретики) вызывают снижение объема циркулирующей крови. Вначале фуросемид несколько расширяет вены (вызывает венодилатацию), а затем, воздействуя на почечные канальца, оказывает мочегонное действие (усиливает выведение ионов натрия, кальция, магния и хлора).
При внутривенном использовании терапевтическое действие наблюдается уже через 10 минут, а при приеме внутрь (таблетированная форма) – в течение 30 – 60 минут.
|
Прием препаратов, блокирующих АПФ (ангиотензинпревращающий фермент).
Препараты данной группы (эналаприлат) вводятся внутривенно в разовой дозе от 1,25 до 5 миллиграмм.
|
Блокаторы АПФ в определенной степени снижают объем циркулирующей крови за счет уменьшения уровня особого фермента ангиотензина. Данный фермент не только суживает сосуды, но также и повышает выработку гормона альдостерона, который вызывает задержку жидкости в организме.
Данные лекарственные средства способны расширять артериолы (артерии мелкого калибра) и тем самым уменьшать нагрузку на левый желудочек сердца.
|
Помимо вышеперечисленных мероприятий, лечение должно быть также направлено на причину, которая вызвала отек легких.
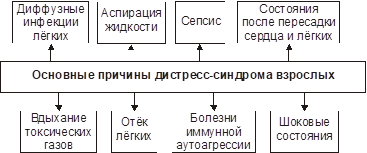
46.Дать определение понятия «Респираторный дистресс-синдром».Назвать причины и условия развития.
Респираторный дистресс-синдром взрослых («влажное лёгкое»): типовая форма патологии cистемы внешнего дыхания, характеризующаяся острой дыхательной недостаточностью, преимущественно гипоксемического типа.
(
47.Перечислить и охарактеризовать основные звенья патогенеза респираторного дистресс-синдрома.
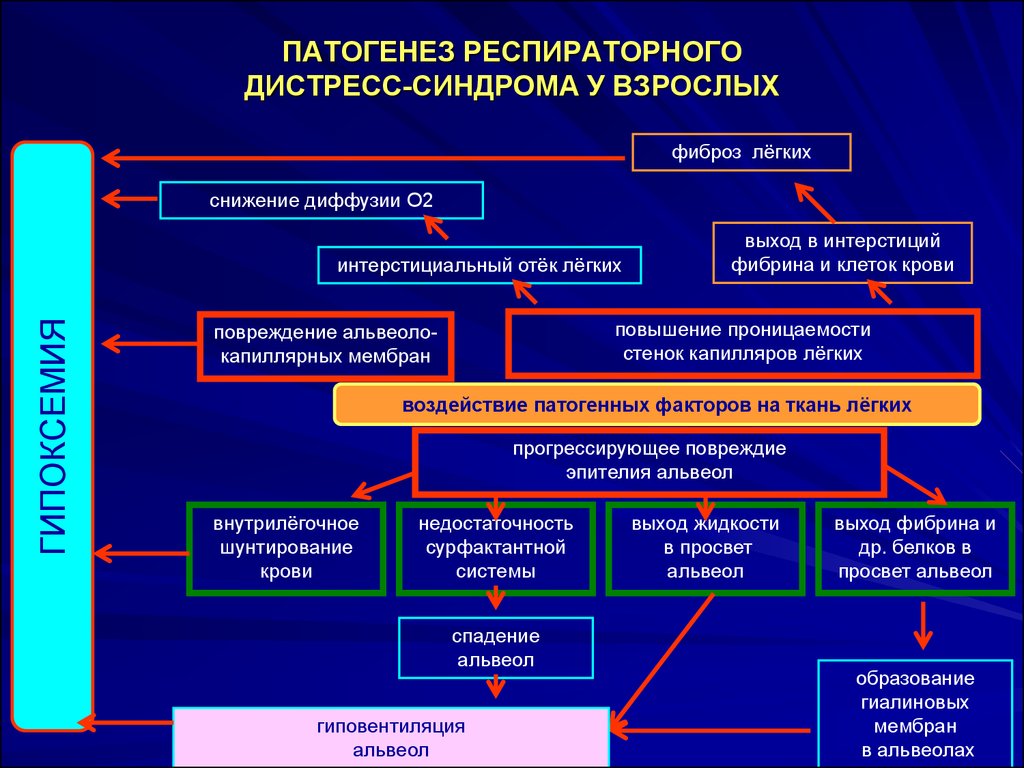
Основным звеном патогенеза РДСВ является повреждение АКМ этиологическими факторами (например, токсическими газами) и большим количеством биологически активных веществ (БАВ). К последним относятся агрессивные вещества, выделяющиеся в легких в ходе выполнения ими недыхательных функций при деструкции задержанных легкими жировых микроэмболов, тромбов из фибрина, агрегатов тромбоцитов и др. клеток, поступивших в легкие в большом количестве из различных органов при их повреждении (например, при панкреатите). Таким образом, можно считать, что возникновение и развитие РДСВ является прямым следствием перегрузки недыхательных функций легких - защитной (очистка крови и воздуха) и метаболической (участие в гемостазе). К БАВ, секретируемым различными клеточными элементами легких и нейтрофилами при РДСВ, относятся: ферменты (эластаза, коллагеназа и др.), свободные радикалы, эйкозаноиды, хемотаксические факторы, компоненты системы комплемента, кинины, ПДФ и др. В результате действия этих веществ отмечаются: бронхоспазм, спазм легочных сосудов, повышение проницаемости АКМ и увеличение внесосудистого объема воды в легких, т.е. возникновение отека легкого, усиление тромбообразования.
В патогенезе РДСВ выделяют 3 патогенетических фактора:
|
|
|
 Скачать 5.74 Mb.
Скачать 5.74 Mb.







