Лекции Лаборант школы (химия). 1 посуда лабораторная
 Скачать 1.87 Mb. Скачать 1.87 Mb.
|
Высушивание твердых веществПосле отделения твердого вещества от раствора следует стадия вы- сушивания. Высушивание – это освобождение вещества от воды или ее паров. При высушивании веществ в химической лаборатории необходимо учиты- вать их реакционную способность, стойкость к повышенной температуре, окислению, гигроскопичность и т.д. Высушивание на воздухе небольшого количества вещества проводят на часовом стекле или в чашке Петри. Для этого на чистый лист фильтро- вальной бумаги тонким слоем насыпают влажное твердое вещество. Высушивание твердых веществ на открытом воздухе при комнатной температуре используют лишь в том случае, если продукт негигроскопи- чен. Для ускорения высушивания сырое вещество можно несколько раз отжать между листами фильтровальной бумаги. Для более полного удаления влаги и для сушки гигроскопических веществ используют эксикаторы. Нижняя часть эксикатора заполнена во- допоглощающим веществом: прокаленым хлоридом кальция, концентри- рованной серной кислотой, силикагелем, гранулированным оксидом алю- мия, синтетическим цеолитом. При высушивании кристаллогидратов подбирают такой реагент, ко- торый при высушивании не отнимает кристаллизационную воду. Емкость с охлаждаемым веществом помещают на фарфоровую пла- стинку. Края эксикатора и крышки должны быть смазаны вазелином для герметичного закрывания. Открывать и закрывать надо скользящими дви- жениями крышки по краю эксикатора.  
Рис. 20. а) эксикатор без крана, б) эксикатор с краном для высущива- ния под вакуумом или в атмосфере инертного газа Так как иногда процесс сушки довольно длителен, то применяют и вакуум-эксикаторы. При этом скорость испарения влаги увеличивается. Высушивание в сушильном шкафу происходит по следующей мето- дике. Вещества, устойчивые на воздухе и не разлагающиеся при нагрева- нии, лучше всего сушить в сушильном шкафу при 60 – 80°С до постоян- ства массы, определяемой периодическим взвешиванием охлажденного в эксикаторе продукта. Сухое вещество не должно прилипать к стеклянной палочке и стенкам сосуда, а его масса должна оставаться неизменной при дальнейшем выдерживании в сушильном шкафу. Высушивание газов – освобождение газов от содержащихся в них паров воды. Для сушки газы пропускают через концентрированную сер- ную кислоту или через слой твердого осушителя, при этом осушаемый газ должен быть инертен по отношению к осушаемому веществу. Процесс вы- сушивания проводят в склянке Дрекселя или стеклянной трубке-адсорбере. Способы очистки веществ от примесейМетоды очистки веществ от примесей различны и зависят от свойств веществ и их применения. Наиболее распространенными методами очист- ки являются для твердых веществ перекристаллизация и возгонка (субли- мация), для жидкостей – фильтрование и перегонка (дистилляция), для га- зов – поглощение примесей различными веществами. Перекристаллизацияприменяется в двух основных случаях. Во- первых, многие кристаллогидраты при длительном хранении выветрива- ются (или, наоборот, расплываются), и их точный состав неизвестен. При перекристаллизации из раствора выделяются кристаллогидраты стехио- метрического состава. Во-вторых, перекристаллизацию применяют для очистки твердых растворимых в воде веществ от содержащихся в них примесей. Перед рассмотрением процесса перекристаллизации введем несколь- ко понятий. Насыщеннымпри данной температуре является раствор, находящийся в равновесии с твердой солью. В такой системе неопреде- ленно долго могут сосуществовать без каких-либо изменений раствор и избыток растворяемого вещества. Добавление к нему твердой соли не вы- зовет ее растворения. Ненасыщенным является раствор с концентрацией меньшей, чем концентрация насыщенного раствора. Если к нему добавить твердую соль, по крайней мере, часть ее растворится. Наконец, косвенным путем можно получить растворы, в которых концентрация растворенного вещества выше, чем в насыщенном растворе. Такой раствор называется пересыщенным. Подобное состояние неустой- чиво. Если к пересыщенному раствору добавить буквально один-два кри- сталлика растворенного вещества, мельчайшие кусочки стекла и т.п., они сыграют роль центров кристаллизации и начнется интенсивное выпадение кристаллов из раствора – до тех пор, пока концентрация его не станет рав- ной концентрации насыщенного раствора. Иногда для снятия пересыще- ния достаточно встряхнуть стакан с раствором. Метод перекристаллизации основан на различной растворимости вещества в данном растворителе в зависимости от температуры. Под рас- творимостью понимают содержание растворенного вещества в насыщен- ном растворе. Растворимость обычно выражается в граммах растворенного вещества на 100 граммов растворителя или 100 мл растворителя (для воды эти величины совпадают). Встречается и другой способ выражения рас- творимости – в граммах на 100 грамм раствора. Поэтому при работе со справочной литературой следует обратить внимание на то, каким спосо- бом выражена растворимость. Зависимость растворимости веществ от температуры выражается кривыми растворимости. Принцип перекристаллизации состоит в получении насыщенного при высокой температуре раствора данного вещества. С понижением тем- пературы растворимость большинства веществ уменьшается, поэтому при охлаждении горячего насыщенного раствора часть вещества будет выде- ляться из раствора в виде, как правило, хорошо оформленных кристаллов. Если раствор охлаждать медленно, выпадают крупные кристаллы, если быстро – мелкие. Нерастворимые примеси отделяются на первой стадии – при раство- рении основного вещества, а растворимые – на второй: при кристаллиза- ции основного вещества они остаются в растворе. Однако незначительное количество примесей при кристаллизации захватывается основным веще- ством за счет адсорбции, поэтому перекристаллизацию повторяют иногда несколько раз. Процесс перекристаллизации состоит из нескольких этапов: приго- товление насыщенного раствора, фильтрование горячего раствора, охла- ждение, кристаллизация, отделение кристаллов от маточного раствора. Перекристаллизацию проводят по следующей схеме: Основываясь на данных по растворимости, рассчитывают тео- ретический процент потерь при перекристаллизации, на основании этого - необходимую навеску вещества и объем воды. Необходимо взять прибли- зительно 20% избыток вещества и растворителя по отношению к необхо- димому. Растворяют вещество при нагревании в дистиллированной во- де или в подходящем органическом растворителе при определенной тем- пературе. В горячий растворитель небольшими порциями вводят кристал- лическое вещество до тех пор, пока оно перестанет растворяться, то есть образуется насыщенный при данной температуре раствор. Горячий раствор отфильтровывают на воронке для горячего фильтрования. Охлаждают полученный маточный раствор сначала до комнат- ной температуры, а затем до 0°С в охлаждающей смеси. Выпавшие кристаллы переносят на воронку Бюхнера и промы- вают холодным маточным раствором (если вещество плохо растворяется в воде, можно дополнительно промыть его холодной дистиллированной во- дой). В зависимости от свойств перекристаллизуемого вещества, его высушивают на воздухе, между листами фильтровальной бумаги или в электрическом сушильном шкафу. Взвешивают полученное вещество, рассчитывают процент по- терь по отношению к массе взятого вещества и с учетом растворимости вещества в воде при 0°С При перекристаллизации веществ, растворимость которых мало из- меняется с изменением температуры, применяют метод высаливания. К растворам таких веществ добавляют вещества, понижающие их растворимость. Растворимость электролита уменьшается при введении в раствор другого электролита с одноименным ионом. Например, при вве- дении ионов хлора Cl в насыщенный раствор хлорида натрия NaС1(р) рав- новесие смещается влево, в результате чего выпадают кристаллы соли, не содержащие примесей. Возгонка(илисублимация)– это процесс превращения твердого вещества в газообразное (без стадии плавления, минуя жидкое состояние) и последующей кристаллизации образовавшихся паров на охлаждаемой поверхности. Возгонкой пользуются тогда, когда основное вещество обладает, а примеси не обладают свойством возгоняться. Возгонкой можно очистить йод, хлорид аммония, серу, нафталин и др. От перекристаллизации возгонка отличается более высоким выхо- дом чистого продукта и происходит при более низкой температуре, чем температура плавления вещества. Ее применяют тогда, когда нельзя очи- стить вещество перекристаллизацией, так как оно разлагается при темпе- ратуре плавления. Возгоняемое вещество нагревают. Достигнув темпера- туры возгонки, твердое вещество без плавления переходит в пар, который конденсируется в кристаллы на поверхности охлажденных предметов. На рисунке 21 представлен опыт, позволяющий наблюдать возгонку иода. Слева - при нагревании иод возгоняется, оседая в виде блестящих тонких пластинок. Справа – в охлаждаемой части прибора для возгонки иод конденсируется с образованием кристаллов. Возгонка служит для очистки иода в лабораториях и в промышленности  Рис. 21. Возгонка иода Возгонка – достаточно длительный процесс, поэтому данный метод используют для очистки небольших количеств веществ. Область примене- ния данного метода ограничена тем, что не все твердые вещества способ- ны сублимироваться. Фильтрование заключается в пропускании суспензии через пори- стую перегородку – фильтр, задерживающий твердые частицы. Фильтром может служить специальная бумага, ткань, пористая керамика, пористое стекло, слой песка и другие пористые материалы. При обычных условиях фильтрование идет медленно. Для ускорения его проводят под вакуумом: в приемнике для жидкости с помощью насоса создают разрежение, вслед- ствие чего на жидкость над фильтром начинает действовать атмосферное давление, и чем больше разность давлений (атмосферного и в приемнике), тем быстрее идет фильтрование. Перегонка (или дистилляция) применяется для очистки жидкостей от растворенных примесей, а также для разделения жидких веществ с раз- личной температурой кипения. Перегонка основана на превращении жид- кости в пар с последующей конденсацией пара в жидкость. По сравнению с перекристаллизацией перегонка при меньших затратах времени дает, как правило, больший выход чистого продукта. Перегонкой пользуются тогда, когда перегоняемые вещества при нагревании не претерпевают каких-либо изменений или когда очищаемые жидкости имеют определенную разницу температур, но не слишком высокую температуру кипения. Различают три способа перегонки жидкостей: а) при атмосферном давлении (простая перегонка); б) при уменьшенном давлении (вакуум-перегонка); в) перегонка с водяным паром. 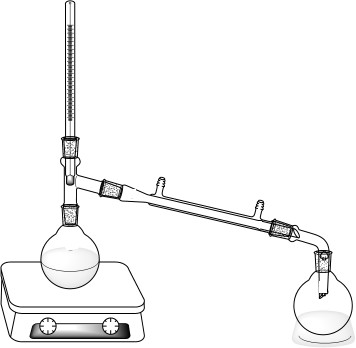 Простая перегонка применяется тогда, когда надо отделить целевой продукт от практически нелетучих примесей. Например, очистка воды от нелетучих солей. Для этого собирают традиционную установку, состоя- щую из перегонной колбы (колбы Вюрца), прямого холодильника и при- емника (рис. 22). Простая перегонка применяется тогда, когда надо отделить целевой продукт от практически нелетучих примесей. Например, очистка воды от нелетучих солей. Для этого собирают традиционную установку, состоя- щую из перегонной колбы (колбы Вюрца), прямого холодильника и при- емника (рис. 22).Рис. 22. Установка для простой перегонки жидкостей Перегонную колбу заполняют перегоняемой жидкостью не более чем на 2/3 ее объема, но и не менее чем на 1/2 объема колбы. Когда весь при- бор собран, тщательно проверяют, хорошо ли подобраны пробки, правиль- но ли установлен термометр. Включают воду для охлаждения холодильни- ка. Подставляют приемник для сбора перегоняемой жидкости и начинают нагревать раствор до кипения. Колбу нагревают на водяной (песчаной или масляной) бане, реже на пламени горелки через асбестовую сетку. Темпе- ратуру паров отгоняемого вещества измеряют термометром, установлен- ным на 1 см ниже отводной трубки колбы Вюрца. Для предотвращения внезапного вскипания перегоняемой жидкости и попадания ее в холодиль- ник в колбу кладут длинные капилляры, запаянные с одного конца или не- большие кусочки фарфора (кипелки). Перегонку при низком давлении (вакуум-перегонку) применяют, ес- ли жидкость, подлежащая перегонке в обычных условиях, не выдерживает нагревания до температуры ее кипения. Установка для такой перегонки более сложная. Для отгонки веществ, нерастворимых в воде, используют перегонку с водяным паром (рис. 23).  Рис. 23. Установка для перегонки жидкостей с водяным паром 1 – колба с водой, 2 – электроплитки, 3 – баня, 4 – перегонная колба, 5 – каплеуловитель, 6 – нисходящий холодильник, 7 - приемник |
