рад гигиена. 1. Радиационная гигиена как наука и область практической деятельности врачей. Применение радиоактивных веществ и источников ионизирующего излучения (ИИ) в современных условиях.
 Скачать 3.83 Mb. Скачать 3.83 Mb.
|
Роль свободных радикалов в развитии патологических процессовСвободные радикалы отличаются от обычных молекул тем, что у них на внешней электронной оболочке имеется неспаренный (одиночный) электрон. Это делает их химически активными, поскольку они стремятся вернуть себе недостающий электрон, отняв его от окружающих молекул и тем самым повреждая их. Свободные радикалы вступают в реакции с неорганическими и органическими соединениями - белками, липидами, углеводами, нуклеиновыми кислотами, инициируют аутокаталитические реакции, в ходе которых молекулы, с которыми они реагируют, также превращаются в свободные радикалы. Таким образом, свободные радикалы - высокоактивные молекулы, способные разрушать структуры клетки. Повреждающее действие пероксидации липидовПерекисное окисление липидов (ПОЛ) — это разветвленная цепная реакция, идущая с участием активных форм кислорода (свободных радикалов): участвует в обновлении клеточных мембран (регуляции липидного состава мембран); влияет на активность мембраносвязанных ферментов; участвует в синтезе простагландинов, лейкотриенов; участвует в процессах эндоцитоза, фагоцитоза; играет существенную роль в патогенезе опухолей, атеросклероза, ишемических повреждений сердца, мозга, почек, в развитии стресса ═> «свободно-радикальные болезни». Основными мишенями ПОЛ в мембранных структурах клеток являются либо белковые структуры, либо липидный бислой в целом. 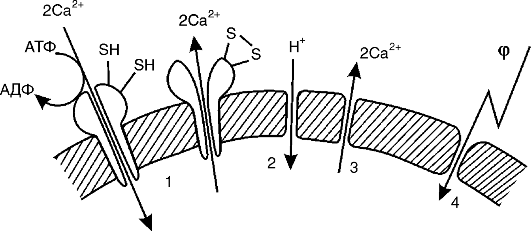 Рис. 2. Повреждающее действие перекисного окисления липидов на биологические мембраны (по В.В. Новицкому и соавт., 2009) Наиболее чувствительны к перекисному окислению липидов сульфгидрильные, или тиоловые, группы (SH) мембранных белков: ферментов, ионных каналов и насосов. В ходе окисления тиоловых групп образуются радикалы (S), которые затем либо взаимодействуют друг с другом с образованием дисульфидов (SS), либо связываются с кислородом с образованием сульфитов и сульфатов (SO3 и SO4). Большую роль в патологии клетки играет также повреждение ионтранспортирующих ферментов (например, Ca2+, Мg2+-АТФазы), в активный центр которых входят тиоловые группы. Инактивация Са2+-АТФазы приводит к замедлению откачивания из клетки ионов кальция и ускорению их «протечки» в клетку (где их концентрация меньше). Это вызывает рост уровня ионов кальция в цитоплазме и повреждение клеточных структур. Окисление тиоловых групп мембранных белков приводит к появлению дефектов в мембранах клеток и митохондрий. Под действием электрического поля через такие дефекты в клетки входят ионы натрия, а в митохондрии — ионы калия. В результате происходит увеличение осмотического давления внутри клеток и митохондрий и их набухание. Это приводит к еще большему повреждению мембранных структур. Наряду с белками и нуклеиновыми кислотами мишенью повреждающего действия ПОЛ служит сам липидный бислой. Было показано, что продукты ПОЛ делают липидную фазу мембран проницаемой для ионов водорода и кальция. Это приводит к тому, что в митохондриях окисление и фосфорилирование разобщаются, и клетка оказывается в условиях энергетического голода. Одновременно из митохондрий в цитоплазму выходят ионы кальция, которые повреждают клеточные структуры. Возможно, наиболее важный результат пероксидации — это уменьшение электрической стабильности липидного слоя, которое приводит к электрическому пробою мембраны собственным мембранным потенциалом. Электрический пробой вызывает полную потерю мембраной ее барьерных функций. 6. биологические стадии воздействия ии. Повреждения функции клеток. Нарушение генома соматический и половых клеток. Понятие о радиционных мутациях. I. Физическая стадия. В течение очень короткого промежутка времени (в пределах 10- 13 секунды) происходит поглощение энергии ионизирующих излучений биомолекулами и компонентами окружающей их среды (молекулами воды и других веществ). В результате возникают возбужденные и ионизированные атомы и молекулы. II. Физико-химическая стадия. Вследствие возбуждения и ионизации молекул в них происходят внутренние перестройки за счет миграции энергии и заряда внутри молекулы или между молекулами. Возникают первично поврежденные биомолекулы и продукты их деградации – ионы и химические радикалы. Примерно 50% всех возникающих радикалов образуются из молекул воды, составляющих около 70% массы живых организмов. 4 III. Химическая стадия. Ионы и химически активные радикалы по месту их образования и на некотором удалении от него (в среднем 300-350 нм) атакуют биомолекулы, повреждая их. Это происходит также в течение короткого промежутка времени (10-10 -10-6 секунды). В результате возникают вторично (химически) поврежденные биомолекулы. IV. Биологическая стадия. Сроки формирования этой стадии находятся в широких пределах – от 10-6 секунды до многих лет. В основе развивающихся в этот период процессов лежат изменения внутриклеточного (межуточного) обмена веществ. В зависимости от полученной дозы ионизирующих излучений внутриклеточный обмен веществ нарушается в различной степени – от небольших сдвигов с последующим восстановлением до полного и стойкого срыва, приводящего к гибели клетки Репродуктивная гибель клеток характерна для всех быстропролиферирующих тканей, она наступает не сразу после облучения, а в ходе нескольких циклов деления. Основной причиной репродуктивной гибели являются структурные повреждения ДНК. Интерфазная гибель клетки наступает до вступления клетки в митоз. Для большинства клеток соматических тканей животных и человека интерфазная гибель регистрируется при облучении в высоких дозах, проявляется в виде различных дегенеративных изменений ядра и цитоплазмы и происходит или непосредственно «под лучом», или в первые часы после облучения. Исключением являются лимфоциты, для которых интерфазный тип постлучевой гибели является основным и регистрируется уже после облучения в дозах 1-2 Гр. Радиоционная мутация- .возникновение наследуемых изменений (мутаций) у организмов в результате их облучения 7.понятие о радиочувствительности. Факторы, определяющие радиочувствительность к воздействию повешенных доз ИИ. Понятие радиоустойчивости (радиорезистентности) – подразумевает способность организма выжить при облучении в определенных дозах или проявить ту или иную реакцию на облучение. наиболее чувствительные к ионизирующему излучению ткани содержат клетки: Находящиеся в момент облучения в процессе активного деления. Проходящие многие трансформации в своем жизненном цикле. Не имеющие четкой специализации по своей структуре и функциям. На радиочувствительность существенное влияние оказывает и кислородный эффект. Клетки с нормальным содержанием кислорода значительно чувствительней к действию редкоионизирующего излучения, чем находящиеся в состоянии гипоксии Температура также влияет на радиочувствительность. Понижение температуры тела способно повысить сопротивляемость организма к действию ионизирующего излучения. В некоторых случаях это ведет лишь к отсроченности наступления радиационных последствий. Относительная биологическая эффективность излучений, показатель, с помощью которого определяют, во сколько раз биологическое действие ионизирующих излучений данного типа (например, альфа-, бета-лучи, нейтроны и т.д.) больше (или меньше) действия на тот же биологический объект стандартного излучения (жесткие рентгеновские или гамма-лучи). О. б. э. вычисляют (при линейной зависимости изучаемого эффекта от дозы обоих сравниваемых типов ионизирующих излучений) как отношение угла наклона дозовой прямой тестируемого излучения к углу наклона аналогичной прямой стандартного излучения; при иной дозовой зависимости — как отношение изоэффективных (обусловливающих одинаковый эффект) доз стандартного и тестируемого излучений. Во втором случае О. б. э. может меняться с дозой облучения и величиной наблюдаемого эффекта, поэтому нужно указывать, для какого уровня эффекта вычислено значение О. б. э. Например, если О. б. э. нейтронов по сравнению с гамма-лучами при ЛД50/30 для мышей равна 2, то это означает, что в отношении гибели половины мышей в течение 30 сут после облучения нейтроны вдвое эффективнее гамма-лучей. Зависимость О. б. э. от дозы может быть различной. О. б. э. излучений зависит главным образом от различий в пространственном распределении поглощённой энергии в облучаемом биосубстрате, измеряемых линейными потерями энергии (ЛПЭ) на единицу длины пробега ионизирующей частицы. Зависимость О. б. э. от ЛПЭ варьирует у разных объектов и в разных биологических реакциях на облучение. Эффективность излучений с низкими ЛПЭ обычно сходна. С возрастанием ЛПЭ О. б. э. обычно также возрастает. Коэффициент О. б. э. для электронного, позитронного, рентгеновского и гамма-излучения, а также для быстрых протонов, как правило, близок к 1; для альфа-частиц и быстрых нейтронов возрастает до 10, для тяжёлых многозарядных ионов и ядер отдачи — до 20. 8 Основные реакции организма на действия ионизирующего излучения. Стохастический эффект - виды особенности. Коллективная эффективная доза. Вероятность возниконовениястохастичесих эффектов в популяции в зависимости от КЭД. Различают два вида радиобиологических эффектов: детерминированные (нестохастические) и стохастические. 1. Детерминированные - клинически выявляемые вредные биологические эффекты, вызванные ионизирующими излучениями, в отношении которых предполагается существование порога, ниже которого эффект отсутствует, а выше – тяжесть эффекта зависит от полученной дозы. Клиническая медицина к таким эффектам относит: лучевую болезнь, лучевой дерматит, лучевую катаракту, лучевое бесплодие, аномалии в развитии плода и др. 2. Стохастические радиобиологические эффекты – вредные биологические эффекты, вызванные ионизирующими излучениями, не имеющие дозового порога возникновения и для которых тяжесть проявления не зависит от дозы. Клинически беспороговые эффекты диагностируются как злокачественные опухоли, лейкозы, а также наследственные болезни. Стохастические радиобиологические эффекты разделяют на соматические и наследственные. Соматические эффекты проявляются у самого облученного лица, а наследственные – у его потомков. Основным отдаленным соматическим эффектом является повышенная частота развития у облученного населения раковых заболеваний, появление которых будет происходить в течение нескольких десятилетий (первые 50 лет) после облучения. Наследственные эффекты появляются вследствие облучения гонад у лиц репродуктивного возраста. коллективная эффективная доза мера коллективного риска возникновения стохастических эффектов облучения; она равна сумме индивидуальных эффективных доз. Единица эффективной коллективной дозы — человеко-зиверт Номинальные коэффициенты вероятности стохастических эффектов [5]
9. Детерминированные эффекты: особенности и основные виды. Острые и отдаленные радиационные поражения. Различают два вида радиобиологических эффектов: детерминированные (нестохастические) и стохастические. Детерминированные - клинически выявляемые вредные биологические эффекты, вызванные ионизирующими излучениями, в отношении которых предполагается существование порога, ниже которого эффект отсутствует, а выше – тяжесть эффекта зависит от полученной дозы. Клиническая медицина к таким эффектам относит: лучевую болезнь, лучевой дерматит, лучевую катаракту, лучевое бесплодие, аномалии в развитии плода и др. При воздействии ИИ на биосубстрат происходит поглощение последним энергии излучения. Это приводит к ионизации атомов и молекул (то есть, потере атомом электрона, оставшаяся часть атома приобретает положительный заряд) или к возбуждению атомов, молекул (переход электрона на более высокий энергетический уровень в пределах атома). Образовавшиеся в результате ионизации атомов ионы и свободные электроны взаимодействуют между собой и с окружающими неповрежденными атомами и молекулами, образуя при этом свободные радикалы. Острая лучевая болезнь – полисиндромное заболевание, развивающееся после однократного непродолжительного воздействия внешнего гамма-нейтронного и рентгеновского облучения в дозе, превышающей 1 Гр, при условии относительно равномерного облучения всего тела. I. По степени тяжести (степень тяжести ОЛБ определяется поглощенной дозой ионизирующих излучений): А) Формы ОЛБ: 1. Костно-мозговая - при поглощенной дозе от 1 до 10 Гр. 2. Кишечная – при поглощенной дозе 10-20 Гр. 3. Токсемическая – при поглощенной дозе 20-80 Гр. 4. Церебральная – при поглощенной дозе свыше 80 Гр. Б) Степени тяжести костно-мозговой формы ОЛБ: I (легкая) – при поглощенной дозе 1-2 Гр. II (средняя) – при поглощенной дозе 2-4 Гр. III (тяжелая) – при поглощенной дозе 4-6 Гр. IV (крайне тяжелая) – при поглощенной дозе 6-10 Гр. II. Периоды течения: 1) начальный – период общей первичной реакции; 2) скрытый – период относительного, или мнимого, благополучия; 3) период разгара – период выраженных клинических проявлений; 4) период восстановления; 5) период исходов и последствий. Основные синдромы острой лучевой болезни 1. Гематологический (панцитопенический) – уменьшение числа клеток в периферической крови вследствие нарушения их продукции. Главную роль в развитии данного синдрома играет поражение стволовой клетки, которые сосредоточены главным образом в органах кроветворения и лишь небольшое их количество циркулирует в периферической крови, а также повреждение созревающих клеток (миелобластов, промиелоцитов, миелоцитов). 2. Геморрагический синдром. Причина: тромбоцитопения, фибринолиз, повышение проницаемости сосудистой стенки. 3. Гастроинтестинальный синдром. Проявляется неукротимой рвотой, поносом, вначале каловым, затем слизисто-кровянистым, нарушением моторики органов ЖКТ, развитием таких осложнений, как паралитическое расширение желудка, динамическая кишечная непроходимость, перфорация. 4. Синдром инфекционных осложнений. Развиваются оро-фарингеальный синдром (язвенно-некротический гингивит, стоматит, глоссит, тонзиллит), пневмонии, эндокардит, герпес, грибковые поражения. 5. Синдром функционального и органического поражения ЦНС: - астенический синдром; - вегетативные расстройства; - церебралгия; - двигательные нарушения, атаксия, дискоординация; - судорожный синдром, гиперкинезы; 6. Эндогенная токсемия вследствие продуктов радиолиза, деструкции радиочувствительных тканей, септикотоксемии. Проявляется тошнотой, рвотой, тахикардией, сухостью слизистых, мышечной слабостью, головной и мышечными болями. 7. Дистрофический синдром при острой лучевой болезни характеризуется развитием выраженной кахексии. Масса тела уменьшается на 10-20%. 8. Эндокринные расстройства: - гиперкортицизм вследствие повышенной выработки АКТГ; - снижение секреции СТГ способствует гибели лимфоидных клеток, угнетению клеточной пролиферации; - повышение выработки тиреотропного гормона; - угнетение сперматогенеза, нарушение менструального цикла. Особенности острой лучевой болезни при внешнем неравномерном облучении В боевой обстановке лучевые поражения будут неравномерными из-за прикрытия в момент облучения отдельных участков тела элементами сооружений, боевой техники, вооружения и т.п. При преимущественном облучении головы и шеи характерны выраженная первичная реакция: фонтанирующая рвота, сильная головная боль, гиперемия и отек лица (при дозе 4-5 Гр.), в дальнейшем происходит эпиляция бровей и ресниц. При дозе облучения свыше 10 Гр возникает отек головного мозга с неврологическими проявлениями, оро-фарингеальный синдром. В периферической крови и стернальном пунктате отчетливых признаков угнетения кроветворения, как правило, не обнаруживается. При преимущественном облучении грудного сегмента первичная лучевая реакция минимальная. Характерны в первые двое суток неприятные ощущения в области сердца вплоть до ангинозных болей, различные нарушения ритма сердца и соответствующие изменения на ЭКГ. В стернальном пунктате – угнетение кроветворения, а в периферической крови – изменений мало. Эта характерная для случаев облучения грудной клетки диссоциация в показателях стернального пунктата и периферической крови объясняется усилением кроветворения в других отделах костномозговой ткани. При преимущественном облучении брюшного сегмента вследствие наличия большой рефлекторной зоны характерны выраженная первичная реакция и симптомы поражения органов брюшной полости, отличающихся наибольшей радиопоражаемостью (радиационный гастрит, колит, энтерит). Определяются значительные изменения почек и мочевого пузыря. Картина крови изменяется незначительно, опустошение костного мозга наблюдается только в тех костях, которые подверглись облучению. В связи с этим при неравномерном облучении для объективной оценки функции кроветворения необходимо исследовать костномозговой пунктат из разных костей (грудина, гребешок подвздошной кости, пяточная кость и др.).  | |||||||||||||||||||
