Химия (расчет ионной силы раствора). 1. Расчет ионной силы раствора
 Скачать 0.98 Mb. Скачать 0.98 Mb.
|
3.3. Растворимость в многокомпонентной системе с индифферентным электролитомВ этом случае расчет растворимости сводится к влиянию ионной силы раствора на растворимость трудно растворимого соединения. Ионную силу раствора следует вычислять, ориентируясь на соотношение концентраций в растворе трудно растворимой соли и соли, содержащей одноименный ион. Если разница между ними не велика, то в уравнении ионной силы следует учитывать все ионные компоненты раствора. Если концентрация электролита, содержащего одноименный ион, в 10 и более раз превышает растворимость осадка, то значением растворимости при расчете ионной силы раствора можно пренебречь. Пример 23Рассчитать растворимость Ag2SO4 в растворе нитрата натрия, концентрацией 0,1 моль/кг, если его растворимость в воде составляет 0,0228 моль/кг. Решение. 1. Вычислить ионную силу раствора, содержащего сульфат серебра и нитрат натрия 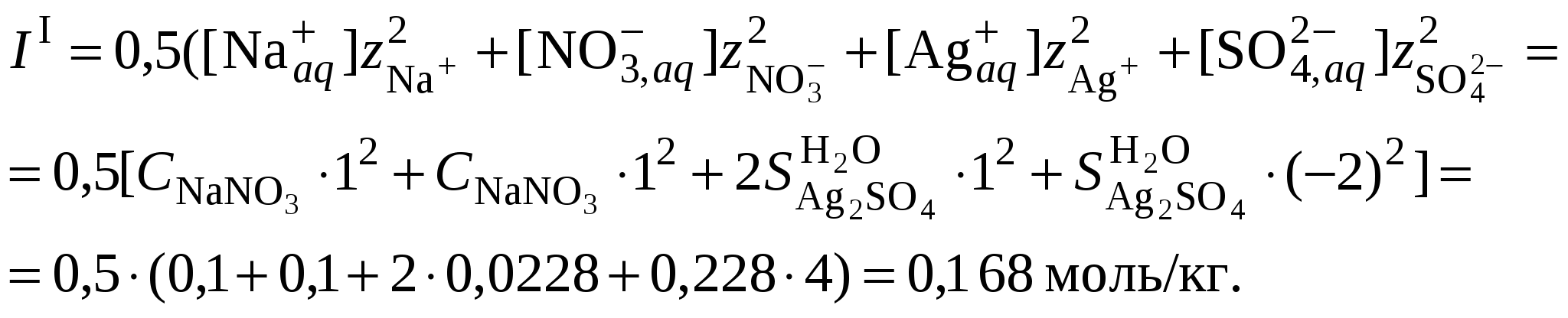 2. Вычислить средний ионный коэффициент активности сульфата серебра 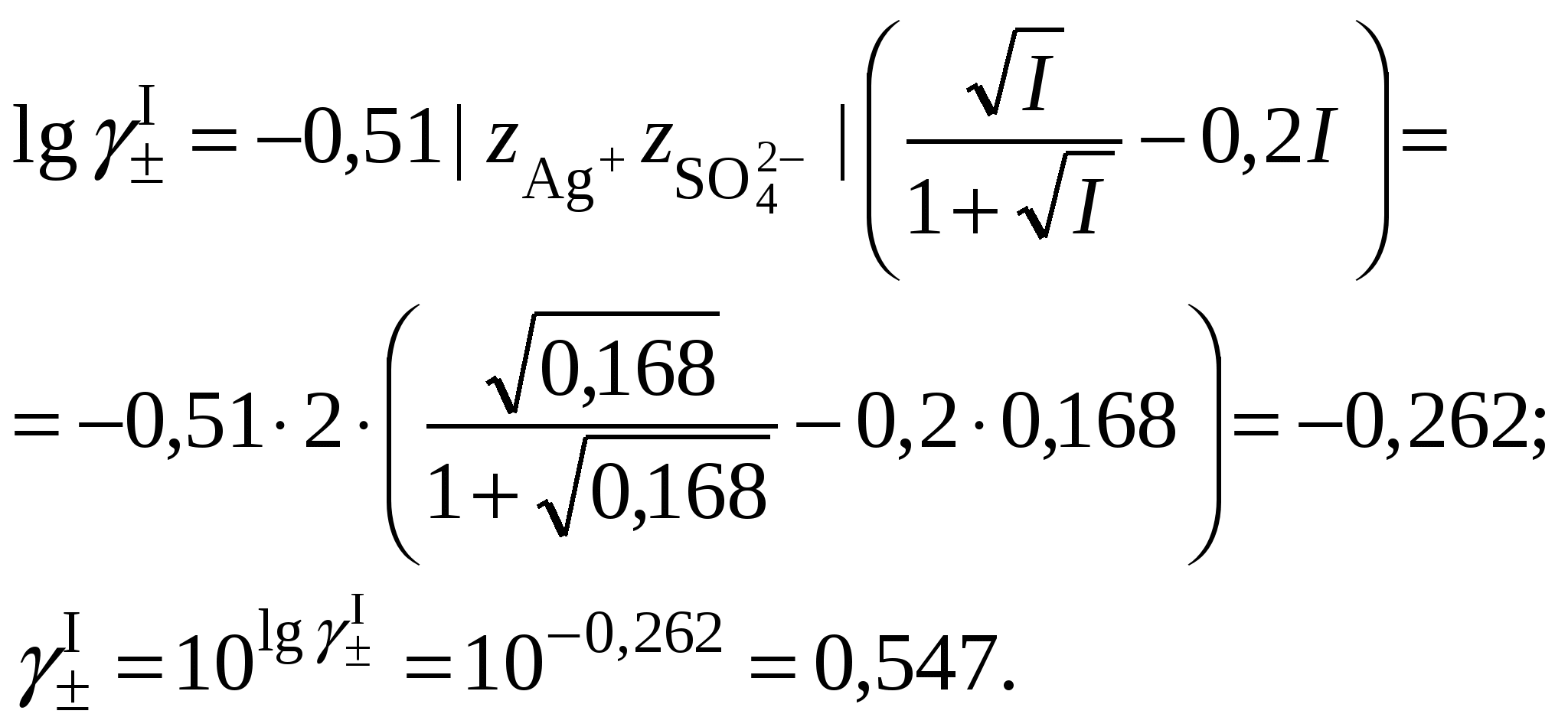 3. Вычислить растворимость сульфата серебра в присутствии нитрата натрия 4. Пересчитать ионную силу раствора с учетом растворимости сульфата серебра, вычисленной в п. 3 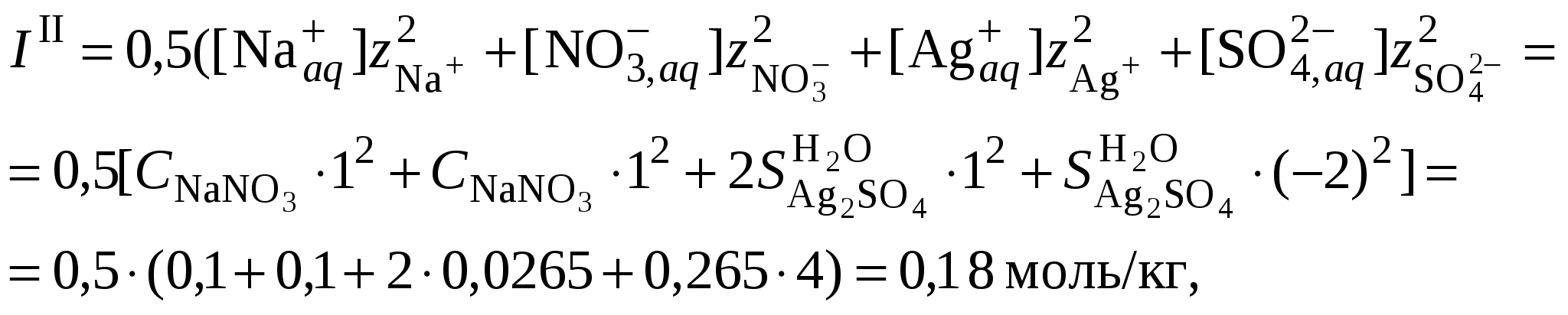 средний ионный коэффициент активности сульфата серебра 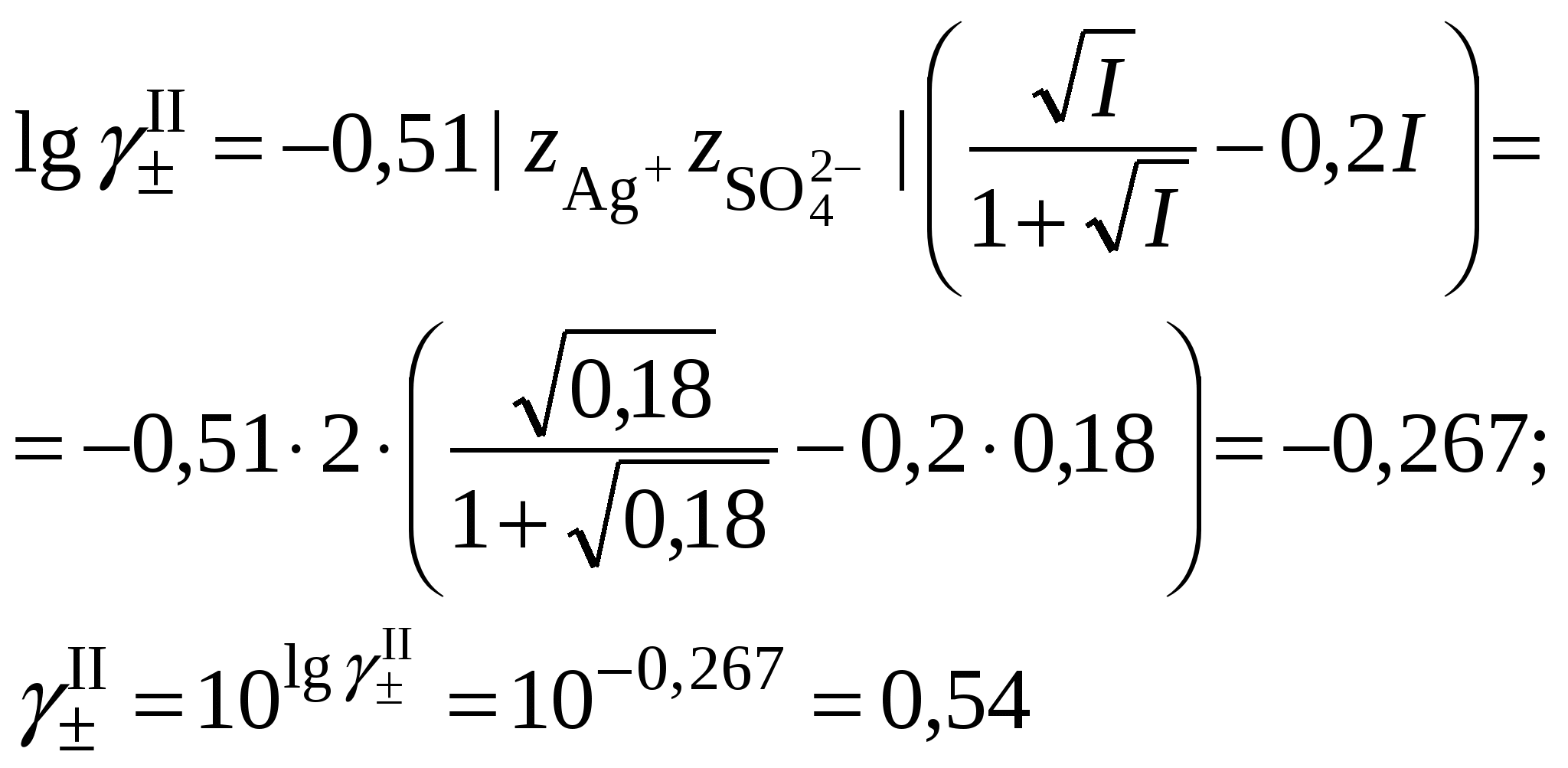 и растворимость сульфата серебра в присутствии нитрата натрия 5. 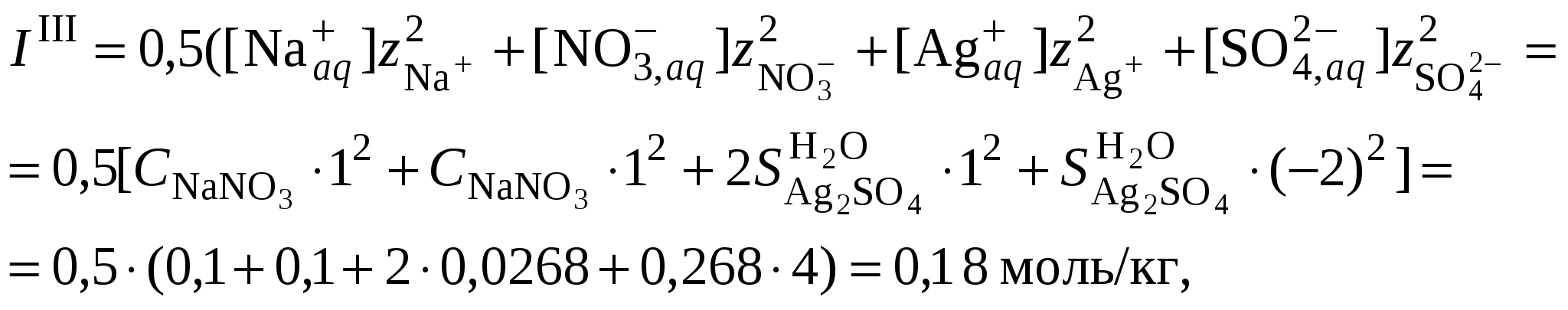 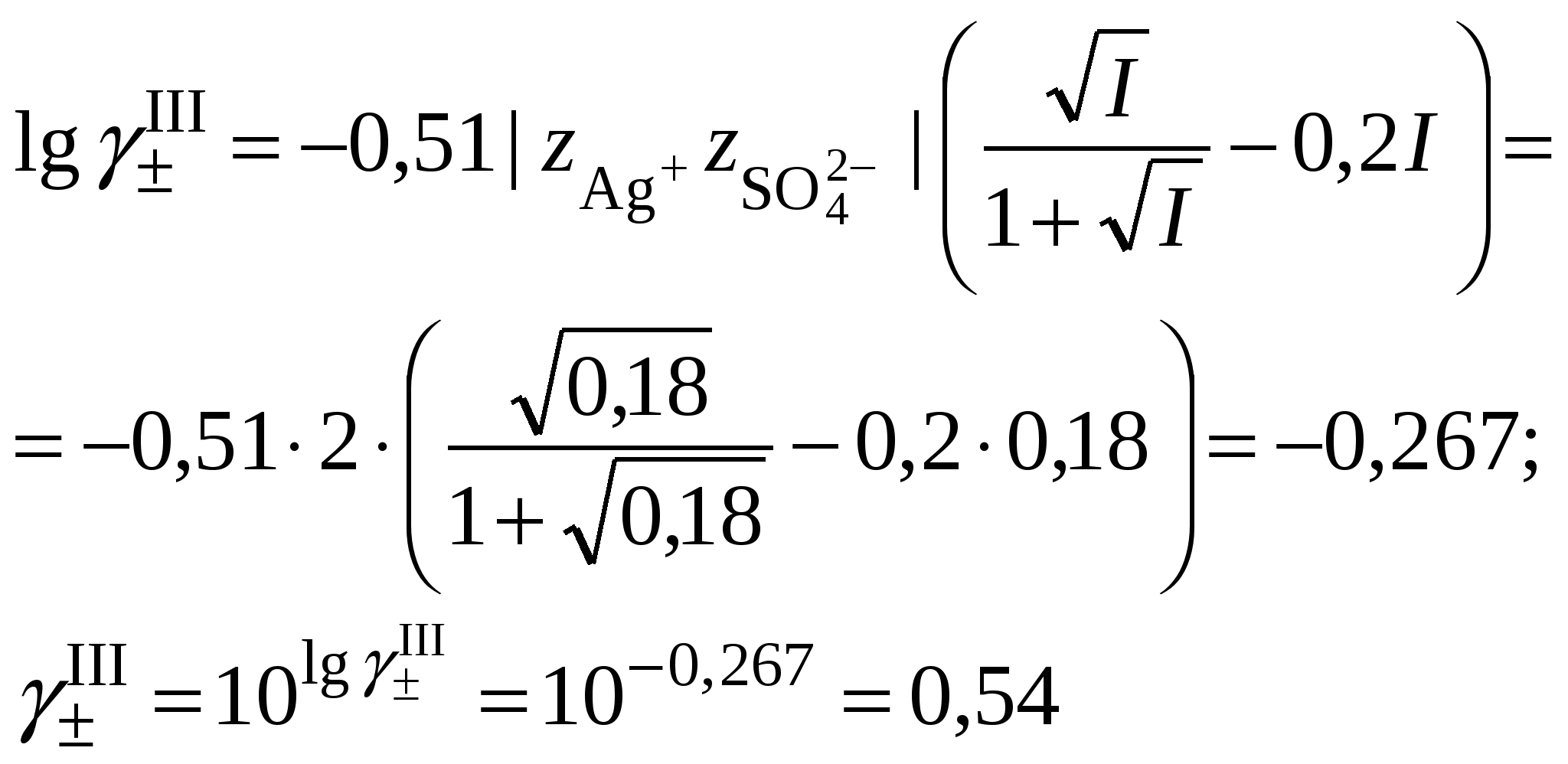 6. Полученное значение растворимости сульфата серебра в присутствии постороннего электролита превышает найденное для бинарной системы сульфат серебра – вода (0,0228 моль/кг). При повышении ионной силы раствора растворимость малорастворимого соединения должна увеличиваться, что согласуется с полученными расчетными данными. Пример 24.Вычислить растворимость сульфата бария (L = 10–10) в растворе хлорида кальция концентрацией 0,1 моль/кг. Решение. 1. Составить уравнение растворимости сульфата бария его произведение растворимости и вычислить ориентировочное значение растворимости сульфата бария в воде 2. Вычислить ионную силу раствора, содержащего сульфат бария и хлорид кальция. Очевидно, что ионная сила раствора будет определяться только концентрацией индифферентного электролита 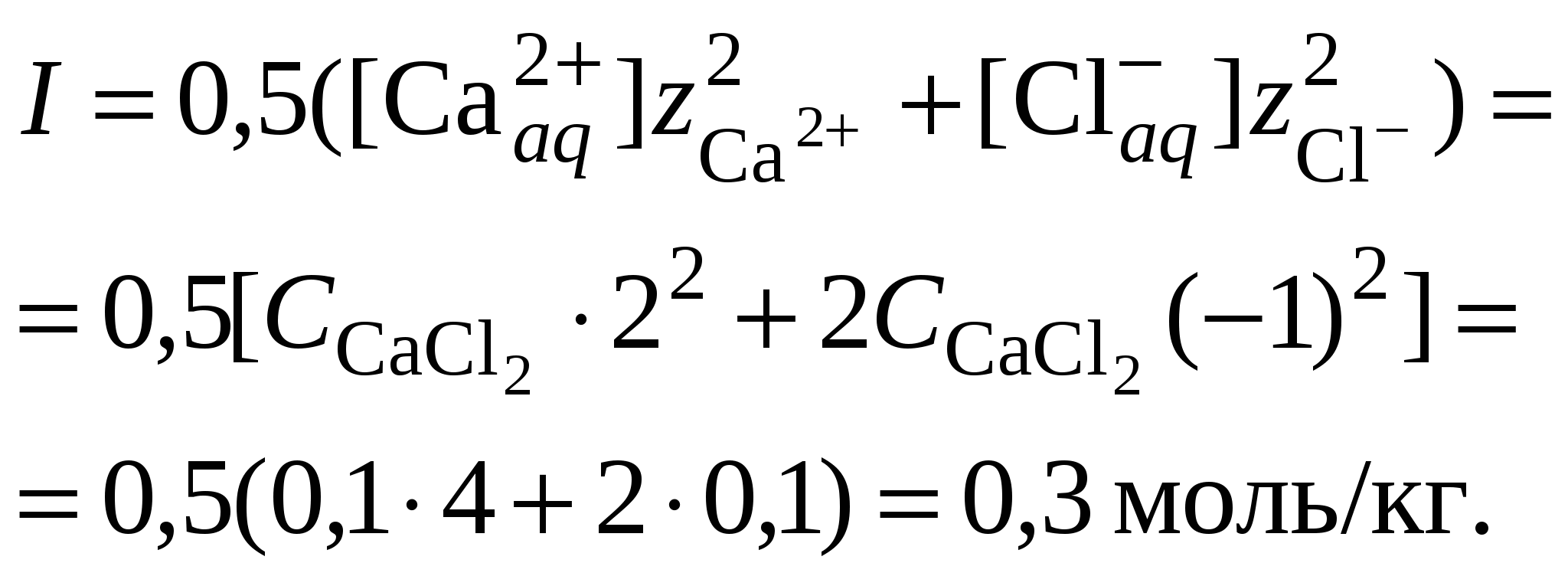 3. Вычислить средний ионный коэффициент активности сульфата бария 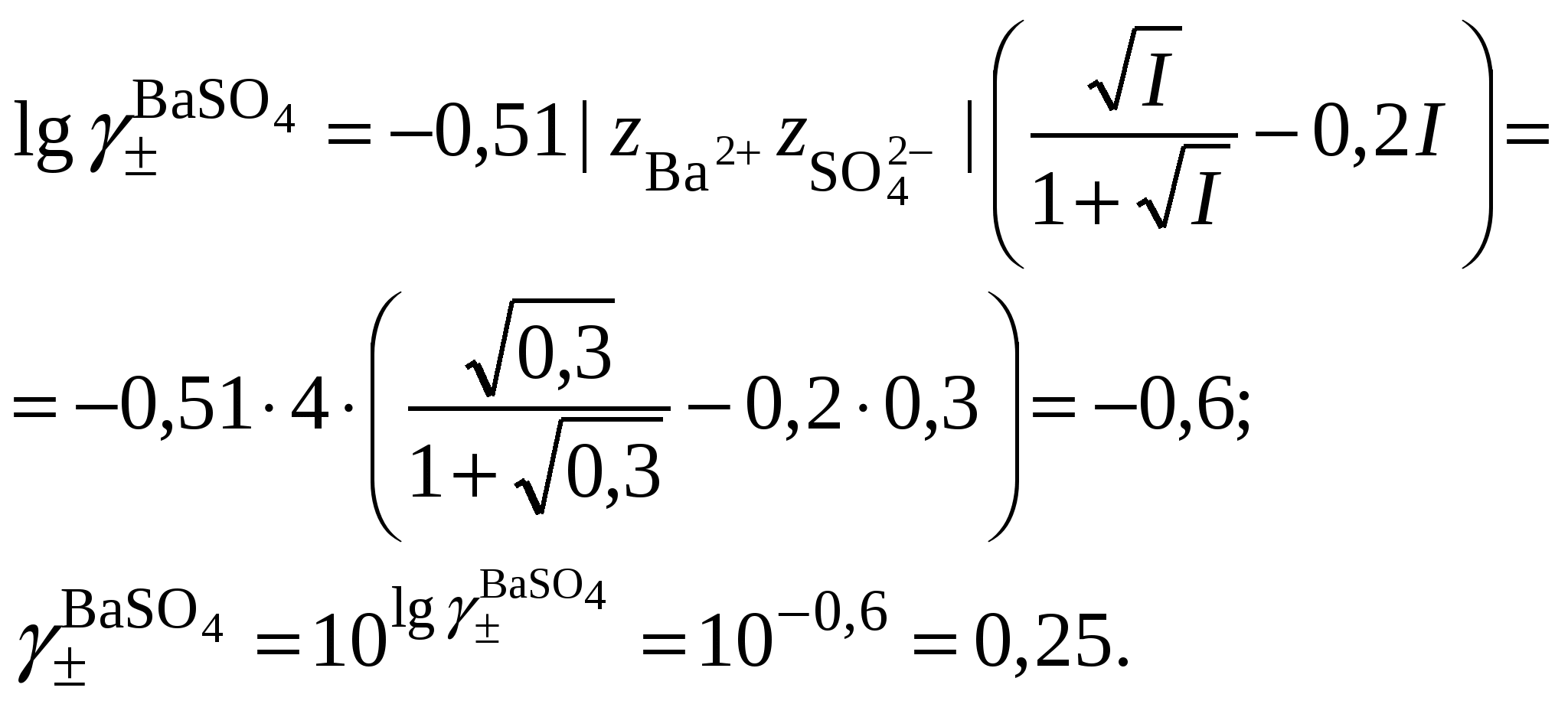 4. Рассчитать растворимость сульфата бария в присутствии хлорида кальция 3.4. Растворимость в многокомпонентной системе с одноименными ионамиВ этом случае раствор содержит, помимо трудно растворимой соли, другой сильный электролит, как правило, хорошо растворимую соль, имеющий в своем составе одноименные с составом осадка ионы, например: В этом случае при составлении уравнения закона действующих масс следует учитывать, что концентрация катиона или аниона может складываться из нескольких источников. В присутствии одноименного аниона Например, уравнение закона действующих масс для системы В присутствии одноименного катиона Например, уравнение закона действующих масс для системы В обоих случаях приходится решать степенное уравнение второго или более высокого порядка. Ионную силу раствора в присутствии одноименного иона следует вычислять, ориентируясь на соотношение концентраций в растворе трудно растворимой соли и соли, содержащей одноименный ион. Если разница между ними не велика, то в уравнении ионной силы следует учитывать все ионные компоненты раствора. Если концентрация электролита, содержащего одноименный ион, в 10 и более раз превышает растворимость осадка, то значением растворимости при расчете ионной силы раствора можно пренебречь. Следует запомнить, что растворимость в присутствии одноименных ионов всегда понижается. Пример 25.Вычислить растворимость сульфата серебра в растворе сульфата натрия концентрацией 0,1 моль/кг, если растворимость сульфата серебра в воде составляет 0,0228 моль/кг. Решение. 1. Вычислить ионную силу раствора, содержащего сульфат серебра и сульфат натрия 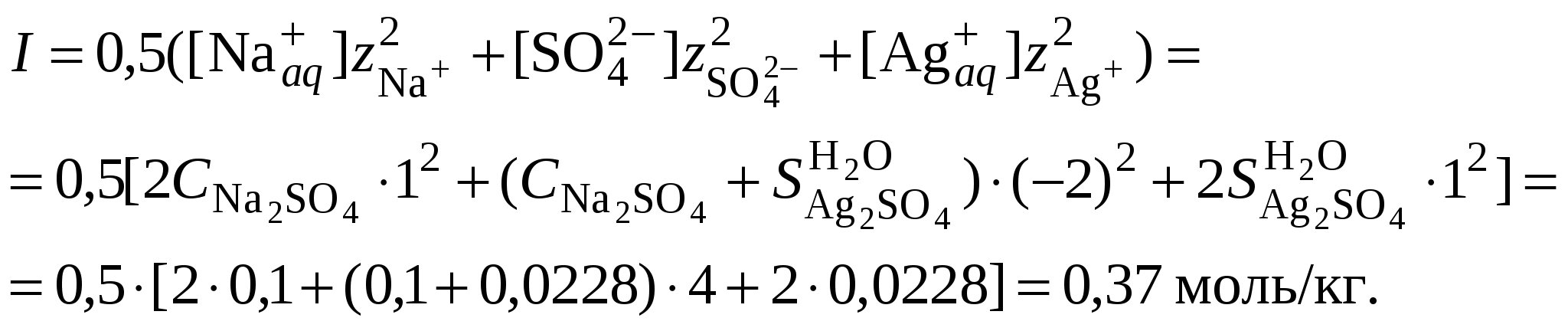 2. Вычислить средний ионный коэффициент активности сульфата серебра 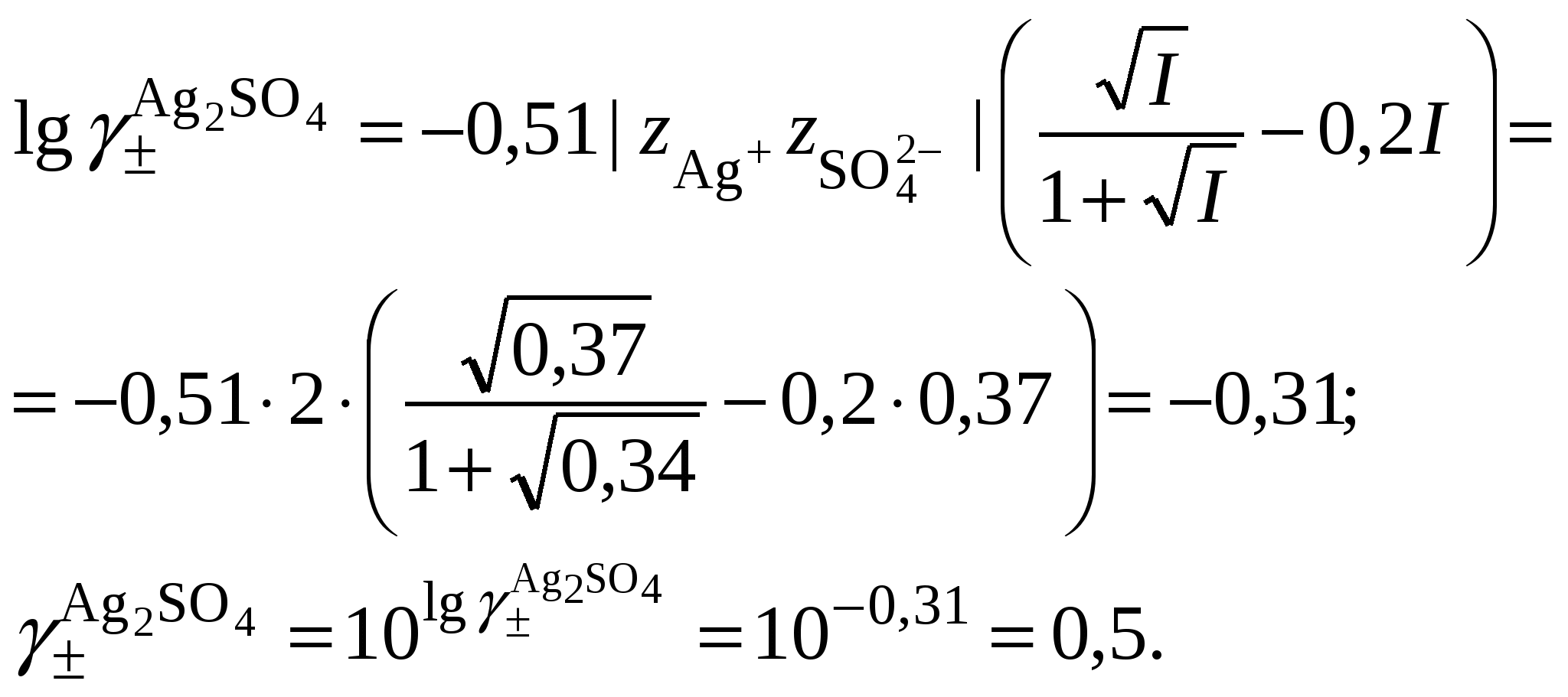 3. В уравнении произведения растворимости сульфата серебра концентрация сульфат-ионов будет суммой растворимости сульфата серебра в присутствии сульфата натрия (S) и концентрации Na2SO4 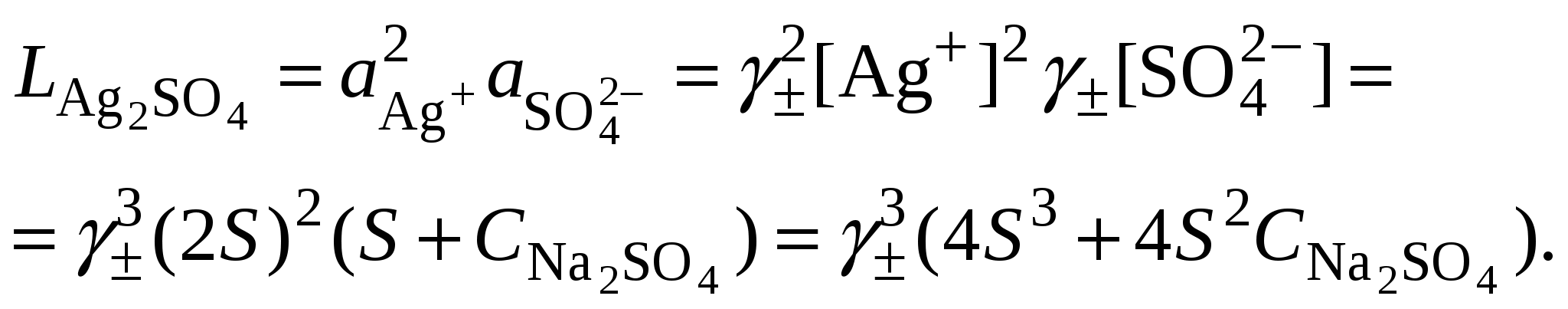 4. Вычислить растворимость сульфата серебра в присутствии сульфата натрия, пренебрегая 4S3 как бесконечно малой величиной: 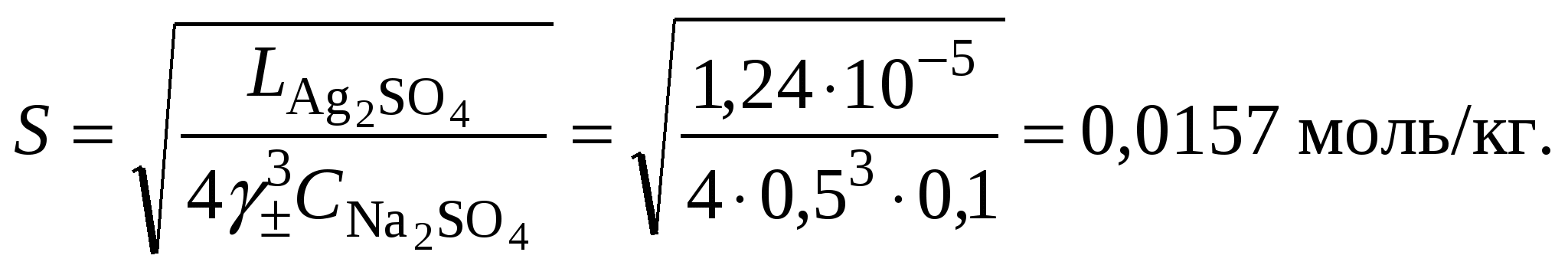 Полученное значение растворимости сульфата серебра в присутствии одноименного иона (0,0157 моль/кг) меньше найденное для бинарной системы сульфат серебра – вода (0,0228 моль/кг). В присутствии одноименного иона растворимость малорастворимого соединения должна уменьшаться, что согласуется с полученными расчетными данными. |
