ответы. процессы и аппараты. 1 вопрос. Виды процессов массопередачи
 Скачать 1.06 Mb. Скачать 1.06 Mb.
|
|
Диаметр аппарата. Расчет диаметра производится по уравнению расхода: 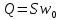 где Q-объемный расход фазы, скорость которой определяет площадь поперечного сечения аппарата, например, газа-в процессе абсорбции, пара-в процессе ректификации и т.д.; 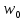 -фиктивная, или приведенная, скорость той же фазы, т.е. скорость, отнесенная к полному сечению аппарата; S-площадь поперечного сечения аппарата. -фиктивная, или приведенная, скорость той же фазы, т.е. скорость, отнесенная к полному сечению аппарата; S-площадь поперечного сечения аппарата.Для круглого поперечного сечения 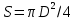 и, следовательно и, следовательно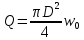 Откуда диаметр аппарата:  (31) (31)Выбор скорости необходимо осуществлять на основе следующих общих соображений. С увеличением скоростей потоков, как правило, возрастают коэффициенты массопередачи, а иногда и удельная поверхность контакта фаз (например при барботаже), в результате чего уменьшается требуемый рабочий объем аппарата. Вместе с тем при увеличении скоростей потоков возрастает гидравлическое сопротивление аппарата, что приводит к увеличению расхода энергии на проведение процесса. Поэтому наиболее правильным является определение (на основе технико-экономических соображений) оптимальной скорости газа или пара. Технико-экономический расчет позволяет найти наивыгоднейший диаметр аппарата, при котором стоимость эксплуатации его будет наименьшей. Однако на практике часто ограничиваются расчетом фиктивной скорости, исходя из максимального ее значения. Упрощенный подход к вычислению фиктивной скорости обусловлен тем, что во многих случаях ее предельное значение определяется наступлением «захлебывания» в противоточных аппаратах или чрезмерным возрастанием брызгоуноса. В процессах массообмена, где повышенное гидравлическое сопротивление не имеет весьма существенного значения, например, при ректификации или при абсорбции, проводимых под избыточным давлением, оптимальная скорость обычно близка к предельной и может быть, в первом приближении, принята равной скорости захлебывания, уменьшенной, например, на 10—20%. В остальных случаях следует учитывать, что в массообменных аппаратах, ‚по мере увеличения относительной скорости фаз, возникают различные гидродинамические режимы, отличающиеся последовательно повышающейся интенсивностью массопередачи. Поэтому выбор фиктивной скорости производят в соответствии с намечаемым гидродинамическим режимом работы аппарата, проверяя выбранную скорость по величине предельно допустимой. Высота аппарата. Высота массообменного аппарата определяется в зависимости от того, является контакт фаз в нем непрерывным или ступенчатым. Высота аппаратов с непрерывным контактом. При непрерывном контакте фаз высоту аппарата можно найти на основе уравнения массопередачи, выраженного через объемный коэффициент массопередачи. Учитывая, что поверхность контакта фаз 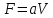 , где V-рабочий объем аппарата и a-удельная поверхность контакта фаз, уравнение массопередачи может быть записано в виде: , где V-рабочий объем аппарата и a-удельная поверхность контакта фаз, уравнение массопередачи может быть записано в виде: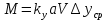 (32) (32)Или 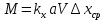 (33) (33)Рабочий объем аппарата 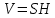 , где S-площадь поперечного сечения аппарата в м3 и H-рабочая высота аппарата в м. Подставляя значение V в уравнения (32) и (33) и решая их относительно H, находим рабочую высоту аппарата: , где S-площадь поперечного сечения аппарата в м3 и H-рабочая высота аппарата в м. Подставляя значение V в уравнения (32) и (33) и решая их относительно H, находим рабочую высоту аппарата: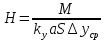 (34) (34)или 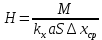 (35) (35)Высота аппаратов со ступенчатым контактом. Для расчета Н через число ступеней в аппаратах со ступенчатым контактом необходимое число ступеней определяется аналитическими и графическими методами. До недавнего времени обычно пользовались методами, основанными на понятии о теоретической ступени изменения концентрации, или о теоретической тарелке. Такая ступень или тарелка соответствует некоторому гипотетическому участку аппарата, на котором жидкость полностью перемешивается, а концентрации удаляющихся фаз (например, жидкости и газа) являются равновесными. Методу теоретических ступеней (тарелок) присущи серьезные недостатки, и обоснованный переход `от теоретических к действительным тарелкам затруднителен. В связи с этим разработаны более совершенные методы, позволяющие определить аналитически или графически непосредственно число действительных ступеней (тарелок) аппарата. Рабочую высоту аппарата находят через число действительных ступеней, пользуясь зависимостью: 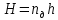 Где h-расстояние между ступенями (тарелками), которое принимают или определяют расчетом. Вопрос 15. Графический метод определения теоретического и действительного числа ступеней Определение числа действительных ступеней Этот метод основан на построении так называемой кинетической кривой. Для построения этой кривой на диаграмме y-x (рисунок 1) проводят произвольно вертикальные отрезки между равновесной и рабочей линиями (например, отрезки 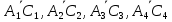 ). Эти отрезки делят в отношении, равном коэффициенту извлечения ). Эти отрезки делят в отношении, равном коэффициенту извлечения 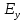 . Как видно из рисунка III, отрезок . Как видно из рисунка III, отрезок 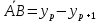 и отрезок и отрезок 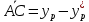 . .Следовательно: 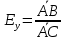 Далее по известному значению 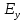 откладывают отрезки откладывают отрезки 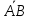 (отрезки (отрезки 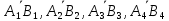 . Через полученные точки B проводят кинетическую кривую DE. Затем в пределах от точки M (с координатами . Через полученные точки B проводят кинетическую кривую DE. Затем в пределах от точки M (с координатами 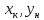 ) до точки N ( ) до точки N (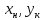 ) вписывают «ступеньки» между рабочей линией и кинетической кривой. Каждая «ступенька» состоит из горизонтального отрезка, представляющего собой изменение состава фазы Фx (жидкости), и вертикального отрезка, выражающего изменение состава фазы Фy (газа) на реальной ступени. Таким образом, число «ступенек» между рабочей линией и кинетической кривой определяет число действительных ступеней, или тарелок, массообменного аппарата со ступенчатым контактом. ) вписывают «ступеньки» между рабочей линией и кинетической кривой. Каждая «ступенька» состоит из горизонтального отрезка, представляющего собой изменение состава фазы Фx (жидкости), и вертикального отрезка, выражающего изменение состава фазы Фy (газа) на реальной ступени. Таким образом, число «ступенек» между рабочей линией и кинетической кривой определяет число действительных ступеней, или тарелок, массообменного аппарата со ступенчатым контактом.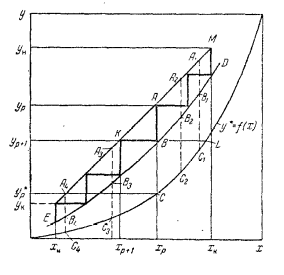 Рисунок 1-Определение числа ступеней методом построения кинетической кривой Определение числа теоретических ступеней Для первой (нижней) ступени состав поступающего на него газа y1 и состав удаляющейся из аппарата жидкости x1 изображаются точкой M на рабочей линии (рисунок 2). Для теоретической ступени состав удаляющегося со ступени газа y2 и состав стекающей с нее жидкости x1 равновесны друг другу, поэтому они изображаются координатами точки С, лежащей на линии равновесия. Следовательно, процессу изменения состава газовой фазы на теоретической ступени соответствует вертикальный отрезок  . .Согласно материальному балансу, состав жидкости x2, стекающей со второй ступени, и состав газа y2, удаляющегося с первой ступени, отвечают точке А на рабочей линии. Значит, горизонтальный отрезок 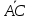 характеризует изменение состава жидкой фазы на теоретической ступени. характеризует изменение состава жидкой фазы на теоретической ступени.«Ступенька» ACM изображает изменение составов обеих фаз, т.е. весь процесс, протекающий на теоретической ступени. Строя последовательно подобные «ступеньки» до пересечения с ординатой, отвечающей составу газа, удаляющегося с верхней (последней) теоретической ступени, находят число теоретических ступеней, или теоретических тарелок, nT. При этом величина nT может не быть целым числом. 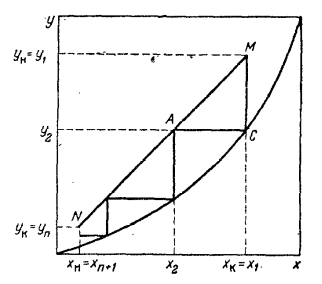 Рисунок 2-Определение числа теоретических ступеней графическим методом Вопрос 16. АБСОРБЦИЯ. Равновесие в системе газ-жидкость. Закон Генри. Закон Дальтона А6сор6цией называют процесс поглощения газов или паров из газовых или паро-газовых смесей жидкими поглотителями (абсорбентами). При физической абсорбции поглощаемый газ (абсор6тив) не взаимодействует химически с абсорбентом. Если же абсорбтив образует с абсорбентом химическое соединение, то процесс называется хемосор6йией. Физическая абсорбция в большинстве случаев обратима. На этом свойстве абсорбционных процессов основано выделение поглощенного газа из раствора-десорбция. Равновесие между фазами. При абсорбции Содержание газа в растворе зависит от свойств газа и жидкости, давления, температуры и состава газовой фазы (парциального давления растворяющегося газа в газовой смеси). В случае растворения в жидкости бинарной газовой смеси (распределяемый компонент А, носитель В) взаимодействуют две фазы (Ф=2)‚ число компонентов равно трем (К = 3) и, согласно правилу фаз число степеней свободы системы равно трем. Для данной системы газ—жидкость переменными являются температура, давление и концентрации в обеих фазах. Следовательно, в состоянии равновесия при постоянных температуре и общем давлении зависимость между парциальным давлением газа А (или его концентрацией) и составом жидкой фазы однозначна. Эта зависимость выражается законом Генри: парциальное давление 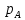 растворенного газа пропорционально его мольной доле растворенного газа пропорционально его мольной доле 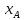 в растворе в растворе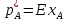 (36) (36)Или растворимость газа (поглощаемого компонента А) в жидкости при данной температуре пропорциональна его парциальному давлению над жидкостью 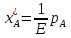 (37) (37)Где 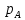 -парциальное давление поглощаемого газа, находящегося в равновесии с раствором, имеющим концентрацию -парциальное давление поглощаемого газа, находящегося в равновесии с раствором, имеющим концентрацию 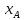 (в мольных долях); (в мольных долях); 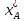 -концентрация газа в растворе (в мольных долях), равновесном с газовой фазой, в которой парциальное давление поглощаемого компонента равно -концентрация газа в растворе (в мольных долях), равновесном с газовой фазой, в которой парциальное давление поглощаемого компонента равно 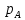 ; E-коэффициент пропорциональности, называемый коэффициентом, или константой Генри. ; E-коэффициент пропорциональности, называемый коэффициентом, или константой Генри.Числовые значения коэффициента Генри для данного газа зависят от природы поглотителя или газа и от температуры, но не зависит от общего давления в системе. Зависимость E от температуры выражается уравнением: 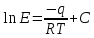 (38) (38)Где q-дифференциальная теплота растворения газа; R-газовая постоянная; C-постоянная, зависящая от природы газа и поглотителя. Если 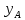 -мольная доля извлекаемого компонента А в газовой смеси и P-общее давление в системе, то парциальное давление -мольная доля извлекаемого компонента А в газовой смеси и P-общее давление в системе, то парциальное давление 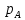 , по закону Дальтона можно выразить зависимостью , по закону Дальтона можно выразить зависимостью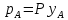 (39) (39)Подставив значение 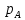 в уравнение (36), получим в уравнение (36), получим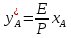 (40) (40)Или закон Генри может быть представлен в форме 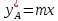 (41) (41)Где 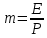 -коэффициент распределения, или константа фазового равновесия. -коэффициент распределения, или константа фазового равновесия.Уравнение (41) показывает, что зависимость меду концентрациями данного компонента в газовой смеси и в равновесной с ней жидкости выражается прямой линией, проходящей через начало координат и имеющей угол наклона‚ тангенс которого равен m.Числовые значения величины m зависят от температуры и давления в системе: уменьшаются с увеличением давления и снижением температуры. Таким образом, растворимость газа в жидкости увеличивается с повышением давления и снижением температуры. Закон Генри применим к растворам газов, критические температуры которых выше температуры раствора, и справедлив только для идеальных растворов. Поэтому он с достаточной точностью применим лишь к сильно разбавленным реальным растворам, приближающимся по свойствам к идеальным, т. е. соблюдается при малых концентрациях растворенного газа или при его малой растворимости. Для хорошо растворимых газов, при больших концентрациях их в растворе, растворимость меньше, чем следует из закона Генри. Для систем, не подчиняющихся этому закону, коэффициент m в уравнении (41) является величиной переменной, и линия равновесия представляет собой кривую, которую строят обычно по опытным данным. Вопрос 17. Материальный баланс абсорбции Примем расходы фаз по высоте аппарата постоянными и выразим содержание поглощаемого газа в относительных мольных концентрациях. Обозначим: G-расход инертного газа, кмоль/сек;  и и 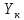 -начальная и конечная концентрации абсорбтива в газовой смеси, кмоль/кмоль инертного газа; L-расход абсорбента, кмоль/сек ; его концентрации -начальная и конечная концентрации абсорбтива в газовой смеси, кмоль/кмоль инертного газа; L-расход абсорбента, кмоль/сек ; его концентрации 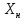 и и 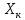 , кмоль/кмоль абсорбента. , кмоль/кмоль абсорбента.Тогда уравнение материального баланса будет: 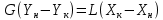 (42) (42)Отсюда общий расход абсорбента (в кмоль/сек):  (43) (43)А его удельный расход (в кмоль/кмоль инертного газа): 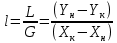 (44) (44)Или 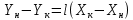 (45) (45)Уравнение (45) показывает. Что изменение концентрации в абсорбционном аппарате происходит прямолинейно и, следовательно, в координатах Y-X рабочая линия процесса абсорбции представляет собой прямую с углом наклона, тангенс которого равен 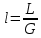 . .Вопрос 18. Расчет линии равновесия с учетом теплоты абсорбции Если абсорбцию ведут без отвода тепла или с недостаточным его отводом, то температура повышается вследствие выделения тепла при поглощении газа жидкостью, что необходимо учитывать при расчете. Для технических расчетов можно пренебречь нагреванием газовой фазы и считать, что выделяющееся при абсорбции тепло затрачивается только на нагрев жидкости. Если линия равновесия при температуре 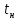 поступающей жидкости изображается кривой OD (рисунок 3), то при температуре уходящей жидкости линия равновесия расположится выше (кривая OC) и действительная линия равновесия при переменной температуре жидкости изобразится кривой AB. поступающей жидкости изображается кривой OD (рисунок 3), то при температуре уходящей жидкости линия равновесия расположится выше (кривая OC) и действительная линия равновесия при переменной температуре жидкости изобразится кривой AB. Рисунок 3-Кривая равновесия при неизотермической абсорбции Ординату 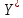 некоторой точки O’ на кривой равновесия, соответствующую составу жидкости X, можно найти, если известна температура t при данном составе жидкости. Для этого необходимо составить уравнение теплового баланса для части абсорбционного аппарата, расположенной выше некоторого произвольного сечения с текущими концентрациями X и Y жидкости и газа соответственно: некоторой точки O’ на кривой равновесия, соответствующую составу жидкости X, можно найти, если известна температура t при данном составе жидкости. Для этого необходимо составить уравнение теплового баланса для части абсорбционного аппарата, расположенной выше некоторого произвольного сечения с текущими концентрациями X и Y жидкости и газа соответственно: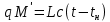 (46) (46)Где q-дифференциальная теплота растворения газа, кДж/моль; M’-количество газа, поглощенного в рассматриваемой части абсорбера, кмоль/сек; L-расход абсорбента, кмоль/сек; с-теплоемкость жидкости, кДж/(кмоль·град); t-температура жидкости в данном сечении, °С; 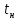 -начальная температура жидкости, °С. -начальная температура жидкости, °С.Так как 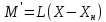 , то , то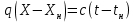 Тогда  (47) (47)Задаваясь рядом произвольных значений X в интервале между известными значениями 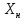 и и 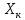 , с помощью уравнения (47) вычисляют t. По опытным данным находят соответствующие значения , с помощью уравнения (47) вычисляют t. По опытным данным находят соответствующие значения 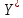 и строят линию равновесия (по точкам О1, О2 и т.д.). и строят линию равновесия (по точкам О1, О2 и т.д.).Вопрос 19. Определение минимального расхода поглотителя В реальном абсорбционном аппарате равновесие между фазами не достигается и всегда 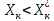 , где , где 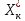 -концентрация поглощаемого газа в жидкости, находящейся в равновесии с поступающим газом. Отсюда следует, что значение l всегда должно быть больше минимального значения -концентрация поглощаемого газа в жидкости, находящейся в равновесии с поступающим газом. Отсюда следует, что значение l всегда должно быть больше минимального значения 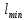 , отвечающего предельному положению рабочей линии (линия BA3 на рисунке 4). Значение , отвечающего предельному положению рабочей линии (линия BA3 на рисунке 4). Значение 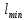 можно определить по уравнению (44) при замене можно определить по уравнению (44) при замене 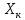 на на 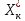 : :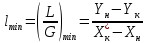 (48) (48)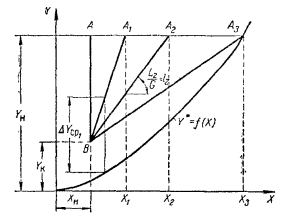 Рисунок 4-К определению удельного расхода абсорбента Вопрос 20. Виды абсорберов Аппараты, в которых осуществляются абсорбционные процессы, называют абсор6ерами. Как и другие процессы массопередачи, абсорбция протекает на поверхности раздела фаз. Поэтому абсорберы должны иметь развитую поверхность соприкосновения между жидкостью и газом. По способу образования этой поверхности абсорберы можно условно разделить на следующие группы: 1) поверхностные и пленочные; 2) насадочные З) барботажные (тарельчатые); 4) распыливающие. Поверхностные и пленочные абсорберы В абсорберах этого типа поверхностью соприкосновения фаз является зеркало неподвижной или медленно движущейся жидкости, или же поверхность текущей жидкой пленки. |
