Азот. 8 АЗОТ. Азот Азот неметаллический элемент Va группы периодической таблицы Д. И. Менделеева. Составляет 78% воздуха. Входит в состав белков, являющихся важной частью живых организмов.
 Скачать 1.02 Mb. Скачать 1.02 Mb.
|
|
Азот Азот - неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав белков, являющихся важной частью живых организмов. Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью азота.  Общая характеристика элементов Va группы От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону. Азот, фосфор и мышьяк являются неметаллами, сурьма - полуметалл, висмут - металл. 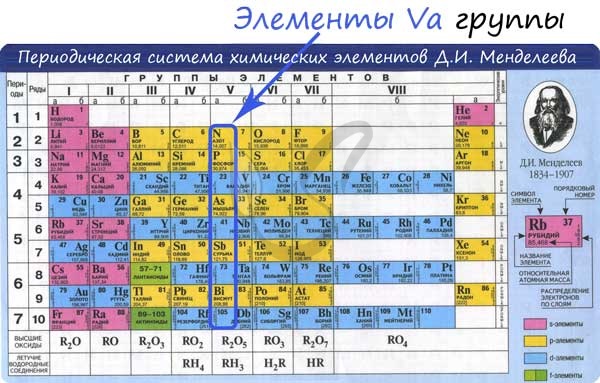 Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3: N - 2s22p3 P - 3s23p3 As - 4s24p3 Sb - 5s25p3 Bi - 6s26p3 Основное и возбужденное состояние азота При возбуждении атома фосфора электроны на s-подуровне распариваются и переходят на p-подуровень. Однако с азотом ситуация иная. Поскольку азот находится во втором периоде, то 3ий уровень у него отсутствует, а значит распаривание электронов на s-подуровне невозможно - возбужденное состояние у азота отсутствует. Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна. 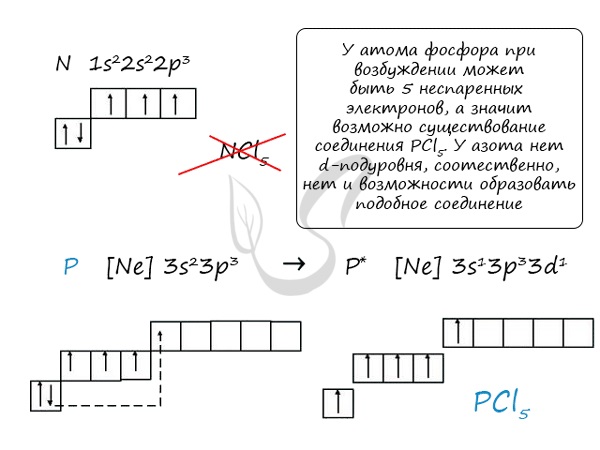 Природные соединения В природе азот встречается в виде следующих соединений: Воздух - во вдыхаемом нами воздухе содержится 78% азота Азот входит в состав нуклеиновых кислот, белков KNO3 - индийская селитра, калиевая селитра NaNO3 - чилийская селитра, натриевая селитра NH4NO3 - аммиачная селитра (искусственный продукт, в природе не встречается) Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако, следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.  Получение В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения из сжиженного воздуха получают азот. Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород. 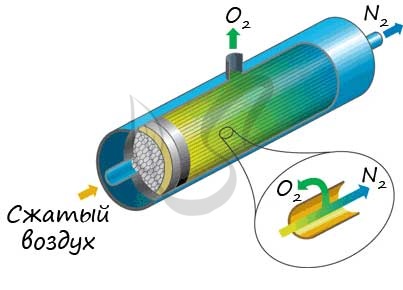 В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония NH4NO2 → (t) N2 + H2O Также азот можно получить путем восстановления азотной кислоты активными металлами. HNO3(разб.) + Zn → Zn(NO3)2 + N2 + H2O 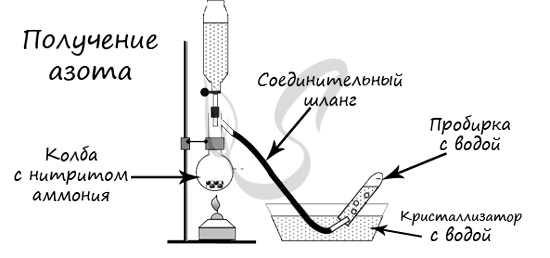 Химические свойства Азот восхищает - он принимает все возможные для себя степени окисления от -3 до +5. 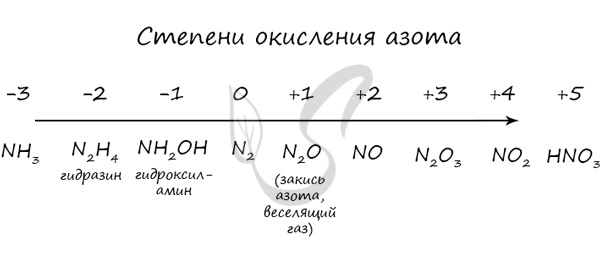 Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении. 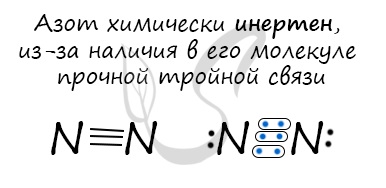 Реакция с металлами Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами. N2 + Li → Li3N (нитрид лития) N2 + Mg → (t) Mg3N2 N2 + Al → (t) AlN Реакция с неметаллами Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств. N2 + H2 ⇄ (t, p) NH3 Аммиак Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях, называется нашатырным спиртом. 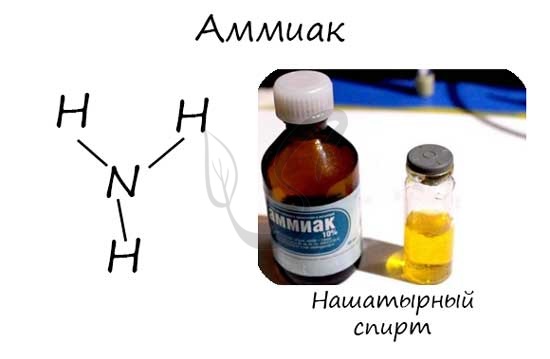 Получение В промышленности аммиак получают прямым взаимодействием азота и водорода. N2 + H2 ⇄ (t, p) NH3 В лабораторных условиях сильными щелочами действуют на соли аммония. NH4Cl + NaOH → NH3 + NaCl + H2O Химические свойства Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет. Реакция с водой Образует нестойкое соединение - гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак. NH3 + H2O ⇄ NH4OH Основные свойства Как основание аммиак способен реагировать с кислотами с образованием солей. NH3 + HCl → NH4Cl (хлорид аммония) NH3 + HNO3 → NH4NO3 (нитрат аммония)  Восстановительные свойства Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные восстановительные свойства. Его используют для восстановления металлов из их оксидов. NH3 + FeO → N2↑ + Fe + H2O NH3 + CuO → N2↑ + Cu + H2O Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается выделением NO. NH3 + O2 → (t) N2 + H2O NH3 + O2 → (t, кат) NO + H2O  Соли аммония Получение NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты) 3NH3 + H3PO4 → (NH4)3PO4 Химические свойства Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода - реакция идет. Реакции с кислотами NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑ Реакции с щелочами В реакциях с щелочами образуется гидроксид аммония - NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак. NH4Cl + KOH → KCl + NH3 + H2O Реакции с солями (NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl Реакция гидролиза В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония. NH4+ + H2O ⇄ NH4OH + H+ NH4OH ⇄ NH3 + H2O Реакции разложения NH4Cl → (t) NH3↑ + HCl↑ (NH4)2CO3 → (t) NH3↑ + H2O + CO2↑ NH4NO2 → (t) N2↑ + H2O NH4NO3 → (t) N2O↑ + H2O (NH4)3PO4 → (t) NH3↑ + H3PO4  Оксид азота I - N2O Закись азота, веселящий газ - N2O - обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.  Получают N2O разложением нитрата аммония при нагревании: NH4NO3 → N2O + H2O Оксид азота I разлагается на азот и кислород: N2O → (t) N2 + O2 Оксид азота II - NO Окись азота - NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV. Получение В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака. NH3 + O2 → (t, кат) NO + H2O В лабораторных условиях - в ходе реакции малоактивных металлов с разбавленной азотной кислотой. Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O Химические свойства На воздухе быстро окисляется с образованием бурого газа - оксида азота IV - NO2. NO + O2 → NO2  Оксид азота III - N2O3 При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.  Получение Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой (две реакции, в которых образуется смесь оксидов азота), затем охлаждением полученной смеси газов до температуры - 36 °C. As2O3 + HNO3 + H2O → H3AsO4 + NO↑ As2O3 + HNO3 + H2O → H3AsO4 + NO2↑ При охлаждении газов образуется оксид азота III. NO + NO2 → N2O3 Химические свойства Является кислотным оксидом. соответствует азотистой кислоте - HNO2, соли которой называются нитриты (NO2-). Реагирует с водой, основаниями. H2O + N2O3 → HNO2 NaOH + N2O3 → NaNO2 + H2O Оксид азота IV - NO2 Бурый газ, имеет острый запах. Ядовит.  Получение В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при разложении нитратов. Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O 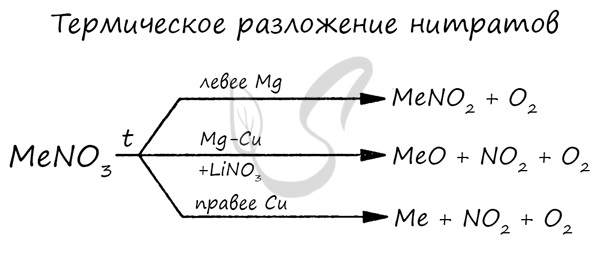 Cu(NO3)2 → (t) CuO + NO2 + O2 Pb(NO3)2 → (t) PbO + NO2 + O2 Химические свойства Проявляет высокую химическую активность, кислотный оксид. Окислительные свойства Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем. NO2 + C → CO2 + N2 NO2 + P → P2O5 + N2 Окисляет SO2 в SO3 - на этой реакции основана одна из стадий получения серной кислоты. SO2 + NO2 → SO3 + NO Реакции с водой и щелочами Оксид азота IV соответствует сразу двум кислотам - азотистой HNO2 и азотной HNO3. Реакции с водой и щелочами протекают по одной схеме. NO2 + H2O → HNO3 + HNO2 NO2 + LiOH → LiNO3 + LiNO2 + H2O Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота. NO2 + H2O + O2 → HNO3  Блиц-опрос по теме Азот 1. Самым большим радиусом атома среди элементов V группы обладает  Мышьяк Мышьяк Азот Азот Сурьма Сурьма Висмут Висмут2. Количество электронов на внешнем уровне у элементов V группы  Пять Пять Шесть Шесть Семь Семь Восемь Восемь3. Количество валентных электронов у элементов V группы (в основном состоянии)  Один Один Три Три Два Два Четыре Четыре4. В промышленности аммиак получают  Разложением гидроксида аммония Разложением гидроксида аммония Реакцией соединения между азотом и водородом Реакцией соединения между азотом и водородом Разложением нитрита аммония Разложением нитрита аммония Разложением нитрата аммония Разложением нитрата аммония5. Выберите формулу закиси азота (веселящего газа)  NH3 NH3 NO2 NO2 N2O N2O NO NOАзотная кислотаАзотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы. Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.  Получение В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах. NH3 + O2 → (кат. Pt) NO + H2O NO + O2 → NO2 NO2 + H2O + O2 → HNO3 Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты: KNO3 + H2SO4(конц.) → KHSO4 + HNO3↑ Химические свойства Кислотные свойства Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита. CaO + HNO3 → Ca(NO3)2 + H2O HNO3 + NaOH → NaNO3 + H2O Na2CO3 + HNO3 → NaNO3 + H2O + CO2↑  Термическое разложение При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте. HNO3 → (hv) NO2 + H2O + O2 Реакции с неметаллами Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2, если разбавленная - до NO. HNO3(конц.) + C → CO2 + H2O + NO2 HNO3(конц.) + S → H2SO4 + NO2 + H2O HNO3(разб.) + S → H2SO4 + NO + H2O HNO3(конц.) + P → H3PO4 + NO2 + H2O  Реакции с металлами В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты. Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2. Cu + HNO3(конц.) → Cu(NO3)2 + NO2 + H2O С разбавленной азотной кислотой газообразным продуктом преимущественно является NO. Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3. Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях. Zn + HNO3(70% - конц.) → Zn(NO3)2 + NO2 + H2O Zn + HNO3(35% - ср. конц.) → Zn(NO3)2 + NO + H2O Zn + HNO3(20% - разб.) → Zn(NO3)2 + N2O + H2O Zn + HNO3(10% - оч. разб.) → Zn(NO3)2 + N2 + H2O  Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности. 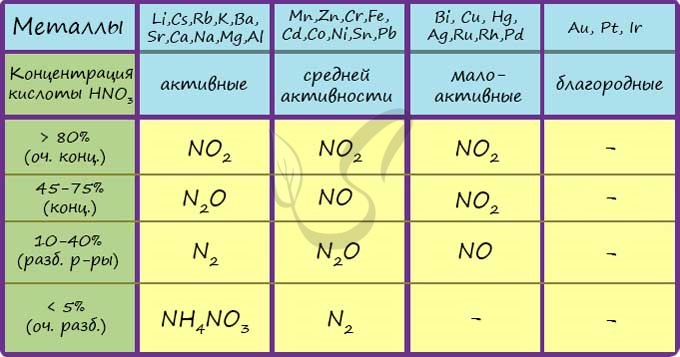 Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы. Al + HNO3(конц.) ⇸ (реакция не идет) При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается. Al + HNO3 → (t) Al(NO3)3 + NO2 + H2O Соли азотной кислоты - нитраты NO3-Получение Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями. Fe + HNO3(разб.) → Fe(NO3)2 + N2O + H2O В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется. MgO + HNO3 → Mg(NO3)2 + H2O Cr(OH)3 + HNO3 → Cr(NO3)3 + H2O  Нитрат аммония получают реакция аммиака с азотной кислотой. NH3 + HNO3 → NH4NO3 Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная кислота - до +2. Fe + HNO3(разб.) → Fe(NO3)2 + N2O + H2O Fe + HNO3(конц.) → Fe(NO3)3 + NO + H2O Химические свойства Реакции с металлами, основаниями и кислотами Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода). Hg(NO3)2 + Mg → Mg(NO3)2 + Hg Pb(NO3)2 + LiOH → Pb(OH)2 + LiNO3 AgNO3 + KCl → AgCl↓ + KNO3  Ba(NO3)2 + Na2SO4 → BaSO4 + NaNO3 Разложение нитратов Нитраты разлагаются в зависимости от активности металла, входящего в их состав.  Pb(NO3)2 → (t) PbO + NO2 + O2 NaNO3 → (t) NaNO2 + O2 Cu(NO3)2 → (t) CuO + NO2 + O2 PtNO3 → (t) Pt + NO2 + O2 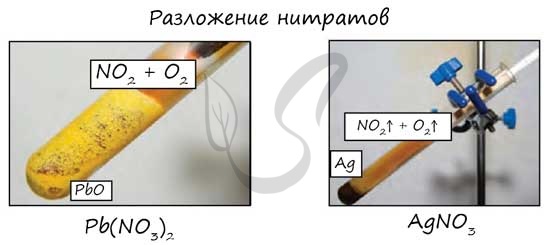 Блиц-опрос по теме Азотная кислота 1. Холодная концентрированная кислота с алюминием  Реагирует с выделением N2 Реагирует с выделением N2 Реагирует с выделением NO2 Реагирует с выделением NO2 Не реагирует Не реагирует Реагирует с выделением NH4NO3 Реагирует с выделением NH4NO32. Реакция концентрированной азотной кислоты с малоактивными металлами сопровождается выделением газа  N2 N2 NO2 NO2 NH3 NH3 N2O N2O3. Если в результате реакции активного металла с азотной кислотой выделилось твердое вещество, то речь идет о  NH4NO3 NH4NO3 NH3 NH3 N2 N2 NO2 NO24. При разложении нитрата серебра выделяется  Ag2O, NO2, O2 Ag2O, NO2, O2 AgO, NO2, O2 AgO, NO2, O2 Ag, NO2, O2 Ag, NO2, O2 Ag, NO2 Ag, NO25. Ожоги кожи азотной кислотой внешне окрашены в ... цвет  Зеленый Зеленый Красный Красный Черный Черный Желтый Желтый |
