Билет 1 1 белки как основа жизни. Роль белков
 Скачать 1.24 Mb. Скачать 1.24 Mb.
|
|
3) Тимиловая проба(проба Маклагана) -осадочная (коагуляционная) проба, предназначенная для обнаружения изменений качественного и количественного состава белков сыворотки крови при различных заболеваниях. основана на осаждении белков путем добавления насыщенного раствора тимола. при положительном результате происходит помутнение исследуемой сыворотки. степень мутности определяется фотоколорометрическим методом. результат выражают в единицах Маклагана( ед. М). проба отрицательна - 0-5 ед, положительна- более 5 ед. отрицательная проба означает, что нарушения белкового состава сыворотки нет, положительная - что нарушения имеются. 4) 7-8-летнему ребенку необходимо определить сахар крови на предмет выявления сахарного диабета. Ребенок перед проведением пробы в лаборатории очень волновался, много плакал. Установлено, что у ребенка уровень сахара в крови выше нормы. Можно ли утверждать по результатам исследования, что у ребенка диабет? Данные результаты не могут считаться достоверными, поскольку повышение глюкозы в крови может быт результатом стресса. В этом случае выделяется в кровь адреналин, который усиливает распад печеночного гликогена и увеличивает уровень глюкозы в крови. Билет 18 1)Витамин В2… Витамин В2 (рибофлавин). В основе структуры витамина В2 лежит структура изоаллоксазина, соединённого со спиртом рибитолом. Главные источники витамина В2 - печень, почки, яйца, молоко, дрожжи. Витамин содержится также в шпинате, пшенице, ржи. Частично человек получает витамин В2 как продукт жизнедеятельности кишечной микрофлоры. Суточная потребность в витамине В2 взрослого человека составляет 1,8-2,6 мг. Биологические функции. В слизистой оболочке кишечника после всасывания витамина происходит образование коферментов FMN и FAD. Клинические проявления недостаточности рибофлавина выражаются в остановке роста у молодых организмов. Часто развиваются воспалительные процессы на слизистой оболочке ротовой полости, появляются длительно незаживающие трещины в углах рта, дерматит носогубной складки. Типично воспаление глаз: конъюнктивиты, васкуляризация роговицы, катаракта. Кроме того, при авитаминозе В2 развиваются общая мышечная слабость и слабость сердечной мышцы 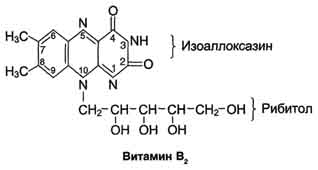 2) Обмен глицерофосфолипидов… Обмен глицерофосфолипидов. Начальные этапы синтеза глицерофосфолипидов и жиров происходят одинаково до образования фосфатидной кислоты. Фосфатидная кислота может синтезироваться двумя разными путями: через глицеральдегид-3-фосфат и через дигидроксиацетонфосфат. На следующем этапе фосфатидаза отщепляет от фосфатидной кислоты фосфатный остаток, в результате чего образуется диацилглицерол. Дальнейшие превращения диацилглицерола также могут идти разными путями. Один из вариантов - образование активной формы "полярной головки" фосфолипида: холин, серии или этаноламин превращаются в ЦДФ-холин, ЦДФ-серин или ЦДФ-этаноламин. Далее диацилглицерол взаимодействует с ЦМФ-производными, при этом выделяется ЦМФ, и образуется соответствующий фосфолигщц, например фосфатидилхолин. Между глицерофосфолипидами возможны различные взаимопревращения. Фосфатидилхолин может образовываться и другим путём: из фосфатидилэтаноламина, получая последовательно 3 метальные группы от SAM. Фосфатидилсерин может превращаться в фосфа-тидилэтаноламин путём декарбоксилирования. Фосфатидилэтаноламин может превращаться в фосфатидилсерин путём обмена этаноламина на серии. Катаболизм глицерофосфолипидов. Различные типы фосфолипаз, локализованных в клеточных мембранах или в лизосомах, катализируют гидролиз глицерофосфолипидов. Гидролиз некоторых глицерофосфолипидов под действием фосфолипаз имеет значение не только как путь катаболизма, но и как путь образования вторичных посредников или предшественников в синтезе биологически активных веществ - эйкозаноидов. Кроме того, фосфолипазы А1 и А2 участвуют в изменении состава жирных кислот в глицерофосфолипидах, например при синтезе в эмбриональном периоде развития дипальмитоилфосфатидилхолина - компонента сурфактанта. 3) Мочевина крови Мочевина образует с диацилмонооксимом в присутствии тиосемикарбазида и ионов железа в сильно кислой среде комплекс, окрашенный в красный цвет. Интенсивность окраски пропорциональна концентрации мочевины в сыворотке крови. Развивающуюся окраску сравнивают со шкалой стандартных растворов мочевины 2,5-8,3 ммоль/л, 15-50 мг% Сдвиги концентрации мочевины крови зависят от соотношения процессов ее синтеза в гепатоцитах и экскреции почками. Повышение мочевины в крови в норме может наблюдаться при потреблении большого количества белка пищи. В условиях патологии ее концентрация, в основном, нарастает при почечной недостаточности, а также при усиленном распаде белков организма (диабет). Снижение уровня мочевины в крови имеет место при ослаблении ее синтеза клетками печени (печеночная недостаточность, цирроз печени и др.), а также при диете с недостаточным содержанием белка, белковом истощении. 4) В клинике у больных исследуют белковый спектр крови методом электрофореза. В каком порядке располагаются белковые фракции сыворотки крови на электрофореграмме? Почему для проведения электрофореза белков сыворотки крови используют буферные растворы с щелочным значением рН? В буферном растворе с рН>7 все белки сыворотки крови приобретают отрицательный заряд и движутся от катода к аноду, причем дальше всего уходят альбумины, имеющие меньшую молекулярную массу, затем располагаются α1-, α 2-, β- и γ-глобулины. Иногда каждая из этих основных фракций может разделиться на несколько подфракций. Билет 19 1)Витамин С… Витамин С (аскорбиновая кислота). Источники витамина С - свежие фрукты, овощи, зелень. Суточная потребность человека в витамине С составляет 50-75 мг. Биологические функции. Образование коллагена, серотонина из триптофана, образование катехоламинов, синтез кортикостероидов. Аскорбиновая кислота также участвует в превращении холестерина в желчные кислоты. Витамин С необходим для детоксикации в гепатоцитах при участии цитохрома P450. Витамин С сам нейтрализует супероксид-анион радикал до перекиси водорода. Клинические проявления недостаточности витамина С. Недостаточность аскорбиновой кислоты приводит к заболеванию, называемому цингой (скорбут). Цинга, возникающая у человека при недостаточном содержании в пищевом рационе свежих фруктов и овощей, описана более 300 лет назад, со времени проведения длительных морских плаваний и северных экспедиций. Это заболевание связано с недостатком в пище витамина С. Болеют цингой только человек, приматы и морские свинки. Главные проявления авитаминоза обусловлены в основном нарушением образования коллагена в соединительной ткани. Вследствие этого наблюдают разрыхление дёсен, расшатывание зубов, нарушение целостности капилляров (сопровождающееся подкожными кровоизлияниями). Возникают отёки, боль в суставах, анемия 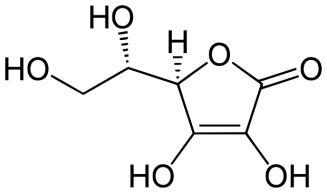 2)Обмен ацетоукс. К-ты… В печени часть жирных кислот превращается в так называемые кетоновые тела – ацетоуксусную и β-гидроксимасляную кислоты. Эти вещества затем поступают в кровь и используются как источники энергии в других органах и тканях. Непосредственным предшественником кетоновых тел служит ацетил-КоА, который может образоваться как из жирных кислот так из углеводов. Однако для синтеза кетоновых тел используется преимущественно ацетил-КоА, образующийся из жирных кислот. Это происходит в результате действия специальных регуляторных механизмов. Содержание кетоновых тел в крови увеличивается в таких состояниях когда основным источником энергии для организма служат жирные кислоты –при длительной мышечной работе, при голодании, при некоторых болезнях. Через двое суток голодания концентрация кетоновых тел в крови достигает 5-8мг/дл через неделю 40-50мг/дл. При сахарном диабете концентрация кетоновых тел может повышаться до 300-400мг/дл, что приводит к метаболическому ацидозу. Кетонемия и кетонурия. Вследствие недостаточности инсулина уменьшается отношение инсулина/глюкагон, т.е. имеется относительное избыточность глюкагона. Однако скорость синтеза кетоновых тел может превышать даже увеличенное в этих условиях их потребление тканями (концентрация кетоновых тел в крови в норме меньше 2мг/дл, при голодании до 30 мг/дл). При диабете кетонемия часто бывает 100 мг/дл, а может достигать и 350 мг/дл. При такой кетонемии возникает и кетонурия - с мочой выделяется до 5г кетовых тел в сутки. В тканях происходит декарбоксилирование ацетоуксусной кислоты: от больных исходит запах ацетона, который ощущается даже на расстоянии). Кетовые теля, являясь кислотами, снижают буферную емкость крови, а при высоких концентрациях снижают и рН крови - возникает ацидоз. В норме рН крови равна 7,4+0,04. При содержании кетовых тел 100мг/дл и больше рН крови может быть близко к 7,0. Ацидоз такой степени резко нарушает функции мозга, вплоть до потери сознания. 3. Количественное определение активности амилазы (диастазы) мочи по Вольгемуту. Моча разводится в геометрической прогрессии. Каждое разведение инкубируют с крахмалом в течение 30 минут. Негидролизованный крахмал определяют по реакции с иодом. Активность амилазы расчитывается по наибольшему разведению, способному гидролизовать крахмал. 16-34 мг крахмала, гидролизованного за 30 мин 1 мл мочи Увеличивается при острых панкреатитах (10-30 раз), обострениях хронических панкреатитах, опухолях и травмах поджелудочной железы. Гиперамилаземия наблюдается при паротитах, опухолях и травмах слюнных желез, слюнокаменной болезни. Снижение активности амилазы наблюдается при сахарном диабете. 4) Больной длительное время находился в постели в неподвижном состоянии по поводу болезни сердца. Проведенный анализ мочи показал нарастание содержания солей Са2+. Связано ли это с основной болезнью сердца или с какой-либо другой причиной? Одной из функций кальция является участие в мышечном сокращении, при длительном нахождении в неподвижном состоянии, происходит вымывание его из мышц и повышение в крови. Билет 20 1)Витамин В1… Витамин B1 (тиамин). Структура витамина включает пиримидиновое и тиазоловое кольца, соединённые метановым мостиком. Источники. Он широко распространён в продуктах растительного происхождения (оболочка семян хлебных злаков и риса, горох, фасоль, соя и др.). Суточная потребность взрослого человека в среднем составляет 2-3 мг витамина В1. Биологическая роль витамина В, определяется тем, что в виде ТДФ он входит в состав как минимум трёх ферментов и ферментных комплексов: в составе пируват - и оскетоглутаратдегидрогеназных комплексов он участвует в окислительном декарбоксилировании пирувата и оскетоглутарата; в составе транскетолазы ТДФ участвует в пентозофосфатном пути превращения углеводов. Основной, наиболее характерный и специфический признак недостаточности витамина В1- полиневрит, в основе которого лежат дегенеративные изменения нервов. Вначале развивается болезненность вдоль нервных стволов, затем - потеря кожной чувствительности и наступает паралич (бери-бери). Второй важнейший признак заболевания - нарушение сердечной деятельности, что выражается в нарушении сердечного ритма, увеличении размеров сердца и в появлении болей в области сердца. К характерным признакам заболевания, связанного с недостаточностью витамина В1относят также нарушения секреторной и моторной функций ЖКТ; наблюдают снижение кислотности желудочного сока, потерю аппетита, атонию кишечника. 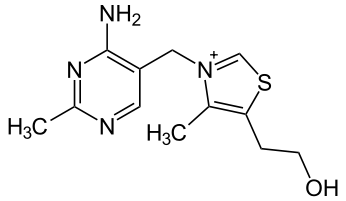 2)Холестерин… Синтез холестерина. Многоэтапный процесс синтеза холестерина (ХЛ) подразделяется на 3 стадии: 1. Образование мевалоновой кислоты из ацетил-КоА, 2. Образование «активного изопрена» и реакции конденсации с образованием сквалена, 3. Реакции циклизации сквалена с образованием стеранового скелета. Начальные реакции синтеза ХЛ сходны с начальными реакциями синтеза кетоновых тел (до образования ОМГ-КоА). Отличием является локализации процессов: синтез кетоновых тел происходит в МХ, а синтез ХЛ-ЦЗ. 1) 2 ацетил-КоА → ацетил-КоА → ОМГ-КоА тиолаза ОМГ-синтаза 2) ОМГ-редуктаза – регуляторный фермент, лимитирующий скорость биосинтеза ХЛ в целом. Её активность подавляется избытком пищевого холестерина. І стадия. Активация мевалоновой кислоты. ІІ стадия. Мевалонат---сквален. Через образование различных эфиров с Р-кислотой(5-фосфорный эфир,5-пирофосфорный эфир). Декарбоксилирование и дефосфорилирование активной мевалоновой кислоты (фермент декарбоксилаза и фосфорилаза). Активный изопрен (изопентинилпирофосфат и димитилаллилпирофосфат ) является предшественником не только ХЛ. В клетках растений и бактерий из него образуются каротиноиды, убихинон, хлорофилл, каучук. Оба изомерных изопентилпирофосфата конденсируются с высвобождением пирофосфата и образованием геранилпирофосфата С10. К геранилпирофосфату вновь присоединяется изопентил пирофосфат, образуя в результате этой реакции фарнезилпирофосфат С15 В заключительной реакции данной стадии в результате НАДФН2- зависимой восстановительной конденсации 2 молекул фарнезилпирофосфата образуется сквален С30 ІІІ стадия. Реакции конденсации изопрена: Сквален (С30) → ланостерин → холестерин. Реакции конденсации и циклизации углеродного скелета требуют большого количества энергии в форме АТФ. Гидроксилирование стеранового кольца предшественника ХЛ протекает с участием монооксигеназной цепи мембран ЭПС. Эфиры ХЛ образуются путем переноса активной жирной кислоты на гидроксильную группу ХЛ. Перенос осуществляют ферменты либо холестерол-ацил- трансфераза(ХАТ) либо лецитин-ХАТ (ЛХАТ). а сутки у здорового человека синтезируется около 2 г ХЛ (с пищей поступает 0,4-0,5 г экзогенного ХЛ). Транспорт ХЛ от печени и кишечника к органам. ХЛ синтезируется в печени как для собственных нужд, так и на «экспорт». Вновь образованный ХЛ и его эфиры включаются вместе с ТАГ в ЛПОНП и поступают в плазму крови. После освобождения ЛПОНП от ТАГ, происходящего на поверхности адипоцитов, из них образуется ЛПНП с высоким содержанием в них ХЛ. На поверхности клеток внутренних органов ЛПНП соединяются с специфическими рецепторами и поглощаются этими клетками. В лизосомах клеток происходит гидролитический распад ЛП. Освободившиеся ХЛ встраивается в клеточные мембраны. Изменение соотношения в плазме фракций ЛП- одна из причин нарушения обмена ХЛ. Пищевой (экзогенный) ХЛ транспортируется ХМ от кишечного эпителия к печени. Избыток ХЛ с желчью выводится в кишечник, где восстанавливается ферментами микрофлоры до копростерина и вместе с небольшим количеством не измененного ХЛ выделяется с калом. Выведению избытка ХЛ из кишечника в значительной мере способствует клетчатка, содержащаяся в пище. Желчнокаменная болезнь. У здорового человека ХЛ в желчи находится в определенном соотношении с ФЛ и желчными кислотами, образую с ними растворимые мицеллы. При увеличении концентрации ХЛ в составе мицелл или снижении содержания желчных кислот и ФЛ, ХЛ выпадает в осадок кристаллизируется и формирует холестериновые камни. Этому способствует застой желчи. 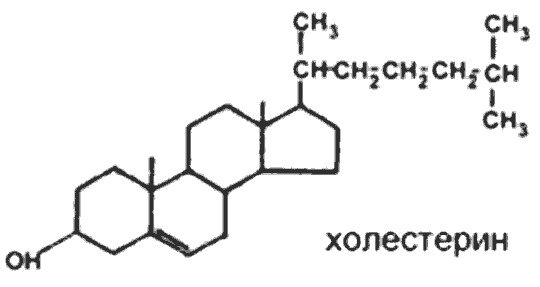 3) сахарная кривая(тетрадь) 4) В хирургическую клинику поступил больной, попавший в автомобильную катастрофу. В крови и моче обнаружено (в динамике) нарастание аминного азота, высокое содержание метионина и цистеина, тирозина и глутаминовой кислоты. Чем можно объяснить эти изменения у данного больного? Нарастание показателей аминного азота является следствием усиленного распада белков, вызванного повреждением тканей. Билет 21 1)Вит В6… ВитаминВ6 (пиридоксин, пиридоксаль, пиридоксамин) В основе структуры витамина В6 лежит пиридиновое кольцо. Известны 3 формы витамина В6, отличающиеся строением замещающей группы у атома углерода в п-положении к атому азота. Все они характеризуются одинаковой биологической активностью. Источники витамина В6 для человека - такие продукты питания, как яйца, печень, молоко, зеленый перец, морковь, пшеница, дрожжи. Некоторое количество витамина синтезируется кишечной флорой. Суточная потребность составляет 2-3 мг. Биологические функции. Все формы витамина В6 используются в организме для синтеза коферментов: пиридоксальфосфата и пиридоксаминфосфата. Коферменты образуются путём фосфорилирования по гидроксиметильной группе в пятом положении пиримидинового кольца при участии фермента пиридоксалькиназы и АТФ как источника фосфата. Клинические проявления недостаточности витамина. Авитаминоз В6 у детей проявляется повышенной возбудимостью ЦНС, периодическими судорогами, что связано, возможно, с недостаточным образованием тормозного медиатора ГАМК, специфическими дерматитами. У взрослых признаки гиповитаминоза В6 наблюдают при длительном лечении туберкулёза изониазидом (антагонист витамина В6). При этом возникают поражения нервной системы (полиневриты), дерматиты 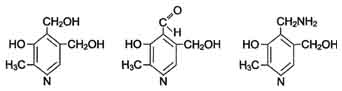 2)Биохим.св-ва раз-я атеросклероза… Факторы риска развития атеросклероза. Основное биохимическое проявление АС – отложение ХЛ в стенках артерий. Болезнь является результатом нарушения любого звена сложной метаболической системы, включающей: 1. синтез ХЛ 2. транспорт и выведение ХЛ 3. рецепция ЛПНП клетками тканей, в т.ч. сосудистой стенки 4. состояние клеточных мембран эндотелия сосудов 5. соотношение ЛПНП и ЛПВП в плазме. Следствием нарушения путей системы является гиперхолестеринемия, преобладание в плазме ЛПНП, которые на фоне поврежденного эпителия сосудов сопровождается увеличением его проницаемости для ХЛ и накопление последнего в сосудистой стенке. Это приводит к нарушению клеток, выведение ХЛ в межклеточное пространство, разрастанию и кальцификации соединительной ткани и образованием атеросклеротических бляшек. ЛПНП (бета-ЛП), вводящие ХЛ в клетки, вызываются атерогенными. ЛПВП (альфа-ЛП) удаляют ХЛ из тканей и поэтому являются антиатерогенными. Вероятность развития атеросклероза прогнозируется «индексом атерогенности», который представляет собой отношение ХЛ в ЛПНП к ХЛ в составе ЛПВП. У взрослых людей до 30 лет индекс 2-2,8; у лиц старше 30 лет 3-3,5. При АС индекс 4-6 и выше. Факторы риска развития АС: 1. Гиподинамия. Следствием её является накопление АТФ, ослабление реакции биологического окисления, торможение реакций ЦТК, усиление свободнорадикального окисления мембранных липидов, гиперхолестеринемия. 2. Гипоксия, следствием которой является ослабление реакций биологического окисления и ЦТК, накопление ацетил-КоА, гиперхолестеринемия. 3. Избыточное УВ питание, способствующие интенсивному синтезу ТАГ и ХЛ. 4. Стресс, следствием которого является мобилизация гликогена, усиленный синтез ТАГ и ХЛ 5. Избыток жиров в рационе. |
