Билет 1 1 белки как основа жизни. Роль белков
 Скачать 1.24 Mb. Скачать 1.24 Mb.
|
|
3) Количественное определение активности трансаминазы в сыворотке крови. 4) Больной страдает от жажды и мочеизнурения. При каких патологических процессах имеются такие симптомы? Как следует проводить биохимическую дифференциальную диагностику? Такие симптомы наблюдаются при сахарном и гипофизарном (несахарном) диабетах. Биохимическими симптомами сахарного диабета являются гипергликемия и глюкозурия. При гипофизарном диабете уровень сахара в крови остается в норме, а полиурия развивается без глюкозурии и является следствием отсутствия вазопрессина. Билет 22 1)Панпотеновая кислота… Пантотеновая кислота (лекарственная форма — пантотенат кальция, витамин B5, неверное обозначение — витамин B3). Пантотеновая кислота требуется для обмена жиров, углеводов, аминокислот, синтеза жизненно важных жирных кислот, холестерина, гистамина, ацетилхолина, гемоглобина. Пантотеновая кислота чувствительна к нагреванию, при термической обработке теряется почти 50 % витамина. Суточная потребность человека в пантотеновой кислоте (5—10 мг) удовлетворяется при нормальном смешанном питании, так как пантотеновая кислота содержится в очень многих продуктах животного и растительного происхождения (дрожжи, икра рыб, яичный желток, зелёные части растений, молоко, морковь, капуста и т. д.). Симптомы гиповитаминоза: 1.усталость 2.депрессия 3.расстройство сна 4.повышенная утомляемость 5.головные боли 6. Тошнота 7. мышечные боли 2)Прямое и непрямое дезамнирование ак… Дезаминирование АК — реакция отщепления α-аминогруппы от АК, в результате чего образуется соответствующая α-кетокислота и выделяется молекула аммиака. Прямое дезаминирование - это дезаминирование, которое происходит в 1 стадию с участием одного фермента. Прямому дезаминированию повергаются глу, гис, сер, тре, цис. Окислительное дезаминирование - самый активный вид прямого дезаминирования АК. 1. Глутаматдегидрогеназа (глу-ДГ) - олигомер, состоящий из 6 субъединиц (молекулярная масса 312 кД), содержит кофермент НАД+. Глу-ДГ катализирует обратимое дезаминирование глу, очень активна в митохондриях клеток практически всех органов, кроме мышц. Глу-ДГ аллостерически ингибируют АТФ, ГТФ, НАДH2, активирует избыток АДФ. Индуцируется Глу-ДГ стероидными гормонами (кортизолом). Реакция идёт в 2 этапа. Вначале происходит ферментативное дегидрирование глутамата и образование α-иминоглутарата, затем — неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется α-кетоглутарат. При избытке аммиака реакция протекает в обратном направлении (как восстановительное аминирование α-кетоглутарата). 2. Оксидаза L-аминокислот. В печени и почках есть оксидаза L-АК, способная дезаминировать некоторые L-аминокислоты: Оксидаза L-АК имеет кофермент ФМН. Т.к. оптимум рН оксидазы L-АК равен 10,0, активность фермента очень низка и вклад ее в дезаминирование незначителен. 3. Оксидаза D-аминокислот. Оксидаза D-аминокислот также обнаружена в почках и печени. Это ФАД-зависимый фермент, с оптимумом рН в нейтральной среде. Оксидаза D-аминокислот превращает, спонтанно образующиеся из L-аминокислот, D-аминокислоты в кетокислоты. 3)Количественное определение общего холестерина в сыворотке крови методом Златкис-Зака. При взаимодействии холестерина с хлоридом железа в присутствии ледяной уксусной кислоты, конц. серной кислоты появляется фиолетовое окрашивание, интенсивность которого пропорциональна содержанию холестерина. 3.9- 6.6 ммоль/л 150 – 250 мг% Гиперхолестеринемия наблюдается при: атеросклерозе, наследственных гиперхолестеринозах, сахарном диабете, гепатитах, нефрозах, ожирении. 4) В стационар поступил больной, у которого выражена желтушность склер, слизистой рта и кожи. Определение какого компонента мочи поможет врачу в постановке правильного диагноза? Объясните происхождение этих компонентов. Данные симптомы имеют общее название «желтуха», в зависимости от пигментного става мочи различают несколько видов «желтух». Гемолитическая – возрастает количество уробилина в моче, паренхиматозная – снижается количество уробилина в моче и появляется прямой билирубин, обтурационная – уробилин в моче полностью отсутствует, а темная окраска мочи обусловлена большой концентрацией прямого билирубина. Билет 23 1)Фолиевая кислота… Фолиевая кислота (витамин Вc, витамин B9). Источники. Значительное количество этого витамина содержится в дрожжах, а также в печени, почках, мясе и других продуктах животного происхождения. Суточная потребность в фолиевой кислоте колеблется от 50 до 200 мкг; однако вследствие плохой всасываемости этого витамина рекомендуемая суточная доза - 400 мкг. Биологическая роль фолиевой кислоты определяется тем, что она служит субстратом для синтеза коферментов, участвующих в реакциях переноса одноуглеродных радикалов различной степени окисленности: метальных, оксиметильных, формильных и других. Эти коферменты участвуют в синтезе различных веществ: пуриновых нуклеотидов, превращении сУМФ в сПГМФ, в обмене глицина и серина. Наиболее характерные признаки авитаминоза фолиевой кислоты - нарушение кроветворения и связанные с этим различные формы малокровия (макроцитарная анемия), лейкопения и задержка роста. При гиповитаминозе фолиевой кислоты наблюдают нарушения регенерации эпителия, особенно в ЖКТ. Витамин В12 (кобаламин). Источники. Это единственный витамин, синтезируемый почти исключительно микроорганизмами: бактериями, актиномицетами и сине-зелёными водорослями. Из животных тканей наиболее богаты витамином В12 печень и почки. Суточная потребность в витамине В12 крайне мала и составляет всего 1-2 мкг. Биологическая роль. Витамин В12 служит источником образования двух коферментов: метилкобаламина в цитоплазме и дезоксиаденозилкобаламина в митохондриях. Основной признак авитаминоза В12 - макроцитарная (мегалобластная) анемия. Для этого заболевания характерны увеличение размеров эритроцитов, снижение количества эритроцитов в кровотоке, снижение концентрации гемоглобина в крови. Нарушение кроветворения связано в первую очередь с нарушением обмена нуклеиновых кислот, в частности синтеза ДНК в быстроделящихся клетках кроветворной системы. 2)Трансаминирование… Трансаминирование — биохимическая ферментативная реакция обратимого переноса аминогруппы с аминокислоты на кетокислоту без промежуточного образования аммиака. Ферменты, катализирующие процесс, назвали трансаминазами, или аминотрансферазами. Продуктами чаще всего являются аланин, аспарагин и глутамат, так как соответствующие им кетокислоты образуются в процессе метаболизма углеводов. Трансаминирование играет важную роль в процессах мочевинообразования, глюконеогенеза, путях образования новых аминокислот. Трансаминирование аминокислот с образованием глутаминовой кислоты в сочетании с ёё дезаминированием НАД(Ф)-зависимой глутаматдегидрогеназой называется непрямым дезаминированием аминокислот (трансдезаминирование). 3) Белок плазмы крови А) экспресс-метод (метод «висящей» капли) В основу метода положена зависимость между содержанием белков в плазме и цельной крови и ее удельным весом. Определение удельного веса плазмы и цельной крови осуществляется путем погружения капли в растворы CuSO4 известного веса. Тот раствор CuSO4 , в котором капля сначала повисает, а затем опускается, равен удельному весу исследуемой жидкости. 65-85 г/л 6.5-8.5 мг% Гиперпротеинемия – увеличение общего содержания белков плазмы крови наблюдается при диарее у детей, рвоте, непроходимости верхнего отдела тонкой кишки, обширных ожогах. Потеря воды организмом приводит к повышению концентрации белка в крови: а) относительная гиперпротеинемия связана с потерей воды организмом (диарея, рвота, ожоговая болезнь, травмы); б) абсолютная гиперпротеинемия обусловлена резким нарастанием глобулинов при инфекциях, а также синтезом патологических белков или белков «острой фазы». Гипопротеинемия – снижение общего содержания белков плазмы может быть обусловлено с несколькими причинами: а) нарушение белок-синтезирующей функции печени (паренхиматозная желтуха, гепатиты, цирроз печени). Происходит снижение белкового коэффициента за счет снижения синтеза альбуминов; б) задержкой воды при заболеваниях сердечно-сосудистой системы; в) потерей белка с мочой при патологии почек; г) кровопотерями при травмах и операциях Б) биуретовый метод Метод основан на образовании биуретового комплекса Cu(OН)2 с пептидными связями, имеющего розово-фиолетовое окрашивание. Интенсивность окраски пропорциональна количеству пептидных связей. В) метод Лоури. Метод основан на способности белков образовывать окрашенные комплексы синего цвета при осуществлении двух цветных реакций – биуретовой и реакции Фолина (восстановление белками смеси фосфорновольфрамовой и фосфорномолиюденовой кислот – реактив Фолина). Интенсивность окраски зависит от количества белка. 4) Больной диабетом худеет. Объясните почему? У больных диабетом, нелеченных инсулином, бывают обмороки. Объясните почему? При сахарном диабете, нехватка инсулина приводит к невозможности тканей утилизировать глюкозу, в этом случае в клетках наблюдается нехватка энергии и подключается альтернативный источник – жиры, которые распадаются до Ацетил-КоА. Транспортной формой его по крови являются кетоновые тела, их избыток токсичен для мозга и может вызвать обмороки и кому. Билет 24 1)Витамин Е и К… Витамины группы Е (токоферолы) найдены в природных источниках. Все они - метальные производные исходного соединения токола, по строению очень близки и обозначаются буквами греческого алфавита. Наибольшую биологическую активность проявляет α-токоферол. Источники витамина Е для человека - растительные масла, салат, капуста, семена злаков, сливочное масло, яичный желток. Суточная потребность взрослого человека в витамине примерно 5 мг. Биологическая роль. По механизму действия токоферол является биологическим антиоксидантом. Он ингибирует свободнорадикальные реакции. Клинические проявления недостаточности витамина Е. Дефицит витамина Е проявляется развитием гемолитической анемии. Витамины К (нафтохиноны) существует в нескольких формах в растениях как филлохинон (К1), клетках кишечной флоры как менахинон (К2). Источники витамина К - растительные (капуста, шпинат, корнеплоды и фрукты) и животные (печень) продукты. Суточная потребность в витамине взрослого составляет 1-2 мг. Биологическая функция витамина К связана с его участием в процессе свёртывания крови. Он участвует в активации факторов свёртывания крови. Витамин К участвует в реакциях карбоксилирования в качестве кофермента. Основное проявление авитаминоза К - сильное кровотечение, часто приводящее к шоку и гибели организма 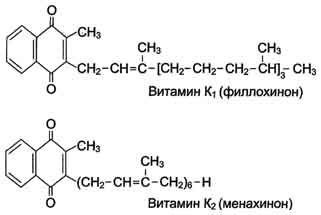 2)Мочевина как конечный продукт… Мочевина — химическое соединение, диамид угольной кислоты. Белые кристаллы, растворимые в полярных растворителях (воде, этаноле, жидком аммиаке). Мочевина является конечным продуктом метаболизма белка у млекопитающих. Производные нитрозомочевин находят применение в фармакологии в качестве противоопухолевых препаратов. Анализ на мочевину входит в биохимический анализ крови. Нормы:
Синтез мочевины — циклический процесс состоит из пяти реакций, катализируемый пятью отдельными ферментами. Суммарное уравнение: СO2+NH3+2H2O+Аспарат → H2N—CO—NH2+Фумарат. При недостаточной активности ферментов орнитинового цикла возникают гипераммониемии — патологические состояния сопровождающиеся повышением концентрации аммиака в крови. 3) Количественное определение глюкозы в крови глюкозооксидазным методом. Глюкоза окисляется глюкозооксидазой с образованием Н2О2. Перекись водорода образует окрашенное соединение с энзимохромогенным реактивом, интенсивность которого соответствует концентрации глюкозы. Определение на ФЭКе. 3.3 – 5.5 ммоль/л 60 - 100 мг% Гипергликемии наблюдаются при: сахарном диабете, с. Иценко-кушинга, акромегалии, панкреатитах, тиреотоксикозе, феохромоцитоме, шоке. Также при увеличении приема глюкозы в пище, при психическом возбуждении. Гипогликемии наблюдаются при: мальабсорбции дисахаридов и глюкозы-галактозы, галактоземии, гликогенозах I, II, VI, гипогликемии новорожденных, инсулиновом шоке, ацетономической –рвоте, квашиоркоре, болезни Аддисона, гипофункции гипофиза, щитовидной железы. 4. У больного желтуха. Какие причины могут привести к этому заболеванию? В чем сущность биохимической диагностики желтухи? Для правильной постановки диагноза необходимо определить пигментный состав крови, мочи и кала. При усиленном гемолизе эритроцитов (гемолитическая желтуха) – увеличивается уровень общего билирубина в крови, стеркобилина в кале и уробилина в моче; при нарушении целостности гепатоцитов (паренхиматозная желтуха) - увеличивается уровень общего билирубина в крови, снижается количество стеркобилина в кале и уробилина в моче, появляется в моче прямой билирубин; при нарушении оттока желчи (обтурационная желтуха) - увеличивается уровень общего билирубина в крови, отсутствует стеркобилин в кале и уробилин в моче, а темная окраска мочи обусловлена большой концентрацией прямого билирубина. Билет 25 1)Гормоны-регуляторы обм.процессов… Гормоны – вещества органической природы, вырабатывающиеся в специализированных клетках желез внутренней секреции, поступающие в кровь и оказывающие регулирующее влияние на обмен веществ и физиологические функции. В это определение необходимо внести соответствующие коррективы в связи с обнаружением типичных гормонов млекопитающих у одноклеточных (например, инсулин у микроорганизмов) или возможностью синтеза гормонов соматическими клетками в культуре ткани (например, лимфоцитами под действием факторов роста). Гормоны классифицируют в зависимости от места их природного синтеза, в соответствии с которым различают гормоны гипоталамуса, гипофиза, щитовидной железы, надпочечников, поджелудочной железы, половых желез, зобной железы и др. Современная классификация гормонов, основанной на их химической природе. В соответствии с этой классификацией различают три группы истинных гормонов: 1) пептидные и белковые гормоны, 2) гормоны – производные аминокислот 3) гормоны стероидной природы. Четвертую группу составляют эйкозаноиды – гормоноподобные вещества, оказывающие местное действие. Пептидные и белковые гормоны включают от 3 до 250 и более аминокислотных остатков. Это гормоны гипоталамуса и гипофиза (тиролиберин, соматолиберин, соматостатин, гормон роста, кортикотропин, тиреотропин), а также гормоны поджелудочной железы (инсулин, глюкагон). Гормоны – производные аминокислот в основном представлены производными аминокислоты тирозина. Это низкомолекулярные соединения адреналин и норадреналин, синтезирующиеся в мозговом веществе надпочечников, и гормоны щитовидной железы (тироксин и его производные). Гормоны 1-й и 2-й групп хорошо растворимы в воде. Гормоны стероидной природы представлены жирорастворимыми гормонами коркового вещества надпочечников (кортикостероиды), половыми гормонами (эстрогены и андрогены), а также гормональной формой витамина D. Эйкозаноиды, являющиеся производными полиненасыщенной жирной кислоты (арахидоновой), представлены тремя подклассами соединений: простагландины, тромбоксаны и лейкотриены. Эти нерастворимые в воде и нестабильные соединения оказывают свое действие на клетки, находящиеся вблизи их места синтеза. Гормоны первого типа связываются поверхностными рецепторами, расположенными на плазматической мембране. Различают три вида взаимодействия гормонов с плазматической мембраной. При взаимодействии первого вида гормонрецепторный комплекс, находящийся на поверхности клеток, вызывает образование так называемого второго посредника — циклического аденозин-3,5-монофосфата (цАМФ), и последующие действия гормона опосредуются цАМФ. Этот механизм характерен для некоторых белковых гормонов и биогенных аминов. При взаимодействии второго вида рецептор клеточной поверхности индуцирует продукцию или высвобождение иных вторых посредников, например кальция. Этот механизм характерен для некоторых нейротрансмиттеров и РТГ. При взаимодействии третьего вида комплекс поверхностный рецептор — гормон интернализуется внутрь клетки. К последней категории гормонов относится инсулин. Некоторые гормоны, такие как стероидные гормоны и гормоны щитовидной железы, по свойствам являются гидрофобными. В плазме крови для их транспортировки используются специальные белки-транспортеры. В комплексе с этими белками они не способны взаимодействовать с мембранными рецепторами, но способны отрываться от них и диффундировать через клеточную мембрану внутрь клетки. После перехода в цитозоль гормоны немедленно подхватываются другими белками, которые уже являются рецепторами. Комплекс гормон-рецептор в некоторых случаях дополнительно модифицируется и активируется. Далее он проникает в ядро, где может связываться сядерным рецептором. В результате гормон приобретает сродство к ДНК. Связываясь с гормон-чувствительным элементом в ДНК, гормон влияет на транскрипцию определенных генов и изменяет концентрацию РНК в клетке и, соответственно, количество определенных белков в клетке 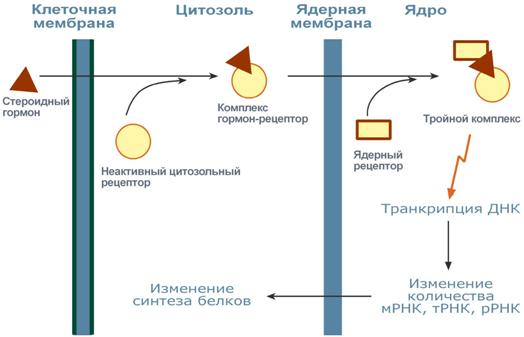 |
