|
|
Шпора по химии №1(ULTIMATE). Билет 1 Химический элемент
БИЛЕТ №4 Атом - наименьшая частица химического элемента. Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов. В ядро атомов всех элементов (за исключением 'Н) входят протоны и нейтроны. Протон (р ) - элементарная частица с единичным положительным зарядом и массой покоя 1,00728. Число протонов в ядре определяет заряд ядра и принадлежность атома к данному химическому элементу. Нейтрон (п°)-элементарная частица, не обладающая зарядом, с массой покоя 1,00867. Сумма протонов и нейтронов называется массовым числом атома (ядра). Атомы, обладающие одинаковым зарядом ядра, но разным числом нейтронов, называются изотопами данного химического элемента. Электрон (е") - элементарная частица с единичным отрицательным зарядом.
При всех химических процессах ядра атомов элементов не изменяются. Энергия химических превращений связана только с энергией электронов.
Идея о том что все вещества состоят из атомов возникла до н.э. – Эвклид. Далее Эпикур выдвинул идею о том, что атомы взаимодействуют между собой и образует вещества. В начале XIX века Дальтон – составил основные положения строения атома. Факты подтверждающие:
- Фотоэффект – явление отрывания е, с поверхности металлов под действием света.
- Открытие катодных лучей.
- Рентгеновское излучение – происходит под действием катодных лучей.
- Явления радиоактивности.
Модели атомов:
Томпсон:
Резерфорд:
nZ+=ne.
В 1920 г. Чедвиг – заряд ядра равен порядковому номеру в таблице Менделеева. Св-ва простых веществ, а также свойства и формы их соединений находятся в периодической зависимости от заряда ядра атома. Недостатки: Атом вечен и устойчив. Спектр излучения атомов линейчатые спектры говорят о том, что энергия излучения е не может быть любой, а имеет дискретный характер.
Квантовая теория света: свет распространяется порциям (фотонами) E=h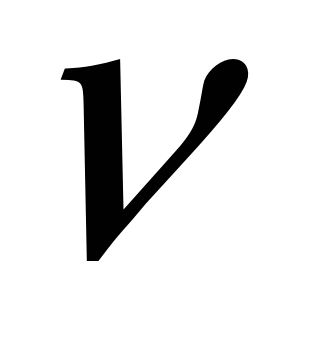 . Столетов в 1890 г. Изучая фотоэффект установил, что величина потоков е зависит от величины освещенности. А энергия фото-е зависит только от . Столетов в 1890 г. Изучая фотоэффект установил, что величина потоков е зависит от величины освещенности. А энергия фото-е зависит только от 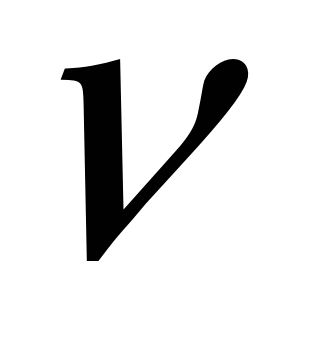 . .
Основные положения КТС:
- Фотон – это неделимая порция энергии которая взаимодействует с е атомов металла.
- Фотон ведет себя подобно матер. Частицам.
- Фотон отличается от классической частицы тем, что его местоположение точно определить невозможно как для любой волны.
- Фотон отличается от волны тем, что его нельзя поделить на части.
|
Бор сослался на планетарную модель Резерфорда, учел квантовую природу света и линейчатый спектр. Постулаты Бора:
- е вращается вокруг ядра не по любым, а лишь по некоторым орбиталям, которые называются стационарными.
- Двигаясь по стац. орбиталям е не излучает энергии.
- Излучение происходит при скачкообразном переходе е с одной орбиты на другую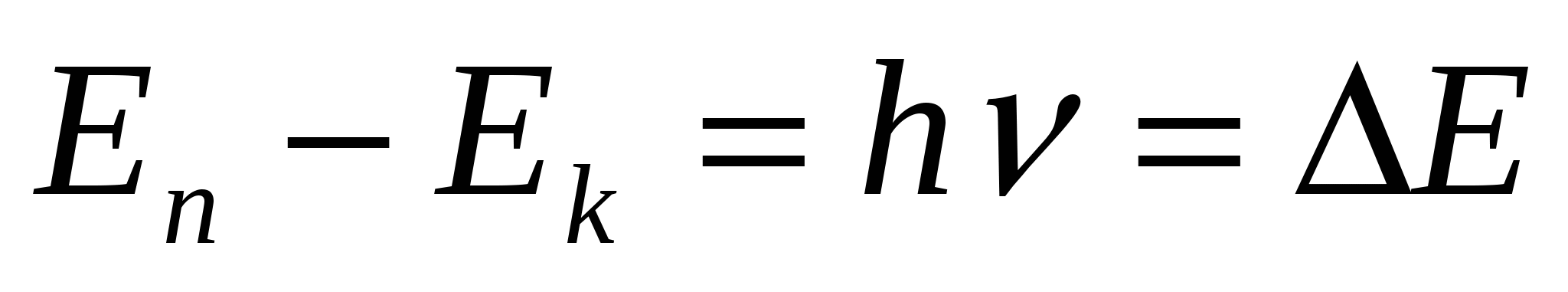 , , 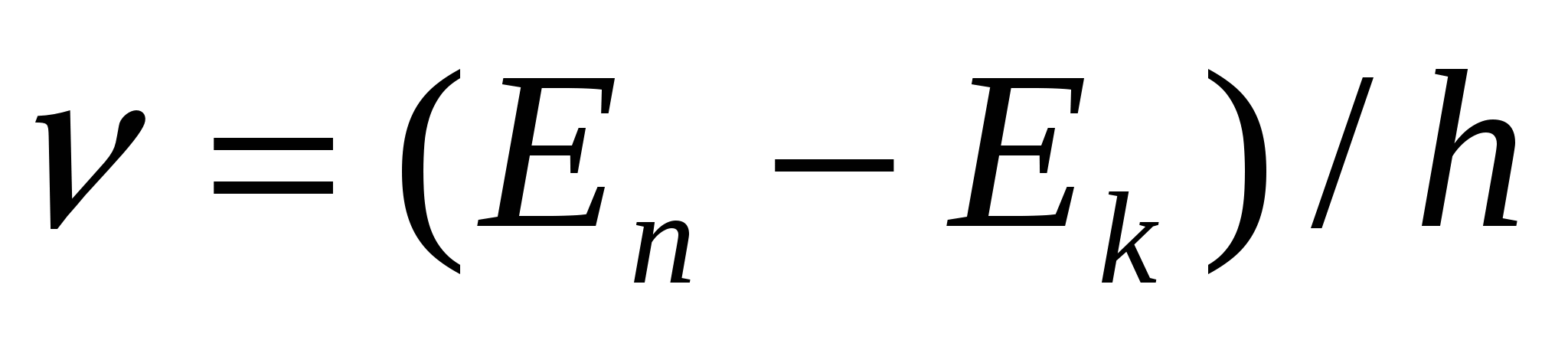 . .
Противоречия: Где находится е в момент перескока, сверхтонкое расщепление, образование хим. связи Околоядерное пространство, где с наибольшей вероятностью может находиться электрон, называется атомной орбиталыо (АО). Она характеризуется тремя координатами-квантовыми числами, определяющими размер (л), форму (/) и ориентацию (т/) АО в пространстве.
Решение уравнения Шреденгера показывает что распределение е в атоме описывается тремя квантовыми числами. Главное квантовое число (n) определяет энергетический уровень электрона в атоме. Для электронов в невозбужденных атомах п принимает значения от 1 до 7 (соответственно номеру периода в ПСЭ). Совокупность электронов с одинаковым n - электронный слой:
Главное квантовое число я 1234567
Электронный слой К L М N О Р Q
Орбитальное квантовое число (/) указывает на различие энергий связи электронов в пределах одного энергетического уровня, определяет форму электронного облака и принимает целочисленные значения от 0 до ( п - I). Для я = 1 / = 0; для я = 2 / = О, 1; для я = 3 / = О, 1, 2, для я = 4 / = 0,1,2,3. Электроны данного энергетического уровня группируются в подуровни; число подуровней на каждом уровне равно я. Больше четырех подуровней не заполняется, т.к. для описания электронов в атомах всех известных элементов достаточно значений / = 0,1,2,3.
Орбитали с / = 0,1,2,3 называют s-, p-, d-, f-орбиталями, соответственно, а электроны, занимающие эти орбитали, называются - s-, p-, d-, f- электронами.
Магнитное квантовое число - т характеризует магнитный момент и пространственное расположение электронного облака Число возможных значений т при заданном / равно
21+1, при этом т изменяется от -/ до +/. Так при / =2 miимеет 5 значений:-!, -1. О, 1,2.
Спиновое квантовое число - sхарактеризует движение электрона вокруг своей оси. sимеет всего два значения: +1/2 и -1/2.
Распределение электронов в атомах по атомным орбиталям определяется принципом Паули, принципом наименьшей энергии и правилом Хунда.
|
|
БИЛЕТ №5 Принцип Паули. В атоме не может быть двух электронов, имеющих одинаковый набор всех четырех квантовых чисел. Максимальное число электронов на уровне N = 2п2. Так как каждая атомная орбиталь описывается лишь тремя квантовыми числами ( л, /, т ), то на ней может находиться не более двух электронов с противоположными спинами (+1/2, -1/2).
Принцип наименьшей энергии. Последовательность размещения электронов по атомным орбиталям в невозбужденном атоме должна отвечать наибольшей связи их с ядром, т.е. электрон должен обладать наименьшей энергией. Поэтому сначала заполняются те подуровни, для которых сумма значений п+lявляется меньшей; если суммы значений л+/ равны, то сначала идет заполнение подуровня с меньшим значением п - главного квантового числа.
Шкала энергий:
Is2<2s2<2p6<3s2<3p6<4s2<3d10<4p6<5s2<4d10<5p6<6s2<5d1<4f14<5d2-10<6p6<7s2<6d1<5f44<6d2-10<7p6, где s,p,d,f - энергетические подуровни, цифра впереди букв означает номер энергетического уровня, на котором находятся электроны; индекс наверху справа показывает максимальное число электронов на подуровне.
Из шкалы энергий видно, что после Зр-подуровня ( п+l= 3+1=4 ) заполняется 48-подуровень (п+1 - 4+0 = 4 ), затем Sd-nonypoeeHb ( я+/ = 3+2 =5), 4р-подуровень ( п+1 =4+1=5) и 58-подуровень (л+/ = 5+0=5).
Правило Хунда. Орбитали в пределах данного подуровня заполняются так, чтобы суммарное спиновое число электронов на подуровне было максимально. Суммарный спин спаренных электронов равен нулю (-1/2+1/2=0).
Энергетическое состояние электрона схематически можно представить в виде квантовых ячеек. Для s-электронов (/=0) отводится одна ячейка, где может быть один (s =+1/2)] или два электрона (я = +1/2 и s = -1/2), для р-электронов отводится три ячейки, где может быть от 1 до 6 электронов; для d-электронов (/=2) отводится пять ячеек, где может быть от 1 до 10 электронов; для f-злектронов (/=3) отводится семь ячеек, где может быть от 1 до 14 электронов
|
БИЛЕТ №6 Строение электронных оболочек атомов тесно связано с ПСЭ Д.И.Мендедеева. Если провести вертикальную черту в шкале энергий перед каждым значением главного квантового числа л, то получим максимальную емкость энергетического уровня, а также число элементов в периоде: n=1 (I период), емкость 2 элемента, я=2 (II период) - емкость 8 элементов; n=3 (III период) – 8 элементов; n=4 (IV период) - 18 элементов; n=5 (V период) -18 элементов; n=6 (VI период) - 32 элемента, n =7 (VII период) - 32 элемента. В зависимости от того, на какой энергетический подуровень в атоме поступает последний электрон,
химические элементы делятся на s-, p-, d-, f-элементы. Их положение в ПСЭ следующее:
s-элементы I, II группы, главные подгруппы - (ns1, ns2) (H2, He); р-элементы III - VIII группы, главные подгруппы (ns2np1"6); d-элементы I - VIII группы, побочные подгруппы [ns2(n-l)dM0]; f-элементы III группа, побочная подгруппа- лантаноиды и актиноиды
Валентные электроны у s- и р-элементов находятся на внешнем энергетическом уровне, у
d-элементов-на s-подуровне внешнего энергетического уровня (ns2) и предвнешнего (n-l^1"10
незавершеного подуровня.Свойства элементов тесно связаны со строением их атомов. «Периодическая повторяемость свойств элементов обусловлена периодическим повторением электронных оболочек атомов» - это современная формулировка периодического закона. Созданная Менделеевым периодическая
система элементов является графическим выражением периодического закона. Атомы элементов в
одной подгруппе данной группы имеют одинаковую электронную конфигурацию. Для главных
подгрупп ПСЭ связь между электронной конфигурацией и числом валентных электронов атомов
можно представить в виде :
Номер периода
|
I
|
II
|
III
|
IV
|
V
|
VI
|
VII
|
VIII
|
Электронная конфигурация внешнего слоя (валентные электроны)
|
ns1
|
ns2
|
ns2np1
|
ns2np2
|
ns2np3
|
ns2np4
|
ns2np5
|
ns2np6
|
|
s-элементы
|
р-элементы
|
Химические свойства элемента зависят от способности его атома терять (А°- е = А+1) или обретать (А°+е = А") электроны, превращаясь в положительно или отрицательно заряженные ионы. Это количественно оценивается через энергию ионизации атома и энергию сродства атома к электрону.
|
|
БИЛЕТ №7 Относительная электроотрицательность ОЭО - получается отношением ЭО элемента к ЭО атома фтора, для которого значение ОЭО принято равным 4. Величина ОЭО позволяет оценить способность атома элемента к оттягиванию на себя электронной плотности атомов других элементов.
В ПСЭ Д.И. Менделеева в пределах главных подгрупп (s-, р-элементы) сверху вниз значения ОЭО уменьшаются, следовательно, в главных подгруппах сверху вниз увеличиваются металлические и восстановительные свойства элементов, основные свойства их гидроксидов.
В периодах ПСЭ слева направо значения ОЭО увеличиваются, следовательно, здесь постепенно ослабляются металлические и нарастают окислительные свойства. Самый активный неметалл F, он же наиболее сильный окислитель. Самые активные металлы Fr, Cs, Rb являются наиболее сильными восстановителями, а их гидроксиды - самыми сильными основаниями.
Номер группы ПСЭ, в которой стоит элемент, показывает высшую степень окисления его атома в химических соединениях, его высшую валентность. Исключение составляют кислород, фтор (р-семейство); медь, серебро, золото и некоторые другие элементы d-семейства могут проявлять в соединениях валентность большую, чем номер группы.
|
Номер периода
|
Степень окисления
1—————————————
|
I
|
II
|
III
|
IV
|
V
|
VI
|
VII
|
VIII
|
|
Высшая
|
+1
|
+2
|
+3
|
+4
|
|
+5
|
+6
|
+7
|
0
|
Низшая
|
-
|
-
|
-
|
-4
|
-3
|
-2
|
-1
|
0
|
|
Форма и свойства соединений данного элемента зависят от степени окисления его атомов. Если элемент проявляет переменную степень окисления и образует несколько оксидов и гидроксидов, то с ее увеличением их свойства меняются от основных через амфотерные к кислотным. Например, Мn образует пять оксидов: МnО, Мn2О3, MnO2, МnО3, Mn2O7? Первые два обладают основными свойствами (Мn(OH)2, Мn(OH)3, МnО2 амфотерен (MnO(OH)2, Н2МnО3), а последние два МnО3 и Мn2О7 - кислотообразующие, являются ангидридами марганцовистой (Н2МnО4) и марганцевой кислот (HMnO4), соответственно (МnО3 и Н2МnО4 в свободном состоянии не выделены, а их существование можно предположить по образованию солей марганцовистой кислоты манганатов).
Используя представления о распределении металлических и неметаллических свойств элементов в периодах, а также о зависимости высшей степени окисления от номера группы, можно изменения химических свойств элементов III периода представить в следующей таблице:
Номер группы
|
I
|
II
|
III
|
IV
|
V
|
VI
|
VII
|
Элемент
|
Na
|
Mg
|
Al
|
Si
|
P
|
S
|
Cl
|
Валентные электроны
|
3s1
|
3s2
|
3s23p1
|
3s23p2
|
3s23p3
|
3s23p4
|
3s23p5
|
Высшая степень окисления
|
+1
|
+2
|
+3
|
+4
|
+5
|
+6
|
+7
|
Формула оксида
|
Na2O
|
MgO
|
Al2O3
|
SiO2
|
P2O5
|
SO3
|
Cl2O5
|
Формула гидроксида
|
NaOH
|
Mg(OH)2
|
Al(OH) 3 H3AlO3
|
H2SiO3
|
H3PO4
|
H2SO4
|
HClO4
|
Химический характер гидроксида
|
основной
|
основной
|
амфотерный
|
кислый
|
кислый
|
кислый
|
кислый
|
| | |
|
|
 Скачать 0.71 Mb.
Скачать 0.71 Mb.