ПосФХпроцЧ1.АтмосфХОС05. Физикохимические процессы в атмосфере
 Скачать 1.58 Mb. Скачать 1.58 Mb.
|
|
САРАТОВСКИЙ ВОЕННЫЙ ИНСТИТУТ РАДИАЦИОННОЙ, ХИМИЧЕСКОЙ И БИОЛОГИЧЕСКОЙ ЗАЩИТЫ Т.Г. ДМИТРИЕНКО ФИЗИКО-ХИМИЧЕСКИЕ ПРОЦЕССЫ В АТМОСФЕРЕ Учебное пособие САРАТОВ - 2006 ББК 20.1 я 73 Т.Г. Дмитриенко Ф  изико-химические процессы в атмосфере: Учебное пособие. – Саратов: СВИРХБЗ, 2006. – 103 с. изико-химические процессы в атмосфере: Учебное пособие. – Саратов: СВИРХБЗ, 2006. – 103 с.Учебное пособие по химии окружающей среды охватывает вопросы физико-химических процессов, происходящих в атмосфере, и подготовлено традиционным способом: включает теоретическое введение, примеры решения типовых задач и задачи для самостоятельного решения. Пособие содержит вопросы и задачи для самостоятельной подготовки к учебному модулю, являющимся итоговой оценкой по теме: «Физико-химические процессы в атмосфере». Приводимое в учебном пособии краткое изложение темы курса, примеры решения задач, вопросы для самопроверки и контрольные задачи должны способствовать повышению эффективности самостоятельной работы студентов, являющейся основой успешного образования. Структура пособия соответствует традиционной структуре курса «Химия окружающей среды» и может быть использовано для подготовки к семинарским и практическим занятиям. Рецензенты: доктор химических наук, профессор Древко Б.И. кандидат химических наук, доцент Ястребова Н.И.  Саратовский военный институт радиационной, химической и биологической защиты, 2006 ФИЗИКО-ХИМИЧЕСКИЕ ПРОЦЕССЫ В АТМОСФЕРЕПредмет и содержание курса «Химия окружающей среды» Химия окружающей среды базируется на основных законах и понятиях классической химии, однако объекты исследования в этом случае находятся в биосфере. Необходимо подчеркнуть; что химия окружающей среды как сравнительно молодая область знания в настоящее время интенсивно развивается в нашей стране и за рубежом. Предметом курса «Химия окружающей среды» являются основные физико-химические процессы, протекающие с участием абиотических компонентов биосферы в естественных условиях, и изменения в этих процессах, связанные с влиянием антропогенных факторов. Усиление техногенного воздействия на природную среду вызвало деградацию качества окружающей среды и породило целый ряд связанных с этим проблем, наиболее острая из которых – состояние атмосферного воздуха. По сравнению с другими земными оболочками атмосфера имеет ряд присущих только ей особенностей – высокую подвижность, изменчивость ее компонентов, своеобразие физико-химических процессов. Состояние атмосферы определяет тепловой режим поверхности Земли, ее озоновый слой защищает живые организмы от жесткого ультрафиолетового излучения. Распределение тепла и влаги в атмосфере – основная причина существования природных зон на Земле, определяющих особенности гидрологического режима, состояние почвенно-растительного покрова и важные процессы формирования рельефа. Физико-химические превращения компонентов атмосферы являются важнейшим разделом химии окружающей среды. Специфические особенности этих превращений связаны как с природными (фаза солнечной активности, географическое положение, время суток), так и с антропогенными факторами. Знание механизмов и кинетики образования конечных продуктов реакций необходимо для разработки методов защиты окружающей среды от промышленных загрязнений. 1. Состав и строение атмосферы Общая масса газовой оболочки нашей планеты – атмосферы – составляет 5,14 . 1015 т. Это примерно одна миллионная часть массы Земли. Состав атмосферы претерпевал серьезнейшие изменения в различные геологические эпохи. В настоящее время состав атмосферы находится в состоянии динамического равновесия, поддерживаемого в результате действия живых организмов, геохимических явлений и хозяйственной деятельности человека. Таблица 1. Состав атмосферы вблизи земной поверхности
Главными компонентами атмосферы (таблица 1) являются азот, кислород и аргон: на их долю в приземном слое приходится соответст-венно 78,21 и 0,9% (об.). На долю всех остальных компонентов приходится менее 0,1% (об.), но роль их в общей динамике состояния атмосферы чрезвычайно велика. Объемные концентрации постоянно содержащихся в атмосфере (так называемых «квазипостоянных») компонентов (N2, О2, Аr, Не, Хе, Кr, Н2) остаются практически неизменными вплоть до высоты 100 км. Содержание других («активных») газов и аэрозолей существенно меняется в зависимости от сезона, географического положения и высоты над уровнем моря. Антропогенное влияние на состав атмосферы ограничено в основном изменениями концентрации «активных» газов и аэрозолей. Для измерения содержания примесей в атмосфере помимо % (об.) часто используются другие единицы измерения концентрации газообразных компонентов в смеси. Для выражения объемной концентрации широкое распространение получили млн–1 и млрд–1 (в англоязычном варианте – ppm и ррb соответственно). Эти единицы измерения показывают количество объемов данной примеси в одном миллионе или миллиарде объемов газовой смеси. Массовые концентрации примесей определяют массу соответствующей примеси в единице объема газовой смеси. Наиболее часто для выражения массовых концентраций «активных» примесей в газовой фазе используются такие единицы, как мг/м3 или мкг/м3. Содержание примесей в воздухе измеряют и по количеству молекул соответствующих газов в кубическом сантиметре или кубическом метре воздуха – мол./см3 или мол./м3; часто слово «молекула» («мол.») опускается и дается упрощенная запись – см –3 или м –3. Содержание газов и паров в воздухе может быть выражено и их парциальным давлением. В этом случае используются стандартные единицы измерения давления Па или кПа (в СИ). В литературе встречаются и устаревшие единицы измерения давления – атмосфера (атм), миллиметры ртутного столба (мм рт. ст.), бар и торр. Одним из важных показателей, характеризующих поведение примесей в атмосфере, является время их пребывания в рассматриваемом объеме атмосферы. В случае динамического равновесия – равенства скоростей поступления примеси из всех возможных источников и суммарного стока примеси из резервуара – время пребывания примеси и ее общая масса в резервуаре связаны уравнением: Qисточник = Qсток = А/ (1) где Qисточник и Qсток – скорости поступления и стока вещества соответст-венно для произвольного резервуара, атмосферы в целом или ее части (единицы массы/единицы времени); А – общая масса примеси, содержащейся в произвольном резервуаре, атмосфере в целом или в ее части (единицы массы); – время пребывания примеси в произвольном резервуаре, атмосфере в целом или в ее части (единицы времени). По вертикали атмосфера имеет слоистое строение. Наиболее распространенное деление атмосферы на слои основано на изменении температуры с высотой. По мере удаления от поверхности Земли температура сначала снижается (тропосфера), затем практически не меняется (тропопауза), в дальнейшем начинает повышаться (стратосфера), на определенном участке опять остается практически неизменной (стратопауза), вновь начинает падать (мезосфера), проходит через слой с практически неизменными значениями (мезопауза) и далее увеличивается (термосфера). Представленные в таблице 2 и на рисунке 1 сведения характеризуют температурные границы соответствующих слоев для так называемой «стандартной атмосферы», в которой не принимаются во внимание участки с неизменной по высоте температурой. Безусловно, в реальных условиях границы соответствующих слоев не являются строго фиксированными и меняются в достаточно больших пределах, однако профили температур в слоях остаются неизменными. Использование понятия «стандартной атмосферы» облегчает задачу определения параметров атмосферы на заданной высоте и позволяет провести необходимые оценки.   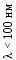 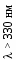 Рис. 1. Строение атмосферы Таблица 2. Характеристика изменения температуры в основных слоях, выделяемых в атмосфере
Очень часто отдельные слои атмосферы объединяют в две группы. При этом тропосферу и стратосферу относят к «нижним слоям атмосферы», а мезосферу и термосферу объединяют понятием «верхние слои атмосферы». Ионизованная часть верхних слоев атмосферы называется ионосферой. Верхние слои атмосферы по составу образующих их компонентов в значительной степени отличаются от нижних слоев. Нижние слои более плотные, в них сосредоточена основная масса атмосферы; известно, что около 50% общей массы атмосферы приходится на нижний слой толщиной всего 5 км, а масса слоя в 30 км составляет примерно 90% всей массы атмосферы. При нормальных условиях газы, входящие в состав атмосферы, мало отличаются по своему поведению от идеального газа. Поэтому для реальной атмосферы справедлива формула, представляющая собой уравнение состояния идеального газа: P = nkT, (2) где P – давление газа; n – концентрация частиц; k– постоянная Больцмана; Т – температура. Распределение давления в атмосфере по высоте Hописывается так называемой «барометрической формулой»: Pн = где 0иP0 – плотность и давление при Н = 0 (т. е. на уровне моря), причем Р0 = 101,3 кПа; g – ускорение силы тяжести. Если выражать высоту в километрах, то барометрическую формулу удобно представить (принимая Т = 273 К) в следующем виде: Pн = P0 exp(–H/7,99), (4) Распределение концентрации составляющих атмосферу компонентов по высоте имеет вид: nH = n0exp[-mqH/(kT)]=n0exp[-MqH/(RT)],(5) где m – масса молекулы компонента; n0 – количество молекул в единице объема на высоте Н = 0 (на уровне моря); k – постоянная Больцмана; М – молярная масса газа; R – универсальная газовая постоянная. Атмосфера Земли, как и атмосферы других планет, не находится в равновесном состоянии. Вследствие этого ее температура не постоянна, а изменяется по высоте. Если бы равновесное состояние было возможно, то плотность атмосферы должна была бы изменяться с высотой по формуле Больцмана, которая принимает в этом случае вид n(r) = n(r0)exp{–[GmM/(kT)] (1/ro-1/r)}, (6) где учтено выражение для потенциальной энергии U(r)частицы массы m в поле тяготения шарообразного небесного тела массы М: U(r) = где G – гравитационная постоянная; r0 – радиус планеты; r– расстояние от центра планеты до частицы. Формула (6) показывает, что при r плотность стремится к пределу: n(r n(r0)exp{–[GmM/(kT)] 1/r0} (8) Если в атмосфере имеется конечное число молекул, то они должны быть распределены по всему космическому пространству, т.е. атмосфера рассеяна. Поскольку в конечном счете все системы стремятся к равновесно-му состоянию, то атмосфера планет постепенно рассеивается. У некоторых из небесных тел, например у Луны, атмосфера полностью исчезла, другие, например Марс, имеют очень разреженную атмосферу. Таким образом, атмосфера Луны уже достигла равновесного состояния, а атмосфера Марса близка к достижению равновесного состояния. У Венеры атмосфера очень плотная и, следовательно, находится в начале пути к равновесному состоянию. Для количественного рассмотрения вопроса о потере атмосферы планетами необходимо принять во внимание распределение молекул по скоростям. Силу земного притяжения могут преодолеть лишь молекулы, скорость которых превосходит вторую космическую. Эти молекулы находятся в «хвосте» распределения Максвелла – Больцмана и их относительное число невелико. Тем не менее за значительные промежутки времени потеря молекул является чувствительной. Поскольку вторая космическая скорость у тяжелых планет больше, чем у легких, интенсивность потери атмосферы у массивных небесных тел меньше, чем у легких, т, е. легкие планеты теряют атмосферу быстрее, чем тяжелые. Время потери атмосферы зависит также от радиуса планеты, температуры, состава атмосферы и т. д. Полный количественный анализ этого вопроса является сложной задачей. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
