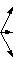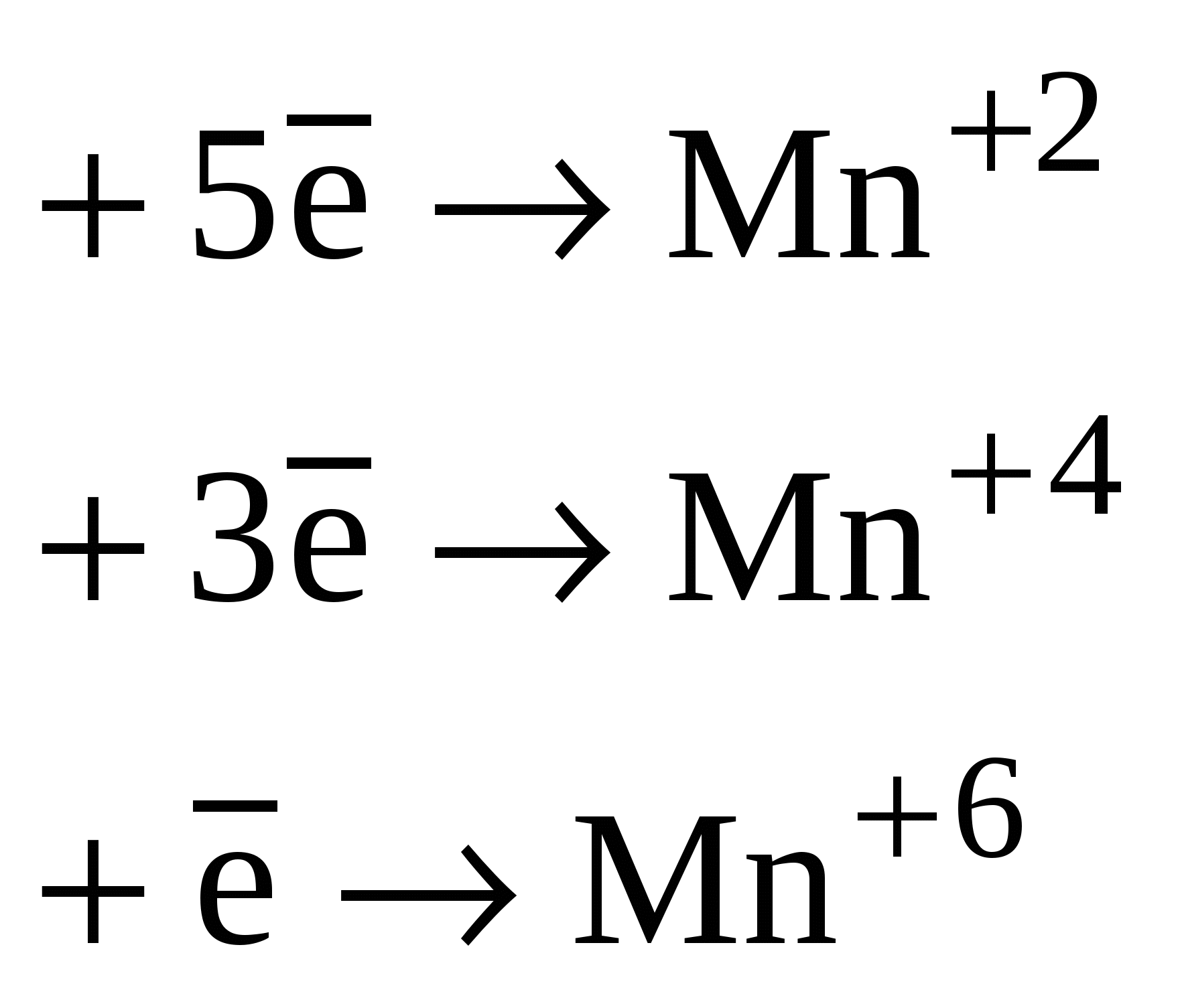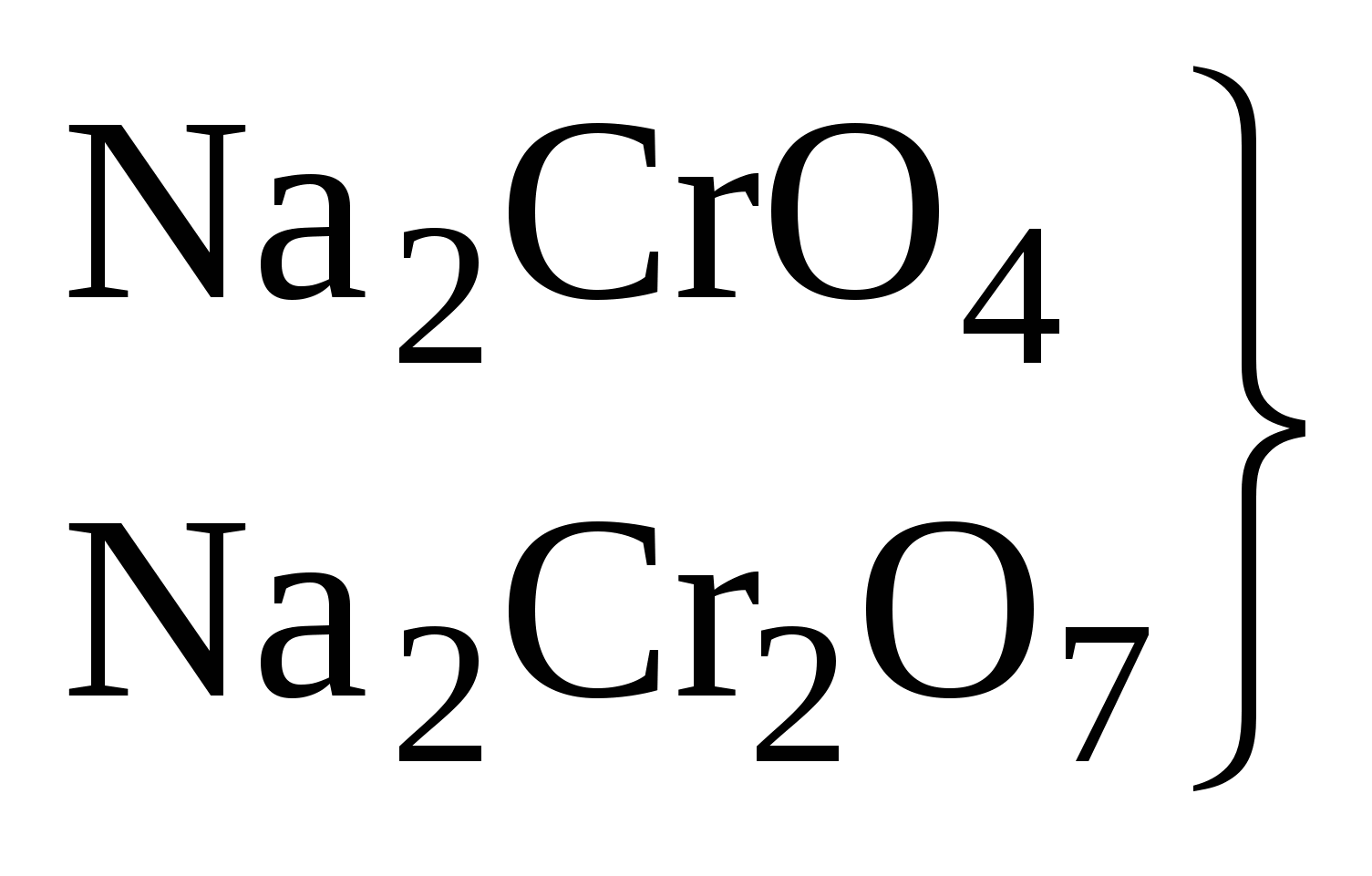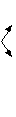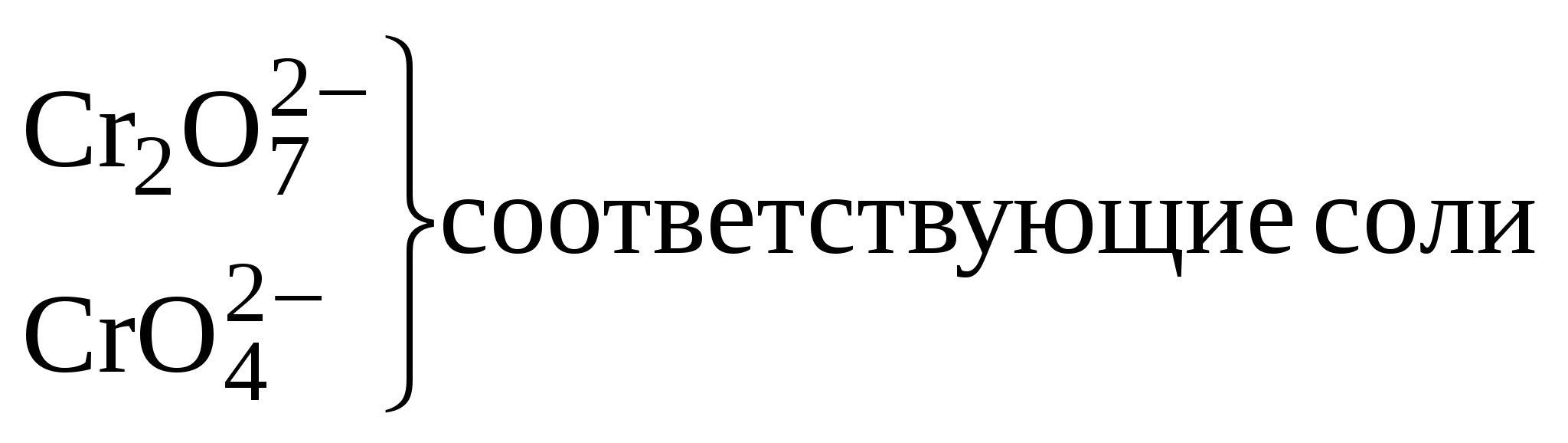Г. В. Плеханова (технический университет) к афедра общей и физической химии общая химия Сборник задач
 Скачать 2.09 Mb. Скачать 2.09 Mb.
|
6. Окислительно-восстановительные реакцииОкислительно-восстановительными называются химические реакции, сопровождающиеся изменением степени окисления атомов элементов. Окислением называется процесс отдачи электронов, а восстановлением процесс принятия электронов. Окисление и восстановление взаимосвязаны. Окислителем называется вещество, атомы которого принимают электроны, при этом он восстанавливается. Восстановителем называется вещество, атомы которого отдают электроны, при этом он окисляется. Все окислительно-восстановительные реакции классифицируют следующим образом: 1. Межмолекулярные реакции. Это реакции, в которых окислитель и восстановитель являются различными веществами. где Mn+4 – окислитель, Cl–1 – восстановитель. 2. Реакции внутримолекулярного окисления. Это реакции, которые протекают с изменением степеней окисления атомов различных элементов одного и того же вещества. где Mn+7 – окислитель, а O-2 – восстановитель. 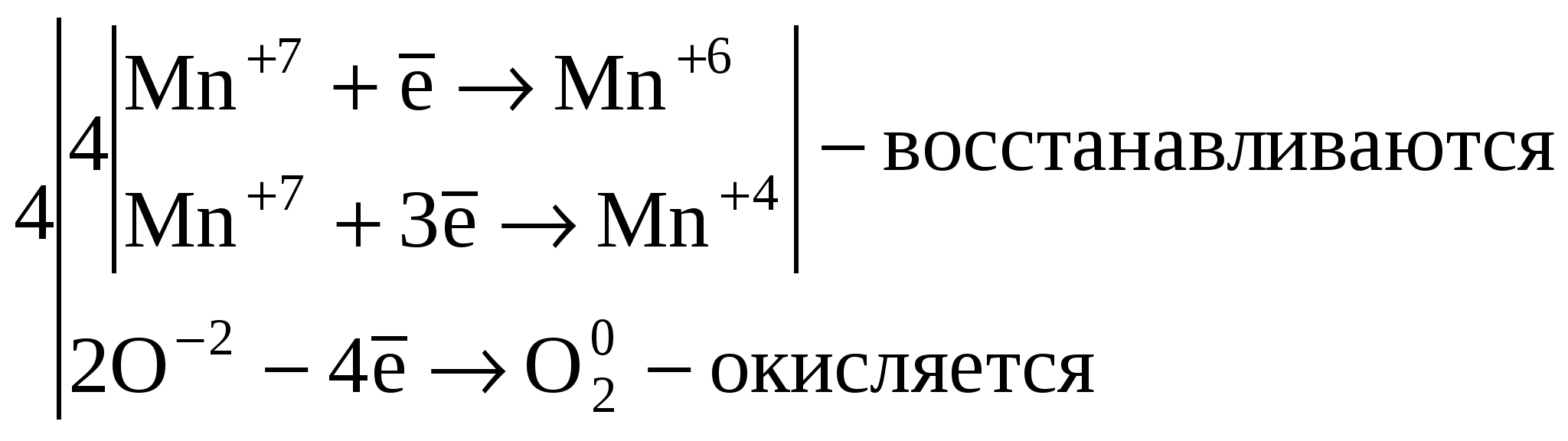 3. Реакции диспропорционирования. В этих реакциях и окислителем и восстановителем является элемент находящийся в промежуточной степени окисления в составе одного и того же вещества. где Cl20 – окислитель и восстановитель. О возможности того или иного вещества проявлять окислительные, восстановительные или двойственные свойства можно судить по степени окисления элементов, выполняющих эти функции. Элементы в своей высшей степени окисления проявляют только окислительные свойства, а в низшей степени окисления проявляют только восстановительные свойства. Элементы, имеющие промежуточную степень окисления, могут проявлять как окислительные, так и восстановительные свойства. Некоторые окислители и восстановители приведены ниже.
|