Хроматографические методы анализа и их использование в анализе объектов окружающей природной среды
 Скачать 330.89 Kb. Скачать 330.89 Kb.
|
10–8%. [1-3]Хроматографический способ анализа. Хроматографические системы можно разделить по следующим принципам: – агрегатное состояние подвижной и неподвижной фаз; – геометрические характеристики системы; – механизм взаимодействия между разделяемым веществом и фазами. В качестве подвижной фазы используется газ или жидкость. В качестве неподвижной, или стационарной, фазы применяются твердые вещества или жидкости. По расположению фаз хроматографические системы подразделяют на две группы: плоскостные и колоночные. Последние, в свою очередь, разделяются на: – насадочные, заполненные зернистым твердым материалом (мелкие шарики), либо являющимся разделительной средой, либо служащим носителем неподвижной жидкой фазы; – капиллярные, внутренние стенки которых покрыты пленкой неподвижной жидкости или слоем твердого адсорбента (поглотитель). Взаимодействие между разделяемым веществом и фазами хроматографической системы может осуществляться или на поверхности фазы, или в объеме. В первом случае хроматография называется адсорбционной, во втором – распределительной. Механизмы разделения молекул в хроматографических системах чаще всего сводятся к следующим: – неподвижная фаза физически поглощает (сорбирует) разделяемые вещества; – неподвижная фаза химически взаимодействует с разделяемыми веществами; – неподвижная фаза растворяет разделяемые вещества из раствора в несмешивающемся растворителе; – неподвижная фаза имеет пористую структуру, затрудняющую диффузию молекул разделяемых веществ в этой фазе. Хроматография, начавшись с самодельных устройств типа полоски бумаги, опущенной в растворитель, в настоящее время представлена сложнейшими инструментальными системами, основанными на современных точнейших, или прецизионных, принципах и оснащенными компьютерным обеспечением. Схема процесса хроматографирования, в сущности, очень проста и показана на рис. 3. Далее примерно в такой последовательности будет рассмотрен принцип работы хроматографа.  1.1 Основные виды хроматографии К основным видам хроматографии относят адсорбционную, ионообменную, жидкостную, бумажную, тонкослойную, гель-фильтрационную и афинную хроматографию. Адсорбционная хроматография. В этом случае разделение веществ осуществляется за счет выборочной (селективной) адсорбции веществ на неподвижной фазе. Такая селективная адсорбция обусловлена сродством того или иного соединения к твердому адсорбенту (неподвижной фазе), а оно, в свою очередь, определяется полярными взаимодействиями их молекул. Поэтому часто хроматографию такого типа используют при анализе соединений, свойства которых определяются числом и типом полярных групп. К адсорбционной хроматографии причисляют ионообменную, жидкостную, бумажную, тонкослойную и газо-адсорбционную хроматографию.  Рис. 4. Изображение структуры частицы ионообменной смолы: – заряженные функциональные группы, ковалентно связанные с нитями решетки; – свободно перемещающиеся противоположно заряженные протовоионы, электростатически связанные с частицей смолы, способные претерпевать обмен с другими ионами. Ионообменная хроматография. В качестве неподвижной фазы используют ионообменные смолы (рис. 4) как в колонках, так и в виде тонкого слоя на пластинке или бумаге. Разделение обычно проводят в водных средах, поэтому этот метод используется главным образом в неорганической химии, хотя применяются и смешанные растворители. Движущей силой разделения в этом случае является различное сродство разделяемых ионов раствора к ионообменным центрам противоположной полярности в неподвижной фазе. Жидкостная хроматография. В этом случае неподвижной фазой служит жидкость. Наиболее распространенным случаем является адсорбционный вариант жидкостной колоночной хроматографии. Пример разделения природных пигментов представлен на рис. 5. 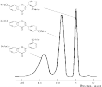 Рис. 5. Хроматографическое разделение природных пигментов (флавонов и изофлавонов) Бумажная хроматография. В качестве неподвижной фазы используют полосы или листы бумаги (рис. 6). Разделение происходит по адсорбционному механизму, причем иногда его проводят в двух перпендикулярных направлениях.  Рис. 6. Схема разделения методом бумажной хроматографии: А, Б и В – положения компонентов смеси по окончании хроматографического разделения. Подвижная фаза впитывается в бумагу (неподвижная фаза) под действием капиллярных сил и переносит индивидуальные компоненты смеси с различными скоростями, зависящими от отношений растворимости этих компонентов в обеих фазах. Отношение а/б = Rf (фактор запаздывания) характеризует данное разделяемое вещество Тонкослойная хроматография – это любая система, в которой неподвижной фазой является тонкий слой, в частности слой оксида алюминия (толщина 2 мм) в виде пасты, нанесенной на стеклянную пластинку. Пример такой системы и результаты разделения показаны на рис. 7.  Рис. 7. Камера для тонкослойной хроматографии:а – общий вид; б – схематический разрез; 1 – подложка со слоем сорбента; 2 – край камеры; 3 – емкость для растворителя Гель-фильтрационная, или молекулярно-ситовая, хроматография. Принцип разделения в таких системах несколько иной, чем в предыдущих случаях. Неподвижной фазой являются материалы, обычно гели, со строго контролируемой пористостью, в результате чего одни компоненты смеси в соответствии с размером и формой молекул могут проникать между частицами геля, а другие не могут. Наиболее часто этот вид хроматографии используется для разделения высокомолекулярных соединений. Один из вариантов применения этого метода – определение молекулярных масс разделяемых веществ, часто необходимых для химических исследований (рис. 8).  Рис. 8. Схема разделения методом гель-хроматографии: а – начало разделения б – разделение в – конец разделения; большие кружки – частицы геля, большие точки – молекулы соединений с большой молекулярной массой, маленькие точки – молекулы соединений с меньшей молекулярной массой Афинная хроматография. Этот вид хроматографии основан на взаимодействии между веществом, с одной стороны, способным реагировать с выделяемым соединением, а с другой – связанным с твердым носителем неподвижной фазы. Такое вещество обладает сродством к выделяемому соединению и называется афинным лигандом. Наиболее часто этот метод находит применение в биохимическом анализе. Например, при пропускании через целлюлозу, активированную бромцианом, биологических объектов-антигенов, содержащих белки, происходит их специфическое удерживание, как показано на схеме 1.  По другому способу для присоединения белков к гидроксильной группе целлюлозы последнюю сначала обрабатывают 2-амино-4,6-дихлор-сим-триазином, а затем продукт их взаимодействия вступает в реакцию с аминогруппой белка по схеме 2: 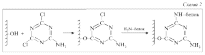 Конечно, число способов хроматографирования не ограничивается перечисленными выше. Часто хроматографию сочетают с другими физико-химическими методами, например с масс-спектрометрией, но в данной статье стоит задача познакомить читателя лишь с общими принципами хроматографии. Поэтому далее рассмотрим обработку результатов хроматографирования. 1.2 Методы проявления хроматограмм Проявлением называется процесс переноса разделяемых веществ подвижной фазой. Проявление можно осуществить тремя основными способами: фронтальным анализом, вытеснением и элюированием. Наиболее широко используется элюирование. Фронтальный анализ. Это случай наиболее простой, т. к. здесь проба и служит подвижной фазой. Ее непрерывно добавляют в систему, поэтому нужны большие объемы пробы. Результаты показаны на рис. 9. 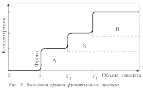 Образование нескольких зон обусловлено различным сродством разных компонентов к неподвижной фазе. Передний край называют фронтом, отсюда и название. В первой зоне находится только наименее удерживаемое вещество А, которое движется быстрее всего. Вторая зона содержит вещество А и Б. Третья зона – смесь веществ А, Б и В. Во фронтальном анализе только компонент А получают в жидком виде. Вытеснительный анализ. В этом случае подвижная фаза обладает большим сродством к неподвижной фазе, чем разделяемое вещество. В неподвижную фазу вводят небольшую пробу. Но из-за большого сродства подвижная фаза вытесняет и проталкивает все компоненты. Она вытесняет наиболее сильно сорбирующийся компонент В, который, в свою очередь, вытесняет вещество Б, а тот вытесняет наименее сорбирующийся компонент А. В отличие от фронтального анализа с помощью этого способа можно получить все основные компоненты в индивидуальном (жидком) виде. Элюентный анализ. Подвижную фазу для перемещения растворенного вещества пропускают через хроматографическую систему. Разделение происходит за счет различного сродства компонентов смеси к неподвижной фазе и, следовательно, за счет разных скоростей их перемещения. Пробу малого объема вводят в хроматографическую систему. В итоге зоны с компонентами будут постепенно образовывать отдельные участки, разделенные чистым элюентом. Благодаря высокой эффективности разделения метод получил наиболее широкое распространение и в значительной степени вытеснил другие варианты разделения. Поэтому далее рассмотрим теорию и аппаратное оформление этого метода. Хроматографические процессы часто удобно рассматривать как серии экстракционных процессов, при этом могут быть разделены вещества с очень близкими свойствами, т. к. в ходе хроматографических процессов быстро и одновременно происходят сотни и даже тысячи циклов экстракции. Для оценки эффективности хроматографических процессов, исходя из теоретического представления о дистилляции (по аналогии с разделением нефти на ректификационных колоннах, где теоретическая тарелка соответствует части ректификационной колонны, в которой пар и жидкость находятся в равновесии), вводят понятие «высота, эквивалентная теоретической тарелке» (ВЭТТ). Хроматографическая колонка, таким образом, рассматривается как набор гипотетических слоев (тарелок). Под ВЭТТ обычно подразумевают такую толщину слоя, которая необходима для того, чтобы смесь, поступившая из предыдущего слоя, пришла в равновесие со средней концентрацией вещества в подвижной фазе этого слоя. Ее можно описать следующей формулой: ВЭТТ = L/N, где L – длина колонки, N – число теоретических тарелок. ВЭТТ является суммарной характеристикой разделения веществ. Однако разделить компоненты смеси важно, но недостаточно. Необходимо идентифицировать каждый компонент и определить его количество в пробе. Обычно это осуществляют с помощью обработки хроматограмм – зависимости интенсивности сигнала, пропорционального концентрации вещества, от времени разделения. Некоторые примеры хроматограмм показаны на рис. 9. 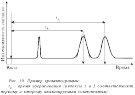 Время от момента ввода пробы в колонку до момента регистрации максимума пика называется временем удерживания (tR). В оптимальных условиях оно не зависит от количества введенной пробы и с учетом геометрических параметров колонки определяется строением того или иного соединения, т. е. является качественной характеристикой компонентов. Количественное содержание компонента характеризуется величиной пика, точнее его площадью. Подсчет площади пика обычно осуществляют автоматически с помощью прибора интегратора, который фиксирует и время удерживания, и площадь пика. Современная аппаратура позволяет сразу получать компьютерную распечатку с указанием содержания всех компонентов разделяемой смеси. 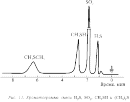 1.3 Работа хроматографа Схема установки наиболее простого газового хроматографа приведена на рис. 12. Она состоит из газового баллона, содержащего подвижную инертную фазу (газ-носитель), чаще всего гелий, азот, аргон и др. С помощью редуктора, уменьшающего давление газа до необходимого, газ-носитель поступает в колонку, представляющую собой трубку, заполненную сорбентом или другим хроматографическим материалом, играющим роль неподвижной фазы. 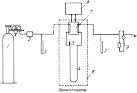 Рис. 10. Схема работы газового хроматографа: 1 – баллон высокого давления с газом-носителем; 2 – стабилизатор потока; 3 и 3 ' – манометры; 4 – хроматографическая колонка; 5 – устройство для ввода пробы; 6 – термостат; 7 – детектор; 8 – самописец; 9 – расходомер Хроматографическая колонка – это «сердце» хроматографа, поскольку именно в ней происходит разделение смесей. Колонки чаще всего изготавливают из стекла; бывают стальные, тефлоновые, а также капиллярные колонки. Вблизи от ввода газа в колонку устанавливают устройство для ввода пробы. Чаще всего вводят пробу с помощью шприца, протыкая резиновую мембрану. Анализируемая смесь разделяется в колонке и поступает в детектор – прибор, преобразующий результаты разделения в форму, удобную для регистрации. Одним из наиболее используемых детекторов является катарометр, принцип действия которого основан на измерении теплоемкости разных тел. На рис. 11 показана схема катарометра. В цилиндрическую полость помещена металлическая спираль (нить сопротивления), нагревающаяся в результате прохождения через нее постоянного электрического тока. При протекании через нее газа-носителя c постоянной скоростью температура спирали остается постоянной. Однако если состав газа меняется при появлении элюируемого вещества, то температура спирали меняется, что и регистрируется прибором. 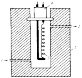 Рис. 11. Схема катарометра: 1 – ввод газа из хроматографической колонки; 2 – вывод продуктов в атмосферу; 3 – нить сопротивления; 4 – изолятор; 5 – металлический блок катарометра Другой распространенный детектор – пламенно-ионизационный, схема которого представлена на рис. 12. Он гораздо более чувствителен, чем катарометр, но требует подачи не только газа-носителя, но и водорода. Выходящий из колонки газ-носитель, содержащий элюент, смешивается с водородом и проходит в форсунку горелки детектора. Пламя ионизирует молекулы элюента, в результате чего электрическое сопротивление между электродами уменьшается, а ток увеличивается. 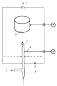 Рис. 12. Схема пламенно-ионизационного детектора: 1 – ввод водорода; 2 – ввод газа из хроматографической колонки; 3 – ввод воздуха; 4 – катод; 5 – горелка; 6 – собирающий электрод; 7 – вывод продуктов горения в атмосферу. В жидкостной хроматографии применяются спектрофотометрические детекторы (в видимой, УФ - и ИК-областях), а также рефрактометрические детекторы, основанные на измерении показателей преломления растворов. |


