Курсовая работа. Инулин из листьев матьимачехи. Экстракция, методы количественного и качественного анализа. Стандартизация сырья
 Скачать 296.36 Kb. Скачать 296.36 Kb.
|
|
Глава 4. Стандартизация сырья мать-и-мачехи Требования к качеству мать-и-мачехи листьев регламентирует ФС 2.5.0027.15 (ГФ XIV), согласно которой определение основных групп БАВ проводят методом ТСХ (флавоноиды) и с помощью качественных реакций (углеводы) [4]. Этапы ТСХ-исследования: -Приготовление испытуемого раствора: получают спиртовое извлечение из сырья (экстрагент – спирт этиловый 96%) в соотношении 1:10. Выбор экстрагента связан с растворимостью флавоноидов листье мать-и-мачехи в спирте; -Нанесение испытуемого раствора и раствора СО (рутина) на хроматографическую пластинку; -Хроматографирование в системе растворителей этилацетат-муравьиная кислота безводная-вода (40:4:6) восходящим способом; -Детекция пятен осуществляется в УФ –свете при λ=365 нм после последовательной обработки дифенилборной кислоты аминоэтилового эфира раствором 1% в спирте и нагревании при 100-105°С в течение 5 мин. На хроматограмме испытуемого раствора должны обнаруживаться выше зоны адсорбции СО рутина с флуоресценцией желтого цвета: зона с голубой флуоресценцией, почти не разделенная с зоной адсорбции с флуоресценцией желтого цвета над ней, выше них зона адсорбции с флуоресценцией желтого цвета; над ними две зоны с голубой флуоресценцией. Допускается обнаружение других зон адсорбции (флавоноиды) [4]. Детекция флавоноидов основана на способности продуктов их реакции (образуется батохромный комплекс) с комплексообразователем (производное борной кислоты) поглощать немонохроматический свет при определенной длине волны в УФ-области спектра. Для проведения качественных реакций получают водное извлечение из сырья в соотношении 1:50 при экстракции на кипящей водяной бане [4]. При добавлении к 10 мл извлечения 30 мл спирта 96% должны появиться хлопьевидные сгустки, выпадающие в осадок при стоянии (полисахариды). Реакция основана на растворимости полисахаридов в воде и их нерастворимости в спирте. После фильтрации осадка через стеклянный фильтр ПОР 16, осадок с фильтра переносят в мерную колбу (50 мл), доводят раствором натрия гидроксида до метки. К 1 мл полученного раствора прибавляют 0,25 мл карбазола раствора 0,5% и 5 мл концентрированной серной кислоты. При нагревании на водяной бане в течение 10 минут появляется красно-фиолетовое окрашивание (галактуроновая кислота) [4]. Анализ основан на цветной реакции карбазола с продуктами окисления моносахаров, образующихся после разрушения полимерных молекул полисахаридов концентрированной серной кислотой [3]. При нагревании производных уроновых кислот с концентрированной серной кислотой главным продуктом реакции является довольно устойчивая в этих условиях 5-формилфуран-2-карбоновая кислота, способная давать окрашенные продукты с разнообразными органическими реагентами, в частности, с некоторыми ароматическими азотистыми гетероциклами и фенолами. В качестве таких реагентов в разное время были предложены карбазол, индол, 3-гидроксибифенил и 3,5-диметилфенол. Основной показатель качества сырья - содержание суммы полисахаридов и свободных сахаров [4]. В основе метода количественного определения сахаров лежит цветная реакция моносахаридов с пикриновой кислотой с образованием аминопикриновой кислоты в результате восстановления сахаром группы N02 в NH2. Полученные восстанавливающие моносахариды с пикриновой кислотой в щелочной среде имеют максимум поглощения в диапазоне 440-460 нм [17]. Этапы (стадии) анализа: 1.Подготовительный этап – включает подготовку ЛРС, измельчение (до размера частиц 0,5 мм), взятие навесок (2,0 – масса пробы для количественного анализа), подготовку химической посуды для анализа, реактивов Двухкратная экстракция полисахаридов и свободных сахаров из сырья подкисленной водой (на 40 мл воды – 4 мл концентрированной хлористоводородной кислоты) в течение 30 минут. Извлечения фильтруют в мерную колбу на 100 мл (раствор А). В мерной колбе (50 мл) к 10 мл раствора А добавляют по каплям 40% раствор NaOH до pH 4,0-4,5, доводят объем раствора до метки водой и перемешивают (раствор Б). В мерную колбу (100 мл) помещают 2,5 мл 1% раствора пикриновой кислоты и 7,5 мл 20% раствора Na2CO3, затем 5 мл раствора Б. Колбу нагревают в течение 10 мин на кипящей водяной бане, затем охлаждают, доводят объем водой до метки (раствор В). Оптическую плотность раствора В измеряют относительно раствора сравнения (2,5 мл пикриновой кислоты раствора 1 %, 7,5 мл натрия карбоната раствора 20 % и вода, помещенные в мерную колбу вместимостью 100 мл) на спектрофотометре при длине волны 470 нм. Содержание суммы полисахаридов и свободных сахаров в пересчете на глюкозу в абсолютно сухом сырье в процентах (Х) вычисляют по формуле: 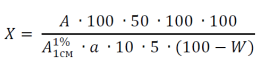 где А – оптическая плотность раствора В; Согласно требованиям ГФ XIV содержание суммы полисахаридов и свободных сахаров в пересчете на глюкозу должно быть не менее 10% [4]. Заключение Настоящая работа посвящена рассмотрению научных данных по полисахаридному составу листьев мать-и-мачехи и методам его анализа. В первой главе рассматривается строение и функции инулина и других фруктанов, приведены его природные источники. Инулин представляет собой полимер, состоящий из нескольких остатков фруктозы (от 10 до 36) в форме фуранозы. Данный полисахарид является вторым по распространенности после крахмала запасным углеводом у растений и наиболее характерен для представителей семейств Asteraceae и Campanulaceae. Наибольшее содержание инулина обнаруживается в корнях таких растений семейства астровых, как Arctium sp. (Лопух), Cichorium sp. (Цикорий), Taraxacum sp. (Одуванчик), Smallanthus sp. (Якон), Inula sp. (Девясил) и других. В промышленных масштабах инулин получают из цикория, топинамбура и агавы. Во второй главе дана подробная фармакогностическая характеристика мать-и-мачехе. Приведена её ботанико-географическая характеристика, краткое описание сырьевой базы, химический состав, особенности заготовки и хранения сырья, макродиагностические признаки сырья, требования к качеству согласно действующей Государственной фармакопее, фармакологические свойства и описание препаратов на их основе, применяемых в медицинской практике. Третья глава посвящена обзору современных исследований по выделению и методам количественного и качественного анализа полисахаридов мать-и-мачехи. Рассмотрен подход к анализу фруктанов листьев мать-и-мачехи. Приведены оригинальная авторская методика количественного определения из одной навески группового состава углеводного комплекса растительных объектов (свободные углеводы, водорастворимые полисахариды, пектиновые вещества и гемицеллюлозы) и результаты её апробации для анализа листьев мать-и-мачехи. Подробно рассмотрены методики выделения водорастворимых полисахаридных комплексов из листьев мать-и-мачехи и изучения их состава (фракционный состав, содержание уроновых кислот, белка, нуклеиновых кислот). При изучении компонентного состава полисахаридного комплекса листьев мать-и-мачехи установлено, что он состоит из двух основных компонентов соответственно в соотношении 33% к 67%: рамногалактуронана I и нейтральных полисахаридов, представленных суммой арабиногалактана, рамнана и галакторамнана. В четвертой главе подробнее рассмотрены вопросы стандартизации сырья мать-и-мачехи, а именно метода идентификации и определения содержания основных БАВ. Обнаружение основных групп БАВ проводят методом ТСХ (флавоноиды) и с помощью качественных реакций (осадительная реакция полисахаридов со спиртом; карбазолсерная реакция определения уроновых кислот). Количественное определение полисахаридов и свободных сахаров проводят спектрофотометрическим методом после их реакции с пикриновой кислотой. Список литературы Evans W. Trease and Evans Pharmacognosy. – 16th ed. – 2009. – 604 р. Shikov A.N., Pozharitskaya O.N., Makarov V.G., Wagner H., Verpoorte R., Heinrich M. Medicinal plants of the Russian Pharmacopoeia: their history and applications / Journal of Ethnopharmacology. — 2014. — Vol. 154. — P. 481-536. Гашевская А.С. Потенциометрический и карбазол-серный методы определения галактуроновой кислоты в растительных полисахаридах / Успехи современного естествознания. — 2016, №2. — С. 9-15. Государственная фармакопея Российской Федерации XIV. — Том 4. — 2018. Режим доступа: http://resource.rucml.ru/feml/pharmacopia/14_4/HTML/index.html Корж А.П. Исследование структуры полисахаридов мать-и-мачехи обыкновенной и разработка параметров их стандартизации: Автореф… дис. канд. фарм. наук. — Самара, 2012. — 24 с. Корж А.П., Гурьев А.В., Белоусов М.В., Юсубов М.С. Определение содержания уроновых кислот в полисахаридах мать-и-мачехи, клевера, девясила / Химия растительного сырья. — 2011, №4. — С. 259-264. Корж А.П., Гурьев А.В., Белоусов М.В., Юсубов М.С., Белянин М.А. Моносахаридный состав полисахаридного комплекса листьев мать-и-мачехи / Бюллетень сибирской медицины. — 2011, №5. — С. 62-65. Корж А.П., Гурьев А.В., Белоусов М.В., Юсубов М.С., Белянин М.А., Байков А.Н. Водорастворимые полисахариды подземной части Inula helenium L. (Asteraceae) / Растительные ресурсы. — 2011, №3. — С. 88-92. Куприянова Л.А. Род Tussilago L. — мать-и-мачеха / Флора СССР. — Т. 26. 1961. — М.; Л. : Издательство АН СССР. — С. 641—642. Куркин В.А. Фармакогнозия: учебник для студентов фармацевтических вузов. — Самара: Офорт, СамГМУ, 2004. — 1180 с. Оленников Д.Н., Кащенко Н.И. Полисахариды. Современное состояние изученности: экспериментально-наукометрическое исследование / Химия растительного сырья. — 2014, №1. — С. 5-26. Оленников Д.Н., Танхаева Л.М. Исследование колориметрической реакции фруктозы с резорцином в зависимости от условий её проведения / Химия растительного сырья. — 2008, №2. — С. 69-74. Оленников Д.Н., Танхаева Л.М. Методика количественного определения суммарного содержания полифруктанов в корнях лопуха (Arctium spp.) / Химия растительного сырья. — 2010, №1. — С. 115-120. Оленников Д.Н., Танхаева Л.М. Методика количественного определения группового состава углеводного комплекса растительных объектов / Химия растительного сырья. — 2006, №4. — С. 29-33. Растительные ресурсы России: Дикорастущие цветковые растения, их компонентный состав и биологическая активность. Т.5. Семейства Asteraceae (Compositae). Часть 2. Роды Echinops - Youngia / Отв. ред. А.Л. Буданцев. — СПб.; М. : Товарищество научных изданий КМК, 2013. — 312 c. Сербаева Э.Р., Якупова А.Б., Магасумова Ю.Р., Фархутдинова К.А., Ахметова Г.Р., Кулуев Б.Р. Инулин: природные источники, особенности метаболизма в растениях и практическое применение / Биомика. — 2020. — Т.12, №1. – С.57-79. Тринеева О.В., Сливкин А.И. Определение суммы полисахаридов и простых сахаров в листьях крапивы двудомной / Вестник ВГУ. — 2017, №1. — С. 164-169. Фармакогнозия. Лекарственное сырьё растительного и животного происхождения: учебное пособие / Г.М. Алексеева [и др.]. под ред. Г.П. Яковлева. — Санкт-Петербург : СпецЛит, 2013. — 847 с. Olennikov D.N., Tankhaeva L.M., Rokhin A.V. Glucofructans from Saussurea lappa roots / Chemistry of Natural Compounds. — 2011. — Vol. 47, №3. — P. 339-342. |
