реферат. Каталитический крекинг НАЗАРИЙ МАЪЛУМОТЛАР. Каталитический крекинг. Химические основы процесса. Превращения алканов, циклоалканов, алкенов и аренов
 Скачать 1.43 Mb. Скачать 1.43 Mb.
|
Каталитический крекинг алкановПервичным актом при крекинге алканов является образование карбкатиона (инициирование процесса) Для твердых кислотных катализаторов (цеолитов) предложены следующие гипотезы инициирования процесса: -карбениевый ион образуется при отрыве гидрид-иона сильным кислотным центром Бренстеда с образованием в качестве продукта водорода; -исходный нон представляет собой пентакоординированный углерод (карбониевый ион), образующийся присоединением протона, отрываемого от сильного центра Бренстеда; -карбениевый ион образуется благодаря адсорбции па центрах Бренстеда олефинов, полученных при термическом крекинге исходного вещества; -карбкатион образуется при поляризации молекулы сырья под воздействием сильных электрических полей в порах цеолита. Наиболее принята гипотеза, основанная на образовании карбениевых ионов из олефинов, образующихся при термическом распаде в газовой фазе, на кислотных центрах Бренстеда Образующиеся олефины присоединяют протоны, находящиеся на катализаторе (центры Бренстеда) и превращаются в карбкатионы: Образовавшийся ион карбения отрывает гидрид-ион от молекулы исходного алкана: 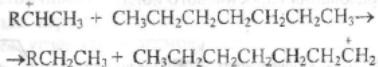 Далее реакция развивается по цепному пути. Образовавшийся ион карбения подвергается β-распаду с образованием небольших карбкатионов и газообразных α‑олефинов. При этом одновременно протекают реакции изомеризации карбениевых ионов. Изомеризация происходит как путем перемещения гидрид-иона (изомеризация заряда), так и при перемещении метиланиона (скелетная изомеризация). Тепло, выделяющееся при изомеризации, затрачивается на расщепление. Превращение протекает по схеме: 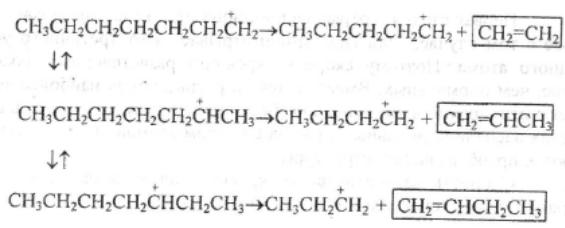 Высокая скорость изомеризации ионов приводит к тому, что этилена - продукта распада первичного карбкатиона образуется очень мало. Скелетная изомеризация дает продукты с разветвлением углеводородного скелета: 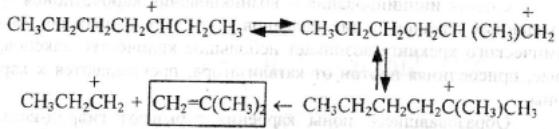 Чередование экзотермической изомеризации и эндотермического β-распада продолжается до образования карбкатионов, содержащих 3-5 атомов водорода. Тепловой эффект измеризации этих ионов уже не компенсирует затрат тепла на расщепление. Поэтому карбкатионы С3-С5 после изомеризации отрывают гидрид-ион от молекулы исходного углеводорода: 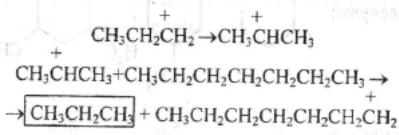 Затем весь цикл процесса повторяется. Обрыв цепи происходит при встрече карбкатиона с анионом катализатора: Первая стадия - отрыв гидрид-иона от алкана - протекает быстрее в том случае, если гидрид-ион отрывается от третичного углеродного атома. Поэтому скорость крекинга разветвленных алканов выше, чем нормальных. Вместе с тем, и распад ионов наиболее легко идет с отщеплением третичных карбкатионов, в результате чего в продуктах распада нормальных алканов с числом атомов углерода четыре И более преобладают изоструктуры. Скорость каталитического крекинга алканов на один-два порядка выше скорости их термического крекинга. Каталитический крекинг циклоалкановСкорость каталитического крекинга циклоалканов близка к скорости крекинга алканов с равным числом атомов углерода и увеличивается при наличии третичного атома углерода. Стадия инициирования - возникновения карбкатионов - для насыщенных алканов и циклоалканов протекает одинаково. За счет термического крекинга возникает небольшое количество алкенов, которые, присоединяя протон от катализатора, превращаются к карбкатионы. Образовавшиеся ионы карбения отрывают гидрид-ионы от молекулы циклоалкана. Отщепление гидрид-иона от третичного углеродною атома протекает легче, чем от вторичного, поэтому глубина крекинга возрастает с увеличением числа заместителей в кольце 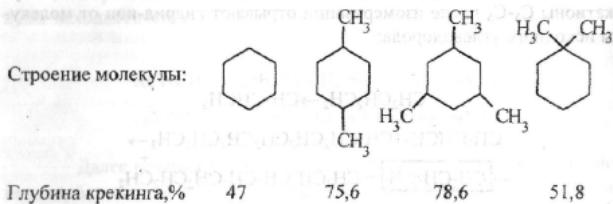 Распад циклогексильного иона может происходить двумя путями: 1) с разрывом кольца и 2) без разрыва кольца. 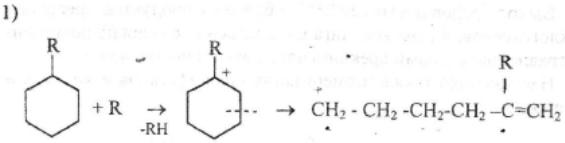 При разрыве β-С-С-связи образуется алкенильный ион, который легко изомеризуется в ион аллильного типа: 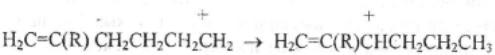 Последний может расщепиться по β-правилу, оторвать гидрид-ион от исходного углеводорода или передать протон молекуле алкена или катализатора 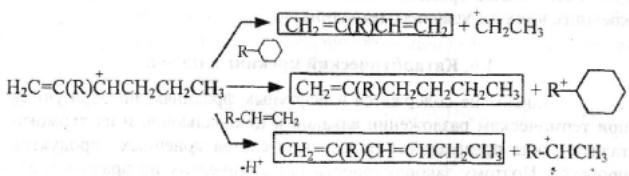 При крекинге по этому пути из гомологов циклогексана образуются алкены и диены. 2) Циклогексильный ион может передать протон алкену или катализатору и превратиться в циклоалкен 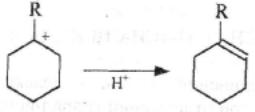 Этот путь энергетически выгоднее, чем распад по С-С-связи (1). Циклоалкены крекируются быстрее, чем циклоалканы, со значительным выходом аренов. Выход аренов достигает 25% и более от продуктов превращения циклогексанов, а газы крекинга циклоалкенов содержат повышенное по сравнению с газами крекинга алканов количество водорода. Наблюдается также изомеризация циклогексанов в циклопентаны и обратно 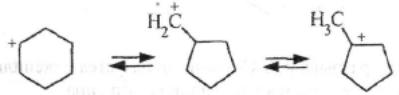 Циклопентаны в условиях каталитического крекинга более устойчивы, чем циклогексаны. При наличии длинных боковых цепей в молекуле циклоалкана возможны изомеризация боковой цепи и деалкилирование молекулы. Бициклические циклоалканы ароматизируются в большей степени, чем моноциклические. Так, при каталитическом крекинге декалина (500°С) выход аренов составляет ≈33% на превращенный декалин. Еще больше ароматических соединений (87,6%) образуется при крекинге в тех же условиях тетралина. Каталитический крекинг алкенов Алкены не содержатся в нефтяных фракциях, но образуются при термическом разложении алканов и циклоалканов, и их термокаталитические превращения определяют состав конечных продуктов процесса. Поэтому закономерности каталитических превращений алкенов в условиях каталитического крекинга представляют особый интерес. Скорость каталитического крекинга алкенов на два-три порядка выше скорости крекинга соответствующих алканов, что объясняется легкостью образования из алкенов карбениевых ионов: 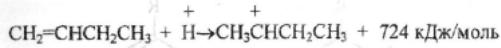 При присоединении протона к молекуле алкена образуется такой же ион, как и при отщеплении гидрид-иона от алкана, что определяет общность их реакций при каталитическом крекинге. Кроме образования низших алканов и алкенов каталитический крекинг алкенов приводит к образованию циклоалканов и аренов. Механизм этих процессов может быть представлен схемой: 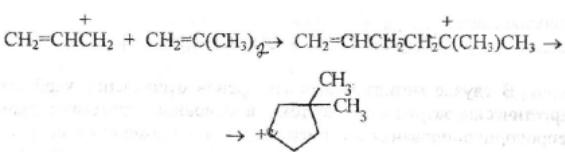 Далее может произойти изомеризация в шестичленный цикл и превращение в арен. Каталитический крекинг алкилароматических углеводородов Незамещенные арены в условиях каталитическою крекинга устойчивы. Метилзамещенные арены реагируют со скоростью, близкой к алканам. Алкилпроизводные аренов, содержащие два и более атомов углерода в цепи, крекируются примерно с такой же скоростью, что и алкены. При крекинге алкилароматических углеводородов бензольное кольцо не затрагивается, тогда как боковые цепи во всех случаях, кроме толуола, отщепляются с образованием олефина. Влияние длины цепи и ее разветвленное на энергию активации (в кДж/моль) показано ниже:  Обычно скорость крекинга боковых цепей возрастает при переходе от первичного к вторичному и третичному углеродным атомам, соединяющим цепь с кольцом. Для одного и того же типа присоединения скорость растет при увеличении длины боковой цепи. 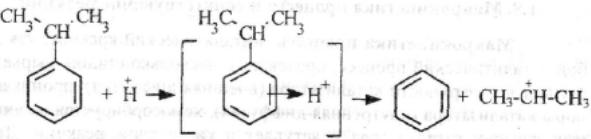 В случае метилзамещенных аренов отщепление карбкатиона энергетически затруднено, поэтому в основном протекают реакции диспропорционирования и изомеризации по положению заместителей. В случае толуола доминирующей реакцией является диспропорционирование в бензол и ксилол, а не крекинге отщеплением метана. Полиметилбензолы претерпевают главным образом изомеризацию и диспропорционирование. Например, ксилолы в присутствии кислотных катализаторов изомеризуются и диспропорцинируются в соответствии со следующей схемой: 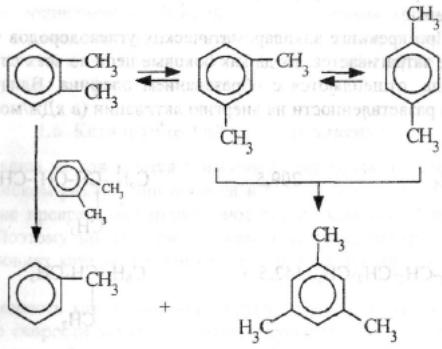 Полициклические арены прочно сорбируются на катализаторе и подвергаются постепенной деструкции и перераспределению водорода с образованием кокса. 18. Каталитический крекинг. Принципиальная технологическая схема. Режим процесса. Чаще всего сырьем для каталитического крекинга является широкие вакуумные фракции (350-500оС). Кроме того, каталитическому крекингу можно подвергать сырье вторичного происхождения: газойли коксования, термического крекинга и гидрокрекинга. На рис. 7 приведена принципиальная технологическая схема установки каталитического крекинга Г-43-107. производительность по сырью 160 т/ч. 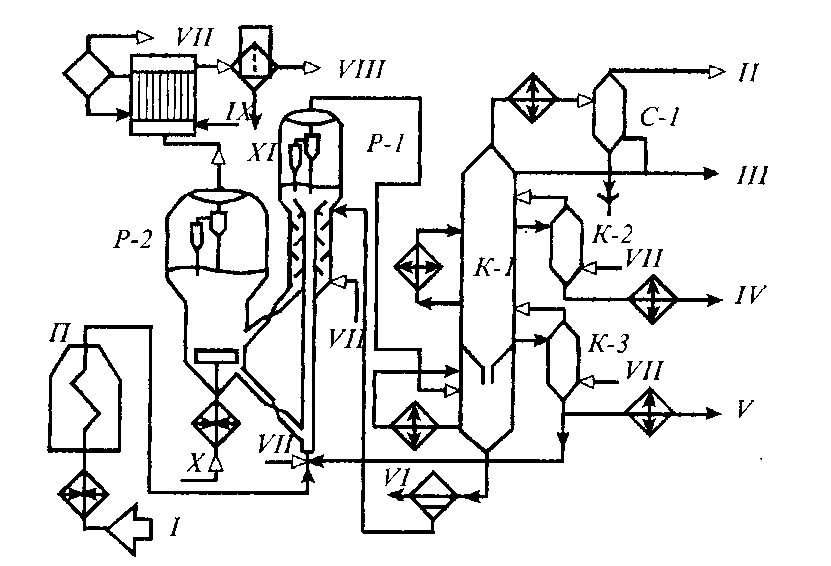 Рисунок 7. Принципиальная технологическая схема установки КК. I— гидроочищенное сырье; II — газы на ГФУ; III — нестабильный бензин; IV— легкий газойль; V — тяжелый газойль; VI — декантат; VII — водяной пар; VIII— дымовые газы; IX — вода; X — воздух; XI — катализаторная пыль. Гидроочищенное сырье нагревается в теплообменниках и печи (до 340оС) смешивают с рециркулятом и водяным паром и направляют в узел смешения прямоточного лифт-реактора Р-1. При контакте с регенерированным горячим цеолитсодержащим катализатором сырье испаряется и подвергается каталитическому крекингу в лифт реакторе (при температуре 540-560оС). Затем сырье с катализатором поступает в зону форсированного кипящего слоя в реактор Р-1. Продукты реакции отделяют от катализаторной пыли в двухступенчатых циклонах и направляют в нижнюю часть ректификационной колонны К-1 на дальнейшее разделение. Отработанный, закоксованный катализатор (с содержанием кокса 0.5-0.6%) из отпарной зоны Р-1 по наклонному катализаторопроводу направляют в зону кипящего слоя регенератора Р-2, где происходит выжиг кокса в режиме полного окисления оксида углерода (при температуре 640-650оС). Затем регенерированный катализатор (с содержанием кокса 0.005-0.1%) по нижнему наклонному катализаторопроводу поступает в узел смешения лифт-реактора. Воздух для регенерации катализатора нагнетают воздуходувкой в реактор Р-2. При этом дымовые газы проходят через внутренние двухступенчатые циклоны и затем их направляют на утилизацию теплоты в котел-утилизатор и перед сбросов в атмосферу очищают от пыли на электрофильтрах. В колонне К-1 предусмотрено верхнее (острое) и промежуточное циркуляционное орошение (в средней и нижней части колонны). Легкий и тяжелый газойль отбирают через отпарные колонны К-2 и К-3. При этом нижняя часть колонны играет роль скруббера для каталитического шлама, который возвращают в отпарную зону реактора Р-1. В качестве рециркулята часть тяжелого газойля подают в узел смешения лифт-реактора. Смесь паров бензина, воды и газов выводят с верха колонны. Затем эту смесь охлаждают в холодильнике и разделяют в газосепараторе С-1. Газы направляют на установку ГФУ, нестабильный бензин на стабилизацию, а водный конденсат после очистки от сернистых соединений выводят с установки. Таким образом, в результате каталитического крекинга фракции 350-500оС (содержание серы 0.2%)получается, % мас.: 1.96 – сухой газ; 5.61 – пропан-пропиленовая фракция; 9.04 – бутан-бутиленовая фракция; 43.04 – бензиновая фракция (С5- 195оС); 28.0 – легкий газойль (дизельная фракция 195-350оС); 8.35 – тяжелый газойль (более 350оС); 4 – кокс + потери.  Каталитический риформинг. Химические основы процесса. Превращения алканов, циклоалканов. Целевыми в процессах каталитического риформинга являются реакции образования аренов за счет: дегидрирования шестичленных цикланов 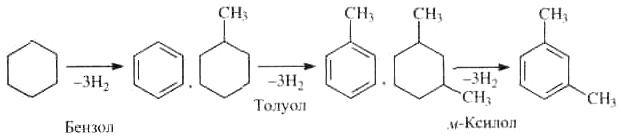 дегидроизомеризация циклопентанов 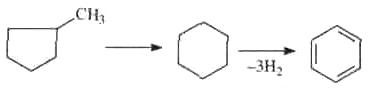 дегидроциклизации алканов 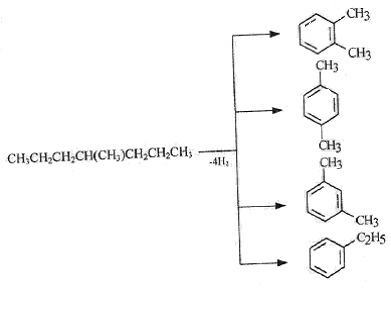 В процессе параллельно протекают и нежелательные реакции гидрокрекинга с образованием как низко-, так и высокомолекулярных углеводородов, а также продуктов уплотнения - кокса, откладывающегося на поверхности катализаторов. Наиболее важные реакции риформинга, ведущие к образованию аренов из цикланов и алканов, идут с поглощением тепла, у реакций изомеризации тепловой эффект, близкий к 0, а реакции гидрокрекинга экзотермичны. В условиях каталитического риформинга наиболее легко и быстро протекают реакции дегидрирования гомологов циклогексана. Относительно этой реакции скорость ароматизации из 5-членных цикланов примерно на порядок ниже. Наиболее медленной из реакций ароматизации является дегидроциклизация алканов, скорость которой лимитируется наиболее медленной стадией циклизации (на 2 порядка ниже). Относительные скорости и тепловые эффекты реакций каталитического риформинга
Превращения цикланов и алканов в арены - обратимые реакции, протекающие с увеличением объема и поглощением тепла. Следовательно, по правилу Ле-Шателье, равновесная глубина ароматизации увеличивается с ростом температуры и понижением парциального давления водорода. Однако промышленные процессы каталитического риформинга вынужденно осуществляют либо при повышенных давлениях с целью подавления реакций коксообразования (при этом снижение равновесной глубины ароматизации компенсируют повышением температуры), либо с непрерывной регенерацией катализатоpa при пониженных давлениях. 20. Каталитический риформинг. Влияние гетероатомных соединений и металлов, коксообразование на катализаторах. Соединения, содержащие гетероатомы N, S, О и металлы (Pb, As, Сu). Эти соединения необратимо сорбируются на платиновом катализаторе и быстро отравляют его. Поэтому присутствие гетероатомных соединений в сырье риформинга нежелательно: содержание серы должно быть не более 1 мг/кг; азота—до 0,5 мг/кг; концентрация Pb, As, Сu не должна превышать нескольких миллиграммов на тонну. Для удаления гетероорганических и металлорганических соединений сырье риформинга предварительно подвергают гидроочистке. Коксообразование на катализаторе. Закоксовывание катализатора снижает его активность. Механизм образования кокса изучен недостаточно. На платине при умеренных температурах (<427°С) кокс образуется, по-видимому, в результате диссоциативной адсорбции углеводородов. Поверхностные соединения обеднены водородом, прочно удерживаются на поверхности и находятся в квазиравновесии с газофазным водородом. При более высокой температуре (>477°С) и атмосферном давлении происходит диссоциация связей С—С, и на поверхности металла образуется углерод. Возможность образования углерода на катализаторе в нормальных условиях риформинга не очевидна, так как процесс осуществляется под давлением водорода. Однако существование поверхностных соединений в реальных условиях риформинга доказано экспериментально. Модифицированный оксид алюминия по характеру действия аналогичен алюмосиликатному катализатору каталитического крекинга, хотя и обнаруживает меньшую активность. Коксообразование на кислотных центрах катализатора риформинга, как и при крекинге, протекает за счет полимеризации, перераспределения водорода, циклизации, конденсации и других реакций непредельных и ароматических соединений. Образовавшийся кокс состоит из полициклических ароматических колец, связанных с алкеновыми и циклоалкановыми фрагментами. При всех отличиях механизма коксообразования на платине и оксиде алюминия действие их взаимосвязано: ненасыщенные углеводороды, образующиеся на платине, служат источником кокса на Аl2O3. Углеродистые отложения с платины могут мигрировать на Аl2O3. С другой стороны, продукты уплотнения, в частности полициклические арены, образующиеся на кислотных центрах, достаточно подвижны и могут блокировать металлические центры катализатора. Таким образом, на коксообразование влияют обе функции катализатора. Степень дезактивации катализатора зависит от закоксованности как платины, так и Аl2O3, так как важнейшие реакции риформинга протекают по бифункциональному механизму. | ||||||||||||||||||||||||||||||
