вариант 2. Контрольная работа 1 по дисциплине токсикологическая химия для студентов 4 курса фармацевтического факультета гбоу во оргму
 Скачать 287.07 Kb. Скачать 287.07 Kb.
|
|
6. Химико-токсикологический анализ соединений мышьяка. Соединения мышьяка на протяжении веков привлекали, да и сейчас продолжают привлекать внимание фармацевтов, токсикологов и экспертов-химиков. Профессор А. В. Степанов, характеризуя мышьяк как яд, отмечал, что судебная химия делала на нем свои первые шаги. В руководствах по судебной (токсикологической) химии мышьяку всегда уделялось большое внимание. При разработке методов минерализации критерием для их оценки всегда являлось наиболее полное обнаружение и определение мышьяка (и ртути). В настоящее время, несмотря на появление большого количества веществ, представляющих токсикологический интерес, мышьяк и его соединения не утратили своего значения. Причиной этого является широкое применение различных препаратов мышьяка в народном хозяйстве и медицине и их токсичность. Особенно велико в настоящее время значение следующих препаратов мышьяка: мышьяковистого ангидрида (As2O3), применяемого в качестве инсектицида и консерванта в сельском хозяйстве, в стекловарении для обесцвечивания стекла, в кожевенной промышленности, медицине и т. д., а смесь натриевых солей орто- и метамышьяковистых кислот (Na3AsО3 и NaAsО2), применяемых в сельском хозяйстве в качестве инсектицидов. Изумрудно-зеленая окраска содержимого желудков трупов животных, пищевых продуктов и других объектов исследования неоднократно являлась наводящим указанием для исследования их на наличие мышьяка и меди. Имеют токсикологическое значение и медицинские препараты мышьяка: Фаулеров раствор, арсенат натрия, миарсенол, новарсенол, осарсол и др. Представляет токсикологический интерес и газообразный мышьяковистый водород, который может быть причиной как производственных, так и бытовых отравлений. Соединения мышьяка издавна являлись орудиями преступления, что было связано с их повсеместной известностью, доступностью для широких слоев населения, отсутствием запаха, сладковатым вкусом таких препаратов, как, например, мышьяковистый ангидрид. Сходство картины отравления мышьяком с течением некоторых тяжелых хронических заболеваний, особенно когда небольшие дозы яда давались в течение длительного времени, приводило к тому, что отдельные преступления оставались нераскрытыми. Причинами отравлений соединениями мышьяка в настоящее время могут быть неосторожное, небрежное или халатное отношение к хранению и применению препаратов мышьяка в народном хозяйстве, недостаточно четко поставленная техника безопасности и другие упущения. Не исключена возможность и медицинских отравлений. Соединения мышьяка обладают как местным, так и общим действием на организм. Введенный внутрь мышьяк связывается с SH-группами ферментов и нарушает процессы окислительного фосфорилирования. Местно действует прижигающе, вызывая воспаление и омертвение тканей. На некротизирующем действии мышьяка основано применение мышьяковистого ангидрида в зубоврачебной практике. При введении токсических доз препаратов мышьяка внутрь наступает отравление. Различают две основные формы отравления: желудочно-кишечную и нервную. Чаще наблюдается смешанная форма. При первой форме отравления появляются металлический привкус во рту, жжение в зеве, жажда, сильные боли в животе, неукротимая рвота, тяжелый понос. При нервной форме в период от нескольких дней до нескольких недель развивается типичный мышьяковый неврит с парестезией конечностей и языка, иногда довольно стойкими параличами. Мышьяк выделяется с мочой и калом, слюной, желчью, молоком. Процесс ускоряется под влиянием димеркаптола. Через неповрежденную кожу мышьяк и его соли не всасываются. Смертельная доза для неорганических препаратов мышьяка составляет 0,05-0,1 г. Однако иногда и большие дозы могут не привести к смерти. Отмечают как повышенную чувствительность к мышьяку, так и привыкание к нему. Мышьяк обладает способностью кумулироваться. Если при остром отравлении он концентрируется в основном в желудочно-кишечном тракте и паренхиматозных органах, то при хроническом отравлении накапливается преимущественно в костях и ороговевших тканях (волосы, ногти, кожа). Патологоанатомическая картина при быстро протекающих отравлениях нехарактерна. При медленно текущих отравлениях отмечают жировое перерождение печени, почек, сердечной мышцы, местами кровоизлияния в серозных оболочках, жидкое (в виде рисового отвара) содержимое кишечника. Мышьяк хорошо сохраняется в биологическом материале и может быть обнаружен в ней: через несколько лет после смерти. Большое значение придают количественному определению мышьяка в органах, так как он относится к числу чрезвычайно распространенных в природе элементов, содержится в почве, воде и т. п. Поэтому при судебно-химических исследованиях эксгумированных трупов в лабораторию вместе с органами должны быть доставлены образцы земли, изъятой из шести участков с места захоронения (над гробом, под гробом, у боковых поверхностей и концов гроба), а также части одежды, украшения и доски гроба. Содержание мышьяка в серной кислоте может привести к попаданию его в патоку и другие пищевые продукты. В животных и растительных продуктах, например в сырых плодах и овощах, мышьяк может содержаться в значительных количествах. Количество мышьяка, принимаемое человеком с пищей, в зависимости от состава ее колеблется и может достигать 1 мг в сутки. По данным Войнара, содержание мышьяка в органах человека колеблется в пределах 0,008-0,2 мг в 100 г сырого органа, а содержание мышьяка в коже и волосах может достигать 600 мг в 100 г. В большинстве случаев результаты химико-токсикологического исследования помогают решить вопрос, в какой форме или каким путем попал мышьяк в объект исследования. Примерами этому может служить следующее: а) совместное обнаружение в объекте исследования мышьяка и меди при отравлениях швейнфуртской зеленью; б) одновременное нахождение мышьяка в органах эксгумированного трупа и в земле кладбища или нахождение мышьяка в органах трупа и ненахождение его в земле кладбища. Для исследования на растворимые и, следовательно, способные проникнуть в труп соединения мышьяка из земли, находящейся вокруг гроба, 200-500 г земли последовательно извлекают водой, водным раствором аммиака и соляной кислотой. Вытяжки подвергают минерализации и исследуют на мышьяк. в) Одновременное обнаружение мышьяка после минерализации, например, мочи, и получение азокрасителя при наличии в ней органических препаратов мышьяка. Для второй реакции 10 мл мочи подкисляют соляной кислотой, охлаждают до 0°, добавляют осторожно 4-5 капель 0,5 % раствора нитрита натрия и наслаивают 5 мл 1 % раствора резорцина – красное кольцо на границе слоев указывает на наличие в исследуемом материале аминогруппы. г) Обнаружение в объекте исследования крупинок мышьяковистого ангидрида. Крупинки мышьяковистого ангидрида трудно растворимы в воде, возгоняются, давая кристаллические возгоны (тетраэдры и октаэдры), а при нагревании с углем восстанавливают до металлического мышьяка. Растворы соляной кислоты дают и другие качественные реакции на ион мышьяка. Обнаружение мышьяка Применяемые в химико-токсикологическом анализе методы обнаружения мышьяка основаны на переведении его в гидрид мышьяка и на последующем определении гидрида мышьяка при помощи реакций Зангер-Блека и реакции Марша. При этих реакциях из соединений мышьяка выделяется гидрид мышьяка, который летуч и ядовит. Поэтому при выполнении данных реакций требуется особая осторожность. Классическими методами обнаружения мышьяка при химико-токсикологическом анализе является: метод Марша, предложенный английским химиком Джеймсом Маршем 1836 г. Достоинствами способа являются: 1) возможность многократной проверки наличия или отсутствия мышьяка в исследуемой пробе; 2) наглядность, доказательность, специфичность. В то же время обнаружение мышьяка по методу Марша требует затраты значительного количества времени эксперта-химика – более 3-х часов. Поэтому в качестве ориентирующей реакции, имеющей только отрицательное значение, в дробном обнаружении мышьяка введена реакция Зангер-Блека, проведение которой осуществляется в течение 60 мин. Реакция Зангер-Блека неспецифична для мышьяка, что ограничивает значение её в токсикологической химии, но высокочувствительна. Чувствительность реакции достигает 0,1 мкг мышьяка в исследуемом объёме. При отрицательном результате этой чувствительной реакции отпадает необходимость в проведении реакции Марша. При положительном результате, подтверждение обнаружения мышьяка реакцией Марша является обязательным. Реакция Зангер-Блека позволяет сочетать качественное обнаружение мышьяка (при его малых количествах) с полуколичественным определением. Метод основан на восстановлении соединений мышьяка до гидрида мышьяка, который затем реагирует с хлоридом или бромидом ртути (II). Реакция выполняется в специальном приборе (рис. 5). 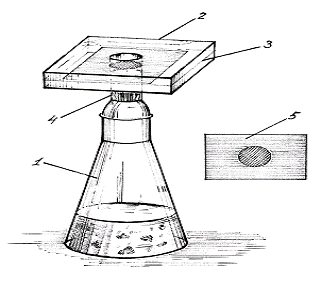 Рис. 1. Прибор Зангер-Блека 1 – колба; 2 – насадка с тампоном ваты, пропитанной раствором свинца ацетата; 3 – бумага, обработанная раствором хлорида ртути (II); 4 – ватный тампон; 5 – проявленная реактивная бумага. Восстановление соединений мышьяка производится водородом в момент его выделения, который получают при взаимодействии металлического цинка с кислотой серной: H2SO4 + Zn → ZnSO4 + H2 Металлический цинк и серная кислота, применяемые для получения водорода должны быть судебнохимически чистые (схч), т.е. не содержать мышьяка. Для ускорения реакции между цинком и серной кислотой применяют «купрированный» цинк. Куприрование осуществляется погружением цинка на несколько минут (до потемнения цинка) в 0,05 % раствор сульфата меди (II) с последующим промыванием водой. Куприрование необходимо потому, что чистый цинк плохо реагирует с серной кислотой. Водород, образовавшийся при взаимодействии серной кислоты и цинка, восстанавливает соединения мышьяка до арсина (AsH3). AsO2– + 7H+ → AsH3 + 2H2O AsO33– + 9H+ → AsH3 + 3H2O AsO43– + 11H+ → AsH3 + 4H2O Скорость восстановления соединений трёх- и пяти-валентного мышьяка (арсенитов и арсенатов) водородом различна. Арсениты восстанавливаются водородом легче, чем арсенаты. В присутствии солей железа (II) или олова (II) арсенаты легко восстанавливаются в арсениты. AsO43– + Sn2+ + 4H+ → AsO2– + Sn4+ + 2H2 AsO2– + 7H+ → AsH3 + 2H2O Образовавшийся гидрид мышьяка реагирует с хлоридом или бромидом ртути (II), которым пропитана фильтровальная бумага. В результате этой реакции образуется ряд окрашенных соединений, которые окрашивают бумагу в виде жёлтого или коричневого пятна: AsH3 + HgCl2 → AsH2(HgCl) + HCl AsH3 + 2HgCl2 → AsH(HgCl)2 + 2HCl AsH3 + 3HgCl2 → As (HgCl) 3 + 3 HCl AsH3 + As(HgCl)3 → As2Hg3 + 3HCl Сероводород, выделяющийся при взаимодействии водорода с серной кислотой, реагирует с хлоридом или бромидом ртути (II). В результате этой реакции образуется сульфид ртути (II) тёмно-коричневого цвета, который маскирует, имитирует окраску пятен. Для связывания сероводорода применяют вату, пропитанную раствором ацетата свинца: H2S + Pb(CH3COO)2 → PbS + 2CH3COOH В колбу прибора Зангер-Блека (рис. 1) вносят 4 мл минерализата, 10 мл 25 % раствора серной кислоты, 5 мл воды, 1 мл 10 % раствора хлорида олова (II) в 50 % растворе серной кислоты и 6-8 гранул купрированного цинка. Колбу закрывают насадкой, в которую вложена бумага, пропитанная хлоридом ртути, а ниже вставлен тампон ваты, пропитанный раствором ацетата свинца. Через 60 мин реактивную бумажку извлекают, отмечают окраску пятна. В зависимости от количества мышьяка, находящегося в объекте исследования, бумажка окрашивается в цвета от светло-жёлтого до тёмно-коричневого. Реакция Марша основана на восстановлении соединений мышьяка водородом в момент его выделения и на последующем термическом разложении образовавшегося при этом гидрида мышьяка: AsO2– + 7H+ → AsH3 + 2H2O 2AsH3 Обнаружение мышьяка проводится на приборе Марша. Прибор Марша в современном варианте состоит из нескольких частей: конической колбы ёмкостью 150 мл, к горлу которой пришлифована капельная воронка и стеклянная трубка, согнутая под прямым углом; хлор-кальциевой трубки; восстановительной трубки, обычно называемой трубкой Марша. Восстановительная трубка изготавливается из тугоплавкого стекла или кварца и имеет в нескольких местах сужения (диаметр 1,5 мм), при внутреннем диаметре трубки 4-5 мм, а конец её согнут почти под прямым углом и оттянут. Работа на приборе Марша включает три этапа. 1. Сборка прибора и вытеснение из него воздуха водородом В колбу прибора Марша помещают 10 г купрированного цинка. В хлоркальциевую трубку помещают безводный гранулированный хлорид кальция, который предназначен для осушения водорода и арсина (AsH3), выходящих из колбы. Колбу, хлоркальциевую и восстановительную трубки соединяют друг с другом (встык) резиновыми трубками. Собранный таким образом прибор Марша должен быть герметичным. В капельную воронку прибора наливают 20 мл 10 % раствора серной кислоты, которую небольшими порциями (по 4-5 мл) приливают к «купрированному» цинку. В капельной воронке необходимо оставлять 8-10 мл раствора серной кислоты, которая препятствует попаданию воздуха в прибор Марша. Воздух может быть причиной взрыва прибора при нагревании восстановительной трубки или при зажигании выходящих из неё газов. В течение 15-20 мин из прибора вытесняют воздух. Чтобы убедиться в полноте вытеснения воздуха водородом из прибора Марша, над выходным отверстием восстановительной трубки помещают узкую пробирку донышком вверх. Через 4-5 мин пробирку закрывают пальцем и, не переворачивая её, относят от прибора и зажигают. В случае если воздух из прибора вытеснен, водород вспыхивает без взрыва (без хлопка). 2. Проверка прибора и реактивов на отсутствие мышьяка После удаления воздуха из прибора приступают к проверке наличия мышьяка в реактивах (серной кислоте, цинке) и посуде. Для этой цели: а) зажигают водород у открытого конца восстановительной трубки. При наличии мышьяка пламя приобретает синеватую окраску; б) восстановительную трубку в широкой её части нагревают до слабо-красного каления, а суженное место восстановительной трубки за нагреваемым широким участком охлаждают. Через час проверяют охлаждаемую часть восстановительной трубки на отсутствие буровато-серого налёта металлического мышьяка. При отрицательных результатах испытания аппарата и реактивов в течение часа переходят к исследованию минерализата. 3. Исследование минерализата: Смешивают 1/10 часть минерализата с 1-2 мл 10 % раствора хлорида олова (II) в серной кислоте (1:3) и жидкость переносят в капельную воронку. Постепенно жидкость вводят в колбу. В процессе исследования в приборе Марша проводят ряд реакций и наблюдений. 1. Отставив горелку от нагретой части трубки и охладив её, наблюдают, не окрашено ли пламя у конца восстановительной трубки в синеватый цвет, характерный для мышьяковистого водорода; не ощущается ли запах чеснока, не появляется ли буровато-серый налёт при внесении холодных частей фарфоровой пластинки в пламя восстановительной трубки. 2. Пламя водорода восстановительной трубки тушат и к отверстию оттянутого конца подносят фильтровальную бумагу, смоченную 2-5 % раствором нитрата серебра. Наблюдают, не появится ли почернение бумаги в результате образования металлического серебра: AsH3 + 3AgNO3 → AsAg3 + 3HNO3 AsAg3 + 3AgNO3 → AsAg3 + 3AgNO3 AsAg3 + 3AgNO3 + 3H2O → 6Ag + H3AsO3 + 3HNO3 Горелку вновь подставляют под трубку Марша и продолжают исследование в течение часа. По истечении указанного времени смотрят, не появилось ли серовато-бурого налёта с металлическим блеском в охлаждаемой части восстановительной трубки. Если значительный тёмный налёт образуется раньше, то не обязательно нагревать в течение часа. Исследование тёмного налёта. В случае получения плотного налёта, его подвергают дополнительному исследованию, т.к. налёты могут давать и другие вещества (сурьма, селен, сера, уголь и др.). Для чего восстановительную трубку отсоединяют от прибора Марша и место налёта осторожно нагревают. Металлический мышьяк и сурьма при этом окисляются и откладываются в виде белого налёта оксидов (As2O3 и Sb2O3) в холодных местах восстановительной трубки. При рассматривании налёта под микроскопом при наличии мышьяка видны характерные кристаллы мышьяковистого ангидрида As2O3 в виде октаэдров, а оксид сурьмы аморфный. Образование кристаллов октаэдрической формы является одним из важнейших доказательств наличия мышьяка в минерализате, а микрофотография кристаллов может служить доказательством правильности выводов эксперта-химика об обнаружении мышьяка в объектах исследования. В случаях, когда налёт мышьяковистого ангидрида в трубке Марша не имеет ясно выраженного кристаллического строения, что бывает при количествах мышьяка менее 0,05 мг, поступают следующим образом: налёт мышьяковистого ангидрида растворяют в 2-3 каплях 50 % раствора азотной кислоты и переносят на предметное стекло. Раствор осторожно упаривают досуха. Сухой остаток растворяют в 1-2 каплях 10 % раствора хлороводородной кислоты, в раствор вносят 1-2 кристалла цезия хлорида (CsCl), а затем, через некоторое время, если никакого осадка не появилось (отсутствие сурьмы), добавляют несколько кристаллов йодида калия – при наличии мышьяка выпадает ярко-красный осадок: Cs2AsI5∙2,5H2O, имеющий под микроскопом вид шестилучевых звёздочек и шести-угольников. Кристаллы Cs2AsI5∙2,5H2O по своему виду напоминают Cs2SbI5∙2,5H2O. При действии пиридина на красный осадок Cs2AsI5∙2,5 H2O последний растворяется, а по краям образуются зеленовато-жёлтые игольчатые кристаллы. При наличии сурьмы кристаллы Cs2SbI5∙2,5H2O теряют окраску, но сохраняют форму |
