ТКМ 5. Кристаллическое строение твердых тел. Модель ближнего взаимодействия
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
|
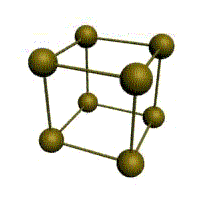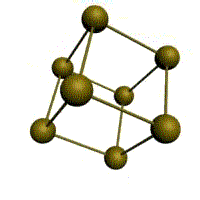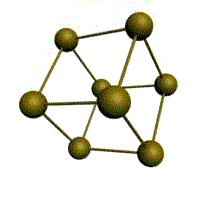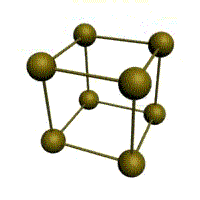
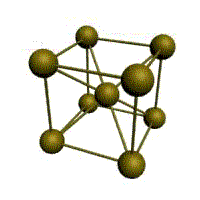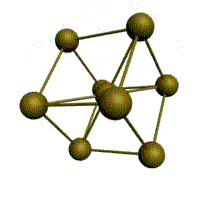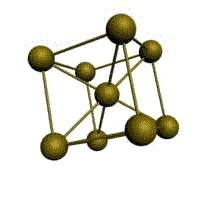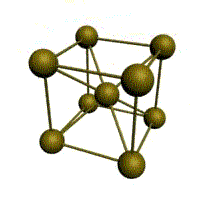
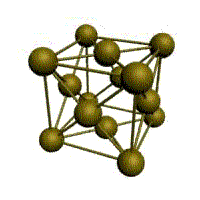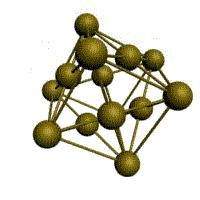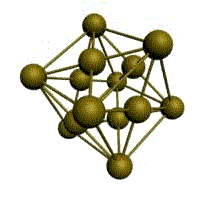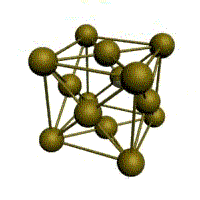
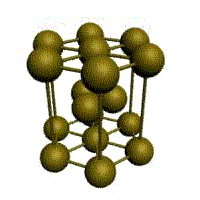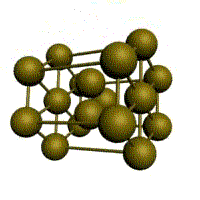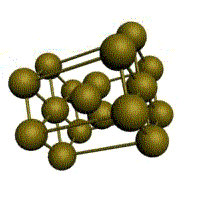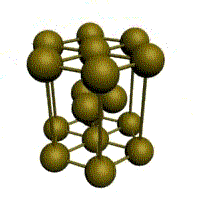
Кристаллическое строение твердых тел. Модель ближнего взаимодействия. Все вещества могут находиться в трех агрегатных состояниях: твердом, жидком и газообразном, переходы между которыми (называемые фазовые переходы) сопровождаются скачкообразными изменениями свободной энергии F (F=U-TS, где U – внутренняя энергия; T – температура; S – энтропия), энтропия плотности и других физических свойств. В кристаллических твердых телах, в том числе и металлах, расположение атомов полностью упорядочено, о чем можно судить по часто встречающейся симметрии их внешней формы, правильной внешней органке. В кристаллах имеет место дальний порядок, т.е. упорядоченное расположение частиц по отношению к любой частице наблюдается в пределах значительного объема. Характерная черта кристаллического состояния, отличающая его от жидкого и газообразного, заключается в наличии анизотропии, т.е. зависимости ряда физических свойств (механических, тепловых, электрических,оптических) от направления. Тела, свойства которых одинаковы по всем направлениям, являются изотропными (газы, жидкости, аморфные тела). Жидкости и твердые тела относят к конденсированному состоянию вещества. В отличие от газообразного состояния у вещества в конденсированном состоянии атомы расположены ближе друг к другу, что приводит к их более сильному взаимодействию и, как следствие этого, жидкости и твердые тела имеют постоянный собственный объем. Для теплового движения атомов в жидкости характерны малые колебания атомов вокруг равновесных положений и частые перескоки из одного равновесного положения в другое. Это приводит к наличию в жидкости только так называемого ближнего порядка в расположении атомов, т. е. некоторой закономерности в расположении соседних атомов на расстояниях, сравнимых с межатомными. Для жидкости в отличие от твердого тела характерно такое свойство, как текучесть. Атомы в твердом теле, для которого в отличие от жидкого тела характерна стабильная, постоянная собственная форма, совершают только малые колебания около своих равновесных положений. Это приводит к правильному чередованию атомов на одинаковых расстояниях для сколь угодно далеко удаленных атомов, т. е существования так называемого дальнего порядка в расположении атомов. Такое правильное, регулярное расположение атомов в твердом теле, характеризующееся периодической повторяемостью в трех измерениях образует кристаллическую решетку, а тела, имеющие кристаллическую решетку, называют твердыми телами. Кроме того, существуют аморфные тела (стекло, воск и т. д.). В аморфных телах атомы совершают малые колебания вокруг хаотически расположенных равновесных положений, т. е. не образуют кристаллическую решетку. Аморфное тело находится с термодинамической точки зрения в неустойчивом (так называемом метастабильном) состоянии и его следует рассматривать как сильно загустевшую жидкость, которая с течением времени должна закристаллизоваться, т. е. атомы в твердом теле должны образовать кристаллическую решетку и превратиться в истинно твердое тело. Аморфное состояние образуется при быстром- (106 О С/с и более) охлаждении расплава. Например, при охлаждении ряда сплавов из жидкого состояния образуются так называемые металлические стекла, обладающие специфическими физико-механическими свойствами. Атомы в кристаллическом твердом теле располагаются в пространстве закономерно, периодически повторяясь в трех измерениях через строго определенные расстояния, т. е. образуют кристаллическую решетку. Кристаллическую решетку можно «построить», выбрав для этого определенный «строи тельный блок» (аналогично постройке стены из кирпичей) и многократно смещая этот блок по трем, непараллельным направлениям. Такая «строительная» единица кристаллической решетки имеет форму параллелепипеда и называется элементарной ячейкой. Все элементарные ячейки, составляющие кристаллическую решетку, имеют одинаковую форму и объемы. Атомы могут располагаться как в вершинах элементарной ячейки, так и в других ее точках (в узлах кристаллической решетки). В первом случае элементарные Типы кристаллических решёток и их основные характеристики. 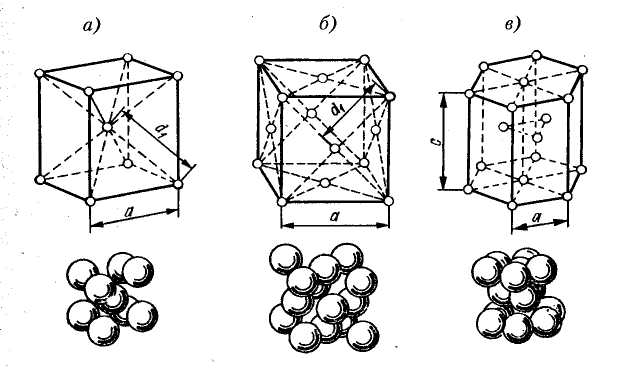 Рисунок 1 – Основные типы кристаллических решеток металлов: а – кубическая объмно-центрированная (ОЦК); б – кубическая гранецентрированная (ГЦК); в – гексагональная плотноупакованная (ГПУ) Общность кристаллического строения металлов обусловливает и общность некоторых свойств. В частности, металлы, кристаллизующиеся в гексагональной и ОЦК - решётках, имеют значительно большую склонность к хрупким разрушениям, чем металлы, кристаллизующиеся в ГЦК - решётке. Так, хром, вольфрам, молибден, ниобий (ОЦК - решётка), а также магний, цинк, кадмий (гексагональная решётка) являются в обычных условиях хрупкими или малопластичными металлами. Вместе с тем, алюминий, медь, никель, серебро, золото, платина, свинец (ГЦК -решётка) обладают весьма высокой пластичностью.
Рис. 1.2.Основные типы кристаллических решеток металлов Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны (так называемый электронный газ). Такой тип структуры называется металлической связью. Тип решетки определяется формой элементарного геометрического тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела. Металлы имеют относительно сложные типы кубических решеток - объемно центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки. Основу ОЦК-решетки составляет элементарная кубическая ячейка (рис. 1.2,б), в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один атом в центре его объема, т. е. на пересечении его диагоналей. Такой тип решетки в определенных диапазонах температур имеют железо, хром, ванадий, вольфрам, молибден и др. металлы. У ГЦК-решетки (рис. 1.2, в) элементарной ячейкой служит куб с центрированными гранями. Подобную решетку имеют железо, алюминий, медь, никель, свинец и др. металлы. Третьей распространенной разновидностью плотноупакованных решеток является гексагональная плотноупакованная (ГПУ, рис. 1.2, г). ГПУ-ячейка состоит из отстоящих друг от друга на параметр спараллельных центрированных гексагональных оснований. Три иона (атома) находятся на средней плоскости между основаниями. У гексагональных решеток отношение параметра с/авсегда больше единицы. Такую решетку имеют магний, цинк, кадмий, берилий, титан и др. Компактностькристаллической решетки или степень заполненности ее объема атомами является важной характеристикой. Она определяется такими показателями как параметр решетки, число атомов в каждой элементарной ячейке, координационное число и плотность упаковки. Параметр решетки - это расстояние между атомами по ребру элементарной ячейки. Параметры решетки измеряется в нанометрах (1 нм = 10-9 м = 10 Å). Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а. Для характеристики гексагональной решетки принимают два параметра - сторону шестигранника аи высоту призмы с.Когда отношение с/а =1,633, то атомы упакованы наиболее плотно, и решетка называется гексагональной плотноупакованной (рис. 1.2 г). Некоторые металлы имеют гексагональную решетку с менее плотной упаковкой атомов (с/а> 1,633). Например, для цинка с/а= 1,86, для кадмия с/а =1,88. Параметры а кубических решеток металлов находятся в пределах от 0,286 до 0,607 нм. Для металлов с гексагональной решеткой алежит в пределах 0,228-0,398 нм, а с в пределах 0,357- 0,652 нм. Параметры кристаллических решеток металлов могут быть измерены с помощью рентгеноструктурного анализа. При подсчете числа атомов в каждой элементарной ячейке следует иметь в виду, что каждый атом входит одновременно в несколько ячеек. Например, для ГЦК-решетки, каждый атом, находящийся в вершине куба, принадлежит 8 ячейкам, а атом, центрирующий грань, двум. И лишь атом, находящийся в центре куба, полностью принадлежит данной ячейке. Таким образом, ОЦК- и ГЦК-ячейки содержат соответственно 2 и 4 атома. Под координационным числом понимается количество ближайших соседей данного атома. 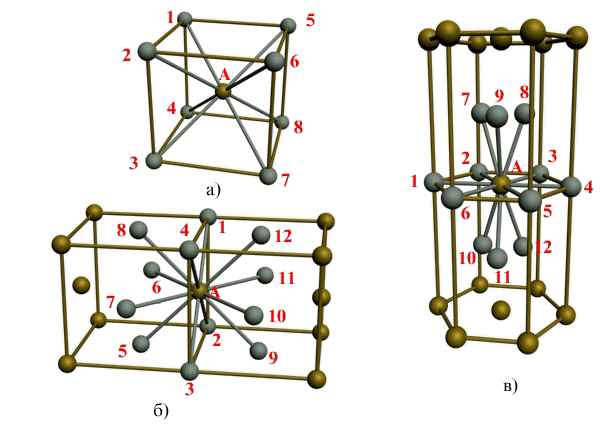 Рис. 1.3. Координационное число в различных кристаллических решетках для атома А: а) - объемноцентрированная кубическая (К8); б) - гранецентрированная кубическая (К12); в) - гексагональная плотноупакованная (Г12) В ОЦК решетке (рис. 1.3, а)атом А(в центре) находится на наиболее близком равном расстоянии от восьми атомов, расположенных в вершинах куба, т. е. координационное число этой решетки равно 8 (К8). В ГЦК решетке (рис. 1.3, б)атом А(на грани куба) находится на наиболее близком равном расстоянии от четырех атомов /, 2, 3, 4,расположенных в вершинах куба, от четырех атомов 5, 6, 7, 8,расположенных на гранях куба, и, кроме того, от четырех атомов 9, 10, 11, 12,принадлежащих расположенной рядом кристаллической ячейке. Атомы 9, 10, 11, 12симметричны атомам 5, 6, 7, 8.Таким образом, ГЦК решетки координационное число равно 12 (К12). В ГПУ решетке при с/а =1,633 (рис. 1.3, в) атом Ав центре шестигранного основания призмы находится на наиболее близком равном расстоянии от шести атомов /, 2, 3, 4, 5, 6,размещенных в вершинах шестигранника, и от трех атомов 7, 8, 9,расположенных в средней плоскости призмы. Кроме того, атом Аоказывается на таком же расстоянии еще от трех атомов 10, 11, 12,принадлежащих кристаллической ячейке, лежащей ниже основания. Атомы 10, 11, 12симметричны атомам 7, 8, 9. Следовательно, для ГПУ решетки координационное число равно 12(Г12). Плотность упаковки представляет собой отношение суммарного объема, занимаемого собственно атомами в кристаллической решетке, к ее полному объему. Различные типы кристаллических решеток имеют разную плотность упаковки атомов. В ГЦК решетке атомы занимают 74 % всего объема кристаллической решетки, а межатомные промежутки («поры») 26 %. В ОЦК решетке атомы занимают 68 % всего объема, а «поры» 32 %. Компактность решетки зависит от особенностей электронной структуры металлов и характера связи между их атомами. От типа кристаллической решетки сильно зависят свойства металла. Основные свойства кристаллов: анизотропия и полиморфизм. Полиморфизм. Для ряда металлов характерно явление полиморфизма. Этим термином называют способность вещества формировать различные типы кристаллических решеток. Так, при разных температурах железо может иметь ОЦК или ГЦК решетку, кобальт — ГЦК или ГПУ решетку. Полиморфизм характерен и для других металлов. Различные кристаллические формы одного и того же вещества называются полиморфнымиили аллотропными модификациями. Превращение одной модификации в другую с изменением кристаллической решетки называется полиморфным превращением. Полиморфное превращение происходит в результате нагрева или охлаждения: в чистых металлах при постоянной температуре, а в сплавах — в интервале температур. Полиморфизмом обладают железо, кобальт, титан олово, марганец, ванадий, стронций, кальций, цирконий и др. Физическая суть полиморфного превращения заключается в том, что кристаллическое вещество при разных температурах переходит в состояние с меньшим запасом свободной энергии. Например, полиморфное равновесие титана наблюдается при 880 °С, а олова - при 13,2 °С. Анизотропия металлов. В кристаллических решетках атомная плотность по различным плоскостям неодинакова — на единицу площади разных атомных плоскостей приходится неодинаковое количество атомов. Сравним, например, для ОЦК решетки количество атомов в плоскости, совпадающей с гранью, и диагональной. Вследствие этого свойства в различных плоскостях и направлениях кристаллической решетки будут неодинаковыми. Различие свойств по разным кристаллографическим направлениям называется анизотропией кристалла. 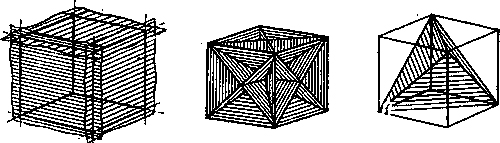 Условные плоскости в кубической решетке с наиболее плотной упоковкой атомов 1 - плоскости (100); 2 - плоскости (110); 3 - плоскости (111); Основные свойства: Свойства металлов, применяемых в строительстве, определяются в основном механическими и технологическими характеристиками. Для строительства представляют наибольший интерес сплавы металлов, особенно железа с углеродом и другими элементами (марганцем, никелем, хромом, титаном, кремнием и др.). Такие сплавы составляют группу черных металлов и носят название чугун и сталь. Большое значение в строительстве имеет также алюминий и его сплавы. Механические свойства металлов характеризуются пределом прочности при растяжении, пределом текучести, относительным удлинением, твердостью, ударной вязкостью; технологические свойства - жидкотекучестью, свариваемостью, ковкостью, электропроводностью, магнитностью и др. Предел прочности при растяжении -напряжение в момент разрушения образца, испытываемого на разрыв. Предел текучести - минимальное напряжение, при котором образец деформируется без увеличения нагрузки. Относительное удлинение - отношение приращения длины образца после деформации растяжения к его первоначальной длине. Максимальное напряжение, при котором сохраняется прямая пропорциональность между удлинением образца и приложенной нагрузкой, называют пределом пропорциональности. Напряжение, соответствующее появлению первых признаков пластической деформации, остающейся после нагрузки образца, называют пределом упругости. Металлы испытывают на растяжение с помощью разрывных машин, оборудованных приспособлением для записи кривой зависимости между нагрузкой и удлинением образца. Такая кривая называется диаграммой растяжения. У одних металлов на диаграмме растяжения фиксируется площадка текучести, указывающая на способность металла подвергаться пластическим деформациям при постоянном напряжении, у других такая площадка отсутствует, что указывает "а непрерывный рост деформации с возрастанием нагрузки. Твердость металла (НВ) является косвенным показателем его прочности. Твердость металла определяют: вдавливанием стального шарика в поверхность металла (метод Бринеля); вдавливанием алмазного конуса или стального шарика с определением твердости по глубине отпечатка (метод Роквелла) и др. В конструкциях и деталях металл под воздействием многократных повторно-переменных нагрузок может разрушаться при напряжении значительно меньшем, чем предел прочности. Это явление называют усталостью металла. Испытывают металл на усталость аппаратами, переменно изгибающими образцы в противоположные стороны, скручивающими их. В металле, работающем длительное время при повышенной температуре, происходят пластические деформации, постепенно увеличивающиеся даже при небольших нагрузках. Это явление называют ползучестью металла. Свойства стали определяют также технологическими пробами изучением химического состава. Технологическими пробами называют испытания, при которых металл деформируется под воздействием внешних сил, действующих на него при обработке или в условиях службы в сооружениях (изгиб в холодном и нагретом состояниях, выдавливание, закаливаемость, свариваемость, осадка в холодном состоянии). Способность расплавленного металла хорошо заполнять литейные формы называется жидкотекучестью. Сокращение объема расплавленного металла при застывании и охлаждении называют усадкой. Способность металла под воздействием внешних сил деформироваться без разрушения и сохранять остаточную деформацию называют пластичностью. Наибольшей электропроводностью обладают медь и алюминий. Некоторые сплавы имеют высокое электросопротивление и используются для превращения электрической энергии в тепловую (нихром). Некоторые металлы (железо, кобальт, никель) обладают магнитными свойствами и носят название ферромагнитных. При нагреве до определенной температуры эти металлы теряют магнитные свойства (например, железо - при 768° С, кобальт-при 1100° С, никель - при 350° С). Коэффициент линейного расширения у различных металлов различен. Наибольшие значения коэффициента расширения имеют цинк, свинец, кадмий, магний, алюминий, хром, олово; наименьшие значения - молибден, вольфрам, железо и др. Температура плавления металлов находится в пределах от 232 (для олова) до 3390° С (для вольфрама). Температура плавления может резко изменяться при вводе в металл новых элементов. Так, чистое железо плавится при температуре 1539° С, а сплав с содержанием 4,3% углерода (чугун) -при температуре около 1130° С. Дефекты кристаллического строения, геометрическая классификация. Дефекты кристаллического строения металлов.В реальном кристалле всегда имеются дефекты строения. Дефекты кристаллического строения подразделяют по геометрическим признакам на точечные, линейные и поверхностные. Точечные дефекты. Эти дефекты малы во всех трех измерениях, и размеры их не превышают нескольких атомных диаметров. К точечным дефектам относятся вакансии, пли дырки», т. е. узлы решетки, в которых атомы отсутствуют. Вакансии чаще образуются в результате перехода атомов из узлов решетки на поверхность (границу зерна, пустоты, трещины и т. д.) или их полного испарения с поверхности кристалла и реже в результате перехода в междоузлие. В кристалле всегда имеются атомы, кинетическая энергия которых значительно выше средней, свойственной данной температуре нагрева. Такие атомы, особенно расположенные вблизи поверхности, могут выйти на поверхность кристалла, а их место займут атомы, находящиеся дальше от поверхности, а принадлежавшие им узлы окажутся свободными, т. е. возникнут тепловые вакансии.С повышением температуры концентрация вакансий возрастает, может достигать 1%по отношению к числу атомов в кристалле. Быстрым охлаждением от данной температуры можно зафиксировать эти вакансии при нормальной температуре (закалка вакансий).Точечные несовершенства кристаллической решетки появляются и в результате действия атомов примесей, которые, как правило, присутствуют даже в самом чистом металле.'Точечные дефекты вызывают местное искажение кристаллической решетки. Смешения вокруг вакансий возникают только в первых двух слоях соседних атомов и составляют доли межатомного расстояния. Вокруг межузельного атома в плотноупакованных решетках смещение соседей значительно больше, чем вокруг вакансий.Точечные дефекты оказывают влияние на некоторые физические свойства металла (электропроводность, магнитные свойства и др.) и предопределяют процессы диффузии в металлах и сплавах.Линейные дефекты. Линейные несовершенства имеют малые размеры в двух измерениях и большую протяженность в третьем измерении. Эти несовершенства называются дислокациями.Краевая дислокация представляет собой локализованное искажение кристаллической решетки, вызнанное наличием в ней «лишней» атомной полуплоскости или экстраплоскости, перпендикулярной к плоскости чертежа.Если экстраплоскость находится в верхней части кристалла, то дислокацию называют положительной, а если в нижней—то отрицательной. Различие между положительной и отрицательной дислокацией чисто условное. Переворачивая кристалл, мы превращаем отрицательную дислокацию в положительную. Знак дислокации важен при анализе их взаимодействия. Кроме краевых различают еще винтовые дислокации. Винтовые дислокации в отличие от краевых располагаются параллельно направлению сдвига. При наличии винтовой дислокации кристалл можно рассматривать как состоящий из одной атомной плоскости, закрученной в виде винтовой поверхности.Дислокации окружены полями упругих напряжений, вызывающих искажение кристаллической решетки. В краевой дислокации выше края экстра-плоскости межатомные расстояния меньше нормальных, а ниже края — больше.Энергия искажения кристаллической решетки является одной из важнейших характеристик дислокации любого типа. Чтобы оценить степень искажения решетки, вызванной линейной дислокацией, следует сравнить совершенный кристалл с кристаллом, содержащим дислокацию. Дислокации образуются в процессе крист.металлов из группы вакансий, а также в процессе пластической деформации и фазовых превращений. Поверхностные дефекты. Они представляют собой поверхности раздела между отдельными зернами или их блоками поликристаллического металла. Каждое зерно металла состоит из отдельных блоков, или субзерен, образующих мозаичную структуру. Зерна обычно разориентированы относительно друг друга на величину, достигающую от нескольких их десятков. Блоки и субзерна, повернуты по отношению др.др. на угол от нескольких секунд до нескольких минут, имеют размеры на три-четыре порядка величины меньше размеров кристаллитов. В пределах каждого блока, или субзерна, решетка почти идеальная, если не учитывать точечных несовершенств. Размеры блоков, или субзерен, оказывают большое влияние на свойства металла. Границы между отдельными кристаллитами представляют собой переходную область шириной в 5-10 межатомных расстояний, в которой решетка одного кристалла, имеющего определенную кристаллографическую ориентацию, переходит в решетку другого кристалла, имеющего иную кристаллографическую ориентацию. В связи с этим на границе зерна атомы расположены менее правильно, чем в объеме зерна. Кроме того, по границам зерен в технических металлах концентрируются примеси, что еще больше нарушает правильный порядок расположения атомов. Несколько меньшие нарушения наблюдаются на границах блоков или субзерен.Границы блоков, а также малоугловые границы зерен образованы дислокациями. С увеличением угла разориентировки блоков или субзерен и уменьшения их величины плотность дислокаций в металле увеличивается. Атомы на границах зерен имеют повышенную потенциальную энергию. Такую повышенную энергию имеют и атомы, расположенные на поверхности кристалла, вследствие нескомпенсированности сил межатомного взаимодействия. Точечные дефекты. Механизмы их образования. Зависимость равновесной концентрации вакансий от температуры. К ним относятся атомы инородных элементов (легирующих элементом или примесей), межузельные атомы (атомы основного элемента, по каким-либо причинам покинувшие узлы кристаллической решетки и застрявшие в междоузлиях), вакансии или не занятые атомами узлы кристаллической решетки. Представление о вакансиях было впервые введено Я. И. Френкелем для объяснения процессов диффузии в металлах - материалах с плотноупакованной кристаллической решеткой. При наличии в кристаллической решетки вакансии атом может перескочить из узла решетки в вакантное место. Тем самым вакансия смещается, и процесс диффузии можно описывать как последовательное перемещение атомов или как движение вакансий. Согласно модели Френкеля, при образовании вакансий атом из узла кристаллической решетки перепрыгивает в междоузлие, и появляется пара дефектов - вакансия и межузельный атом, или пара Френкеля. |