Курсовая работа (Проект) по дисциплине на тему
 Скачать 1.84 Mb. Скачать 1.84 Mb.
|
Глава 44.1 Общие понятия о биологически активных веществах.Для дальнейшего рассмотрения ИК-спектров биологически активных соединений рассмотрим, что представляет класс этих сложных органических соединений. Биологически активные вещества – это очень важный класс органических соединений, отвечающий за правильное регулирование жизнедеятельности всех систем организма. Биохимия изучает свойства веществ и механизмы функциональных групп, входящих в их состав, а также какое действие оказывают биологически активные вещества на синтез ДНК, строение клеток и органов. Живой организм постоянно обменивается энергией с окружающей средой и при этом должен сохранять постоянство химического состава. Эти процессы регулируются разными параметрами, однако главную роль занимают биологически активные компоненты. Часть из них поступает с пищей – витамины, другая синтезируется железами внутренней и внешней секреции – гормоны. К биологически активным веществам относятся: витамины, ферменты, гормоны, лекарства. 4.2 ВитаминыВитамины – низкомолекулярные органические соединения различной химической природы, необходимые для осуществления важнейших процессов, протекающих в живом организме. [15] При этом витамины не участвуют в пластическом и энергетическом обмене. Ещё с древних времён людям было известно, что отсутствие определённых продуктов вызывает заболевания. Однако до 1880 г. никто не предполагал, что в пищевых продуктах содержатся маленькие компоненты, оказывающие большое влияние на организм. Своё название витамины получили от латинского слова vita – жизнь. В настоящее время известно более 30 таких соединений. [16] Для нормального развития человеку необходимо ежедневное поступление 100-120 мг витаминов. На сегодняшний день принято обозначать витамины латинскими буквами: A, B, C, D и т.д.. Классифицируются они на растворимые в воде (B1, B2, B3, B6, B12, H, C, P), растворимые в жирах (A, D, E, K), витаминоподобные вещества (B15, U, ПАБК). [17] Необходимость изучения витаминов вызвана тем, что они влияют практически на все сферы жизни: Улучшают сопротивляемость заболеваниям Поддерживают развитие (особенно подрастающего организма) Способствует усвоению микро- и макроэлементов Регулируют обмен веществ 4.3 ФерментыФерменты – это органические катализаторы белковой природы, которые ускоряют реакции, необходимые для функционирования живых организмов. [18] Благодаря их действию скорости многих реакций проходят в миллион раз быстрее, чем в отсутствие ферментов. Действуя, как катализаторы, они уменьшают энергию активации (энергия необходимая для протекания реакции между веществами), тем самым позволяют взаимодействовать многим важным соединениям. Таким образом, становятся возможны реакции, без дополнительных затрат и повышения температуры. Изначально считалось, что ферменты это небольшие вещества, сорбированные на белках, однако позднее выяснили, что они по своей природе являются белками и делятся на анаболические и катаболические. Первые применяются для синтеза органических веществ, вторые для распада. Как и все белки, ферменты образуют компактные структуры – глобулы. Несмотря на то, что ферменты проявляют свойства присущие всем белкам, они также имеют и специфические особенности: зависимость от интервала температур и pH. Многие ферменты работают только при нормальной температуре человеческого тела. Поэтому во время болезни превышение отметки 37° замедляет обменные процессы, связанные с действием ферментов, и ведёт к гибели. В основном, ферменты проявляют своё действие при pH 7. Изменение этого значения приводит к нарушению соотношения катионильных и анионильных групп. В сильнощелочной и сильнокислой среде ферменты теряют свою активность. На рис. 20 показана активность некоторых ферментов в разных средах. 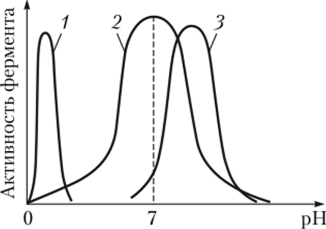 Рис 20. Зависимость активности ферментов от pH среды. 1 – пепсин, 2 – амилаза, 3 – химотриисин. Имея большой запас ферментов, в клетке возможны реакции распада полимерные веществ до их мономеров: жиров до глицерина и жирных кислот, полисахарид до моносахарид, белков до аминокислот. Огромное значение имело открытие в конце прошлого века рибозим (каталитических РНК), т.к. они могут обеспечивать воспроизведение РНК без деятельности белков-ферментов. В настоящее время открыто более 2000 различных ферментов, которые разделены на 6 классов: Оксидоредуктазы (цитохромы) – катализируют ОВР Трансферазы – обеспчивают перенос функциональной группы от одного вещества к другому Гидролазы (эстеразы и пептидазы) – обеспечивают разрыв связей в молекуле путём гидролиза Лиазы – предназначены для разрыва связей С-С, С-О, С-N Изомеразы – обеспечивают изомерные превращения Лигазы – помогают образовать высокоэнергичные связи [19] Необходимость изучения ферментов вызвана невозможностью в их отсутствие протекания реакций живого организма, следовательно и его существования, а также их применением в пищевой промышленности (в пивоварении, сыроварении) и лекарственных препаратах. |
