Курсовая работа (Проект) по дисциплине на тему
 Скачать 1.84 Mb. Скачать 1.84 Mb.
|
ГормоныГормон – это вещество органической природы, которое вырабатывается специализированными клетками желез внутренней секреции, поступает в кровь или лимфу и взаимодействует с клетками мишенями, оказывая влияние на метаболический процессы в них. [20] Гормоны являются биорегуляторами, т.е. помогают синхронизировать функции всех органов. Они осуществляют гуморальную регуляцию по принципу обратной связи, т.е. не только гормоны действуют на систему органов, но и само состояние организма влияет на работу желёз. Например, уменьшение C6H12O6 снижает секрецию гормона инсулина поджелудочной железой. Таким образом, именно гормоны поддерживают гомеостаз – постоянство внутренней среды организма. [21] Гормоны также оказывают влияние на синтез генетической информации, в частности действует на образование соответствующей мРНК, которая служит матрицей для формирования новых ферментов. Таким образом, любое заболевания желез внутренней секреции, вызывает сбой в выработке гормонов, что ведёт к неправильному обмену веществ и нарушению синтеза ферментов. По своей химической природе гормоны можно разделить на 3 группы: Белковые (инсулин, соматропин) – содержат в своём составе большое количество аминокислот Производные аминокислот (тироксин, адреналин) – содержат в своём составе аминогруппу. С  тероидные (кортикостерон, андростандиол, тестестерон, эстрадиол, прогестерон). Являются производными стерана тероидные (кортикостерон, андростандиол, тестестерон, эстрадиол, прогестерон). Являются производными стеранаПептидные (окситоцин, глюкокан, тиреокальцитоин) - представляют собой цепочку соединённых пептидными связями аминокислот Известно, что действие раздражителей возбуждает клетки-рецепторы. Импульсы от них поступают в гипоталамус, где синтезируются первые биологически активные гормоноподобные вещества, они не поступают в кровь, а идут в гипофиз, где выделяются тропные гормоны. Они переносятся через кровь в соответствующие железы внутренней секреции, где вырабатываются сами гормоны. Стоит заметить, что каждые рецептор отвечает за передачу импульса к месту синтеза своего определённого гормона. Например, рецепторы белковых и пептидных гормонов находятся на наружной части клетке, а стероидных во внутренней. [22] Необходимость изучать гормоны вызвана их большой биологической важностью, т.к. они: Регулируют метаболизма Регулируют развитие Обеспечивают адаптацию к окружающей среде Обеспечивают гомеостаз Также необходимо помнить, что избыток или недостаток гормонов, как и витаминов, приводит к заболеваниям. Глава 5 «Применение Ик-спектроскопии в анализе биологически активных соединений»5.1 Интерпретация спектров функциональных групп органических соединенийВсе биологически активные вещества регулируют роль живого организма, а значит, представляют собой углеродные органические структуры. В соответствии с их природой, спектры функциональных групп биологически активных веществ можно рассматривать, как спектры органических соединений. Алкены проявляют полосы поглощения, характерные для двойной связи. У группы =СН2 полосы поглощения находятся в интервале 3060 – 3095 см-1, если же к двойной связи прикреплён радикал, частоты смещаются на 50 см-1 влево. Если водород замещается на фтор, то полосы сдвигаются в правую сторону, однако остальные галогены дают противоположный эффект. Колебания тройной связи алкинов располагаются при 3200 – 3300 см-1 и 2100 – 2300 см-1. При расположении такой связи в конце молекулы можно наблюдать интенсивные пики, но в то же время их практически не заметно при размещении тройной связи в середине. Полосы поглощения ароматических соединений наблюдаются сразу в нескольких областях. Связь С-Н находится в области 3000 – 3100 см-1; скелетная основа С-С 1600, 1580, 1500, 1450 см-1. Как уже было замечено, положение ОН группы органических спиртов во многом определяется наличием водородной связи и степени ассоциации. (Рис. 21) 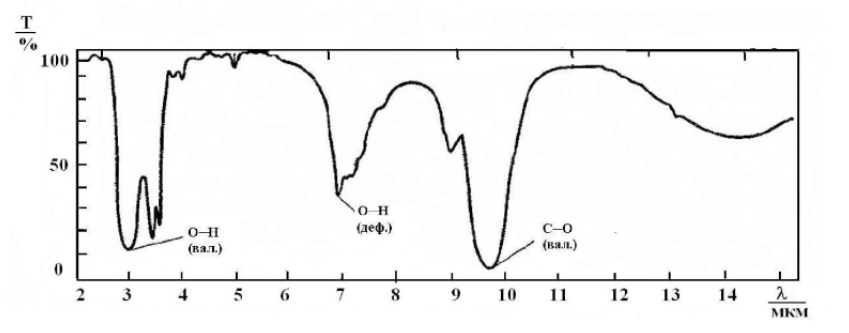 Рис. 21. ИК-спектр алифатического спирта Асимметрические валентные колебания эфирно группы имеют большую интенсивную полосу в области 1150 – 1085 см-1. У альдегидов и кетонов в области 1725 см-1 находится интенсивная полоса валентных колебаний С=О. Если карбонильная группа сопряжена со связью С=С или ароматической системой, максимум полосы поглощения смещается в низкочастотную область: у ароматических альдегидов от 1715 до 1695 см-1, у алкиларилкетонов 1690 см-1, диарилкетонов 1665 см-1. (Рис. 22) 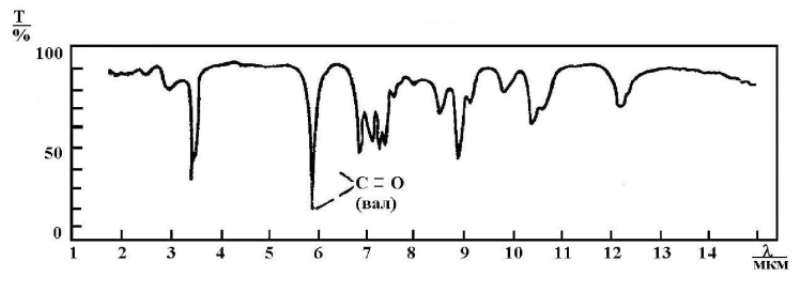 а) 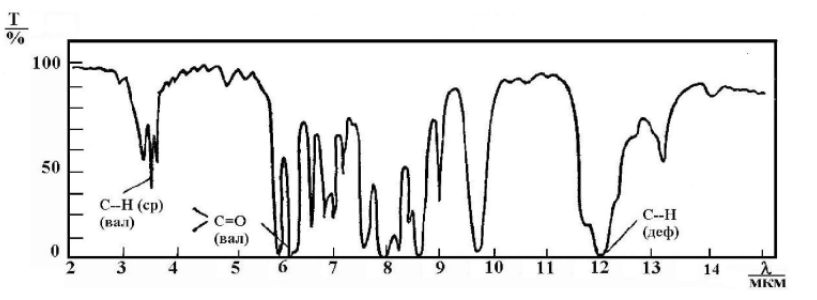 б) Рис. 22. Ик-спектр а) алифатического, б) ароматического альдегида К 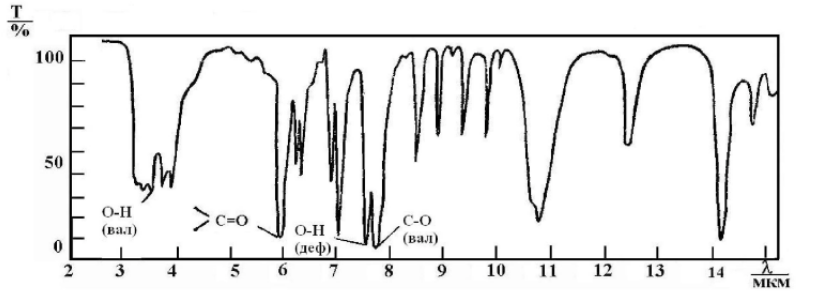 арбоксильные группы вызывают валентные колебания в области 1900 – 1600 см-1, но на частоту этих колебаний оказывают влияние водородные связи, поэтому карбоновую кислоту также можно отличить по пикам ОН группы. (Рис. 23) арбоксильные группы вызывают валентные колебания в области 1900 – 1600 см-1, но на частоту этих колебаний оказывают влияние водородные связи, поэтому карбоновую кислоту также можно отличить по пикам ОН группы. (Рис. 23)Рис. 23. ИК-спектр карбоновых кислот. Нахождение колебаний в спектре аминогруппы определяется агрегатным состоянием вещества, а также наличием водородной связи. В ИК-спектре аминов есть два острых пика при 3500 и 3400 см-1 (Рис. 24), а у вторичных только один. Полосы поглощения алифатических аминов отстают на 300 см-1. Как и гидроксильной группы, при образовании водородной связи, пики амино группы чуть-чуть смещаются в низкочастотную область, однако менее резко, чем у первых. Деформационные колебания это группы находятся при 1650 – 1500 см-1 и 950 – 650 см-1. Полосы поглощения первичных аминов ближе к первому числу, а вторичных к последнему. 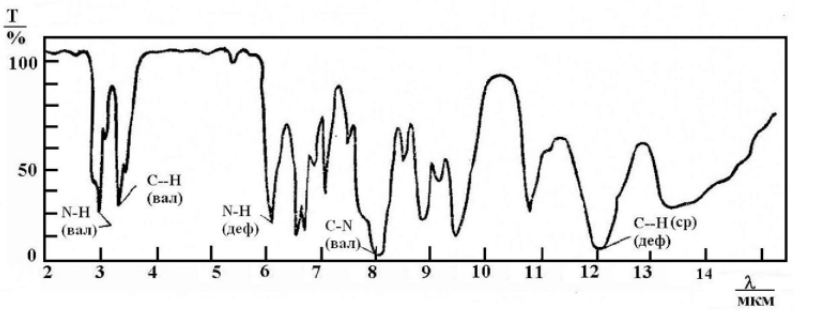 Рис. 24. ИК-спектр ароматического амина. Нитросоединения определяются по двум большим полосами в интервале 1565 – 1545 см-1 и 1385 – 1360 см-1. В ароматических соединениях преимущественно виден пик С-N связи при 870 – 840 см-1. [23]. 5.2 Применение ИК-спектроскопии а анализе витаминовПо ИК-спектрам возможно определять содеждание витаминов группы В, С, А, К во во фруктах и пищевых продуктах. Рассмотрим ИК-спектр витамина С, а именно его важного составного компонента аскорбиновой кислоты. (Рис. 25). Для приготовления пробы понадобится растереть 25 мг кислоты и добавить 5 мл вазелинового масла до получения однородной смеси. Раствор поместить в кюветку и снять спектр. 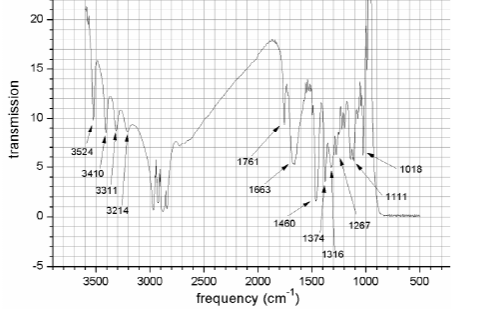 Рис. 25. ИК-спектр аскорбиновой кислоты в вазелиновом масле П 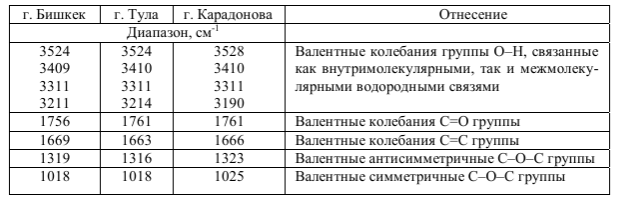 лато в области 2800 – 3000 см-1 совпадает с валентными колебаниями С-Н. Полосы поглощения вазелинового масла приходятся на 1460 и 1374 см-1. Полосы поглощения соответствующие остальным атомам сведены в таблицу 3. [24] лато в области 2800 – 3000 см-1 совпадает с валентными колебаниями С-Н. Полосы поглощения вазелинового масла приходятся на 1460 и 1374 см-1. Полосы поглощения соответствующие остальным атомам сведены в таблицу 3. [24]Табл. 3. Частоты полос поглощения аскорбиновой кислоты, снятые в трёх различных городах www.dic.academic.ru/dic.nsf/enc_colier/5689/СПЕКТРОСКОПИЯ Л. С. Сизова. Аналитическая химия. Оптические методы анализа: учебное пособие для студентов вузов. Кемерово 2006. 96 с. [Электронный ресурс] URL: http://biblioclub.ru/index.php?page=book_view_red&book_id=141307&page_id=95 Л. Ф. Попова. Инструментальные методы анализа. Практикум по аналитической химии. Архангельск, САФУ, 2004. 206 с [Электронный ресурс] URL: http://biblioclub.ru/index.php?page=book_view_red&book_id=436184 Л. Ф. Попова. Инструментальные методы анализа. Практикум по аналитической химии. Архангельск, САФУ, 2004. 206 с [Электронный ресурс] URL: http://biblioclub.ru/index.php?page=book_view_red&book_id=436184 Л. С. Сизова. Аналитическая химия. Оптические методы анализа: учебное пособие для студентов вузов. Кемерово 2006. 97 с. [Электронный ресурс] URL: http://biblioclub.ru/index.php?page=book_view_red&book_id=141307&page_id=95 Луков, В.В. Физические методы исследования в химии : учебное пособие / В.В. Луков, И.Н. Щербаков. – Ростов-на-Дону : Южный федеральный университет, 2016. – 216 с. : схем., табл., ил. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=461932 (дата обращения: 24.04.2020). – Библиогр. в кн. – ISBN 978-5-9275-2023-7. – Текст : электронный. 71 с. Кириллова, Е.А. Методы спектрального анализа : учебное пособие / Е.А. Кириллова, В.С. Маряхина. – Оренбург : Оренбургский государственный университет, 2013. – 105 с. : табл. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=258856 (дата обращения: 29.04.2020). – Текст : электронный. 32 c. Бёккер, Ю. Спектроскопия : монография / Ю. Бёккер ; пер. Л.Н. Казанцева. – Москва : РИЦ Техносфера, 2009. – 528 с. – (Мир химии). – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=88994 (дата обращения: 21.04.2020). – ISBN 978-5-94836-220-5. – Текст : электронный. 142 с. https://studopedia.ru/4_17771_izmerenie-analiticheskogo-signala.html Ефимова А. И. Московский государственный университет имени М. В. Ломоносова. Общий физический практикум. Инфракрасная спектроскопия. – URL: https://docviewer.yandex.ru/view/0/?page=1&*=iL3HKUIKnhxbmCJELj3511pMaNN7InVybCI6Imh0dHA6Ly92ZWdhLnBoeXMubXN1LnJ1L2ZpbGVzL3ByYWN0XzExL2lrLnBkZiIsInRpdGxlIjoiaWsucGRmIiwibm9pZnJhbWUiOnRydWUsInVpZCI6IjAiLCJ0cyI6MTU4NzY0NTMxOTA4NywieXUiOiI5MTM1NTk5ODEzNDU3OTg2MzQiLCJzZXJwUGFyYW1zIjoibGFuZz1ydSZ0bT0xNTg3NjQ1MzEwJnRsZD1ydSZuYW1lPWlrLnBkZiZ0ZXh0PSVEMCVCRiVEMSU4MCVEMCVCOCVEMCVCRCVEMSU4NiVEMCVCOCVEMCVCRislRDElODAlRDAlQjAlRDAlQjElRDAlQkUlRDElODIlRDElOEIrJUQxJTgxJUQwJUJGJUQwJUI1JUQwJUJBJUQxJTgyJUQxJTgwJUQwJUJFJUQwJUJDJUQwJUI1JUQxJTgyJUQxJTgwJUQwJUIwKyVEMCVCOCVEMCVCQSVEMSU4MSsyMislRDAlQkIlRDAlQkUlRDAlQkMlRDAlQkUmdXJsPWh0dHAlM0EvL3ZlZ2EucGh5cy5tc3UucnUvZmlsZXMvcHJhY3RfMTEvaWsucGRmJmxyPTE1Jm1pbWU9cGRmJmwxMG49cnUmc2lnbj01OTMxOTM2N2MwNTVhMzY4ZTFmOGNlMDVjZTgyZDVlZSZrZXlubz0wIn0%3D&lang=ru (дата обращения 23. 04. 2020) 8-9 с. https://studwood.ru/1923012/matematika_himiya_fizika/printsipy_ustroystva_deystviya_spektrometrov В. И. Васильева, О. Ф. Стоянова, И. В. Шкутина, С. И. Карпов, В. Ф. Селеменев, В. Н. Семёнов. Спектральные методы анализа. Практическое руководство. Санкт-Петербург, Москва, Краснодар 2014. 231 с. [Электронный ресурс] URL: https://e.lanbook.com/reader/book/50168/#231 И. В. Колесник, Н. А. Саполетова. Инфракрасная спектроскопия. Методическая разработка МГУ им. М. В. Ломоносова. Москва 2011. URL: https://docviewer.yandex.ru/view/0/?*=KBC9aTasZNN%2BGzScbZZg50LBDJZ7InVybCI6Imh0dHA6Ly93d3cubmFub21ldGVyLnJ1LzIwMDkvMTEvMjkvMTI1OTUyMzE0NzEyMzEvUFJPUF9GSUxFX2ZpbGVzXzEvSVIxLnBkZiIsInRpdGxlIjoiSVIxLnBkZiIsIm5vaWZyYW1lIjp0cnVlLCJ1aWQiOiIwIiwidHMiOjE1ODgwNzQ3NzU4MDYsInl1IjoiOTEzNTU5OTgxMzQ1Nzk4NjM0Iiwic2VycFBhcmFtcyI6Imxhbmc9cnUmdG09MTU4ODA3MjgxMiZ0bGQ9cnUmbmFtZT1JUjEucGRmJnRleHQ9JUQwJUIyJUQwJUJEJUQxJTgzJUQxJTgyJUQxJTgwJUQwJUI1JUQwJUJEJUQwJUJEJUQwJUI1JUQwJUI1KyVEMSU4MyVEMSU4MSVEMSU4MiVEMSU4MCVEMCVCRSVEMCVCOSVEMSU4MSVEMSU4MiVEMCVCMiVEMCVCRStzcGVjdHJ1bStvbmUmdXJsPWh0dHAlM0EvL3d3dy5uYW5vbWV0ZXIucnUvMjAwOS8xMS8yOS8xMjU5NTIzMTQ3MTIzMS9QUk9QX0ZJTEVfZmlsZXNfMS9JUjEucGRmJmxyPTE1Jm1pbWU9cGRmJmwxMG49cnUmc2lnbj01YTQxNmM4YWMwODU2NjJiYzgyYjZiNDlhZjVkNGI1NSZrZXlubz0wIn0%3D&lang=ru (дата обращения 28.04.2020), 33-37 с. https://studme.org/209773/matematika_himiya_fizik/dvuhluchevye_spektrofotometry О. С. Габриелян и др. Учебник, углубленный уровень. Химия 10 класс, ДРОФА, 2014. 299 с. Там же Чиркин, А.А. Биологическая химия : учебник / А.А. Чиркин. – Минск : Высшая школа, 2017. – 432 с. : схем., ил. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=477417 (дата обращения: 18.04.2020). 356 с О. С. Габриелян и др. Учебник, углубленный уровень. Химия 10 класс, ДРОФА, 2014. 307 с. Гидранович, В.И. Биохимия : учебное пособие / В.И. Гидранович, А.В. Гидранович. – 3-е изд. – Минск : ТетраСистемс, 2014. – 528 с. : ил. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=572282 (дата обращения: 19.04.2020). – Библиогр. в кн. – ISBN 978-985-536-397-3. – Текст : электронный. 167-172 с. Биологическая химия : учебник / А.Д. Таганович, Э.И. Олецкий, Н.Ю. Коневалова, В.В. Лелевич ; ред. А.Д. Таганович. – 2-е изд., испр. – Минск : Вышэйшая школа, 2016. – 672 с. : ил. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=235731 (дата обращения: 20.04.2020). – Библиогр.: с. 654. – ISBN 978-985-06-2703-2. – Текст : электронный. 278 с. О. С. Габриелян и др. Учебник, углубленный уровень. Химия 10 класс, ДРОФА, 2014. 318 с. Тихонов, Г.П. Основы биохимии : учебное пособие / Г.П. Тихонов, Т.А. Юдина ; Министерство транспорта Российской Федерации, Московская государственная академия водного транспорта. – Москва : Альтаир : МГАВТ, 2014. – 184 с. : табл., ил. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=430055 (дата обращения: 20.04.2020). – Текст : электронный. 145 c. Кириллова, Е.А. Методы спектрального анализа : учебное пособие / Е.А. Кириллова, В.С. Маряхина. – Оренбург : Оренбургский государственный университет, 2013. – 105 с. : табл. – Режим доступа: по подписке. – URL: http://biblioclub.ru/index.php?page=book&id=258856 (дата обращения: 01.05.2020). – Текст : электронный. 33-39 с. URL: https://docviewer.yandex.ru/view/0/?page=1&*=Uh5DiWDxv5MeLrbuX7tOSzHlUqF7InVybCI6Imh0dHA6Ly92aXRhbC5saWIudHN1LnJ1L3ZpdGFsL2FjY2Vzcy9zZXJ2aWNlcy9Eb3dubG9hZC92dGxzOjAwMDU4MTI5My9TT1VSQ0UxIiwidGl0bGUiOiJTT1VSQ0UxIiwibm9pZnJhbWUiOnRydWUsInVpZCI6IjAiLCJ0cyI6MTU4ODMzMzQ2MTcyMiwieXUiOiI5MTM1NTk5ODEzNDU3OTg2MzQiLCJzZXJwUGFyYW1zIjoibGFuZz1ydSZ0bT0xNTg4MzMzMjM5JnRsZD1ydSZuYW1lPVNPVVJDRTEmdGV4dD0lRDAlQkYlRDElODAlRDAlQjglRDAlQkMlRDAlQjUlRDAlQkQlRDAlQjUlRDAlQkQlRDAlQjglRDAlQjUrJUQwJUI4JUQwJUJBKyVEMSU4MSVEMCVCRiVEMCVCNSVEMCVCQSVEMSU4MiVEMSU4MCVEMCVCRSVEMSU4MSVEMCVCQSVEMCVCRSVEMCVCRiVEMCVCOCVEMCVCOCslRDAlQjQlRDAlQkIlRDElOEYrJUQwJUIwJUQwJUJEJUQwJUIwJUQwJUJCJUQwJUI4JUQwJUI3JUQwJUIwKyVEMCVCMSVEMCVCOCVEMCVCRSVEMCVCQiVEMCVCRSVEMCVCMyVEMCVCOCVEMSU4NyVEMCVCNSVEMSU4MSVEMCVCQSVEMCVCOCslRDAlQjAlRDAlQkElRDElODIlRDAlQjglRDAlQjIlRDAlQkQlRDElOEIlRDElODUrJUQwJUIyJUQwJUI1JUQxJTg5JUQwJUI1JUQxJTgxJUQxJTgyJUQwJUIyJnVybD1odHRwJTNBLy92aXRhbC5saWIudHN1LnJ1L3ZpdGFsL2FjY2Vzcy9zZXJ2aWNlcy9Eb3dubG9hZC92dGxzJTNBMDAwNTgxMjkzL1NPVVJDRTEmbHI9MTUmbWltZT1wZGYmbDEwbj1ydSZzaWduPTMzZWM2YmZhNmRmOGFiMjA1OGRhYTllNjMzZjZiZTY4JmtleW5vPTAifQ%3D%3D&lang=ru Глава 1 Теоретические основы метода ИК-спетроскопии Валентные и деформационные колебания |
