! Лекции БИОЛОГИЯ ЧЕЛОВЕКА. Лекции биология человека
 Скачать 1.29 Mb. Скачать 1.29 Mb.
|
|
Тема 10. Сердечно-сосудистая система 1. Значение системы кровообращения. Общая схема кровообращения. Кровяное давление и факторы, его обуславливающие. Понятие о гипо- и гипертензии. Регуляция кровообращения. 2. Фазы сердечных сокращений. Систолический и минутный объемы крови. 3. Свойства сердечной мышцы. Электрокардиография. Характеристика зубцов и отрезков электрокардиограммы. 4. Проводящая система сердца. Понятие об аритмии и экстрасистолии. Регуляция деятельности сердца. 5. Пороки сердца. Причины и профилактика врожденных и приобретенных пороков сердца. 6. Местные расстройства кровообращения. Артериальная и венозная гиперемия, ишемия, тромбоз, эмболия: сущность процессов, проявления и последствия для организма. 1. Значение системы кровообращения. Общая схема кровообращения. Кровяное давление и факторы, его обуславливающие. Понятие о гипо- и гипертензии. Регуляция кровообращения. Кровообращение — это движение крови по сосудам, обеспечивающее обмен веществ между всеми тканями организма и внешней средой. Система органов кровообращения включает сердце и кровеносные сосуды Основное значение системы кровообращения состоит в снабжении кровью органов и тканей Схема кровообращения по Гарвею Сокращаясь, сердце, как мощный насос, безостановочно гонит кровь по сосудам двух кругов кровообращения (рис. 2). Что же они собой представляют? Большой круг кровообращения начинается от левого желудочка сердца (1), в который кровь поступает из сокращающегося левого предсердия (15). Из левого желудочка кровь проталкивается в самый крупный сосуд — аорту (2), затем по более мелким артериям — печеночной (3), кишечной (4), протекает через артериолы, прекапилляры, капилляры большого круга кровообращения (5), где отдает кислород и питательные вещества всем органам и тканям тела человека. Далее кровь собирается в венулы и вены — воротную (6), печеночную (7), а затем в нижнюю (8) и верхнюю (9) полые вены, открывающиеся в правое предсердие (10), которым и заканчивается большой круг кровообращения. Рис. Схема кровообращения по Гарвею. 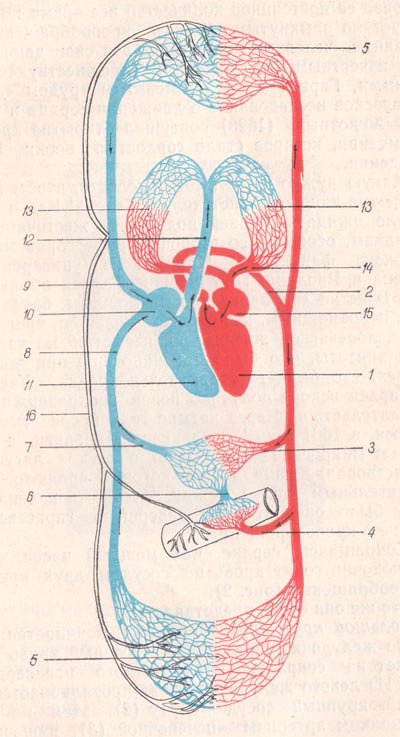 Малый, или легочный, круг кровообращения начинается от правого желудочка (11). Вследствие его сокращения венозная кровь проталкивается в легочную артерию (12), затем в легочные артериолы, прекапилляры и капилляры, которые окружают легочные альвеолы (13), где она, отдавая углекислый газ, насыщается кислородом, собирается в венулы и легочные вены (14). По ним уже насыщенная кислородом артериальная кровь впадает в левое предсердие (15), которым заканчивается малый круг кровообращения. Имеется также и лимфатическая система (16). Кровяное давление — давление, которое кровь оказывает на стенки кровеносных сосудов Обеспечивает возможность продвижения крови по кровеносной системе и тем самым осуществление обменных процессов в тканях организма. На величинукровяного давлениявлияют несколько факторов. 1. Количество крови, поступающее в единицу времени в сосудистую систему. 2. Интенсивность оттока крови на периферию. 3. Ёмкость артериального отрезка сосудистого русла. 4. Упругое сопротивление стенок сосудистого русла. 5. Скорость поступления крови в период сердечной систолы. 6. Вязкость крови 7. Соотношение времени систолы и диастолы. 8. Частота сердечных сокращений. Величина кровяного давления, в основном, определяется работой сердца и тонусом сосудов (главным образом, артериальных). Артериальная гипотензия (от др.-греч. ὑπό — под, внизу и лат. tensio — напряжение) — снижение артериального давления более, чем на 20 % от исходного/обычных значений или в абсолютных цифрах — ниже 90 мм рт. ст. систолического давления или 60 мм рт.ст. среднего артериального давления. Артериальная гипотензия (Гипотония) может быть следствием нервного перенапряжения, она часто развивается как последствие инфекционных и других заболеваний и при недостаточном или беспорядочном питании, ограничительных диетах, дисбалансе в соотношении часов отдыха и труда. Артериа́льная гиперте́нзия (АГ, гипертония) — стойкое повышение артериального давления от 140/90 мм рт.ст. и выше. Для обеспечения кровотока в каждом органе и во всей сердечно-сосудистой системе используют главным образом физиологические свойства собственно структур: в сердце - свойства сократительного миокарда и проводящей системы (автоматизм), в сосудах - специфику распределения МОК между органами (осуществляется в зависимости от анатомических особенностей сосудов - диаметра, элементов стенки, их тонуса). Тонус каждого отдела сосудистого русла зависит от свойств сократительных элементов и объема крови, поступающей. Кроме того, имеют значение содержание в крови вазоактивных соединений (гормонов, метаболитов), базальный уровень нейрогенных тонических влияний, влияние гормонов крови и метаболитов других органов. Благодаря комплексу указанных механизмов поддерживаются соответствующие параметры функции сердца (УО, ЧСС), уровень артериального давления в крупных артериях и венах, а также постоянное количество и состав циркулирующей крови. Основным контрольным механизмом являются рефлекторные механизмы регуляции - барорецепторы крупных сосудов. Главным регулируемым параметром справедливо считается уровень артериального давления (AT). Уровень РС зависит главным образом от УО сердца, в то время как Рд - от сопротивления резистивных сосудов. Эти параметры контролируют барорецепторы, которые в случае отклонения включают соответствующие рефлексы относительно сердца и кровеносных сосудов. В состоянии покоя на кривой записи AT оказываются волны трех порядков. Волны первого порядка обусловлены колебанием систолического и диастолического давления. Волны второго порядка обусловлены влиянием вдоха и выдоха на приток крови к отделов сердца и взаимодействием дыхательного и сосудодвигательного центров ствола головного мозга: во время вдоха в артериях большого круга кровообращения давление уменьшается, а при выдохе увеличивается. Волны третьего порядка является следствием медленного колебания тонуса периферических сосудов с периодичностью 6-20 с. Видимо, они зависят от ритма центральных рефлекторных механизмов, т.е. колебания тонуса центров. Кроме того, можно обнаружить суточные колебания АД, вызванные так называемыми циркадным ритмами: максимальное давление наблюдается в период около 15-часов, а минимальный - в 3-й час. 2. Фазы сердечных сокращений. Систолический и минутный объемы крови.
3. Свойства сердечной мышцы. Электрокардиография. Характеристика зубцов и отрезков электрокардиограммы. Основные свойства сердечной мышцы: возбудимость, проводимость, сократимость и автоматия. Возбудимость - это способность миокарда под действием электриче ских, химических, термических и других раздражителей приходить в состоя ние возбуждения. Процессы возбуждения в сердечной мышце, как и в любой другой ткани, сопровождаются изменением биоэлектрических процессов в мышечных клетках Проводимость (т.е. возможность прохождения возбуждения по ткани) сердечной мышцы очень высока и обеспечивается особым строением межклеточных контактов как в рабочем миокарде, так и в проводящей системе сердца. Сократимость сердечной мышцы отличается от скелетной. Миокард почти не обнаруживает зависимости между силой раздражения и величиной реакции. Сократимость сердечной мышцы определяется особенностями строения ее волокон и соотношением между длиной и напряжением саркомера. Автоматия, способность к ритмическому сокращению без всяких видимых раздражений под влиянием импульсов, возникающих в самом орга не, является характерной особенностью сердца. Электрокардиогра́фия — методика регистрации и исследования электрических полей, образующихся при работе сердца Прямым результатом электрокардиографии является получениеэлектрокардиограммы (ЭКГ) — графического представления разности потенциалов возникающих в результате работы сердца и проводящихся на поверхность тела. Во время сокращений сердца на ленте записываются различные зубцы, повторяющиеся комбинации которых называются комплексами. Они важны для оценки частоты сердечных сокращений, ритма и проводимости 4. Проводящая система сердца. Понятие об аритмии и экстрасистолии. Регуляция деятельности сердца. Проводящая система сердца (ПСС) — комплекс анатомических образований сердца(узлов, пучков и волокон), состоящих из атипичных мышечных волокон (сердечные проводящие мышечные волокна) и обеспечивающих координированную работу разных отделов сердца (предсердий и желудочков), направленную на обеспечение нормальнойсердечной деятельности. ![проводящая система сердца. схема расположения проводящей системы в сердце человека. 1 — узел кис-флака; 2 — узел ашоф-тавара; 3 — пучок гиса; 4 — ножки пучка гиса; 5 — сеть волокон пуркинье; 6 — верхняя полая вена; 7 — нижняя полая вена; 8 — предсердия; 9 — желудочки [1959 станков а г - анатомия человека]](7407_html_m155df92d.png) Проводящая система сердца. Схема расположения проводящей системы в сердце человека. 1 — узел Кис-Флака; 2 — узел Ашоф-Тавара; 3 — пучок Гиса; 4 — ножки пучка Гиса; 5 — сеть волокон Пуркинье; 6 — верхняя полая вена; 7 — нижняя полая вена; 8 — предсердия; 9 — желудочки Проводящая система сердца. Схема расположения проводящей системы в сердце человека. 1 — узел Кис-Флака; 2 — узел Ашоф-Тавара; 3 — пучок Гиса; 4 — ножки пучка Гиса; 5 — сеть волокон Пуркинье; 6 — верхняя полая вена; 7 — нижняя полая вена; 8 — предсердия; 9 — желудочки Аритмии сердца — это нарушения сердечной деятельности, выражающиеся в изменении частоты, силы или последовательности сокращений сердца. Аритмии сердца могут возникать при нарушении выработки импульса к сокращению сердца в синусовом узле при нарушении проведения импульса от предсердий к желудочкам и при появлении в сердечной мышце дополнительных очагов возбуждения, в которых вырабатываются импульсы, помимо синусового узла. Экстрасистолия — нарушение сердечного ритма, связанное с появлением в сердечной мышце дополнительных очагов возбуждения, импульсы из которых вызывают преждевременное сокращение сердца (экстрасистолу). Регуляция деятельности сердца.Сердце - это мощный насос, перекачивающий по кровеносным сосудам около 10 т крови в сутки. Условно их можно разделить на 2 группы: 1) внутрисердечные и 2) внесердечные, или экстракардиальные. Внутрисердечные механизмы регуляции делятся на 3 группы: 1) внутриклеточные, 2) гемодинамические (гетеро- и гомеометрические), 3) внутрисердечные периферические рефлексы. Внутриклеточные механизмы регуляции имеют место, например, у спортсменов. Регулярная мышечная нагрузка приводит к усилению синтеза сократительных белков миокарда и появлению так называемой рабочей (физиологической) гипертрофии - утолщению стенок сердца и увеличению его размеров. Так, если масса нетренированного сердца составляет 300 г, то у спортсменов она увеличивается до 500 г. Гемодинамические, или миогенные, механизмы регуляции обеспечивают постоянство систолического объема крови. Сила сокращений сердца зависит от его кровенаполнения, т.е. от исходной длины мышечных волокон и степени их растяжения во время диастолы. Внутрисердечные периферические рефлексы относятся к третьей группе механизмов регуляции. В сердце независимо от нервных элементов экстракардиального происхождения функционирует внутриорганная нервная система, образующая миниатюрные рефлекторные дуги, в состав которых входят афферентные нейроны, дендриты которых начинаются на рецепторах растяжения на волокнах миокарда и коронарных сосудов, вставочные и эфферентные нейроны (клетки Догеля I, II и III порядка), аксоны которых могут заканчиваться на миокардиоцитах, расположенных в другом отделе сердца. Так, увеличение притока крови к правому предсердию и растяжение его стенок приводит к усилению сокращения левого желудочка. Этот рефлекс можно заблокировать с помощью, например, местных анестетиков (новокаина) и ганглиоблокаторов (беизогексония). Внесердечные (эстракардиальные) механизмы регуляции Эти механизмы также работают по рефлекторному принципу, в них главную роль играют парасимпатическая нервная система (п. vagus) и симпатическая нервная система (п. sympaticus). 5. Пороки сердца. Причины и профилактика врожденных и приобретенных пороков сердца. Порок сердца — врожденное или приобретенное заболевание, основой которого являются дефекты клапанного аппарата сердца, нарушение целостности его стенок и перегородок, а также аномалии крупных сосудов. Пороки сердца могут развиваться еще до рождения младенца на свет, когда в процессе формирования сердечно-сосудистой системы на нее воздействуют повреждающие факторы — радиационные, токсические или воспалительные. Такие пороки называют врожденными. Врожденные пороки сердца, требующие хирургического вмешательства, условно делятся на «синие» и «бледные». К первой группе относят аномалии, при которых венозная и артериальная кровь смешиваются, и все ткани организма начинают страдать от гипоксии. Поэтому кожные покровы таких больных имеют синюшную окраску(цианотичны). «Синий» порок сердца требует скорейшей коррекции, так как длительная гипоксия тканей ухудшает функции всех органов. «Бледные пороки» не вызывают поступления обеденной кислородом крови в ткани, но при них большую нагрузку испытывают правые отделы сердца из-за поступления в него дополнительных порций крови из левого желудочка или предсердия, а левые из-за препятствий кровотоку в виде сужения сосудов или клапанов. «Бледный» порок сердца не требует срочной операции, но в дальнейшем коррекция нарушений необходима. Повышенная нагрузка на сердце приводит к истощению его компенсаторных возможностей, развивается синдром сердечной недостаточности. Существует и группа пороков, которые корректировать нет необходимости, они не нарушают кровообращение и до глубокой старости можно даже не подозревать о них — например, декстрокардия. Причины формирования Причины появления на свет детей с врожденными аномалиями сердца до конца не изучены, но доказано повреждающее действие перенесенных в первом триместре инфекционных или вирусных заболеваний — краснухи, кори, гриппа,цитомегаловирусной инфекции, а также употребление беременной женщиной наркотиков, алкоголя, некоторых лекарств. Приобретённый порок сердца – это порок, возникший в результате различных заболеваний или нарушения режима работы сердца. При этом порок сердца является, как правило, вторичным процессом после основного заболевания. Причинами приобретенных пороков сердца могут стать такие заболевания: Ревматизм (длительный стаж заболевания и неэффективное лечение). Атеросклероз сосудов, приводящий к повышению нагрузки на сердце. Инфекционные заболевания сердца (инфекционный эндокардит). Сифилис. Заболевания соединительной ткани (системная склеродермия, болезнь Бехтерева). Различные травмы в области сердца. Инфаркт миокарда. Традиционных мер профилактики приобретенных пороков сердца нет, но можно существенно снизить риск их возникновения, если своевременно лечить основное заболевание. 6. Местные расстройства кровообращения. Артериальная и венозная гиперемия, ишемия, тромбоз, эмболия: сущность процессов, проявления и последствия для организма. Расстройствами местного кровообращения называются состояния, характеризующиеся изменением кровенаполнения отдельных органов, тканей или их частей. Артериальной гиперемией(греч. «hyper» – сверх, «haema» – кровь) называется состояние повышенного кровенаполнения органа и ткани, возникающее в результате усиленного притока крови к ним по расширенным артериям. Артериальная гиперемия может быть местной и общей. Общее артериальное полнокровиеразвивается при значительном увеличении объема циркулирующей крови – например, при эритроцитозе. Патологическая артериальная гиперемия возникает также в условиях гипертермии при перегревании организма, при лихорадке у больных с инфекционными заболеваниями, при быстром падении барометрического давления. Артериальная гиперемия может носить острый, преходящий характер, может быть часто повторяющейся, хронической. Различают физиологические и патологические артериальные гиперемии. Прифизиологической артериальной гиперемииусиление кровотока адекватно возросшим потребностям органа или ткани в кислороде и энергетических субстратах. Примерами физиологической артериальной гиперемии могут служить рабочая гиперемия, когда к усиленно работающему органу увеличивается приток крови, и гиперемия лица, появляющаяся при чувстве радости, гнева, стыда. Патологическая артериальная гиперемиявозникает вне зависимости от метаболических потребностей органа. По особенностям этиологических факторов и механизмов развития выделяют следующие разновидности патологических артериальных гиперемий: 1) нейропаралитическую; 2) нейротоническую; 3) постишемическую; 4) вакатную; 5) воспалительную; 6) коллатеральную; 7) гипермию вследствие артериовенозного свища. В основе патогенезаартериальных гиперемий лежат следующие механизмы: 1) миопаралитический; 2) нейрогенный (ангионевротический). Миопаралитический механизмсвязан со снижением миогенного тонуса сосудов под влиянием метаболитов (лактата, пуринов, пировиноградной кислоты и др.), медиаторов, внеклеточного увеличения концентрации калия, водорода и других ионов, уменьшения содержания кислорода. Это самый частый механизм развития артериальной гиперемии. Он лежит в основе постишемического, воспалительного, физиологического рабочего артериального полнокровия. Сущность нейрогенного механизмасостоит в изменении нейрогенных констрикторных и дилататорных влияний на сосуды, приводящих к снижению нейрогенного компонента сосудистого тонуса. Данный механизм лежит в основе развития нейротонической, нейропаралитической гиперемии, а также воспалительного артериального полнокровия при реализации аксон-рефлекса. Нейротоническая артериальная гиперемиявозникает при повышении тонуса парасимпатических или симпатических холинергических сосудорасширяющих нервов или при раздражении их центров опухолью, рубцом и т. д. Этот механизм наблюдается только в некоторых тканях. Под влиянием симпатических и парасимпатических вазодилататоров артериальная гиперемия развивается в поджелудочной и слюнной железах, языке, кавернозных телах, коже, скелетных мышцах и др. Постишемическая артериальная гиперемияпредставляет собой увеличение кровотока в органе или ткани после временного прекращения кровообращения. Подобная артериальная гиперемия возникает, в частности, после снятия жгута с конечности, быстрого удаления асцитической жидкости. Реперфузия способствует не только положительным изменениям в ткани. Приток большого количества кислорода и усиленное его использование клетками приводят к интенсивному образованию перекисных соединений, активации процессов перекисного окисления липидов и, как следствие, прямому повреждению биологических мембран и свободно-радикальному некробиозу. Вакатная(лат. «vacuus» – пустой) гиперемия наблюдается при уменьшении барометрического давления над какой-либо частью тела. Данный вид гиперемии развивается при быстром освобождении от сдавления сосудов брюшной полости, например, при стремительном разрешении при родах, удалении опухоли, сдавливающей сосуды, или быстрой эвакуации асцитической жидкости. Воспалительная артериальная гиперемиявозникает под действием вазоактивных веществ (медиаторов воспаления), вызывающих резкое снижение базального тонуса сосудов, а также вследствие реализации в зоне альтерации нейротоничеекого, нейропаралитического механизмов и аксон-рефлекса. Коллатеральная артериальная гиперемияносит приспособительный характер и развивается вследствие рефлекторного расширения сосудов коллатерального русла при затруднении притока крови по магистральной артерии. Гиперемия вследствие артериовенозного свищаможет развиться при повреждении артериальных и венозных сосудов в результате образования соустья между артерией и веной. При этом артериальная кровь под давлением устремляется в венозное русло, обеспечивая артериальное полнокровие. Для артериальной гиперемии характерны следующие изменения микроциркуляции: 1) расширение артериальных сосудов; 2) увеличение линейной и объемной скоростей кровотока в микрососудах; 3) повышение внутрисосудистого гидростатического давления, увеличение количества функционирующих капилляров; 4) усиление лимфообразования и ускорение лимфообращения; 5) уменьшение артериовенозной разницы по кислороду. К внешним признакам артериальной гиперемии относится покраснение зоны гиперемии, обусловленное расширением кровеносных сосудов, увеличением количества функционирующих капилляров и повышением содержания оксигемоглобина в венозной крови. Артериальная гиперемия сопровождается местным повышением температуры, что объясняется усиленным притоком более теплой артериальной крови и повышением интенсивности обменных процессов. Вследствие возрастания крове– и лимфонаполнения зоны гиперемии происходит увеличение тургора (напряжения) и объема гиперемированной ткани. Венозная гиперемия Венозная гиперемия– это состояние повышенного кровенаполнения органа или ткани, обусловленное затрудненным оттоком крови по венам. Венозное полнокровие может быть местным и распространенным. Местное венозное полнокровие возникает при затруднении оттока крови по крупным венозным стволам вследствие закупорки их тромбом, эмболом или при сдавлении вены извне опухолью, рубцом, отеком и т. д. Условием, способствующим венозному застою, является длительное нефизиологическое положение той или иной части тела, неблагоприятное для местного оттока крови. При этом формируется гипостаз – гравитационная венозная гиперемия. Причинами распространенного венозного полнокровия наиболее часто являются: 1) недостаточность функции сердца при ревматических и врожденных пороках его клапанов, миокардитах, инфаркте миокарда; 2) декомпенсация гипертрофированного сердца; 3) уменьшение присасывающего действия грудной клетки при экссудативном плеврите, гемотораксе и т. д. По темпу развития и длительности существования данная патология может носить острый и хронический характер. Длительная венозная гиперемия возможна только при недостаточности коллатерального венозного кровообращения. Микроциркуляторные расстройства при венозной гиперемии характеризуются: 1) расширением капилляров и венул; 2) замедлением кровотока по сосудам микроциркуляторного русла вплоть до стаза; 3) утратой деления кровотока на осевой и плазматический; 4) повышением внутрисосудистого давления; 5) маятникообразным или толчкообразным движением крови в венулах; 6) уменьшением интенсивности кровотока в области гиперемии; 7) нарушением лимфообращения; 8) увеличением артериовенозной разницы по кислороду. К внешним признакам венозной гиперемии относятся: 1) увеличение, уплотнение органа или ткани; 2) развитие отека; 3) возникновение синюшности, т. е. цианотичной окраски. При остром венозном полнокровииможет наблюдаться выход эритроцитов из мелких сосудов в окружающие ткани. При скоплении значительного их количества в слизистых и серозных оболочках, коже формируются мелкие, точечные кровоизлияния. Вследствие усиления транссудации в тканях накапливается отечная жидкость. Количество ее может быть весьма значительным в подкожной клетчатке (анасарка), плевральных полостях (гидроторакс), брюшной полости (асцит), перикарде (гидроперикард), желудочках мозга (гидроцефалия). В условиях гипоксии в клетках паренхиматозных органов развиваются зернистая и жировая дистрофия, мукоидное набухание межуточного вещества. Эти изменения носят, как правило, обратимый характер и при устранении причины острое венозное полнокровие завершается полным восстановлением структуры и функции тканей. При хроническом венозном полнокровиипроисходят развитие дистрофических процессов в тканях, атрофия паренхиматозных элементов с одновременным заместительным разрастанием клеток стромы и накоплением в ней коллагеновых волокон. Необратимое склерозирование и уплотнение органа сопровождается нарушением его функций и называется цианотической индурацией. Тромбоз Тромбоз – прижизненное местное пристеночное образование в сосудах или сердце плотного конгломерата из форменных элементов крови и стабилизированного фибрина, т. е. тромба. Тромбоз – физиологический защитный процесс, направленный на предотвращение кровотечения при травме тканей, на укрепление стенок аневризм, на ускорение стягивания и заживления ран. Однако, если тромбоз избыточен, недостаточен, либо утратил свой обязательно местный ограниченный характер, возможно развитие тяжелой патологии. Тромбы подразделяются на белые, красные и смешанные. Тромбоз как естественный способ остановки кровотечения отражает характер взаимодействия механизмов системы гемостаза и фибринолиза. Принято выделять три основных звена гемостаза: 1) сосудистое звено– гемостатические механизмы сосудистой стенки, направленные на спазм поврежденного сосуда и запуск тромбообразования и свертывания крови; 2) клеточное (тромбоцитарно-лейкоцитарное) звено, которое обеспечивает формирование белого тромба; 3) фибриновое звено– система свертывания, обеспечивающая образование фибрина, в результате чего формируются красные и смешанные тромбы. Все три звена гемостаза включаются одновременно и обеспечивают остановку кровотечения и восстановление целостности сосудистой стенки. Белый тромб формируется за 2 – 5 мин. Образование богатого фибрином красного тромба требует 4 – 9 мин. Процесс тромбообразования начинается с постепенного формирования белого тромба. Белые тромбы обеспечивают остановку капиллярного кровотечения. Красный тромбформируется в условиях преобладания коагуляции над агглютинацией, при быстром свертывании крови и медленном кровотоке. Он способен остановить кровотечение из артериальных и венозных сосудов. Красный тромб состоит из головки, представляющей собой аналог белого тромба, слоистого тела, в котором чередуются тромбоцитарные и фибриновые отложения, и фибринового хвоста, улавливающего эритроциты. Смешанными тромбаминазывают слоистые тромбы с несколькими агглютинационными белыми головками. Кроме того, выделяют особые виды тромбов, образующихся при определенных условиях: 1) септический тромб, образующийся при инфекционных воспалительных поражениях сосудов (флебиты, васкулиты); 2) опухолевый тромб, формирующийся из агглютинированных тромбоцитов и лейкоцитов на клетках проросшей в сосуд опухоли; 3) шаровидный тромб, имеющий смешанный характер и образующийся на основе оторвавшегося пристеночного тромба при нарушениях внутрисердечной гемодинамики вследствие митрального стеноза; 4) вегетации – тромбы, наслаивающиеся на пораженные эндокардитом клапаны сердца; 5) марантический тромб – красный тромб, который формируется при венозном застое на фоне дегидратации и сгущения крови. Тромб следует отличать от кровяного сгустка. Истинный тромб всегда формируется только прижизненно внутри сосудов и прочно спаян с сосудистой стенкой. Сгустки же могут образовываться не только прижизненно, но и в условиях in vitro (посмертно), не только в просвете сосуда, но также и в полостях и в тканях на месте гематом. Сгустки крови в сосудах лежат свободно или сцеплены с сосудистой стенкой рыхло, не имеют структурированности, свойственной тромбам. В основе активации тромбообразования при различных патологических процессах лежит триада Вирхова: повреждение эндотелия сосудистой стенки, замедление кровотока, а также активация коагуляционного гемостаза. Указанный каскад реакций может индуцироваться эндотоксинами грамотрицательных бактерий, экзотоксинами, гипоксией, избыточным накоплением водородных ионов, биогенными аминами, кининами, лейкотриенами, проэтагландинами, свободными радикалами и многими цитокинами, продуцируемыми в избытке нейтрофилами, моноцитами, лимфоцитами. Последствия тромбоза могут быть разнообразны. С одной стороны, тромбоз является защитным механизмом, направленным на остановку кровотечения при повреждении или разрыве сосуда. С другой стороны, тромбоз, возникающий при различных патологических состояниях, ведет к развитию нарушений местного кровобращения, нередко с тяжелыми последствиями для организма. Характер циркуляторных расстройств и степень нарушения функции opганов при тромбозах могут быть различными и зависят от локализации тромба, скорости его образования, возможностей коллатерального кровообращения в данном месте. Эмболия Эмболией называется закупорка кровеносного или лимфатического сосуда частицами, приносимыми с током крови или лимфы, и обычно не встречающимися в крово– и лимфотоке. По направлению движения эмбола различают: 1) ортоградную; 2) ретроградную; 3) парадоксальную эмболии. Ортоградная эмболиявстречается чаще всего и характеризуется продвижением эмбола по направлению тока крови. При ретроградной эмболииэмбол движется против тока крови под действием собственной силы тяжести. Это происходит в венозных сосудах, по которым кровь течет снизу вверх. Парадоксальная эмболияимеет ортоградное направление, но возникает вследствие дефектов межпредсердной или межжелудочковой перегородки, когда эмбол имеет возможность миновать разветвления легочной артерии и оказаться в большом круге кровообращения. Эмболия может быть одиночной и множественной. В зависимости от локализации различают: 1) эмболии лимфатических и кровеносных сосудов; 2) эмболии малого круга кровообращения; 3) эмболии большого круга кровообращения; 4) эмболии системы воротной вены. При эмболии большого круга кровообращения источником эмболов являются патологические процессы (тромбоэндокардиты, инфаркт миокарда, изъязвления атеросклеротических бляшек) в легочных венах, левых полостях сердца, аорте, артериях большого круга кровообращения. Эмболии большого круга кровообращения сопровождаются серьезными расстройствами кровообращения вплоть до развития очагов некроза в органе, сосуд которого закупорен тромбом. Эмболия малого круга кровообращения является результатом заноса эмболов из правой половины сердца и вен большого круга кровообращения. Для эмболии малого круга кровообращения характерны внезапность возникновения, быстрота нарастания чрезвычайно тяжелых клинических проявлений. По характеру эмбола различают экзогенные и эндогенные эмболии. К экзогенным эмболиям относятся: 1) воздушная; 2) газовая; 3) микробная; 4) паразитарная. К эндогенным эмболиям относятся: 1) тромбоэмболии; 2) жировая; 3) тканевая. Воздушная эмболия возникает вследствие попадания в сосудистую систему воздуха из окружающей среды. Причинамивоздушной эмболиимогут быть повреждения крупных вен шеи, грудной клетки, синусов твердой мозговой оболочки, нейрохирургические операции со вскрытием венозных синусов, искусственное кровообращение, лечебные и диагностические пункции легких, газоконтрастные рентгенологические исследования, лапароскопические операции и т. д. Газовая эмболиясвязана с выделением в крови пузырьков растворенных в ней газов (азота и гелия) при быстром переходе от высокого атмосферного давления к обычному или от нормального к пониженному. Такая ситуация может возникнуть при внезапной декомпрессии, например, при быстром подъеме водолаза со значительной глубины (кессонная болезнь), при разгерметизации барокамеры или кабины космического корабля и т. п. Микробная эмболияимеет место при септикопиемиях, когда в кровотоке находится большое количество микроорганизмов. Микробная эмболия может быть причиной развития метастатических абсцессов. Паразитарная эмболиявстречается при гельминтозах. Так, например, при аскаридозе возможна эмболия сосудов легких. Жировая эмболиянаступает при закупорке сосудов эндогенными липопротеидными частицами, продуктами агрегации хиломикронов или экзогенными жировыми эмульсиями и липосомами. При истинной жировой эмболии имеет место высокий уровень свободных жирных кислот в крови, которые обладают аритмогенным действием. Тканевая эмболияподразделяется на: 1) амниотическую; 2) опухолевую; 3) адипоцитарную. Эмболия околоплодными водами приводит к закупорке легочных сосудов конгломератами клеток, взвешенных в амниотической жидкости, и тромбоэмболами, образующимися под действием содержащихся в ней прокоагулянтов. Опухолевая эмболия представляет собой сложный процесс гематогенного и лимфогенного метастазирования злокачественных новообразований. Опухолевые клетки образуют в кровотоке конгломераты с тромбоцитами за счет продукции муцинов и адгезивных поверхностных белков. Тканевая и, в частности, адипоцитарная эмболия может быть результатом травм, когда частички размозженных тканей попадают в просвет поврежденных сосудов. Эмболия инородными телами встречается довольно редко и возникает при ранениях или медицинских инвазивных процедурах. Разновидность эндогенной эмболии – тромбоэмболия– возникает вследствие закупорки сосудов оторвавшимися тромбами или их частицами. Тромбоэмболия является следствием тромбоза или тромбофлебита различных отделов венозной системы организма. Одной из наиболее тяжелых форм тромбоэмболии является тромбэмболия легочной артерии (ТЭЛА), частота встречаемости которой в клинической практике постоянно увеличивается в последние годы. Причиной ТЭЛА в 83 % случаев является флеботромбоз центральных и периферических сосудов, в частности, подвздошной, бедренной, подключичной вен, глубоких вен голени, вен таза и др. Характер клинических проявлений и тяжесть последствий ТЭЛА могут зависеть от калибра окклюзированного сосуда, скорости развития процесса и резервов системы фибринолиза. По характеру течения ТЭЛА различают формы: 1) молниеносную; 2) острую; 3) подострую; 4) рецидивирующую. Молниеносная форма характеризуется развитием основных симптомов в течение нескольких минут, острая – в течение нескольких часов, подострая – в течение нескольких дней. По степени поражения легочного сосудистого русла выделяют формы: 1) массивную; 2) субмассивную; 3) форму с поражением мелких ветвей легочной артерии. Массивная форма возникает при эмболии ствола и главных ветвей легочной артерии, т. е. при поражении более 50 % легочного сосудистого русла. При субмассивной эмболии происходит перекрытие долевых ветвей легочной артерии, т. е. менее 50 % сосудистого русла легких. Ишемия Ишемией (греч. «isho» – задерживаю) называется малокровие тканей, вызванное недостаточным или полным прекращением притока артериальной крови. По причинам возникновения и механизмам развития различают несколько видов ишемии: 1) ангиоспастическую, возникающую в результате спазма артерий, обусловленного либо повышением тонуса вазоконстрикторов, либо воздействием на стенки сосудов сосудосуживающих веществ; 2) компрессионную, вызывающуюся сдавлением артерий рубцом, опухолью, наложенным жгутом, излившейся кровью и т. д.; 3) обтурационную, развивающуюся при частичном или полном закрытии просвета артерии тромбом, эмболом, атеросклеротической бляшкой и т. д.; 4) перераспределительную, имеющую место при межрегиональном, межорганном перераспределении крови; 5) обструктивную, возникающую в результате механического разрушения сосудов при травме; 6) ишемию, обусловленную значительным увеличением вязкости крови в мелких сосудах в сочетании с вазоконстрикцией. Перечисленные виды ишемии чаще всего развиваются достаточно быстро и относятся к категории острых. Хроническая ишемия развивается медленно, при постепенном сужении просвета артерий вследствие утолщения их стенок при атеросклерозе, гипертонической болезни, ревматизме. Ишемизированный участок отличается бледностью, уменьшением объема и тургора вследствие нарушения кровенаполнения. Происходит снижение температуры участка ишемии из-за нарушения притока теплой артериальной крови и уменьшения интенсивности обменных процессов. Снижается величина пульсации артерий в результате уменьшения их систолического наполнения. Вследствие раздражения тканевых рецепторов недоокисленными продуктами обмена веществ возникают боли, парестезии. Ишемия характеризуется следующими нарушениями микроциркуляторного кровотока: 1) сужением артериальных сосудов; 2) замедлением тока крови по микрососудам; 3) уменьшением количества функционирующих капилляров; 4) понижением внутрисосудистого гидростатического давления; 5) уменьшением образования тканевой жидкости; 6) понижением напряжения кислорода в ишемизированной ткани. Вследствие нарушения доставки кислорода и субстратов обмена веществ в ишемизированной ткани развиваются обменные, структурные и функциональные нарушения, выраженность которых зависит от следующих факторов: 1) от скорости развития и продолжительности ишемии; 2) от чувствительности тканей к гипоксии; 3) степени развития коллатерального кровотока; 4) предшествующего функционального состояния органа или ткани. Ишемические участки испытывают состояние кислородного голодания, снижается интенсивность обменных процессов, развивается дистрофия паренхиматозных клеток вплоть до их гибели, исчезает гликоген. При продолжительной запредельной ишемии может наступить омертвение ткани. Так, клетки коры головного мозга погибают через 5 – 6 мин после прекращения притока артериальной крови, сердечная мышца выдерживает гипоксию продолжи |
