лекции токса. Лекции по токсикологической химии
 Скачать 5.01 Mb. Скачать 5.01 Mb.
|
АЛКАЛОИДЫ В ХИМИКО-ТОКСИКОЛОГИЧЕСКОМ ОТНОШЕНИИИз веществ, экстрагируемых органическим растворителем из щелочного раствора, наибольшее токсикологическое значение имеют алкалоиды. Алкалоиды - органические азотистые основания сложного состава, встречающиеся в растениях (реже в животных организмах) и обладающие сильным фармакологическим действием. Токсикологическое значение алкалоидов Токсикологическое значение алкалоидов очень велико и связано со следующими факторами:
Как лекарственные препараты алкалоиды проявляют фармакологический эффект в очень малых дозах. С другой стороны, алкалоиды обладают выраженной токсичностью и при превышении терапевтических доз могут являться причиной отравлений и даже смерти.
Отравления отдельными алкалоидами могут давать характерную картину: тетанические судороги при отравлении стрихнином, расширение зрачков при отравлении тропановыми алкалоидами. Однако, чаще всего картина отравления и, тем более, патологоанатомического исследования нехарактерны. Поэтому главное значение при доказательстве отравлений алкалоидами приобретает химико-токсикологическое (судебно- химическое) исследование. При отравлении растениями большую помощь может оказать фармакогностическое исследование частей растений в содержимом желудка. В зависимости от химического строения алкалоиды, имеющие токсикологическое значение, можно разделить на 10 групп:
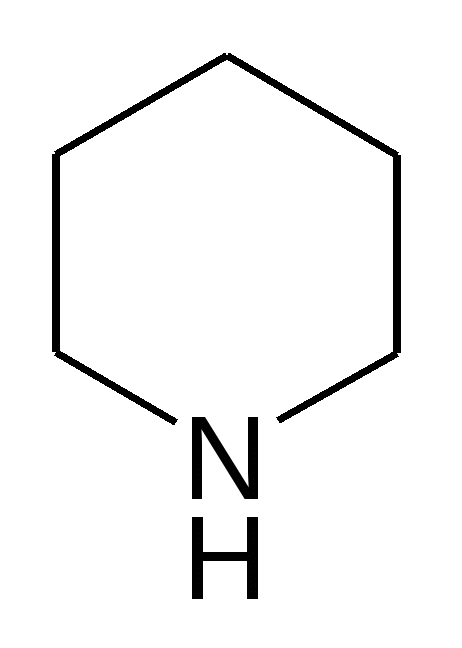 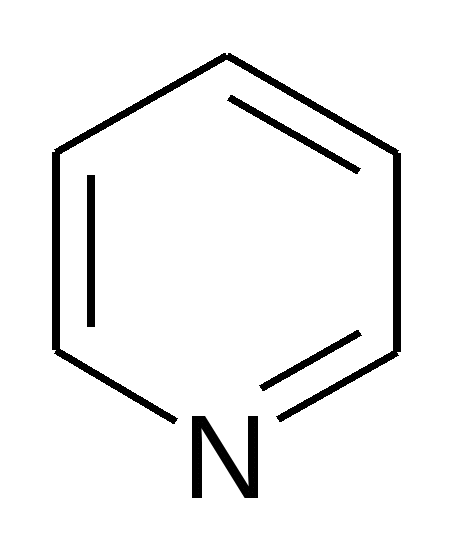 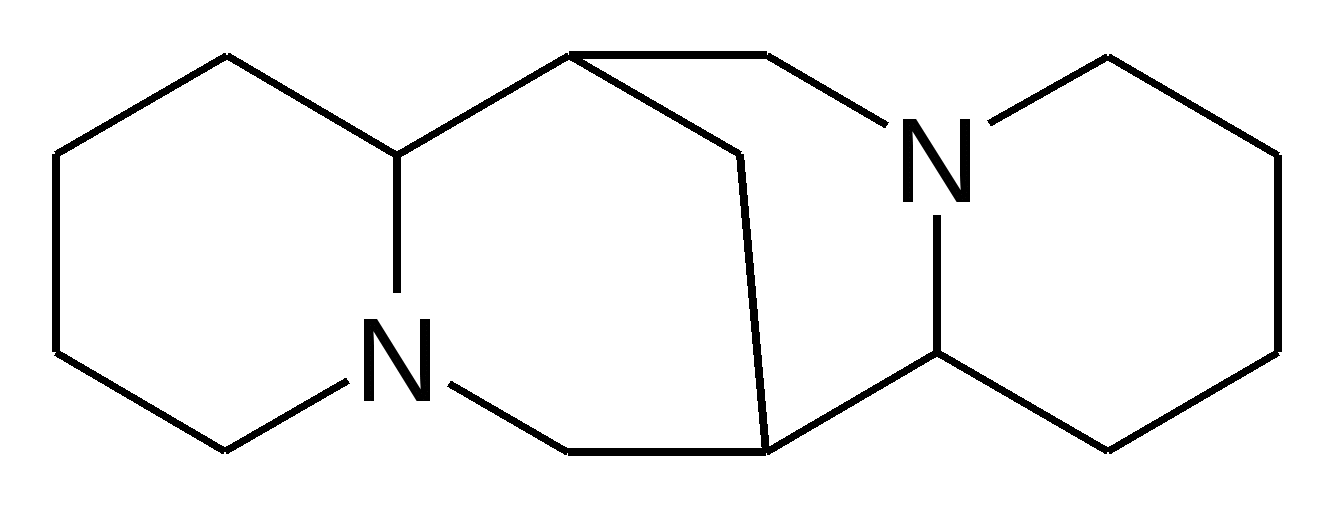 а) моноциклические (кониин, ареколин) б) бициклические (анабазин, никотин) в) полициклические (пахикарпин)
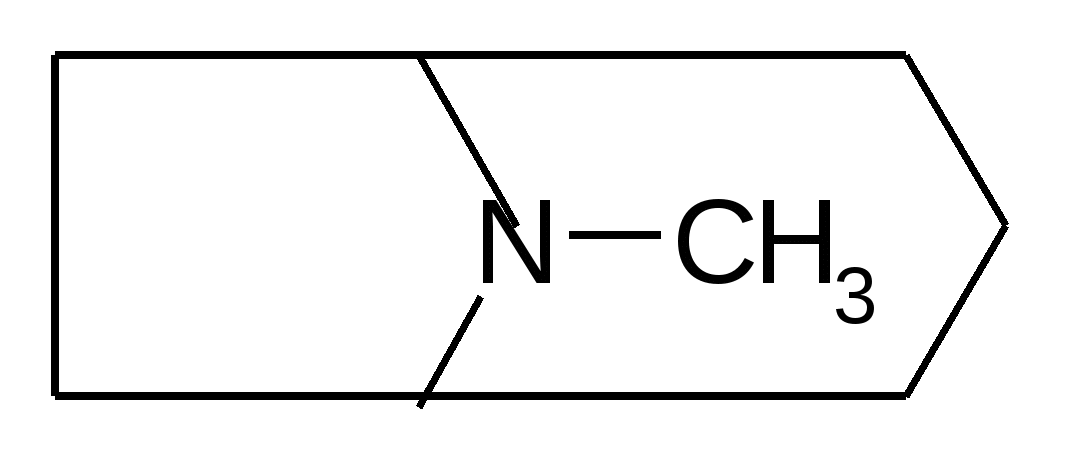 атропин, гиосциамин, скополамин, кокаин
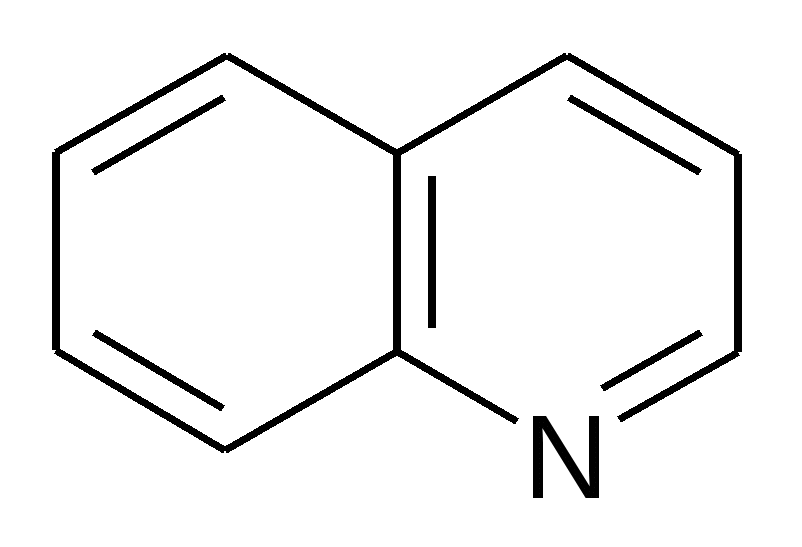 Хинин
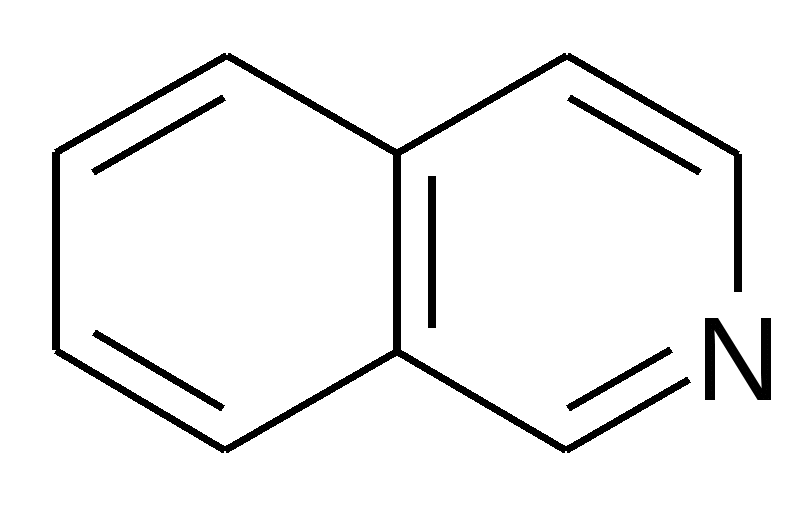 а) производные фенантренизохинолина (морфин, кодеин, дионин, апоморфин, героин) б) производные бензилизохинолина (папаверин, наркотин)
стрихнин, бруцин, резерпин
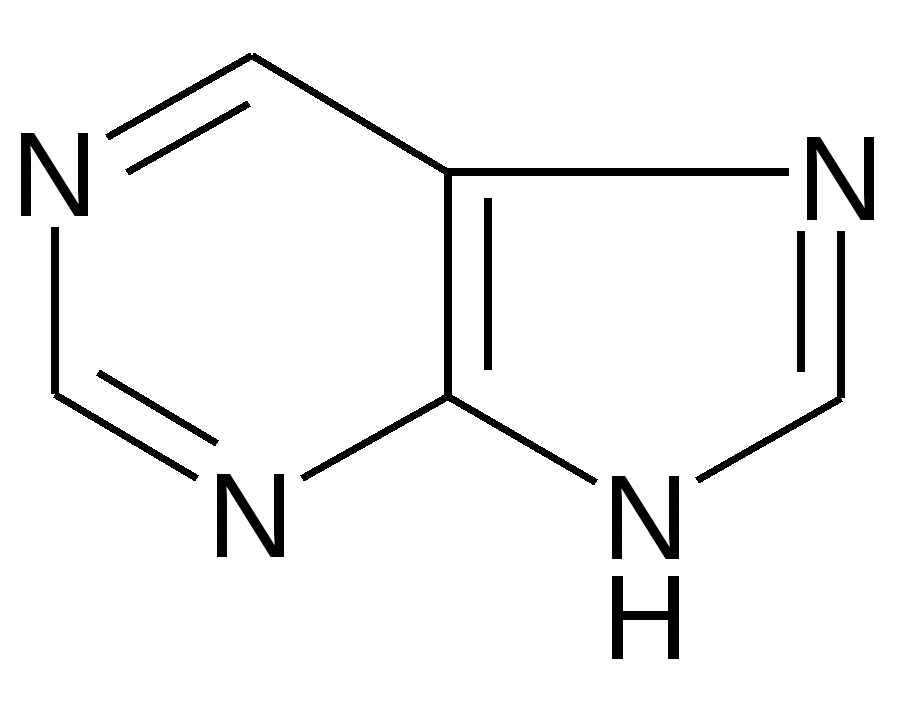 кофеин, теобромин, теофиллин
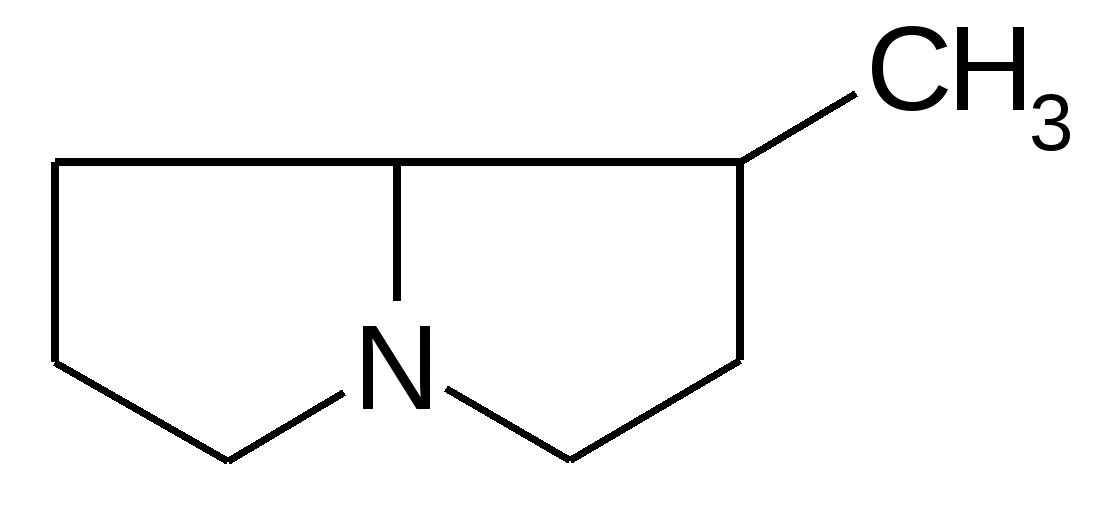 саррацин, платифиллин
Эфедрин
Из перечисленных групп алкалоидов, согласно приказа 1021 от 25.12.73 Министерства здравоохранения СССР, при проведении общего судебно-химического анализа обязательному исследованию подлежат: жидкие алкалоиды - никотин, пахикарпин; тропановые алкалоиды; производные изохинолина (опийные алкалоиды); производные индола - стрихнин. Остановимся на физико-химических свойствах алкалоидов, которые имеют значение в химико-токсикологическом анализе.
Наоборот, соли алкалоидов легко растворимы в воде и спирте, но, как правило, не растворимы в органических растворителях. Однако, алкалоиды-жидкости составляют исключение: их основания растворяются и в воде, и в органических растворителях, что приходится учитывать при проведении судебно-химического исследования на наличие алкалоидов. Соли некоторых алкалоидов, например, хлористоводородные соли кокаина, наркотина, папаверина, йодистоводородная соль пахикарпина способны растворяться в хлороформе. Алкалоиды с малой величиной константы диссоциации (Кд=10-14-10-12) -кофеин, теобромин, теофиллин, папаверин, стрихнин и бруцин - дают непрочные соли, гидролизующиеся даже в кислой среде, поэтому способны экстрагироваться из кислого водного раствора.
а) обладают основными свойствами и дают соли с кислотами (по типу аммиака и аминов); б) вступают во взаимодействие с солями тяжелых металлов, с некоторыми кислотами с образованием нерастворимых осадков (реакции с общеалкалоидными реактивами и микрокристаллоскопические реакции).
Химико-токсикологическое исследование на алкалоидыскладывается из ряда этапов:
Оптимальное значение рН для изолирования алкалоидов на 1 стадии - при настаивании биологического материала с полярными растворителями (вода или этанол) - должно быть 2 -3, чтобы перевести алкалоиды в солеобразные ионизированные формы, хорошо растворимые в воде. При этом степень ионизации 100%. Кислая реакция среды, кроме того, способствует разрушению комплексов алкалоидов с белками, что увеличивает выход алкалоидов. На 2 стадии изолирования - при экстрагирования алкалоидов из жидкой фазы неполярным органическим растворителем - рН устанавливается в пределах 9- 10, что дает возможность перевести алкалоиды из солей в основания, т.е. молекулярные формы, хорошо растворимые в органических растворителях. При этом 0%. Оптимальным экстрагентом для большинства алкалоидов является хлороформ, для некоторых алкалоидов, например, морфина - изоамиловый спирт или дихлорэтан.
Грубая очистка извлечений, содержащих алкалоиды, от балластных веществ, в частности белков, предусмотрена в некоторых методах изолирования. Так, в методе Стаса-Отто проводится осаждение белков абсолютным этанолом, а в методе В.Ф.Крамаренко - сульфатом аммония. Как правило, грубая очистка приводит к потерям алкалоидов за счет их соосаждения с белками. К более тонким методам очистки относятся: 1 - экстракционная очистка 2 - хроматография 3 – электродиализ 1. Экстракционная очистка связана с экстракцией балластных веществ органическими растворителями из кислого водного раствора. При этом алкалоиды в виде солей остаются в водной фазе. Для выделения очищенных алкалоидов из водного раствора водную фазу подщелачивают гидроксидом аммония или натрия. При этом алкалоиды-соли переходят в алкалоиды-основания, которые экстрагируют органическим растворителем (хлороформом). Органическую фазу отделяют, растворитель испаряют, и остаток исследуют на наличие алкалоидов. При сильно загрязненных извлечениях очистку повторяют. Экстракционная очистка связана с частичными потерями алкалоидов за счет их перераспределения между водной и органической фазами. Такой вид очистки предусмотрен в методе В.Ф.Крамаренко, где балластные вещества экстрагируются из кислой водной фазы эфиром. 2. Хроматографические методы очистки являются более экономичными по сравнению с экстракционными. Используются следующие разновидности метода:
Наибольшего внимания из перечисленных методов очистки заслуживает ХТС благодаря своей доступности, простоте выполнения и высокой разрешающей способности.
3. Идентификация выделенных алкалоидов. С этой целью могут быть использованы как химические, так и физико-химические методы анализа. План судебно-химического исследования на наличие алкалоидов включает следующие этапы: а) Анализ начинают с общеалкалоидных осадительных реакций в качестве предварительных групповых проб. б) Затем проводят ХТС-скрининг - также в качестве предварительного теста, но более специфичного благодаря индивидуальным величинам Rf для отдельных алкалоидов. в) Далее выполняют частные реакции на отдельные алкалоиды -реакции окрашивания и микрокристаллические реакции. г) Снимают спектральные характеристики алкалоидов в УФ и ИК-областях спектра. д) Для некоторых алкалоидов проводят фармакологические пробы. Исследованиес общеалкалоидными осадительными реактивами проводится в качестве предварительных испытаний на наличие алкалоидов. Применение этих реактивов основано на свойстве алкалоидов давать даже в разбавленных растворах простые или комплексные соли с некоторыми кислотами, солями тяжелых металлов, комплексными иодидами и рядом других соединений. В литературе описано большое количество осадительных реактивов для алкалоидов. В настоящее время их известно более 250. Общеалкалоидные осадительные реактивы делят на 2 большие группы: 1. Реактивы, дающие с алкалоидами простые соли: - раствор таннина, пикриновая, пикролоновая и некоторые другиеорганические кислоты. 2. Реактивы, дающие с алкалоидами комплексные соединения, которые делятся на 2 подгруппы: а) реактивы, содержащие в своем составе металлоиды:
б) реактивы, содержащие в своем составе металлы: 1) BiI3/KI - реактив Драгендорфа (KBiI4) 2) CdI2/KI - реактив Марме (K2CdI4 ) 3) HgI2/KI - реактив Майера (K2HgI4 ) 4) H2PtCl6 - платинохлористоводородная кислота 5) HAuCl4 - золотохлористоводородная кислота Чувствительность реактивов неодинакова по отношению к различным алкалоидам. Наиболее чувствительными и чаще всего применяемыми в судебно-химической практике являются реактивы Шейблера, Зонненшейна, Драгендорфа и Бушарда-Вагнера (чувствительность реакций лежит в пределах 0,1-0,01 мкг) Обычно предварительные испытания на наличие алкалоидов проводят с двумя-тремя общеалкалоидными реактивами, чтобы получить достоверные результаты (т.к. не все алкалоиды одинаково реагируют со всеми реактивами, и реакции обладают различной чувствительностью). Реакции выполняются с солями алкалоидов. Для того чтобы перевести алкалоид-основание, в виде которого он выделяется из биологического материала, в алкалоид-соль, остаток после испарения хлороформа растворяют в 1-2 каплях 0,1Н раствора НСl . Затем только добавляют реактив и наблюдают за результатом.При наличии алкалоидов наблюдается выпадение осадков или помутнение капли. Судебно-химическая оценка реакций. Все общеалкалоидные осадительные реактивы не являются специфичными для алкалоидов. Кроме алкалоидов, осадки с указанными реактивами дают другие вещества, содержащие гетероатом азота (третичный). Это могут быть синтетические лекарственные вещества, белки и продукты их распада, аминокислоты и многие другие соединения. Исходя из этого, реакциям с общеалкалоидными осадительными реактивами придается толькоотрицательное судебно-химическое значение. Отрицательный результат реакций дает право судебному химику сделать заключение о ненахождении алкалоидов и исключить их из дальнейшего хода исследования. Положительный результат, т.е. получение осадков, свидетельствует о присутствии в исследуемом объекте либо алкалоидов, либо других азотсодержащих веществ основного характера, и требует проведения подтверждающих испытаний. ХТС-скрининг алкалоидов более специфичен по сравнению с общеалкалоидными осадительными реакциями, хотя ему также придается ориентирующее значение в связи с неспецифичностью реагентов-проявителей алкалоидов на хроматограмме. Хроматографирование проводится в тонком закрепленном слое силикагеля. В качестве подвижной фазы используются системы растворителей: -диоксан - хлороформ - ацетон - 25% раствор аммиака (47,5: 45: 5: 2,5) -толуол - ацетон - этанол - 25% раствор аммиака (45: 45: 7,5: 2,5) (в экспресс-анализе интоксикаций, вариант ВЭТСХ). Пробег растворителей составляет 10 см. Детектирование алкалоидов и синтетических лекарственных веществ основного характера на хроматограмме проводится реактивом Драгендорфа. В зонах расположения веществ появляются красно-оранжевые пятна. Чувствительность обнаружения составляет десятые доли микрограмма. Идентификацию алкалоидов и синтетических лекарственных веществ проводят по величине Rf относительно метчиков. В качестве метчиков используют хлороформные растворы стандартных веществ с определенной концентрацией. Величины Rf большинства токсикологически важных алкалоидов и азотсодержащих веществ основного характера приведены в справочных таблицах. Необходимость использования метчиков связана с колебаниями значений Rf ввиду трудностей соблюдения абсолютно стандартных условий хроматографического разделения. ХТС-скринингу придается отрицательное судебно-химическое значение. При отсутствии пятен на хроматограмме можно сделать заключение о ненахождении алкалоидов и других азотсодержащих лекарственных веществ основного характера и исключить их из дальнейшего хода исследования. Совпадение величины Rf испытуемого вещества с величиной Rf метчика дает возможность сделать предварительное заключение об их идентичности. Последующее подтверждение присутствия алкалоида проводится более специфичными реакциями и методами. В качестве подтверждающих реакций после хроматографического исследования используют реакции окрашивания и микрокристаллические реакции.
а) отнятие воды (дегидратация) под действием концентрированной серной кислоты (вератрин, бруцин и др.) б) окисление алкалоидов (кофеин –мурексидная проба, хинин -таллейохинная проба) в) одновременное окисление и отнятие воды (реакция с дихроматом калия в присутствии концентрированной серной кислоты на стрихнин) г) конденсация с альдегидами (реактив Марки с опийными алкалоидами) Чаще всего для реакций окрашивания используются:
Реакции окрашивания выполняются с основаниями алкалоидов. Соответствующий реактив наносится на сухой остаток после испарения хлороформного извлечения. Реакции окрашивания могут быть специфичными для некоторых алкалоидов (бруцин, вератрин), или могут давать возможность обнаружения группы алкалоидов. Например, реактив Марки является групповым реагентом на опийные алкалоиды. Большинство реактивов, используемых для реакций окрашивания, имеют в своем составе концентрированную серную кислоту, поэтому при исследовании сильно загрязненных остатков может наблюдаться обугливание соэкстрактивных органических веществ. Степень чистоты остатка поэтому имеет немаловажное значение. Чувствительность реакций окрашивания составляет от нескольких мкг до сотых долей микрограмма.
Судебно-химическая оценка метода. Микрокристаллические реакции обладают высокой чувствительностью, надежностью и доказательностью. Результаты их наглядны, они могут быть зафиксированы в виде фотографий и представлены судебно-следственным органам в качестве приложения к акту судебно-химической экспертизы. Определение кристаллооптических констант образующихся продуктов значительно повышает надежность микрокристаллических реакций. В области кристаллооптического анализа алкалоидов большая работа проведена профессором В.Т.Поздняковой (Львовский медицинский институт). В ее монографии «Микрокристаллоскопический анализ фармацевтических препаратов и ядов» (1968 г.) рекомендован целый ряд микрокристаллических реакций на алкалоиды, пригодных для исследования биологического материала. Определены кристаллооптические константы продуктов реакций (угол погасания, знак удлинения, показатели преломления). Являясь ценным методом доказательства алкалоидов, микрокристаллические реакции, в то же время, не лишены недостатков: при исследовании биологического материала присутствие соэкстрактивных веществ приводит к появлению кристаллов нехарактерной формы, нарушаются кристаллооптические константы, отмечается полиморфизм (присутствие одновременно кристаллов различных форм), поэтому требуется высокая степень чистоты выделенных веществ. Значительное влияние на надежность метода оказывает квалификация химика, навык в выполнении этих реакций. УФ и ИК спектроскопия является одним из наиболее важных способов идентификации алкалоидов. Для доказательства алкалоидов, выделенных из биологического материала, чаще используют УФ-спектроскопию как наиболее чувствительный метод. Гетероциклы, лежащие в основе строения отдельных групп алкалоидов, часто имеют характерные максимумы поглощения в УФ-свете. Так, производные пиридина имеют максимум при длине волны 260 нм, хинолина (изохинолина) - при 250, 290, 310 нм, индола - 260 (255) и 300 нм, пурина - 220, 260 и 270 нм. Спектральные методы анализа требуют высокой степени чистоты выделенных веществ и сочетаются с предварительной очисткой. Фармакологические пробы. В том случае, если алкалоид оказывает характерное действие на живой организм, могут быть выполнены фармакологические пробы на животных, которые проводятся квалифицированным специалистом-фармакологом. Например, при доказательстве атропина капают водный раствор испытуемого вещества в глаз кошки. При наличии атропина наблюдается характерное стойкое расширение зрачка. Стрихнин и никотин, нанесенные на спинку лягушки, вызывают ее гибель в характерной позе («молящаяся лягушка» - стрихнин, «сидящая» - никотин). Фармакологические пробы оказывают существенную помощь химику-эксперту при доказательстве алкалоидов. В ряде случаев эти пробы не менее чувствительны и более специфичны, чем химические реакции. 4. Количественное определение алкалоидов проводится фотометрическим и спектрофотометрическим методами (в видимой и УФ-областях спектра).
Определение проводится на спектрофотометре, т.к. закон Бера справедлив только для монохроматического излучения.
Окрашенные продукты могут быть получены также в реакциях окисления, восстановления, конденсации, азотосочетания и некоторых других. Измерение абсорбции можно вести как на фотоэлектроколориметрах, так и на спектрофотометрах. Расчет концентрации проводится по калибровочной кривой. При использовании спектрофотометрии можно использовать уравнение Бугера-Ламберта-Бера. Фотометрические методы анализа позволяют определять очень малые (несколько микрограммов) количества алкалоидов, но требуют высокой степени чистоты выделенного вещества, поэтому сочетаются с ХТС – очисткой полученных извлечений. |

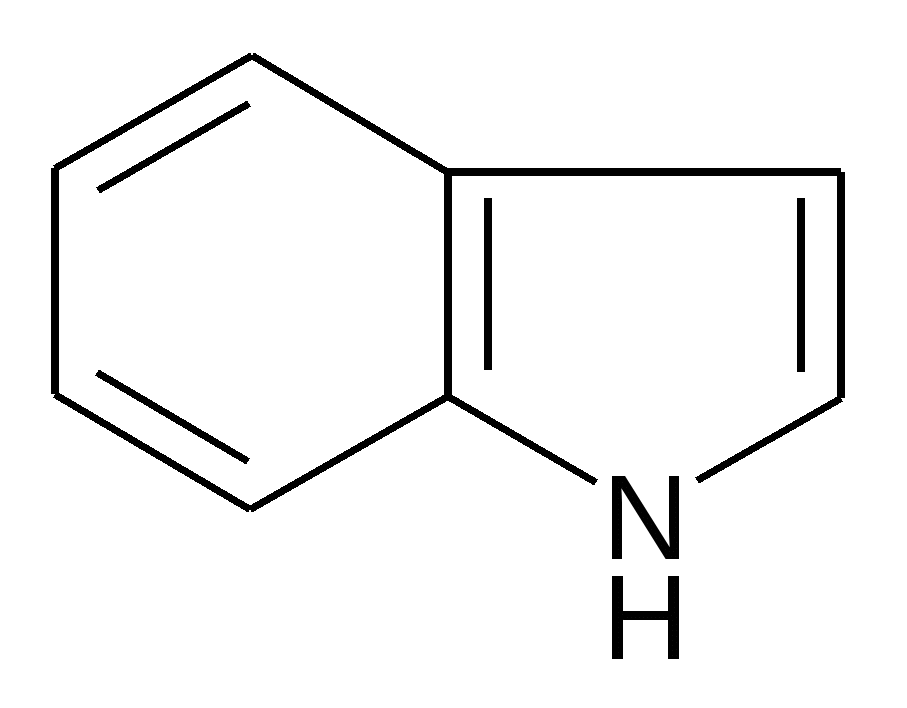 роизводные индола (бензопиррола)
роизводные индола (бензопиррола)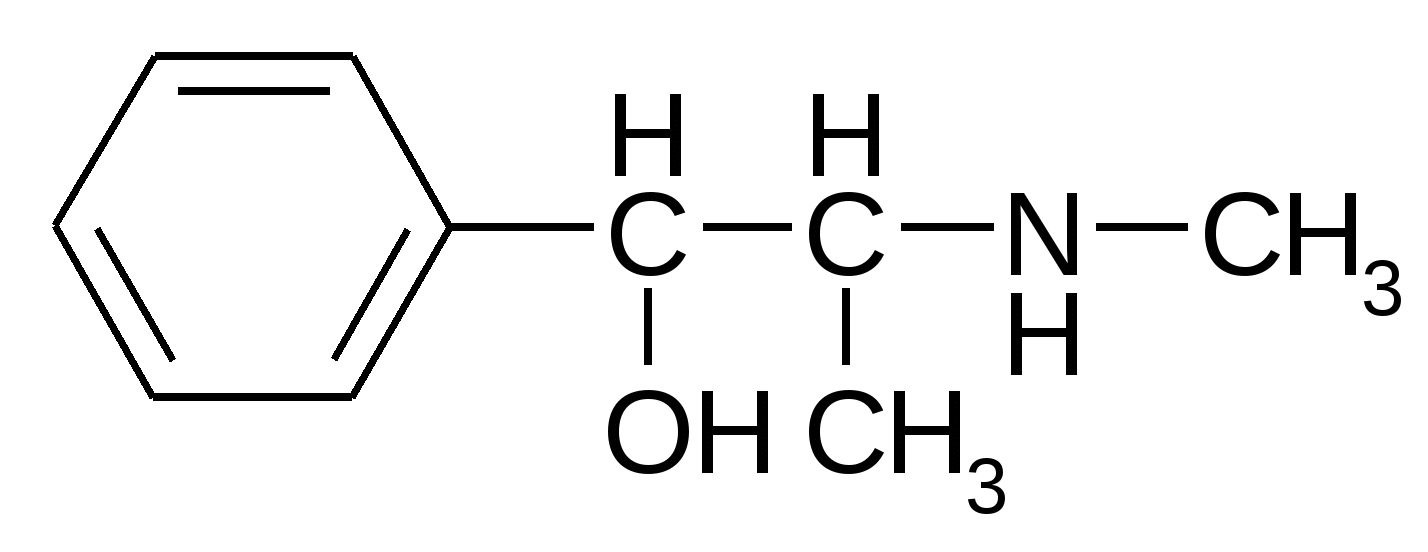 циклические алкалоиды
циклические алкалоиды