лекции токса. Лекции по токсикологической химии
 Скачать 5.01 Mb. Скачать 5.01 Mb.
|
ПРОИЗВОДНЫЕ БАРБИТУРОВОЙ КИСЛОТЫВ ХИМИКО-ТОКСИКОЛОГИЧЕСКОМ ОТНОШЕНИИИз лекарственных веществ, экстрагируемых органическим растворителем из кислого раствора, наибольшее токсикологическое значение имеют производные барбитуровой кислоты. Эта группа веществ подлежит обязательному судебно-химическому исследованию при проведении общего судебно-химического анализа (Приказ МЗ СССР . №1021 от 25.12.73 г.). Первый из барбитуратов – барбитал- синтезирован в 1881 г. В медицинскую практику производные барбитуровой кислоты были введены в 1903 г. Фишером и Мерингом. В настоящее время синтезировано около 2500 производных, из которых в нашей стране применяется 11. Токсикологическое значение производных барбитуровой кислоты очень велико. С одной стороны, барбитураты обладают высокой фармакологической активностью, поэтому их передозировка может привести к различным осложнениям и даже вызвать смертельный исход. С другой - они достаточно доступны для населения, т.к. широко используются в медицинской практике в качестве снотворных, седативных, противосудорожных средств. В технике и в фотографии применяются как ингибиторы и антиоксиданты, в химических лабораториях как реактивы. При длительном применении они вызывают пристрастие и привыкание, т.е. барбитуровую токсикоманию и наркоманию (барбамил и этаминал-натрий официально отнесены к наркотическим средствам). Все эти факторы приводят к тому, что производные барбитуровой кислоты занимают одно из первых мест по количеству вызываемых ими отравлений. В основе химического строения барбитуратов лежит кольцо малонилмочевины, или барбитуровой кислоты, которая может быть получена при взаимодействии мочевины и диэтилового эфира малоновой кислоты. 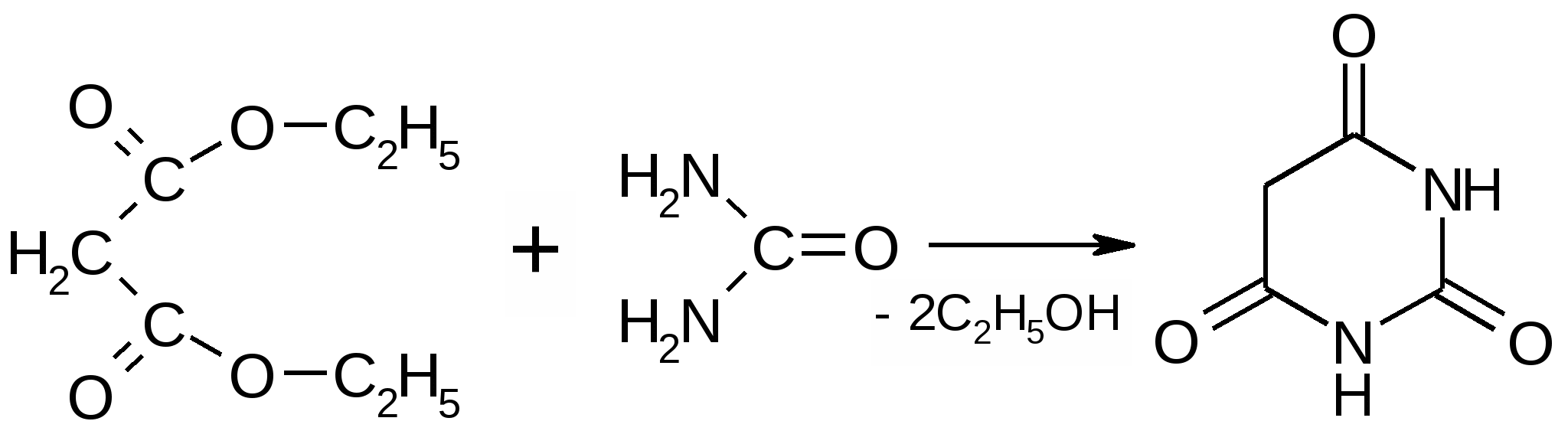 малонилмочевина (2,4,6-триоксипиримидин) Барбитуровая кислота является циклическим уреидом и может рассматриваться как производное пиримидина (2,4,6 - триоксипиримидин). Атомы водорода метиленовой группы в 5-ом положении пиримидинового кольца, а также водород, стоящий у атомов азота в 1-ом и 3-ем положениях, подвижны и способны замещаться различными органическими радикалами, атом кислорода в положении 2 также способен замещаться на атом S. На этих свойствах и основан синтез производных барбитуровой кислоты. Общую формулу барбитуратов можно изобразить следующим образом: 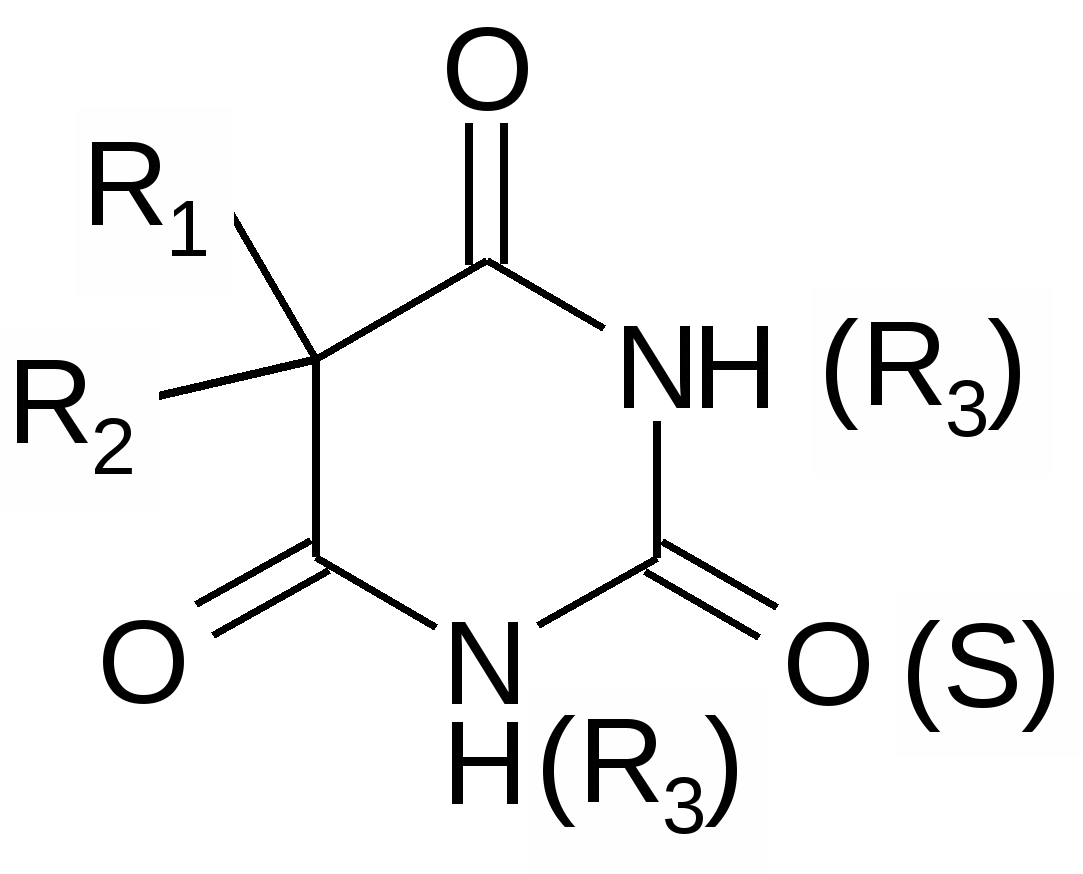
1) 5,5 -замещенные производные (двузамещенные), из которых наиболее часто применяются:
СН3
СН34. Этаминал –натрий R1 - C2H5, R2 – CH - CH2 - СН2 – СН3 CH3
1. Гексенал R1 – CH3, R3 – CH3 2 CH3
CH3
1 По физическим свойствам все интересующие в настоящее время судебно-химическую экспертизу барбитураты представляют собой белые кристаллические вещества без запаха, горького вкуса, лишь тиопентал имеет желтоватый оттенок и обладает слабым запахом серы. Кислотные /молекулярные/ формы барбитуратов растворимы в эфире, хлороформе, спирте и некоторых других органических растворителях, натриевые производные - в воде. Барбитураты имеют высокие температуры плавления. />100С/ и способны возгоняться без разложения, что используется для их очистки от посторонних примесей при выделении из биологического материала. Лактим-лактамная таутомерия барбитуратов. В водных растворах барбитураты обладают кислотными свойствами (рКа 7-8). Это объясняется тем, что барбитураты в зависимости от рН среды способны существовать в нескольких таутомерных формах: 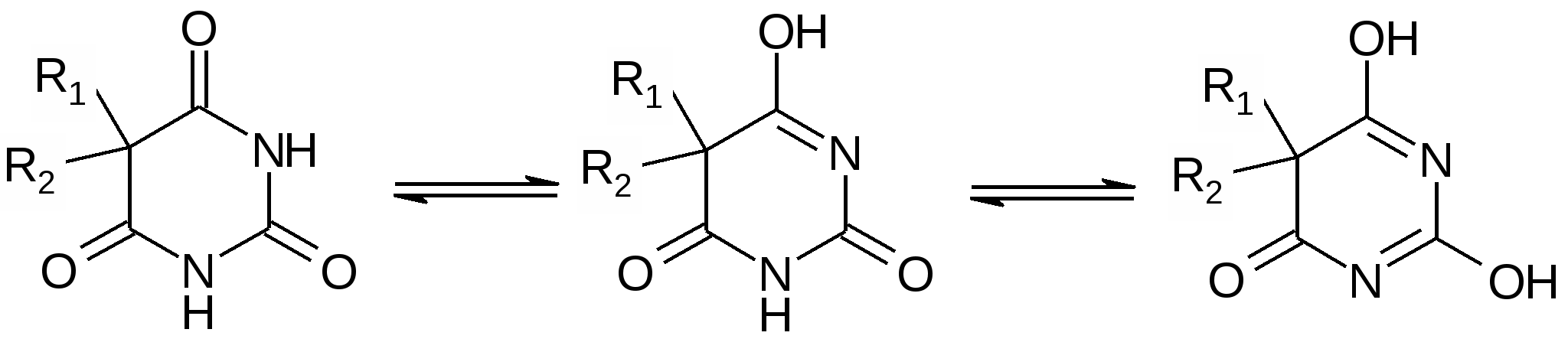 рН=2 рН=10 рН=13 лактамная лактимная дилактимная Форма форма форма В случае N-замещенных производных возможно образование только лактимной структуры, т.к. второй атом N замещен радикалом (R3). Кислотные свойства обусловлены тем, что атомы водорода гидроксильных групп способны отщепляться в виде ионов, подобно тому, как это происходит в фенольном гидроксиле, и замещаться на атом Ме, образуя солеобразные соединения. На лактим-лактамной таутомерии барбитуратов основано получение их натриевых производных, которые, в отличие от лактамных форм, хорошо растворяются в воде (мединал - производное барбитала, барбамил, этаминал-натрий, гексенал, тиопентал). В то же время, Na-производные плохо растворяются в органических растворителях, таких, как эфир, хлороформ, бензол, дихлорэтан и других. Лактамные формы, наоборот, хорошо растворимы в указанных органических растворителях, спирте, щелочах (в последних за счет образования Na-производных). Способность барбитуратов существовать в нескольких таутомерных формах и различная растворимость этих форм в воде и органических растворителях используется для их изолирования и очистки при выделении из биологического материала. На этом же свойстве барбитуратов основано исследование их в УФ-области спектра, т.к. таутомерные формы обладают различным светопоглощением. Химико-токсикологическое исследование биологического материала на наличие производных барбитуровой кислоты состоит из этапов: 1. Изолирование из объекта 2. Очистка полученного извлечения 3. Идентификация 4. Количественное определение 1 Этап. Выбор метода изолирования определяется характером объекта исследования и поставленными перед химиком задачами. Для целей клинического исследования в случае острых отравлений, а также в судебно-химической лаборатории, когда объектами исследования являются промывные воды желудка, диализат, небольшое количество крови и мочи, извлечение барбитуратов проводится непосредственно экстракцией органическим растворителем. В качестве экстрагентов используются эфир, хлороформ, дихлорэтан и др. Количество извлеченных барбитуратов составляет 70-90%. Однако, непосредственная экстракция, как правило, дает извлечения, загрязненные соэкстрактивными веществами (жирами, белками, пигментами) и требует последующей дополнительной очистки. При исследовании трупного материала (внутренних органов) а) при общем (ненаправленном) судебно-химическом анализе изолирование барбитуратов проводится подкисленным спиртом и подкисленной водой. Последующая экстракция их из кислого водного раствора осуществляется органическим растворителем, чаще эфиром или хлороформом. Максимальные количества барбитуратов извлекаются в интервале рН 1-3, т.к. при данном значении рН барбитураты существуют в молекулярной форме, которая хорошо растворяется в органических растворителях и ограниченно в воде. Изолирование подкисленной водой и подкисленным спиртом обеспечивает выход барбитуратов порядка 25-30% (некоторые барбитураты изолируются этанолом на 50% - барбамил, этаминал-Na, фенобарбитал). б) При специальном (частном, направленном) исследовании на производные барбитуровой кислоты проводят извлечение подщелочной водой по методу Валова. Выход барбитуратов> 50% при достаточной чистоте выделенных веществ. Существует ряд методов, основанных на изолировании барбитуратов органическими растворителями (ацетонитрилом, ацетоном, хлороформом, смесью спирта и хлороформа) с последующей очисткой выделенных веществ. 2 Этап. Очистка извлеченных барбитуратов от балластных веществ. Как правило, барбитураты, выделенные из биологического материала, содержат примеси посторонних веществ, которые извлекаются совместно с барбитуратами и являются нормальными компонентами организма (жиры, белки, пигменты, дубильные, смолобразные вещества и др.). Соэкстрактивные (балластные) вещества мешают дальнейшей идентификации и определению барбитурата. Выбор метода очистки зависит, в основном, от количества изолированного вещества и до некоторой степени от его химического строения. При больших количествах барбитуратов чаще используют экстракционный метод очистки и микросублимацию (возгонку). Экстракционная очистка основана на способности барбитуратов к имидо-имидольной таутомерии и на различной растворимости имидной и имидольной форм в воде и органических растворителях. Используя реэкстракцию барбитурата раствором гидроксида натрия из органической фазы, тем самым освобождаются от сопутствующих веществ, не растворимых в воде (натриевые соли хорошо растворимы в воде и извлекаются ею). Последующее выделение барбитурата из водной фазы проводят после подкисления водного раствора (рН 2) экстрагированием органическим растворителем. При этом барбитурат в молекулярной форме извлекается органическим растворителем, а в водной фазе остаются балластные вещества, не растворимые в органическом растворителе. Микросублимация основана на способности барбитуратов возгоняться без разложения при нагревании. Возгонка проводится в нагревательной камере прибора Кофлера, либо, в упрощенном виде, с одного предметного стекла на другое, верхнее из которых охлаждается, а нижнее (с исследуемым остатком) нагревается. При малых количествах выделенных веществ чаще используют хроматографические методы очистки (ионообменную и гель-хроматографию на колонке, ТСХ, ВЭТСХ, ВЭЖХ). С точки зрения простоты, доступности и разрешающей способности наибольшего внимания заслуживают ТСХ, ВЭТСХ. Они позволяют не только очистить выделенные вещества от примесей, но и разделить целый ряд барбитуратов при их совместном присутствии, а также отделить барбитураты от их метаболитов и провести предварительную идентификацию по величине Rf. 3 Этап. Для идентификациибарбитуратов используют химические, физические и физико-химические методы анализа. К химическим методом можно отнести реакции окрашивания барбитуратов. Наиболее известны реакции барбитуратов:
В микрокристаллоскопическом анализе барбитуратов использована их способность давать характерные кристаллические осадки при взаимодействии с солями тяжелых металлов (хлорцинкйодом, железо - и меднойодидным комплексами, меднопиридиновым реактивом) и выпадать в осадок из растворов концентрированной серной кислоты при понижении ее концентрации (выделение кислотной формы барбитурата). Формы образующихся кристаллов характерны для каждого отдельного барбитурата. Чувствительность реакций достигает мкг и даже десятых долей мкг. Обладая высокой чувствительность, доказательностью и специфичностью, микрокристаллические реакции не лишены и ряда недостатков: -их проведение требует высокой степени чистоты исследуемого вещества, -наличие примесей снижает чувствительность реакции, а также мешает правильной кристаллизации, -производные барбитуровой кислоты склонны к полиморфизму образующихся кристаллов. В зависимости от ряда факторов - концентрации вещества, скорости кристаллизации, температуры, наличия посторонних примесей- барбитураты способны образовывать кристаллы различной формы, что затрудняет идентификацию отдельных веществ по форме кристаллов. Из физических и физико-химических методов анализа применение нашли: ТСХ, ВЭТСХ, ВЭЖХ, спектроскопия в УФ и ИК областях спектра. Хроматография в тонком слое и ВЭТСХ используются в качестве предварительного испытания на наличие производных барбитуровой кислоты. Они дают возможность разделить несколько барбитуратов при их совместном присутствии и идентифицировать каждый барбитурат в случае комбинированного отравления. ТСХ позволяет также отделить барбитураты от их метаболитов и провести очистку полученного извлечения от балластных веществ. Хроматографирование ведут на закрепленном слое силикагеля в системах растворителей: 1) хлороформ-ацетон (9:1) -для разделения N - замещенных и 5,5-замещенных производных, система является общей в скрининге лекарственных веществ кислого и нейтрального характера. 2) толуол – ацетон – этанол - 25% раствор аммиака (45:45:7,5:2,5) (применяется в экспресс- анализе интоксикаций) 3) хлороформ - н-бутанол - 25% раствор аммиака (70:40:5) - в качестве частной системы для разделения 5,5 -замещенный барбитуратов. Детектирование веществ на хроматограмме проводится двумя реагентами: дифенилкарбазоном (ДФК) и НgSО4. При этом в местах расположения барбитуратов возникают красно- или сине-фиолетовые пятна. Идентификация проводится по величине Rf (отношение длины пробега вещества к длине пробега растворителя). Хроматографирование ведут параллельно метчикам (А), в качестве которых используют хлороформные растворы барбитуратов с известной концентрацией.
Спектроскопическое исследование барбитуратов чаще проводят в области длин волн 200-400 нм, т.е. в УФ области спектра, получая электронные спектры поглощения (что обусловлено наличием в структуре системы хромофоров и ауксохромов). Способность барбитуратов к абсорбции в УФ области связана с их таутомерными превращениями. Для 5,5-замещенных производных:
В отличие от 5,5-дизамещенных барбитуратов, трехзамещенные имеют лишь одну ионизированную форму (имидольную), поэтому их поглощение не меняется с переходом от рН 10 к рН 13, и они обладают одним максимумом в щелочной среде при длине волны 245 нм. Тиобарбитураты особенно удобны для исследования в УФ области, т.к. имеют два максимума в кислом растворе (239-290 нм), в щелочном при рН=10 также два максимума (255 и 310 нм) и при рН 13 - один (310нм). Таким образом, УФ-спектроскопия дает возможность дифференцировать барбитураты в зависимости от типа замещения в пиримидиновом кольце на: 1. Двузамещенные (рН 2 - нет max, рН 10 - 240 нм, рН 13 -255-260 нм) 2. Трехзамещенные (рН 2 - нет max, рН 10 и рН 13 -245 нм) 3. Тиобарбитураты (рН 2 - 239 нм и 290 нм, рН 10 - 255 и 310 нм, рН 13 - 310 нм). Однако, дифференциация отдельных представителей внутри каждого из типов замещения затруднительна, т.к. их спектры сходны между собой. Применение спектральных методов анализа требует высокой степени чистоты выделенных веществ и должно сочетаться с их хроматографической очисткой. Заключение о присутствии барбитуратов дается по комплексу результатов реакций, ХТС и УФ-спектроскопии. 4 Этап. Для количественного определения барбитуратов в настоящее время используется спектрофотометрический метод. При спектрофотометрическом определении барбитуратов, выделенных из биологического материала, используют принцип дифференциальной спектрофотометрии, т.к. прямому СФ-определению мешают посторонние вещества, извлекающиеся из объекта исследования совместно с барбитуратами. В 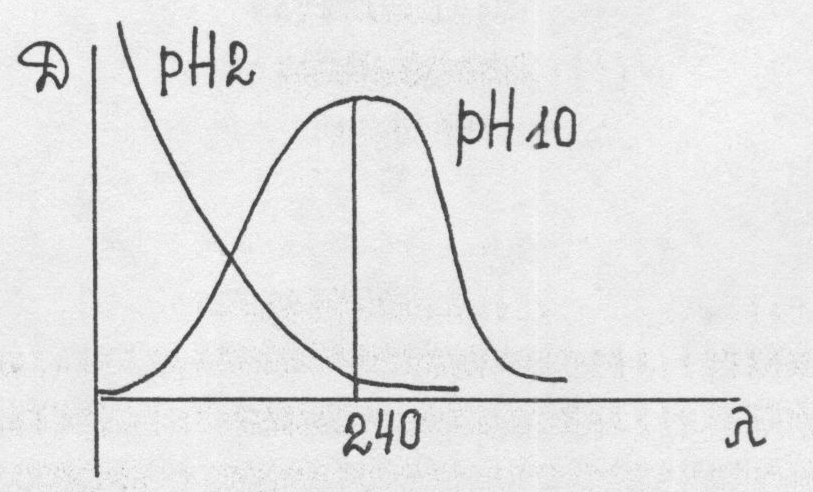 I варианте концентрацию барбитурата в растворе (после его элюирования с хроматограммы) определяют по разности абсорбций в щелочном - рН 10 и кислом - рН 2 растворах при =240 нм. I варианте концентрацию барбитурата в растворе (после его элюирования с хроматограммы) определяют по разности абсорбций в щелочном - рН 10 и кислом - рН 2 растворах при =240 нм.D=DpH10-DpH2 В 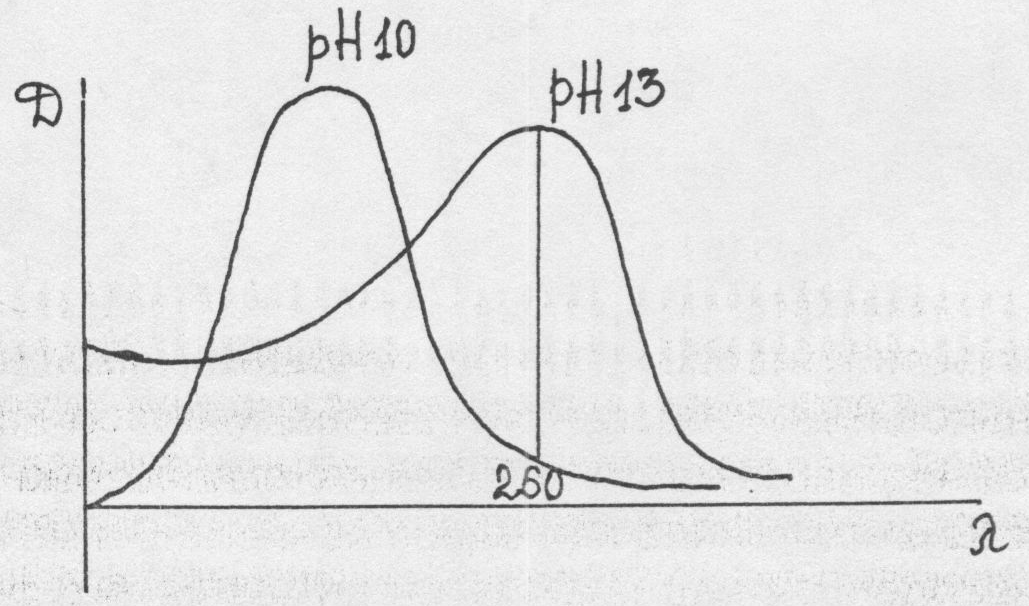 о II варианте - по разности абсорбций в щелочных - рН 13 и рН 10 растворах при =260нм. о II варианте - по разности абсорбций в щелочных - рН 13 и рН 10 растворах при =260нм. D=DpH13-DpH10 Использование принципа дифференциальной спектрофотометрии возможно, когда поглощение примесей при выбранной длине волны не зависит от рН среды. Тогда при вычитании оптических плотностей происходит уничтожение абсорбции примесей, что дает возможность получать истинные результаты количественного определения. Например, В 1 варианте - DpH 10 = D10 + D10 240 нм D pH 2 = 0 2 + D 2 D = DpH10 - DpH2 = (D10 + D10 ) – D2 D10 = D2 D = D10 Если поглощение примесей одинаково при рН 10 и при рН 2 (при 240 нм), то при вычитании они взаимно уничтожаются и остается поглощение барбитурата. Таким образом, снимается влияние примесей на результаты количественного определения во II варианте - D pH13 =D13 + D 13 260 нм D pH10 =D 10 + D 10 D = D pH13 - D pH10 = (D13 + D 13 ) – (D 10 + D 10 ) D 13 = D 10 D = D 13 - D 10 т.е. поглощение D обусловлено самим барбитуратом и нет искажения результатов за счет примесей. Расчет концентрации ведут по уравнению закона Бугера-Ламберта-Бера: D = Е 1% · l · С, откуда С = D/Е 1% · l 1 см 1 см где С - концентрация вещества в %; D - дифференциальная оптическая плотность (абсорбция); Е 1% -удельный показатель поглощения (численно равен поглощению 1% раствора). Рассчитывается заранее для каждого барбитурата по растворам с известной концентрацией. l - толщина светопоглощающего слоя (1 см) С точки зрения чувствительности определения наиболее выгодным оказывается 1 вариант, т.к. он дает большую D. Однако, в коротковолновой области при =240 нм сильнее проявляется мешающее влияние примесей, поэтому чаще этот вариант используют в сочетании с предварительной хроматографической очисткой. Во 2 варианте D несколько меньше, в связи с чем ниже и чувствительность определения, но одновременно снижается влияние примесей в более длинноволновой области при 260 нм. Поэтому увеличивается надежность определения. Этим вариантом можно пользоваться даже без предварительной хроматографической очистки, например, при работе с биологическими жидкостями (кровь, моча), не подвергшимися гнилостному разложению. Определение концентрации барбитуратов в биологических жидкостях позволяет: а) установить тяжесть отравления и контролировать эффективность проводимого лечения в условиях клиники при острых отравлениях барбитуратами. б) в посмертных случаях позволяет сделать заключение о приеме токсических или терапевтических доз, т.е. ответить на вопрос - явилось ли найденное вещество причиной смерти. Токсические уровни барбитуратов в крови обычно превышают десятки мкг/мл, а при тяжелых отравлениях, заканчивающихся смертельным исходом, - сотни мкг/мл. Токсикологическое значение барбитуратов обусловлено, с одной стороны, их сильным фармакологическим действием (список Б, барбамил и этаминал - список А), а с другой стороны - сравнительной доступностью для населения, о чем мы уже говорили выше. Опасность отравления усиливается способностью барбитуратов к кумуляции, т.е. накоплению в организме даже при приеме терапевтических доз. В настоящее время известно о возможном пристрастии к этой группе препаратов и о синергизме при совместном приеме с алкоголем, опиатами и психотропными средствами (транквилизаторами, алкалоидами белладонны и др.), что усиливает токсикологическое значение барбитуратов. Токсичность. Смертельной дозой барбитуратов считают одномоментный прием 10 лечебных разовых доз каждого из препаратов или их смеси с различными индивидуальными различиями (фенобарбитал -2,0, этаминал-Na -1,0). Иногда же эта доза достигает 4 и даже 6-10 г (барбитал). Токсикокинетика барбитуратов(всасывание, распределение, метаболизм, выделение)
Связь барбитуратов с белками плазмы в количественном отношении: барбамил - 50-60% этаминал-натрий -50-55% фенобарбитал - 15% барбитал -5% Свободная фракция барбитуратов, в основном, определяет физиологическую активность препарата. Чем меньше связь барбитуратов с белками плазмы, тем в большей степени они выделяются с мочой в неизмененном виде. Наибольшие концентрации барбитуратов определяются в печени, почках, селезенке, крови и тканях мозга.
б)
а) деметилирование гексенала 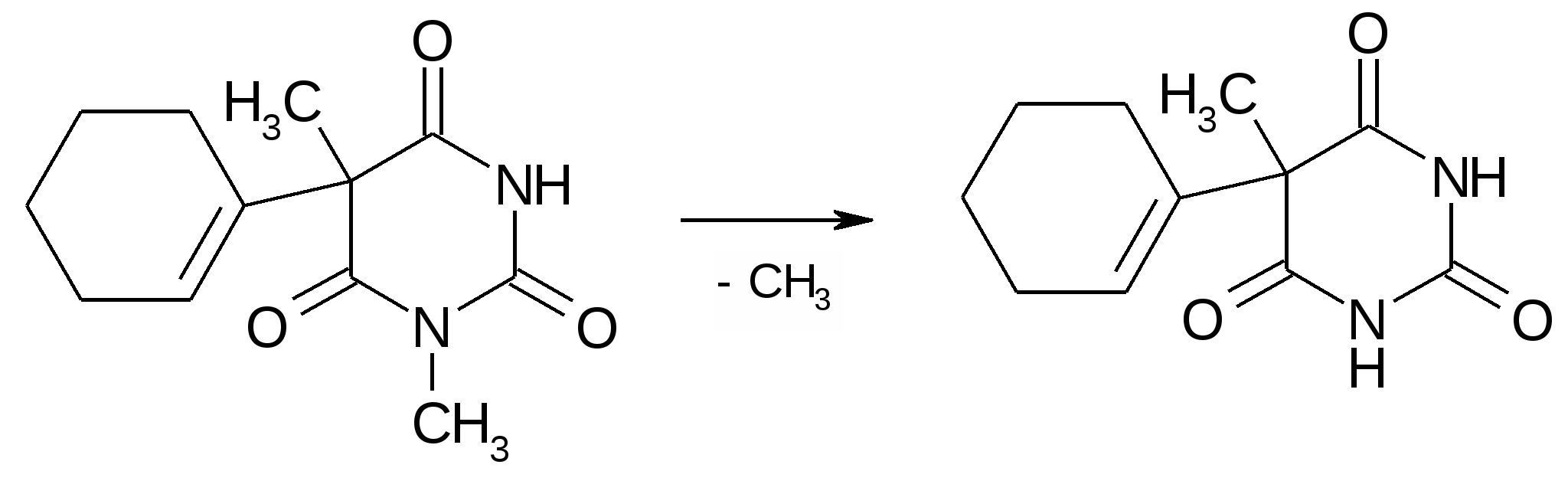 б) дебензоилирование бензонала и бензобамила и превращение их в фенобарбитал и кислотную форму барбамила,соответственно. 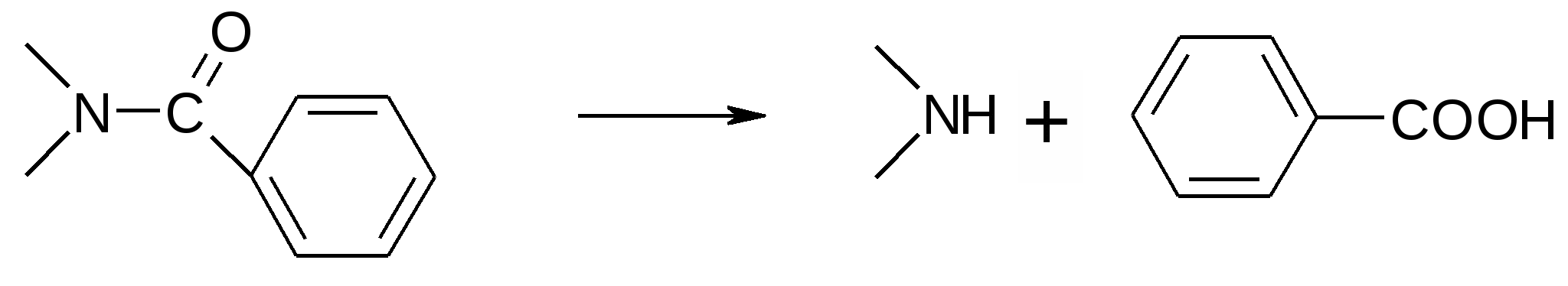 3.Десульфирование тиобарбитуратов: 4.Гидролиз (распад пиримидинового кольца)
Токсикодинамика (развитие отравлений). Барбитураты принадлежат к обширной группе лекарственных препаратов снотворного действия, которые обладают способностью избирательного токсического действия на ЦНС, что приводит к угнетению всех ее основных функций. В клинической картине острых отравлений барбитуратами и другими снотворными и седативными средствами выделяют 4 ведущих клинических синдрома: 1. Коматозное состояние и другие неврологические расстройства (оглушённость, сон, отсутствие рефлексов). 2. Нарушение дыхания. 3. Нарушение функции сердечно-сосудистой системы. 4. Трофические расстройства и нарушение функций почек (соматогенная фаза отравления) (1,2,3 -токсикогенная фаза отравления) 1 синдром: для коматозного состояния, вызванного угнетающим действием барбитуратов на ЦНС, характерна определенная стадийность, когда последовательно развиваются явления: 1. Оглушения и глубокого сна -1 стадия комы;
Глубокая кома сопровождается нарушением дыхания и кровообращения. Определение содержания барбитуратов в крови методом спектрофотометрии позволяет отметить определенную зависимость развития коматозного состояния от уровня этих препаратов в крови. Так, поверхностная кома наблюдается при содержании: этаминала-Na 0,1 г/л (100мкг/мл); барбамила 0,3 г/л (300 мкг/мл); фенобарбитала > 0,4 г/л (400 мкг/мл). Концентрация барбитуратов в спинномозговой жидкости примерно соответствует содержанию их в крови, а в моче значительно выше, но не зависит от глубины коматозного состояния. Таким образом, количественное определение барбитуратов значительно облегчает дифференциальную диагностику отравлений при коме неясной этиологии. 2 синдром: нарушения внешнего дыхания являются наиболее частыми и грозными осложнениями коматозных состояний. Они отмечаются у 11% больных с данной патологией и требуют незамедлительной дыхательной реанимации (бронхорея - слизь в бронхах, гиперсаливация - усиленное слюноотделение, западение языка, ларингоспазм или аспирация (вдыхание) промывной жидкости - аспирационно-обтурационная форма нарушения внешнего дыхания). Центральная форма - как прямое угнетение центров продолговатого мозга (дыхательного центра) снотворными средствами. После ликвидации острых нарушений внешнего дыхания основной причиной дыхательной недостаточности становятся воспалительные процессы в легких - пневмонии и трахеобронхиты. 3 синдром: основными клиническими симптомами нарушения функций сердечно-сосудистой системы при данной патологии служат явления тахикардии и гипотонии. 4 синдром: заметное место в клинической симптоматике отравлений снотворными занимают трофические расстройства. Они отмечаются в виде буллезного дерматита и некротического дерматомиозита, протекающего по типу быстро развивающихся пролежней, что указывает на местное расстройство кровообращения. Возникновение нарушений функции почек при данной патологии, в основном, связано с развитием острой сердечной недостаточности (коллапсом). Смерть при отравлении барбитуратами наступает от паралича дыхательного и сосудодвигательного центров. При смертельных исходах после отравления барбитуратами картина вскрытия нехарактерна, поэтому химико-токсикологическое исследование внутренних органов (особенно печени и мозга), крови и мочи приобретают особое значение. Данные о сохраняемости барбитуратов в трупном материале разноречивы и составляют от нескольких дней до нескольких лет (до 1-3 лет), что зависит от химического строения барбитурата и условий хранения биоматериала. |

 -замещенные барбитураты (трехзамещенные)
-замещенные барбитураты (трехзамещенные)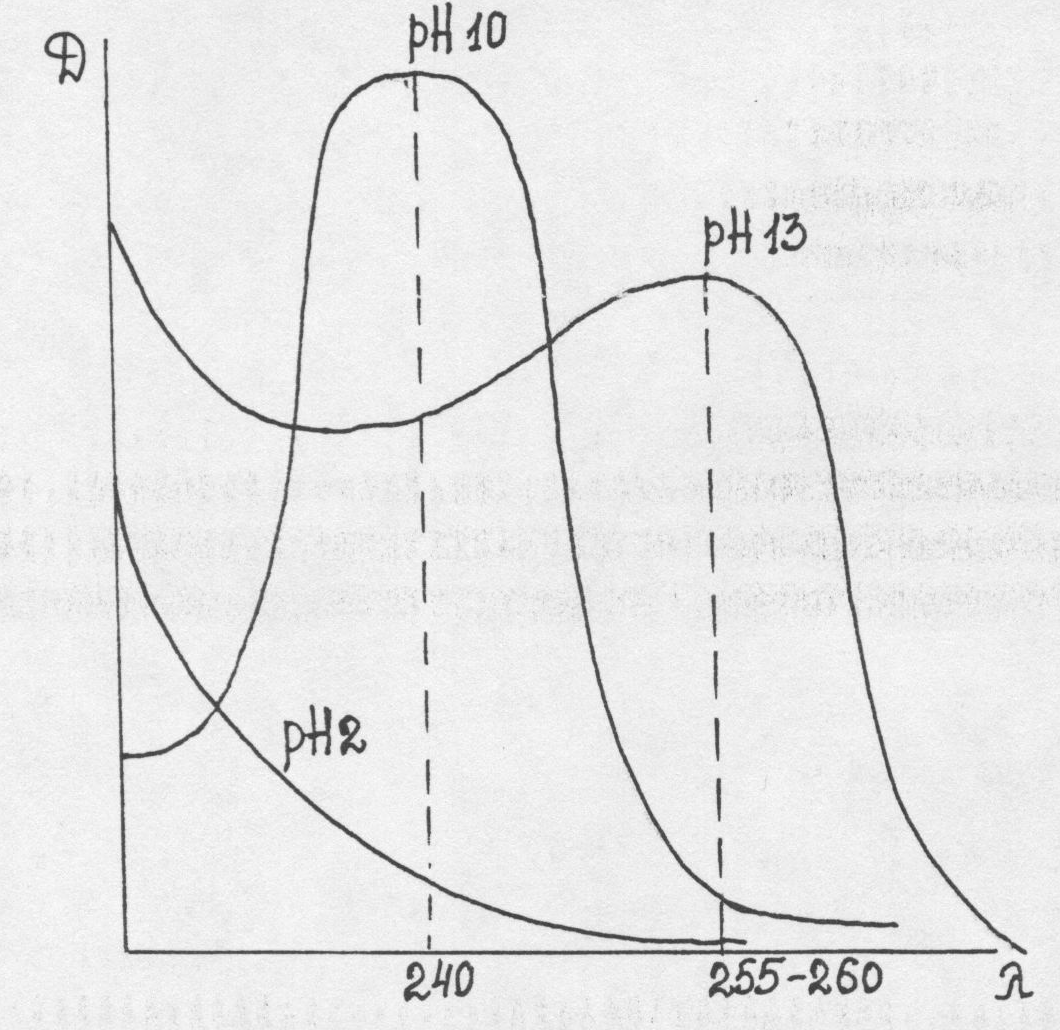
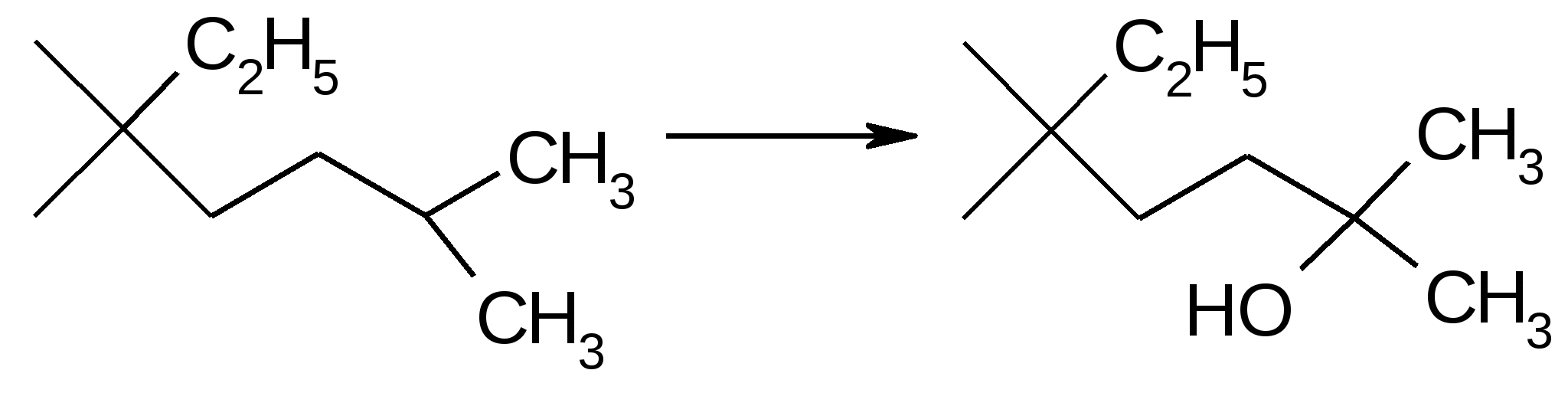
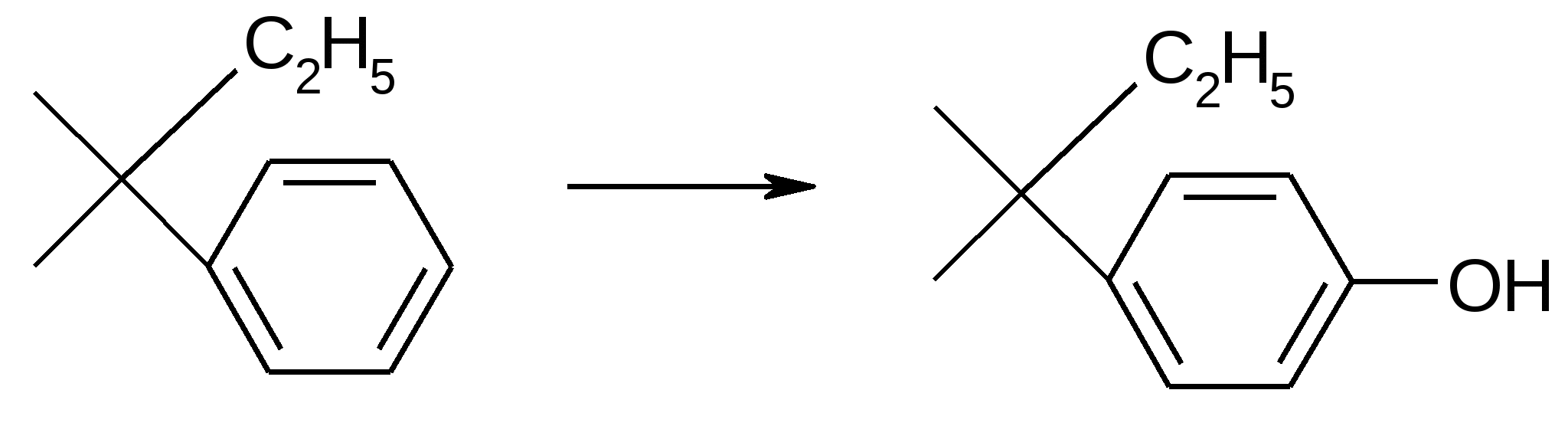 етаболизм. В организме барбитураты могут подвергаться ряду превращений. Выделяются 4 основных типа превращений:
етаболизм. В организме барбитураты могут подвергаться ряду превращений. Выделяются 4 основных типа превращений: