лекции токсикхим. Лекция Предмет, разделы и задачи токсикологической химии. Пищеварение и метаболизм посторонних веществ ядов. Вещества, которые изолируются минерализацией биологического материала (металлические яды)
 Скачать 1.52 Mb. Скачать 1.52 Mb.
|
|
Соединения, которые изолируются из биологического материала перегонкой с водяным паром (летучие яды). Анализ дистиллята химическим методом на синильную кислоту, формальдегид. галогенпроизводные углеводородов, ацетон, метанол, этанол. 1. Для идентификации формальдегида, провизору-аналитику нужно провести реакцию со следующим реактивом: A. Толленса B. Марки C. Хинолином D. Драгендорфа E. Дитизоном 2. При определении достоверности раствора формальдегида 40% с салициловой кислотой, в присутствии H2SO4, провизор-аналитик наблюдает: A. Выделение пузырьков газа B. Красное окрашивание C. Желтое окрашивание D. Характерный запах аммиака E. Выпадение белого осадка 3. Для идентификации альдегидной группы в химической структуре лекарственных препаратов провизору-аналитику следует провести реакцию со следующим реактивом: Драгендорфа Несслера Дениже Швейцера Фолина 4. Для идентификации альдегидной группы в химической структуре лекарственных препаратов провизор-аналитик проводит реакцию, которая сопровождается восстановлением меди (II) до меди (I) с образованием осадка окисла меди (I). С каким реактивом нужно проводить эту реакцию: A. Майера B. Фелинга C. Толленса D. Фолина Е Дениже Эталоны ответов к заданиям: 1-А, 2-В, 3-В, 4-В. 1. Для более полного выделения летучих ядов из биологического материала необходимо провести разрыв связи белок—яд. Для этого используют: A. Настаивание со спиртом B. Минерализацию C. Перегонку с водяным паром D. Диализ E. Экстракция 2. При дистилляции с водяным паром яд начнет перегоняться, когда упругость пара над жидкостью: A. Будет равна или несколько превысит атмосферное давление B. Намного превысит атмосферное давление C. Приблизится к атмосферному давлению D. Будет ниже атмосферного давления
D. Воду дистиллированную E. Пустая колба. 4. При ненаправленном анализе биологического материала на яды, которые изолируются дистилляцией с водяным паром, проводят подкисление объекта. Укажите эту кислоту. A. Винной B. Уксусной C. Серной D. Хлористоводородной E. Фосфорной 5. Состоялось отравление кислотой синильной. При изолировании из биологического материала она попадает: A. В первые порции дистиллята B. Перегоняется в течение всей дистилляции C. Во вторые порции дистиллята D. Во вторые и третьи порции дистиллята E. В последние порции дистиллята 6. После проведения дистилляции с водяным паром первый дистиллят исследуют на наличие кислоты синильной. Образование какого соединения является наиболее доказательным для выявления кислоты синильной? A. Железа (II) роданида B. Полиметинового красителя C. Бензидиновой сини D. Берлинской лазури E. Соли кислоты изопурпурной 7. Необходимо провести исследование второго дистиллята на наличие формальдегида. Какая реакция является специфической для данного яда? A. С раствором резорцина в щелочной среде B. Кислотой сульфитной C. Кодеином в кислоте сульфатной D. Метиленовым фиолетовым E. Возобновление серебра оксида и меди гидроксида 8. При проведении внешнего обзора органов трупа чувствовался запах горького миндаля. На какой яд необходимо выполнить судебно-токсикологическое исследование? A. На фенол B. Ацетон C. Кислоту ацетатную D. Хлороформ E. Кислоту синильную 9. Состоялось отравление формальдегидом. Для какой реакции идентификации формальдегида сине-фиолетовое окрашивание раствора, которое появилось через 30 мин после начала ее проведения, не является доказательством наличия формальдегида в дистилляте? A. С кислотой хромотроповой B. С кодеином в серной среде C. С кислотой фуксинсернистой D. С резорцином в щелочной среде E. С реактивом Фелинга 10. Проведено изолирование ядов дистилляцией с водяным паром. При ненапрявленном анализе вторую и третью порцию дистиллятов собирают: A. В колбу с раствором натрия, гидроксида B. Колбу с водой дистиллирует C. Пустую колбу D. Раствор кислоты хлористоводневої E. Охлажден приемник Эталоны ответов: 1-С, 2-С, 3-В, 4-D, 5-A, 6-В Соединения, которые изолируются из биологического материала перегонкой с водяной паром (летучие яды). Анализ дистиллята химическим методом на синильную кислоту, формальдегид. Методы изолирования веществ из биологического материала Для изолирования «летучих» ядов в химико-токсикологическом анализе существуют такие методы: — перегонка (дистилляция) с водяным паром при атмосферном давлении; — перегонка с водяным паром при уменьшенном давлении; — перегонка с водяным паром при повышенном давлении; — методы микродиффузии; — суховоздушная отгонка; — парофазный метод. В судебно-химических лабораториях изолирования «летучих» ядов из биологического материала чаще всего осуществляют методом перегонки (дистилляции) с водяным паром при атмосферном давлении по методике: 100 граммов биологического материала измельчают, смешивают с дистиллированной водой (Vколби = 1/3 Vсмеси) и помещают в колбу, которую ставят на холодную водяную баню. Потом нагревают парообразователь до появления пара воды, исследуемую смесь подкисляют насыщенным водным раствором щавелевой или винной кислоты к рН = 2—2,5, немедленно соединяют все части (парообразователя, колбу, холодильник и приемник) и только потом нагревают водяную баню. Bcе «летучие» яды делятся по способности смешиваться с водой на: 1. Вещества, которые несмешиваются или плохо смешиваются с водой (бензол, хлороформ), дают после перегонки два четких слоя: вода и вещество, которые легко разделить. 2. Вещества, которые дают с водой смеси, в которых состав пара и жидкости одинаковый (фенол, этанол), — азеотропные смеси. В дистилляте не разделяются. Для разделения азеотропных смесей используют перегонку при снижении или повышении давления (азеотропная смесь этанола с водой — 96 % С2H5OH + 4 % Н20 — перегоняеться при атмосферном давлении при 78 °С. Со снижением давления до 100 мм рт. ст. (« 13,3 кПа) во время дистиляции смесь имеет состав 99,62 % С2H5OH + 4 % Н20 и переганяеться при 34 °С). Если после перегонки с водяным паром состав ядов в дистиллятах малый или в дистилляты попадают вещества, которые образовались в результате гниения биологического материала, то для очищения их поддают фракционной перегонке. При нагревании двукомпонентной смеси, состоящей из практически нерастворимых друг в друге веществ, каждое из них увеличивает упругость своих паров независимо от другого. Когда упругость паров смеси достигает атмосферного давления – жидкость закипает и оба вещества начинают перегоняться с водяным паром. Так как сумма упругостей паров обоих веществ равна атмосферному давлению, температура перегонки каждого вещества в смеси будет ниже температуры кипения каждого компонента в чистом виде ОБЩАЯ СХЕМА АНАЛИЗА ДИСТИЛЛЯТОВ ХИМИЧЕСКИМ МЕТОДОМ АНАЛИЗ ПЕРВОГО ДИСТИЛЛЯТА Анализ начинают с первого дистиллята на наличие синильной кислоты. Синильная кислота Физические свойства— это жидкость без цвета, имеет запах горького миндаля, летучая, температура кипеня — 25,6 °С. Очень слабая кислота Ка = 4,8 • Ю-10, соли ее в воде неустойчивы Токсичное действие. Синильная кислота поражает дыхание, то есть блокирует дыхательный фермент — цитохромоксидазу, при этом кислород от гемоглобина не поступает в ткани. HCN + белок – R – Fe3+ = белок – R – Fe3+ - CN + H+ цитохромоксидаза стойкий комплекс Анализ дистиллята на синильную кислоту начинают с предварительной, высокочувствительной и специфической реакции образования берлинской лазури. Методика проведения перегонки (дистилляции) с водяным паром Исследуемый объект (100 г биологического материала) измельчают, смешивают с водой до получения однородной массы и помещают в колбу. Когда все части прибора соединены, содержимое колбы быстро подкисляют раствором щавелевой кислоты или виннокаменной кислоты до рН = 2. Затем подсоединяют парообразователь и проводят перегонку (дистилляцию) с водяным паром. Объект исследования нельзя подкислять минеральными кислотами, т.к. в случае наличия в исследуемом материале легколетучей циановодородной (HCN) кислоты – она будет выделяться, что может привести к отравлению и смерти. НСN – газ или бесцветная жидкость, температура кипения – 25,6 °С. В воде происходит ее гидролиз: HCN + 2H2O =НCОONH4 Соли циановодородной (синильной) кислоты на воздухе и в растворе реагируют с о диоксидом углерода (СО2) и водой: КCN + СO2 + H2O =КНCО3 + HCN КCN + 2H2O =NН3 + HCООК Обнаружение: 1. Образование берлинской лазури: FeSO4 + 6KCN = K4[Fe(CN)6] + K2SO4 3K4[Fe(CN)6] + 4FeCl3 = Fe4[Fe(CN)6]3 + 12KCl 2. Образование роданида железа: КCN + (NH4)2S2=КSCN + (NH4)2S 3КSCN + FeCl3 + 3H2O =Fe(SCN)3(H2O)3 красное окрашивание 3. Образование бензидиновой сини: Cu(CH3COO)2 + 2HCN = Cu(CN)2 + 2CH3COOH 2Cu(CN)2 = (CN)2 + 2Cu(CN) (CN)2 + H2O = HCN + HCNO HCNO = HCN + O 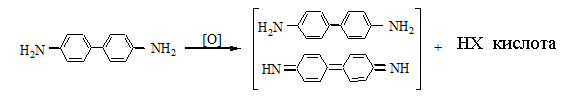 4. Образование соли изопурпурной кислоты по реакции с пикриновой кислотой.  Микрокристаллоскопическая реакция образования цианида серебра Количественное определение: 1. При исследовании свежего трупного материала применяют объемное определение НСN по избытку 0,1 н. раствора AgNO3, избыток которого оттитровывают аммония роданидом – NH4SCN. Индикатором является – железо аммонийные квасцы. 2. При исследовании несвежего трупного материала – весовой метод (описан в учебнике М.Д. Швайковой "Токсикологическая химия"): При исследовании не вполне свежего трупного материала титриметрический метод анализа неприемлем, т.к. Н2S, содержащийся в объекте исследования, будет реагировать с серебра нитратом с образованием сульфида серебра, который будет искажать результаты анализа. В таких случаях обычно применяют гравиметрический (весовой) метод определения цианидов – CN. Весовое (гравиметрическое) определение синильной кислоты сводится к отгонке синильной кислоты из навески объекта исследования, собиранию дистиллятов в 2-3 приемника, содержащие 0,2% раствор серебра нитрата, отделению после подкисления азотной кислотой (не содержащей цианидов – СN) осадка АgСN с возможной примесью Ag2S, обработке полученного осадка избытком раствора аммиака в целях отделения растворимого в нем цианида серебра от нерастворимого сульфида серебра, выделению из раствора с помощью азотной кислоты цианида серебра и определению металлического серебра после высушивания, сжигания и прокаливания фильтра с осадком. Токсикологическое значение Токсикологическое значение НСN объясняется ее сильной ядовитостью; тем, что она связывается с Fe2+ гемоглобина крови и дыхательными ферментами (Fe3+), а также ее широком применении в народном хозяйстве. Соли HCN применяются для получения Au и Ag из руд – цианамидный способ: 4Au + 8KCN + O2 + 2H2O  4K[Au(CN)2] + 4КОН 4K[Au(CN)2] + 4КОНзатем действуют металлическим цинком и получают чистые металлы. Этот метод был предложен в 1843 году Багратионом Петром Романовичем для извлечения золота – Аu из руд методом цианирования. Цианиды применяют в фотографии, в производстве фармацевтических препаратов, в сельском хозяйстве для борьбы с грызунами. В период второй мировой войны фашисты травили людей в газовых камерах ЦИКЛОНОМ (пористый материал, пропитанный HCN). Источником отравления в быту являются ядра горького миндаля, абрикоса, вишни и других плодов семейства розоцветных содержащих гликозид АМИГДАЛИН: 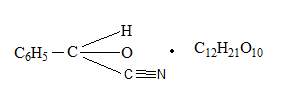 который в кислом растворе расщепляется на виноградный сахар , бензальдегид и HСN. В организме, в тканях трупа, во внешней среде цианиды подвергаются биотрансформации: 1. Гидролиз : НСN + 2Н2О=HCOONH4 2. Превращением в роданиды под влиянием ронидазы (фермент): KCN + S=KSCN 3. Соединяется с гемоглобином крови, образуя циангемоглобин. 4. Связывается с цистеином. 5. Присоединяется к альдегидной группе сахаров: 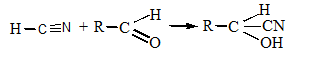 Цианиды на воздухе превращаются в гидрокарбонаты: КСN + СO2 + H2O =KHCO3 + HCN Ввиду всего вышеизложенного химико-токсикологическое определение (идентификация и количественное определение) в биологическом материале проводят в день поступления объектов на анализ. В качестве помощи при отравлении цианидами используют внутривенное введение натрия тиосульфата – Na2S2O3. Синильная кислота (НСN) взаимодействует с дыхательным ферментом, содержащим Fе3+, с которым образует прочное комплексное соединение. В результате тканевое дыхание приостанавливается, несмотря на то, что кровь содержит О2. Смерть наступает в результате паралича дыхания. Антидоты – внутривенно вводят раствор метиленовой сини, дают нюхать амилнитрит (амиловый эфир азотистой кислоты), назначают в виде лекарственных средств – нитриты (в частности натрия нитрит). Обнаружение формальдегида В химико-токсикологическом анализе для обнаружения формальдегида Η—СНО применяют реакции с хромотроповой кислотой, фуксинсернистой кислотой, с раствором кодеина в серной кислоте, с резорцином и др. Реакция с хромотроповой кислотой. Хромотроповая кислота с формальдегидом в присутствии серной кислоты дает фиолетовую окраску. При взаимодействии формальдегида с хромотроповой кислотой концентрированная серная кислота одновременно является водо- отнимающим средством и окислителем. Вначале серная кислота вызывает конденсацию формальдегида с хромотроповой кислотой, а затем окисляет образовавшийся продукт конденсации: 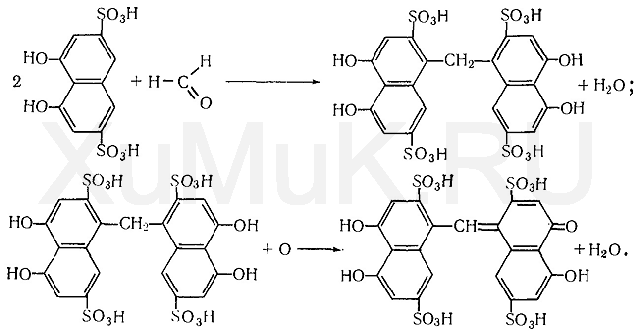 Для успешного протекания указанной выше реакции требуется серная кислота, концентрация которой должна быть не ниже 72 %. Не дают этой реакции альдегиды уксусной, пропионовой и масляной кислот, хлоралгидрат и др. Эту реакцию дают вещества, которые при гидролизе, дегидратации или окислении образуют формальдегид. Реакция с фуксинсернистой кислотой. Фуксинсернистая кислота (реактив Шиффа) с формальдегидом дает синюю или сине-фиолетовую окраску. Для приготовления фуксинсернистой кислоты берут раствор парафуксина (I), имеющий красную окраску, прибавляют водный раствор оксида серы (IV) или пропускают газообразный SO 2. При этом образуется фуксинсернистая кислота(II), не имеющая окраски. Эта кислота с альдегидами образует хиноидный краситель (III) розового цвета: 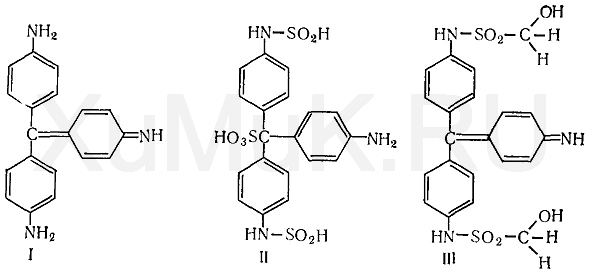 Реакция с кодеином и серной кислотой. При нагревании формальдегида с кодеином в присутствии концентрированной серной кислоты появляется синяя окраска. Эта реакция основана на том, что под влиянием концентрированной серной кислоты от кодеина отщепляется метоксильная группа, в результате чего образуется морфин, содержащий фенольную группу. При взаимодействии морфина с формальдегидом появляется синяя окраска. Реакция с резорцином Альдегиды реагируют с резорцином в его таутомерной форме (кетоформе) с образованием окрашенного соединения:  Реакция восстановления ионов серебра. Из аммиачного раствора солей серебра формальдегид выделяет металлическое серебро Кроме формальдегида эту реакцию дают и некоторые другие восстанавливающие вещества. Реакция с реактивом Фелинга При нагревании реактива Фелинга с формальдегидом выпадает осадок оксида или гидроксида меди. Оксид меди (I) имеет черную окраску. Окраска гидроксида меди (I) зависит от размера частиц. Очень мелкие частицы имеют голубовато-зеленую окраску, а крупные — красную. Поэтому при взаимодействии реактива Фелинга с восстановителями в большинстве случаев выпадает желтый или красный осадок. В реактиве Фелинга, который представляет собой смесь сульфата меди, щелочи и сегнетовой соли, медь входит в состав комплексного иона: 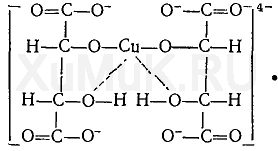 Эта реакция не специфична. Кроме формальдегида ее дают и другие альдегиды алифатического ряда, восстанавливающие сахара и др. Схема анализа дистиллята химическим методом на галогенпроизводные углеводородов Анализ второго дистиллята начинают с исследования ядовитых галогенпроизводных алифатического ряда. |
