лекция. Методы изолирования. Методы очистки и концентрирования вытяжек из биоматериала
 Скачать 90.88 Kb. Скачать 90.88 Kb.
|
МЕТОДЫ ОЧИСТКИ ВЫТЯЖЕК ОТ ПРИМЕСЕЙ И КОНЦЕНТРИРОВАНИЕ ВЫДЕЛЕННЫХ ВЕЩЕСТВДля очистки анализируемых соединений от соэкстрагированных веществ (белки, жиры, пигменты, и др.) существуют разные методы: 1. Фильтрование и центрифугирование. 2. Осаждение белков разными реактивами и способами. 3. Экстракция. 4. Хроматография — на бумаге, колонковая, в тонких слоях сорбента (ТСХ-метод), гелевой хроматографии. 5. Электрофорез. 6. Дистилляция с водяным паром. 7. Сублимация. 8. Диализ. Фильтрование и центрифугирование. Фильтрование позволяет очистить вытяжки от механических загрязнений (мелких частиц биологического материала). Однако при этом возможна адсорбция яда на фильтре и частичная его потеря, а также неполная очистка вытяжки от примесей, ограниченная диаметром пор фильтра. Эти недостатки устраняются центрифугированием. Осаждение белков разными реактивами обусловлено образованием малорастворимых в воде комплексов (фосфорно-вольфрамовая, фосфорно-молибденовая, вольфрамовая, трихлоруксусная, метафосфорная кислоты) или коагуляцией белков (этанол, ацетон). Для осаждения есть разные способы: нагревание, высаливание, изменение рН среды. При повышении температуры свыше 40 °С происходит денатурация белков, снижается их растворимость. Эффективность высаливания как метода очистки вытяжки, зависит от концентрации и природы электролитов. При низких концентрациях электролитов (NaCl, Na2SO4, (NH4)2SO4) повышается растворимость белков, которая объясняется изменением степени диссоциации ионизированных (— СООН; — ОН; — SH) групп белков. Повышение концентрации солей (насыщенные растворы) приводит к перераспределению молекул воды в гидратных оболочках белков и введенных ионов Na+ ; CI- ; SO2-; NH4+, что снижает растворимость белков. Осаждение белков из вытяжек возможно при изменении рН среды к значению, которое будет отвечать изоэлектрической точке белка, в которой белок не несет суммарный заряд. Результатом достижения отмеченного рН раствора является отсутствие электростатического отталкивания молекул белков, которое способствует образованию осадка. Недостатком методов очистки вытяжек при осаждении белков является способность осадков примесей адсорбировать на своей поверхности анализируемые яды, что может быть одной из причин их потерь в ходе исследования. Экстракционный метод очистки. В основе его лежит закон распределения веществ между растворителями, которые не смешиваются, а также их способность растворяться в органических растворителях, а солей, образованных ими, - в воде. Метод простой, доступный и эффективный. Схема экстракционной очистки ядов основного характера кодеин – основание 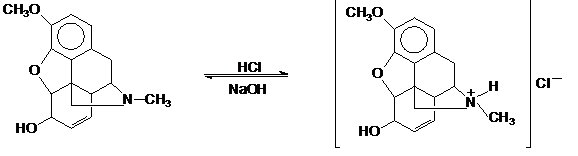
Для экстракции примесей из вытяжек необходимо установление соответствующего значения рН среды и применения соответствующего растворителя. При неправильном выборе этих факторов вместе с примесями могут экстрагироваться и анализируемые яды. Схема экстракционной очистки ядов кислого характера 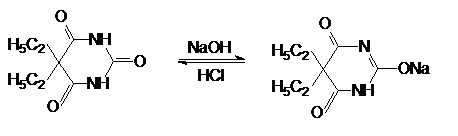
Хроматография. В основе ТСХ-метода лежит распределение нанесенного на твердую подкладку яда междужидкой и твердой фазами. Выбирают системы, в которых примеси остаются на старте или же двигаются вместе с фронтом растворителя. Метод простой, доступный, позволяет не только очистить яды от примесей, но и одновременно выполнить их определение. Для очистки экстрактов, полученных из объектов, которые испытывают гнилостные изменения, эффективное сочетание экстракционного метода с методом тонкослойной хроматографии. Очистка экстрактов с помощью гель-хроматографии базируется на разном поведении молекул относительно пор геля: малые молекулы ядов проникают в поры и задерживаются в них, большие молекулы примесей обходят поры или удерживаются на поверхности геля. Метод гелевой хроматографии пригоден для очистки водных вытяжек. Он трудоемкий, но эффективный. Электрофорез на бумаге. В основе лежит распределение веществ на бумаге, помещенной в электролит, под действием электрического тока. Ионы исследуемой смеси двигаются к електроду противоположного знака. По своей эффективности этот метод приближается к ТСХ-методу, но требует специального оборудования. Дистилляция с водяным паром и метод сублимации основаны на летучести отдельных представителей исследуемой группы ядов (алкалоиды — производные пиридина и пиперидина, барбитураты). Этот метод простой, но его использование рационально при анализе только больших количеств ядов, что случается при проведении химико-токсикологических исследований очень редко. Метод диализа основан на применении полупроницаемых мембран, через поры которых способны проходить ионы, небольшие молекулы органических веществ, в то время как большие молекулы (белки, пептиды и др.) остаются по другой бок мембран. Метод имеет ограниченное для очистки веществ исследуемой группы ядов применение, потому что он долговременный, возможны также значительные потери анализированных соединений. Для проведения анализа экстракты необходимо сконцентрировать (работать с большими объемами неудобно). Существуют разные методы концентрирования экстрактов: — экстракционный; — выпаривание на бумаге при 40 °С; — выпаривание под вакуумом; — адсорбция ядов твердым сорбентом с последующей десорбцией. Выбор метода очистки зависит от состояния объекта и метода изолирования анализированного яда из биологического материала. В состав методов изолирования входят отдельные этапы очистки, но они не могут обеспечить полное удаление примесей. Изолирование и очистка «лекарственных» ядов
Поэтому после изолирования ядов полярными растворителями для очистки вытяжек прибегают к вышеуказанным методам, чаще всего выполняют экстракционную очистку и тонкослойную хроматографию или применяют сразу оба метода. |
