фуыпквярпрол. Методические указания по выполнению контрольной работы предназначены для студентов очной и заочной форм обучения по направлениям подготовки
 Скачать 1.06 Mb. Скачать 1.06 Mb.
|
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКАОсновные понятия и определения термодинамики. Смеси идеальных газов. Основные задачи курса. Предмет и метод технической термодинамики. Энергия, виды энергии и ее свойства. Теплота и работа как формы передачи энергии, Рабочее тело, Параметры определяющие состояние рабочего тела. Термодинамическая система. Тепловое состояние. Равновесные и неравновесные состояния. Термодинамический процесс. Уравнение состояния идеальных газов. Состав смеси в массовых, объемных и молярных долях, соотношение между массовыми и объемными долями. Плотность смеси. Газовая постоянная смеси. Теплоемкость. Первый закон термодинамики. Массовая, объемная и молярная теплоемкости газа и зависимости между ними. Средняя и истинная теплоемкости газа. Теплоемкость при постоянном объеме и при постоянном давлении. Формулы и таблицы для определения теплоемкости газов. Теплоемкости смеси газов. Содержание закона и его формулировки. Аналитическое выражение первого закона термодинамики. Принцип эквивалентности теплоты и работы. Внутренняя энергия и ее свойства. Энтальпия газа. Работа газа, ее определение и графическое изображение в координатах pv. Второй закон термодинамики. Термодинамическая вероятность, необратимость и статистика. Термодинамическая вероятность и энтропия. Энтропия и теплообмен. Энтропия газов. Содержание второго закона и его формулировки. Аналитическое выражение второго закона. Основное уравнение термодинамики и вычисление энтропии. Диаграммы состояния T – s и h – s. Исследование термодинамических процессов. Изохорный, изобарный, изотермический и адиабатный процессы – частные случаи политропного процесса. Их изображение в координатах pv и Ts. Политропный процесс. Уравнение политропы, Определение показателя политропы. Соотношения параметров. Определение работы, теплоемкости и теплоты во всех процессах. Круговые процессы. Общие сведения, термический КПД и холодильный коэффициент циклов. Цикл Карно. Эксергия. Циклы поршневых компрессоров. Циклы теплосиловых установок. Термодинамическая эффективность циклов теплосиловых установок. Циклы поршневых двигателей внутреннего сгорания . Цикл газотурбинной установки . Циклы паротурбинных установок. Парогазовые циклы Водяной пар. Влажный воздух. Процесс парообразования в pv, Ts, hs координатах. Параметры и функции состояния жидкости и пара. Диаграммы состояния водяного пара. Термодинамические процессы водяного пара. Термодинамические таблицы водяного пара. Термодинамика потока газов и паров. Уравнение первого закона термодинамики для потока. Истечение газов и паров. Дросселирование. Вопросы для самостоятельной подготовки Что такое термодинамическая система, термодинамический процесс? Термические параметры состояния. Уравнения состояния для идеальных газов. Что такое работа, теплота. Понятие о внутренней энергии. Изображение работы и тепла в диаграммах P-V и T-S. Математическое выражение первого закона термодинамики для идеальных реальных газов. Теплоемкость. Различные виды теплоемкости и связь между ними. Физическая сущность энтальпии. Зависимость энтропии от основных термодинамических параметров. Исследование изохорного процесса, изобразить в диаграммах P-V и T-S. Исследование изобарического процесса, изобразить в диаграммах P-V и T-S. Исследование изотермического процесса, изобразить в диаграммах P-V и T-S. Исследование адиабатного процесса, изобразить в диаграммах P-V и T- S. Исследование политропного процесса, изобразить в диаграммах P-V и T-S. Сущность второго закона термодинамики и основные его формулировки. Цикл Карно, вывод формулы КПД цикла. Тесты для самостоятельной подготовки Если условно в объеме, который занимает смесь газов, оставить только один компонент, не изменяя температуры, то давление оставленного компонента будет равно: o Абсолютному давлению. o Парциальному давлению. Избыточному давлению Величина µR в уравнении состояния идеального газа носит название: Газовой постоянной. Универсальной газовой постоянной. Постоянной Больцмана. Укажите формулу связи теплоемкостей cv и cp для идеального газа (формулу Майера). сp = сv. o сp - сv = R. сp/ сv = k. Определить массовую теплоемкость ср, если: µср=32,8 кДж/(кмоль∙К); µ=27,8. o 1,18 o 1,26 o 1,46 o 1,09 При увеличении энтропии (S2 > S1): o Теплота не подводится и не отводится. Теплота отводится. o Теплота подводится. Укажите аналитическое выражение второго закона термодинамики. ds ≥ δq/T. δq = du + pdv. o δq = dh – vdp. Для изотермического процесса: o показатель политропы равен 1 o показатель политропы равен 0 o показатель политропы равен k показатель политропы равен ± ∞ Указать формулу изменения энтропии в изохорном процессе. сpln(T2/T1) o сvln(T2/T1) o сvln(T2/T1)+ Rln(v2/v1) o Rln(v2/v1) Цикл с подводом теплоты при постоянном объеме: o реализуется в дизелях o реализуется в дизелях и бензиновых двигателях o реализуется только в бензиновых двигателях реализуется в бензиновых и газовых двигателях К газу в круговом процессе подведено 250 кДж/кг теплоты. Термический КПД равен 0,5. Найти работу, полученную в цикле. o 125 кДж/кг. o 500 кДж/кг. o 250 кДж/кг. Пар, вода и лед одновременно находятся в равновесии в _______точке. тройной критической o кюри o росы П 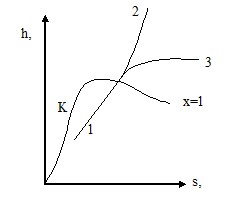 роцесс 1-3, показанный на h-s диаграмме: Изохорный роцесс 1-3, показанный на h-s диаграмме: Изохорный Изобарный Изотермический Укажите температуру начала выпадения влаги из влажного воздуха. При температуре мокрого термометра. o При температуре выше температуры точки росы. При температуре точки росы. Отношение массы водяного пара mп, содержащегося во влажном воздухе, к массе сухого воздуха mв называется… o влагосодержанием относительной влажностью o абсолютной влажностью o точкой росы Типовые задачи для самостоятельной подготовки Ртутный вакуумметр, присоединенный к сосуду (см. рис. 2), показывает разрежение р = 56 кПа (420 мм рт. ст.) при температуре ртути в вакуумметре t = 200С. Давление атмосферы по ртутному барометру В = 102,4 кПа (768 мм рт. ст.) при температуре ртути t = 180С.Определить абсолютное давление в сосуде. Определить абсолютное давление в конденсаторе парвой турбины, если показание присоединенного к нему ртутного вакуумметра равно 94 кПа (705 мм рт. ст.), а показание ртутного барометра, приведенное к 00С, В0 = 99,6 кПа (747 мм рт. ст.). Температура воздуха в месте установки прибором t = 200С. Определить массу кислорода, содержащегося в баллоне емкостью 60 л, если давление кислорода по манометру равно 1,08 МПа, а показание ртутного барометра – 99 325 Па при температуре 25 0С. Резервуар объемом 4 м3 заполнен углекислым газом. Найти массу и силу тяжести (вес) газа в резервуаре, если избыточное давление газа р = 40 кПа, температура его t = 80 0С, а барометрическое давление воздуха В = 102,4 кПа. Определить среднюю массовую теплоемкость при постоянном объеме для азота в пределах 200 – 800 0С, считая зависимость теплоемкости от температуры нелинейной. Вычислить значение истинной мольной теплоемкости кислорода при постоянном давлении для температуры 1000 0С, считая зависимость теплоемкости от температуры линейной. Найти относительную ошибку по сравнению с табличными данными. Мощность турбогенератора 12 000 кВт, к. п. д. генератора 0,97. Какое количество воздуха нужно пропустить через генератор для его охлаждения, если конечная температура воздуха не должна превышать 550 С? Температура в машинном отделении равна 20° С; среднюю теплоемкость воздуха сртпринять равной 1,0 кДж/(кг·К). В котельной электрической станции за 20 ч работы сожжены 62 т каменного угля, имеющего теплоту сгорания 28 900 кДж/кг. Определить среднюю мощность станции, если в электрическую энергию превращено 18% теплоты, полученной при сгорании угля. Какое количество теплоты необходимо затратить, чтобы нагреть 2 м3 воздуха при постоянном избыточном давлении р = 0,2 МПа от t1 = 100° С до t2 = 500° С? Какую работу при этом совершит воздух? Давление атмосферы принять равным 101 325 Па. Определить количество теплоты, необходимое для нагревания 2000 м3 воздуха при постоянном давлении р = 0,5 МПа от t1 = 150° С до t2 = 600° С. Зависимость теплоемкости от температуры считать нелинейной. Найти давление, удельный объем и плотность воды, если она находиться в состоянии кипения и температура ее равна 250 ° С. Найти диаметр паропровода. по каторому протекает пар пр давлении р = 1,2 МПа и температуре t=260 ° С. Расход пара 350 кг/ч, скорость пара ω=50 м/с. Найти массу, внутреннюю энергию, энтальпию и энтропию 6 м3 насыщеного водяного пара при давлении р =1,2 МПа т сухости пара х = 0,9 Задано состояние пара: р= 2 МПа; t = 340 ° С. Определить, пользуясь диаграммой is значения s, tн и перегрев пара |
