Методическое пособие по педиатрии ббк. Методическое пособие по педиатрии включает в себя материал, соответствующий требованиям Программы для студентов по Педиатрии
 Скачать 5.78 Mb. Скачать 5.78 Mb.
|
|
Глава IX. Неинфекционные заболевания системы дыхания РЕСПИРАТОРНЫЙ ДИСТРЕСС-СИНДРОМ НОВОРОЖДЕННЫХ (РДСН) – тяжелое расстройство дыхания у недоношенных новорожденных, обусловленное незрелостью и первичным дефицитом сурфактанта. Синонимы: болезнь гиалиновых мембран, респираторный дистресс-синдром. Эпидемиология. РДСН – наиболее частая причина возникновения дыхательной недостаточности в раннем неонатальном периоде. РДСН выявляется тем чаще, чем меньше гестационный возраст и масса тела ребенка при рождении. У детей, родившихся ранее 30 недель гестации и не получавших пренатальной профилактики бетаметазоном или дексаметазоном, его частота составляет около 65%, при проведении профилактики – 35%; у детей, родившихся при сроке гестации 30-34 недели, без профилактики - 25%, при проведении профилактики – 10%; у детей, родившихся при сроке гестации больше 34 недель, частота развития РДСН не зависит от пренатальной профилактики и составляет менее 5%. Предрасполагающие факторы развития РДСН: - недоношенность; - кесарево сечение до начала родовой деятельности; - тяжелая перинатальная асфиксия; - сахарный диабет у матери (при невынашивании в 4-6 раз чаще, чем у детей аналогичного гестационного возрасте от матерей без диабета); - преждевременная отслойка плаценты; - мужской пол (у мальчиков СДР встречается в 2 раза чаще, чем у девочек); - второй ребенок из двойни; - тяжелая форма гемолитической болезни плода и новорожденного; - гипотермия; - развитие РДСН у родных братьев и сестер (в анамнезе). К факторам, уменьшающим риск развития РДСН, относятся: гипертензионные состояния беременных, серповидно-клеточная анемия у матери, наркотическая зависимость матери, задержка внутриутробного развития и длительный (более 24 часов) безводный промежуток. Существенно снижает риск развития РДСН назначение беременной женщине глюкокортикоидов за 2-7 суток до предполагаемых родов (в период с 23-й по 35-ю неделю гестации). Этиология. Наиболее частыми причинами дыхательных расстройств у новорождённых являются:
Основными причинами развития РДСН являются: 1) нарушение синтеза и экскреции сурфактанта альвеолоцитами II типа, связанное с незрелостью легочной ткани; 2) врожденный дефект структуры сурфактанта; 3) повышенное разрушение сурфактанта на фоне тяжелой перинатальной гипоксии. Сурфактант – группа поверхностно-активных веществ липопротеидной природы, препятствующих спадению альвеол на выдохе, способствующих мукоцилиарному клиренсу и участвующих в регуляции микроциркуляции в легких и проницаемости стенок альвеол. Особенно интенсивный выброс сурфактанта на поверхность альвеол происходит в момент родов, что способствует первичному расправлению легких. Патогенез Дефицит сурфактанта приводит к спадению альвеол, формированию ателектазов. Вследствие этого уменьшается функциональная остаточная емкость, дыхательный объем и жизненная емкость легких, возрастает мертвое анатомическое пространство, а также отношение объема мертвого анатомического пространства к легочному объему. Как следствие, увеличивается работа дыхания, возникает внутриклеточное шунтирование крови, нарастает гиповентиляция легких. На этом фоне повышается проницаемость альвеолярно-капиллярных мембран, отмечается застой крови в капиллярах, диффузный интерстициальный отек и растяжение лимфатических сосудов. Ранними биохимическими последствиями РДСН, связанного с дефицитом сурфактанта, являются: гипоксемия, гиперкапния, респираторно-метаболический ацидоз. На фоне прогрессирующей дыхательной недостаточности с высокой частотой развиваются нарушение функции сердечно-сосудистой системы: вторичная легочная гипертензия с праволевым шунтом крови через функционирующие фетальные коммуникации; транзиторная дисфункция миокарда желудочков; системная гипотензия и нарушение микроциркуляции крови.       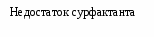               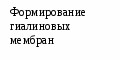 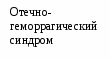        Рис. 2.5. Схема патогенез РДСН Исследования. Общий анализ крови и мочи, гематокрит, определение концентрации РаО2 РаСО2 в артериальной крови, показатели КОС, определение в крови уровней: общего белка, глюкозы, калия, натрия, кальция, мочевины, креатинина, магния, билирубина; показатели коагулограммы, рентгенография органов грудной клетки, ЭКГ, ЭхоКГ, НСГ. Клиника Признаками РДСН являются: - одышка (более 60 дыханий в минуту), возникающая в первые минуты (часы) жизни; - экспираторные шумы («хрюкающий выдох»), обусловленные развитием компенсаторного спазма голосовой щели на выдохе для увеличения функциональной остаточной емкости легких, препятствующей спадению альвеол; - западение грудной клетки на вдохе (втягивание мечевидного отростка грудины, подложечной области, межреберий, надключичных ямок) с одновременным возникновением напряжения крыльев носа, не уменьшающего после оксигенотерапии, раздувание щек (дыхание «трубача»). - цианоз, раздувание щек, пена изо рта. Дыхательная недостаточность в большинстве случаев прогрессирует в течение первых 24-28 часов; в возрасте 3-4 суток, как правило, отмечается стабилизация состоянии. В большинстве случаев РДСН разрешается на 5-7-е сутки жизни. У детей с РДСН отмечается склонность к снижению температуры тела. Со стороны ЦНС появляются признаки угнетения, мышечная гипотония. Часто выявляются периферические отеки. Артериальное давление и диурез нередко снижается. Со стороны кишечника возможны появления симптомов пареза. Классическая клиническая картина РДСН описана преимущественно у детей с гестационным возрастом >30 нед, и характеризуется стадийностью развития клинических и рентгенологических симптомов, появлявшихся через 2–8 ч после рождения: постепенное нарастание одышки, раздувание крыльев носа, щек (дыхание «трубача»), появление звучного выдоха, западение грудины, цианоз, угнетение функционального состояния ЦНС. Аускультативно в легких выслушивается ослабленное дыхание и крепитирующие хрипы. Респираторные расстройства сопровождаются артериальной гипотензией, гипотермией, цианозом и бледностью кожи, ригидностью грудной клетки. При тяжелом РДСН, как правило, наблюдаются признаки сердечно-сосудистой недостаточности, чаще левожелудочковой. Нередко возникает гиповолемия. При необратимых изменениях в легких могут развиться и нарастать отеки, олигурия. Клинические проявления РДС у недоношенных детей с массой тела <1500 г и гестационным возрастом <32 нед имеют свои особенности: симптомы дыхательной недостаточности развиваются медленнее, отмечают очередность появления признаков. Вначале появляется разлитой цианоз на багровом фоне, затем вздутие грудной клетки в передне-верхних отделах, позже – втяжение нижних межреберий и западение грудины. Нарушение ритма дыхания чаще всего проявляется в виде приступов апноэ, нередко наблюдается судорожное и парадоксальное дыхание. Для детей с экстремально низкой массой тела (< 1000 г) такие признаки, как раздувание крыльев носа, звучный выдох, дыхание «трубача», выраженная одышка, нехарактерны. Несмотря на вздутие грудной клетки, перкуторный тон чаще всего укорочен. При аускультации дыхание резко ослаблено, на высоте вдоха с первых часов жизни можно выслушать крепитирующие хрипы. Характерной особенностью РДСН у детей с ЭНМТ является формирование таких осложнений как синдром «утечки воздуха», легочные кровотечения, ФАП. Диагноз Пренатальная диагностика (прогнозирование) проводится на основе исследования липидного состава околоплодных вод, позволяющего судить о степени зрелости легких плода. Наиболее информативны представленные ниже показатели: - Показатель отношения содержания лецитина и сфиногомиелина (в норме он больше 2). Если показатель меньше 1, то вероятность РДСН около 75%. Вместе с тем у новорожденных от матерей с сахарным диабетом РДСН может развиться при показателе больше 2; - Концентрация насыщенного фосфатидилхолина (в норме – более 5 мкмоль/л) или фосфатидилглицерина (в норме – более 3 мкмоль/л). Отсутствие или резкое снижение концентрации насыщенного фосфатидилхолина или фосфатидилглицерина в амниотической жидкости свидетельствует о высокой вероятности развития РДСН; - Дополнительной информативностью обладает «пенный» экспресс-тест Клементса на зрелость сурфактантной системы легких. Путем амниоцентеза получают 3-5 мл амниотической жидкости, помещают ее в пробирку и добавляют 1 мл 95%-ного этилового спирта. Пробирку встряхивают дважды в течение 15с с перерывом в 5 минут, оставляя ее в вертикальном положении. Признаком достаточной зрелости системы синтеза сурфактанта считается наличие пузырьков, покрывающих всю поверхность жидкости; сомнительным результатом – наличие пузырьков по окружности пробирки, отрицательным (наличие РДСН) - отсутствие пузырьков. Диагноз в родильном зале (определение степени риска РДСН) основана на клинической оценке соответствия морфофункциональной зрелости организма ребенка гестационному возрасту и на анализе анамнестических и акушерских факторов риска. В некоторых случаях в родильном зале проводят модифицированный тест Клементса, в котором вместо амниотических вод используется желудочный аспират, полученный у новорожденного в первые 5 минут жизни. Постнатальная диагностика основывается на анализе динамики РДСН у новорожденного ребенка в первые часы (сутки) в жизни и данных рентгенологического исследования легких. Помимо симптомов РДСН в острой фазе заболевания типичным является угнетение нервно-рефлекторной деятельности, развитие признаков застойной сердечной недостаточности в большом круге кровообращения и олигурии. В тяжелых случаях отмечаются: развитие центрального цианоза, приступов апноэ, ригидного сердечного ритма, выделение пены изо рта (при легочном кровотечении, связанном с гемодинамически значимым открытым артериальным протоком; пена розового цвета), отек мягких тканей головы и шеи, кистей и стоп. Одним из наиболее простых и удобных способов клинической оценки тяжести РДСН является модифицированная шкала Даунс (Downes) (табл. 2.44) для доношенных и шкала Сильвермана для недоношенных (табл. 2.45). Клиническая оценка тяжести дыхательных нарушений по Даунс (Downes) и Сильверман (Silverman), широко используемая до последнего времени в нашей стране, имеет не столько диагностическое, сколько прогностическое значение. Так как современная терапевтическая тактика при РДСН направлена на предупреждение развития тяжелых дыхательных расстройств, она не имеет прямой зависимости от клинической оценки тяжести дыхательных нарушений. Крайняя степень дыхательных расстройств в настоящее время должна рассматриваться как показатель неэффективности предшествующей сурфактантной и респираторной терапии. Табл. 2.45.Оценка тяжести РДС (модифицированная шкала Downes)
Оценка в 2–3 балла соответствует легкой тяжести РДСН, в 4–6 баллов – средней тяжести РДСН, более 6 баллов – тяжелому РДСН. Табл. 2.46. Шкала Сильвермана для оценки тяжести СДР у недоношенных детей
Лабораторные исследования КОС - (гипоксемия и смешанный ацидоз). По рентгенологическим признакам выделяют четыре степени тяжести РДСН: I – умеренное снижение пневматизации легких, различимы воздушные бронхограммы, границы сердца четкие; II – снижение пневматизации легких, воздушные бронхограммы, границы сердца на рентгенограмме еще различимы; III – выраженное снижение пневматизации легких, воздушные бронхограммы, границы сердца практически не различимы, стерты; IV – резкое снижение пневматизации легких, воздушные бронхограммы, границы сердца неразличимы, «белые легкие». Дифференциальный диагноз РДСН проводят с сепсисом, пневмонией, транзиторным тахипноэ новорожденных, синдромом аспирации меконием, внутричерепными родовыми травмами. Табл. 2.47. Дифференциальный диагноз РДСН
Лечение, задачи лечения: восстановление адекватной оксигенизации, ликвидация дефицита сурфактанта, поддержание проходимости дыхательных путей, обеспечение температурной защиты, коррекция КОС, ликвидация проявлений полиорганной недостаточности и электролитных нарушений. Схема лечения. Обязательное лечение: температурная защита, оксигенотерапия, ликвидация дефицита сурфактанта, ликвидация гиповолемии. Вспомогательное лечение: закрытие открытого артериального протока, антибиотикотерапия, витаминотерапия, борьба с анемией, гипотонией, инфузионная терапия и питание. Режим. Ребенок с РДСН должен находиться в кувезе (ОРС) с постоянным контролем температуры тела. Диета. Детей с РДСН в первые сутки энтерально не кормят. Кормление (грудное молоко, адаптированные смеси для недоношенных) начинают при уменьшении одышки менее 60 в минуту, отсутствии апноэ, срыгиваний. Вид кормления определяют исходя из срока гестации, способности удерживать питание, наличия сосательного и глотательного рефлексов. Принципы респираторной терапии включают: восстановление проходимости дыхательных путей; обеспечение адекватной оксигенации; обеспечение адекватной вентиляции; заместительную терапию экзогенными сурфактантами. Выбор метода дыхательной терапии зависит от степени выраженности дыхательных расстройств, массы тела при рождении и преморбидного фона. Применяются оксигенотерапия в кислородной палатке, неинвазивный СРАР (постоянное положительное давление в дыхательных путях), традиционная ИВЛ (управляемая, вспомогательная, респираторная поддержка), высокочастотная осцилляторная ИВЛ (ВЧО ИВЛ). Оксигенотерапия в кислородной палатке показана при легкой форме СДР. Показания к профилактическому или раннему (в течение первых 30 мин жизни) применению СРАР: всем новорожденным гестационного возраста 32 нед и менее при наличии у них самостоятельного дыхания. При отсутствии у недоношенного самостоятельного дыхания рекомендуется проведение масочной ИВЛ; после восстановления самостоятельного дыхания начинают СРАР. Терапевтическое использование СРАР показано во всех случаях, когда у ребенка развиваются первые признаки дыхательных расстройств и нарастает зависимость от кислорода. Создание постоянного повышенного давления (ППД) в дыхательных путях ребенка РДСН способствует улучшению оксигенации благодаря увеличению функциональной остаточной емкости легких за счет восстановления дыхательной способности спавших альвеол. Показания для перевода на ИВЛ детей c РДСН: чрезмерная работа дыхания (втяжения уступчивых мест грудной клетки, тахипноэ), даже при отсутствии гипоксемии и гиперкапнии; частые (более 4 в час) или повторяющиеся глубокие (необходимость в масочной ИВЛ) приступы апноэ на фоне CPAP, не поддающиеся лечению метилксантинами; острая сердечно-сосудистая недостаточность (стойкая гипотензия, шок); генерализованные судороги; респираторный или смешанный ацидоз (PaСO2 > 55 мм рт. ст. и рН < 7,25); рефрактерная гипоксемия (PaO2 < 40–50 мм рт. ст. (SpO2 < 86–88%), при СРАР +6 см вод. ст. и FiO2 > 0,4). Показания к ВЧО ИВЛ: неэффективность традиционной ИВЛ; тяжелые формы синдрома утечки воздуха из легких (пневмоторакс, интерстициальная легочная эмфизема). Для успешной экстубации у маловесных пациентов рекомендуется использовать метилксантины с целью стимуляции регулярного дыхания и предотвращения апноэ. Используются: - кофеин-бензоат натрия из расчета 20 мг/кг – нагрузочная доза и 5 мг/кг – поддерживающая; - эуфиллин 6-8 мг/кг – нагрузочная доза и 1,5-2 мг/кг – поддерживающая через 8-12 часов. Сурфактант. Заместительная терапия сурфактантом значительно улучшает оксигенацию и повышает податливость легких при проведении ИВЛ, тем самым улучшает течение и прогноз РДСН. Обязательным условием для применения сурфактанта является интубация, удаление мокроты. В России зарегистрированы 4 препарата сурфактанта: сурфактант HL, и BL, Куросурф и экзосурф неонатал. Коррекция КОС следует проводить при наличии патологического ацидоза (рН менее 7,25 и ВЕ более минус 10 ммоль/л), обязательно на фоне ИВЛ. Антибактериальная терапия при РДСН обязательна, препараты I ряда - ампициллин и гентамицин, в дальнейшем подбор антибиотиков осуществляют по результатам посевов мокроты и крови. Инфузионная терапия – 5-10% глюкоза из расчета 60-80 мл/кг в сутки - на начальном этапе. При тяжелом РДСН проводят парентеральное питание. По мере стабилизации состояния, после пробного введения воды через зонд подключают энтеральное питание грудным молоком или смесями, что уменьшает риск возникновения некротизирующего энтероколита. Течение РДСН имеет некоторые закономерности. Степень тяжести состояния обычно нарастает в первые дни жизни. В дальнейшем (по мере исчезновения гиалиновых мембран) состояние детей постепенно улучшается. Осложнения. В значительном проценте случаев течение РДСН сопровождается развитием осложнений: пневмония, ВЖК, перивентрикулярная лейкомаляция, синдром «утечки воздуха», декомпенсированный ДВС-синдром, некротический энтероколит, электролитные нарушения, бронхолегочная дисплазия, ретинопатия недоношенных. Исходы. Случаи смерти при РДСН связаны с острым нарушением центральной гемодинамики или механической травмой лёгких в результате неадекватной ИВЛ. У 5-15% глубоконедоношенных детей с СДР может развиться хроническое заболевание лёгких – бронхолегочная дисплазия, у 10-70% неврологические нарушения. У детей после РДСН возможно развитие пневмонии. Прогноз при РДСН зависит от степени недоношенности, тяжести заболевания, характера и степени поражения внутренних органов и систем. При своевременном начале и высоком качестве интенсивной терапии прогноз благоприятный. СИНДРОМ АСПИРАЦИИ МЕКОНИЯ (САМ) САМ – дыхательное расстройство, обусловленное попаданием мекония вместе с околоплодными водами в дыхательные пути ребенка до родов или в момент рождения. Меконий встречается в околоплодных водах в 2-10% случаев, однако САМ выявляется в 5-10 раз реже. Он наблюдается преимущественно у переношенных (44%) или доношенных (5-10%) новорожденных, подвергшихся длительной внутриутробной или острой интранатальной гипоксии. Этиология и патогенез. При наличии гипоксии развивается спазм сосудов брыжейки, усиление перистальтики кишечника, расслабление анального сфинктера и выход мекония в околоплодные воды. Это возможно даже при отсутствии асфиксии – при обвитии пуповины вокруг шеи, сдавлении ее, что стимулирует вагусную реакцию и выход мекония. При внутриутробно САМ развиваются четыре основные эффекта: обструкция дыхательных путей, снижение активности сурфактанта, спазм легочных сосудов и воспаление, развивающееся в первые 48 ч жизни. Обструкция глубоких дыхательных путей приводит к формированию «воздушных ловушек», ателектазов. Ателектазы обусловлены как закупоркой бронхов, так и инактивацией сурфактанта, что приводит к спадению альвеол на выдохе. Результаты последних исследований выявили высокое содержание в крови новорожденных с САМ иммунореактивного эндотелина-1, который обладает выраженным сосудосуживающим эффектом, что способствует развитию легочной гипертензии и гиперактивности легочных сосудов. Аспирированный меконий вызывает воспалительную реакцию в трахее, бронхах, легочной паренхиме за счет содержащихся в нем солей желчных кислот, протеолитических ферментов и его повышенной осмолярности. Химическое повреждение бронхиального и альвеолярного эпителия создает предпосылки для развития бактериальной флоры, превращения асептических трахеобрнохита и пневмонии в инфекционный процесс. Помимо химического воспаления и ателектазов в легких возникает отек, перифокальная эмфизема с развитием легочной гипертензии, синдрома «утечки воздуха» (интерстициальная эмфизема, пневмоторакс, пневмомедиастинум, пневмоперикард). Летальность при САМ составляет по данным разных авторов от 4 до 19% и зависит от качества оказания первичной реанимационной помощи в родзале и уровня интенсивной терапии в первые 48 ч жизни.           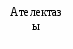 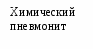 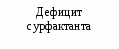          Рис. 2.6. Схема патогенеза аспирации мекония Исследования. Рентгенография органов грудной клетки; общий анализ крови и мочи, гематокрит, определение концентрации РаО2 РаСО2 в артериальной крови, показатели КОС, определение в крови уровней: общего белка, глюкозы, калия, натрия, кальция, мочевины, креатинина, магния, билирубина; показатели коагулограммы, ЭКГ, ЭхоКГ, НСГ. Анамнез, клиника. Дети при САМ, как правило, рождаются с низкой оценкой по шкале Апгар. У переношенных детей часто имеется прокрашивание меконием ногтей, кожи, пуповины. Существуют два варианта клинического течения САМ: 1) у большинства детей с САМ с рождения отмечаются признаки дыхательных расстройств, притупление легочного звука, повышение ригидности грудной клетки, обильные разнокалиберные влажные хрипы в легких, у части – приступы вторичной асфиксии; 2) у некоторых детей с САМ после рождения имеется «светлый» промежуток, после которого (по мере продвижения мелких частиц мекония к мелким бронхам) возникает клиника тяжелой дыхательной недостаточности. В наиболее тяжелых случаях САМ осложняется синдромом персистирующей легочной гипертензии. В процессе ИВЛ нередко выявляется синдром «утечки воздуха». Через 24-48 часов после рождения у большинства детей развиваются с САМ клинические признаки аспирационной пневмонии. У всех новорожденных с тяжелой формой САМ развиваются функциональные изменения со стороны ЦНС: мышечная гипотония, угнетение физиологических рефлексов, фокальные судороги в первые дни жизни. Транзиторная дисфункция миокарда проявляется цианозом, тахикардией, систолическим шумом, иногда ритмом галопа, кардиомегалией, увеличением в размерах печени. Диагноз. Для постановки диагноза САМ используют результаты оценки по шкале Даунса. Диагноз устанавливается на основании данных анамнеза, мекониального характера околоплодных вод клинических и рентгенологических данных. На обзорной рентгенограмме грудной клетки отмечается сочетание крупных участков затемнения, отходящих от корней легких, с участками эмфизематозных вздутий. Характерен симптом «снежной бури», кардиомегалия, в ряде случаев обнаруживаются признаки пневмоторакса. Диафрагма уплощена, переднезадний размер грудной клетки увеличен. Если в мекониальных водах обнаружены плотные фрагменты мекония, то вероятность аспирации мекония и пневмонии гораздо выше, чем когда околоплодные воды просто окрашены меконием. Лабораторные исследования: выраженная гипоксемия и смешанный ацидоз. Дифференциальный диагноз проводят с: РДСН, персистирующей легочной гипертензией, вызванной тяжелой асфиксией, сепсисом, транзиторным тахипноэ. Табл. 2.48. Дифференциальный диагноз синдрома аспирации мекония и РДСН
Лечение. Обязательна аспирация мекония из дыхательных путей сразу после рождения до начала вспомогательной вентиляции легких. Отсасывание мекония при необходимости повторяют неоднократно. Интенсивность и длительность респираторной терапии, а также особенности поддерживающей терапии зависят от тяжести клинической картины и имеют много общего с РДСН. При легких вариантах САМ проводится кислородотерапия при помощи кислородной палатки. Эффект от применения СРАР непредсказуем, его лучше не использовать, при необходимости перейти к ИВЛ (при РаО2<50, РаСО2>60, РН<7,2). При возникновении пневмоторакса – проведение высокочастотной осцилляторной ИВЛ. При тяжелой дыхательной недостаточности проводят терапию экзогенным сурфактантом. Из-за высокого риска пневмонии всем детям с синдромом аспирации мекония необходимо раннее начало антибиотикотерапии. Этим детям показано раннее введение сурфактанта, восполнение ОЦК, коррекция электролитных нарушений, введение допамина. Прогноз. При раннем и своевременном лечении благоприятный. Летальность 4-19%. Высока вероятность неврологических нарушений. Вопросы к экзамену. Синдром дыхательных расстройств (СДР) и массивная аспирация у новорожденных. Этиология. Патогенез. Роль системы сурфактанта в патогенезе СДР. Клинические проявления рассеянных ателектазов, отечно-геморагического синдрома, болезни гиалиновых мембран. Диагностика. Использование шкал Сильвермана и Даунса. Рентгенографические признаки СДР. Дифференциальный диагноз. Течение. Осложнения. Лечение. Естественные и синтетические сурфактанты. Лечение дыхательной недостаточности. Осложнения терапии СДР. Исходы. Прогноз. Пренатальная профилактика. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
