|
|
Методы диагностики и коррекция нарушений водно-электролитного обмена и кислотно-основного состояния (КОС). Методы диагностики и коррекция нарушений водно-электролитного об. Министерство здравоохранения украины
Гиперкальциемия
Гиперкальциемия — это концентрация Са++ в плазме крови более 2,6 ммоль/л.
Этиология: избыточное поступление или усиленная абсорбция кальция в кишечнике, гипервитаминоз витамина D, прием антацидных кальцийсодержащих средств, метаболические нарушения (гиперпаратиреоидизм, гипофосфатемия, тиреотоксикоз), нарушения обмена кальция в костной ткани, процессы, сопровождающиеся разрушением костей, вторичный гиперпаратиреоз (например, при почечной недостаточности), ацидоз.
Клинические признаки: нарушения сознания, вплоть до комы, мышечная слабость, нарушения сердечного ритма, на ЭКГ — укорочение интервала Q—Г (рис. 4), анорексия, тошнота, рвота, ослабление моторики кишечника, патологические переломы костей, преципитация кальция в почечных канальцах с образованием конкрементов.
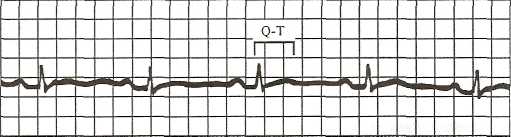
Рис. 4. Укорочение интервала Q — Т на ЭКГ при гиперкальциемии
Лечение: устранение патогенетического фактора, ограничение поступления кальция с пищей, назначение мочегонных средств (фуросемида), внутривенное введение изотонического раствора натрия хлорида. В тяжелых случаях применяют кальцитонин, раствор динатриевой соли этилендиаминтетрауксусной кислоты (ЭДТА) с 5 % раствором глюкозы под контролем уровня кальция в крови.
ОБМЕН МАГНИЯ
Магний - второй после калия внутриклеточный катион. Его концентрация в плазме крови в норме составляет 0,8—1,2 ммоль/л; 33 % магния связаны с белками крови, 67 % — находятся в ионизированном состоянии, 60 % магния в организме содержится в костной ткани. Магний поступает в организм с пищей, выводится через почки и пищеварительный тракт.
Физиологическая роль: принимает участие в обеспечении нервно-мышечной проводимости, окислительно-восстановительных процессах и образовании энергии, уменьшает возбудимость мышечных волокон, в том числе кардиомиоцитов, уменьшает тонус гладкой мускулатуры, понижает АД, регулирует течение метаболических процессов, влияет на внутриклеточное содержание Са++ прежде всего через секрецию паратиреоидного гормона.
Регуляция. Регуляционные механизмы обмена Mg++ изучены недостаточно. Известно, что степень фильтрации в почечных клубочках и реабсорбции Mg++ в канальцах и петле Генле зависит от его концентрации в плазме крови.
Гипомагниемия
Гипомагниемия — это концентрация Mg++ 0,8 ммоль/л.
Этиология: усиленное выведение Mg++ при рвоте, диарее, использовании диуретиков, при ожогах; уменьшение поступления Mg++ с пищей при недостаточном питании или снижении его абсорбции; увеличение поступления Са++ и витамина D, гиперкальцемия, гипопаратиреоидизм, гипоальдостеронизм, прием высоких доз стероидных гормонов, диабетический кетоацидоз, алкоголизм, гипертензия беременных.
Клинические признаки: нарушения памяти, судороги, тремор конечностей, усиление сухожильных рефлексов, нарушения сердечного ритма.
Лечение: терапия основного патологического процесса, коррекция концентрации магния в плазме крови путем введения раствора магния — инфузия 10 % раствора магния сульфата (скорость введения — не более 1,5 мл/мин), коррекция гипокалиемии.
Гипермагниемия
Гипермагниемия — это концентрация Mg++в плазме крови более 1,2 ммоль/л.
Этиология: увеличение поступления Mg++ с пищей, почечная недостаточность, гиперкатаболизм, острый панкреатит, несбалансированная инфузионная терапия.
Клинические принаки: уменьшение сухожильных рефлексов и мышечного тонуса, артериальная гипотензия, брадикардия, нарушения сердечного ритма и вентиляции.
Лечение: коррекция основного заболевания, введение препаратов кальция (кальция глюконата), как антагонистов магния относительно влияния на миокард.
ОБМЕН ХЛОРА
Хлор является главным анионом внеклеточной жидкости. В норме его уровень в плазме крови составляет 95—108 ммоль/л. В организм поступает с пищей - с продуктами, содержащими поваренную соль. В значительной мере метаболизм и физиологическая функция хлоридов определяется обменом натрия и гидрокарбонатных ионов (НСО3
). Важна роль хлора в поддержании осмолярности плазмы и регуляции КОС крови.
Регуляция. Уровень хлора регулируется почечными и внепочечными механизмами. Его реабсорбция в почечных канальцах тесно связана с реабсорбцией Na+ и зависит, главным образом, от продукции альдостерона. Экскреция Сl- почками зависит от его поступления в организм. Кроме почек, Сl- пассивно и активно абсорбируется в кишечнике.
Гипохлоремия
Гипохлоремия — это концентрация Сl- в плазме крови менее 95 ммоль/л, при этом пропорционально увеличиваются для обеспечения электронейтральности реабсорбция и концентрация НСО3-, что приводит к метаболическому алкалозу и гипокалиемии.
Этиология: усиление потери Сl- через пищеварительный канал (рвота, потери желудочного содержимого через гастростому или желудочный зонд), при использовании мочегонных средств увеличивается выведение Сl- с мочой при уменьшении раебсорбции Na+ в почках, дилюционная гипохлоремия при введении избыточного количества воды, бессолевая диета.
Клинические признаки: специфических симптомов нет, клиническая картина во многом зависит от этиологии гипохлоремии, иногда связана с развитием метаболического алкалоза; могут наблюдаться понижение аппетита, уменьшение тургора тканей, артериальная гипотензия, признаки спазмофилии. Если уровень Сl- в плазме крови менее 70 ммоль/л, то могут развиваться судороги, нарушаться функции пищеварительного тракта и почек.
Лечение: терапия основного заболевания, восполнение дефицита Сl- с пищей, внутривенное введение растворов хлоридов натрия, калия, кальция, стабилизация КОС.
Гиперхлоремия
Гиперхлоремия - это концентрация Сl- более 108 ммоль/л, при этом увеличивается объем внеклеточной жидкости.
Этиология: избыток Na+ (гипернатриемия), дефицит НСО3- (метаболический ацидоз), дегидратация, тяжелая почечная недостаточность.
Клинические признаки: специфических симптомов нет, клиническая картина связана с нарушениями водно-электролитного баланса и возможными нарушениями КОС.
Лечение: ограничение употребления натрия хлорида, возобновление употребления воды, применение мочегонных средств (салуретиков), при тяжелой гиперкалиемии — гемодиализ.
ОБМЕН ФОСФАТОВ
Фосфор является важнейшим анионом внутриклеточной среды. В плазме крови он находится в виде моно- и дигидрофосфатных анионов, в норме его концентрация составляет 0,65—1,3 ммоль/л; 80 % фосфора связаны с кальцием и входят в состав костной ткани. В организм поступает с пищей, выводится через почки с мочой.
Физиологическая роль: принимает участие в регуляции КОС, играет важную роль в образовании макроэргических соединений, прежде всего — АТФ, входит в состав фосфолипидов — главного компонента клеточных мембран, обеспечивает функционирование эритроцитов, нервной и мышечной тканей, регулирует метаболизм углеводов, белков и липидов.
Регуляция: при усилении фильтрации фосфора в почечных клубочках увеличивается его реабсорбция в проксимальных канальцах нефрона и наоборот, в случае уменьшения фильтрации — реабсорбция фосфора увеличивается; паратиреоидный гормон ухудшает канальциевую реабсорбцию фосфора и увеличивает его экскрецию, поэтому регуляция обмена фосфора тесно связана с регуляцией обмена кальция.
Гипофосфатемия
Гипофосфатемия — это концентрация ионов фосфора в плазме крови менее 0,65 ммоль/л.
Этиология: недостаточное поступление в организм с пищей (анорексия, нарушения процесса пищеварения), уменьшение реабсорбции в почках (применение диуретиков) или усиление выведения через пищеварительный канал, гипокалиемия, гипомагниемия, метаболический ацидоз, алкоголизм, гиперпаратиреоидизм.
Клинические признаки: мышечная слабость, парестезии, нистагм, нарушения сознания, гемолитическая анемия, нарушения функции тромбоцитов, гиперкальциемия и повышение уровня креатинфосфокиназы.
Лечение: патогенетическое — обеспечение усиленного поступления фосфатов с пищей, внутривенное введение фосфатсодержащих растворов.
Гиперфосфатемия
Гиперфосфатемия — это концентрация фосфора в плазме крови более 1,3 ммоль/л.
Этиология: усиленное поступление фосфора с пищей, гипервитаминоз витамина D, почечная недостаточность, деструкция клеток (химиотерапия по поводу онкологических заболеваний, политравма, рабдомиолиз), гипопаратиреоидизм, остеопороз.
Клинические признаки: спазм мышц, миалгия, гипокальциемия, при продолжительной гиперфосфатемии — кальцификация суставов.
Лечение: ограничение употребления фосфорсодержащих продуктов, коррекция гипокальциемии, в тяжелых случаях — гемодиализ.
КИСЛОТНО-ОСНОВНОЕ СОСТОЯНИЕ
Регуляция кислотно-основного состояния в норме
Поддержание стабильных показателей кислотно-основного состояния является важным компонентом гомеостаза и необходимым условием для обеспечения нормального процесса метаболизма и активности ферментных систем.
Согласно теории Бронстеда (Bronsted), кислотой является вещество, которое отдает ионы водорода в растворе, а основанием является вещество, которое связывает Н+. Поддержание баланса между кислотами и основаниями — это динамический процесс, который зависит от концентрации в жидкостях организма Н+ и ОН-.
В незначительном количестве вода в организме диссоциирует на Н+ и ОН-. При нейтральной реакции раствора в диссоциированном состоянии находится лишь 10-7 молекул воды, или [Н+] = [ОН-] = 10-7. Таким образом, при повышении концентрации Н+ пропорционально снижается концентрация ОН- и наоборот. Реакцию раствора можно определить, зная лишь концентрацию Н+ поскольку при нейтральной реакции раствора [Н+] = 10-7, что равняется 100 нмоль/ л, при кислой — [Н+] > 10-7, при щелочной — [Н+] < 10-7. Во внеклеточной жидкости [Н+] = 10-7,4, или 40 нмоль/л, но на практике такие величины достаточно сложно интерпретировать. В 1909 г. Соренсен предложил для определения концентрации Н+ в растворе использовать показатель рН, который равен отрицательному десятичному логарифму концентрации Н+ в растворе, или рН = —lg [Н+]. Таким образом, при условии нейтральной реакции раствора рН = 7,0, при кислой реакции — менее 7,0 (так как логарифм отрицательный), при основной — более 7,0. В норме рН плазмы крови равняется 7,4 и колеблется в пределах 7,35—7,4.5, следовательно, плазма крови имеет слабоосновную реакцию. При развитии патологических состояний показатель рН может варьировать от 6,8 до 7,8.
Если рН плазмы крови более 7,45, то такое состояние называют алкалозом, если менее 7,35 — ацидозом.
Для поддержания нормального уровня рН в организме функционируют так называемые буферные системы: гидрокарбонатная, фосфатная, белковая и гемоглобиновая. Эти системы уменьшают колебание рН в случае кислотной или щелочной агрессии. Например, гидрокарбонатная буферная система содержит Н2СО3 (угольную кислоту) и НСО3-, при кислотной агрессии в реакцию вступает НСО3-, при щелочной — Н2СО3.
В регуляции рН принимают участие легкие, почки, пищеварительная система.
Через легкие в течение суток выводится 15 000 моль углекислого газа, который образуется в тканях, как конечный продукт аэробного гликолиза. Содержание CO2, в значительной степени влияет на показатель рН, поскольку в растворе в присутствии фермента карбоангидразы при взаимодействии с молекулой воды образуется угольная кислота, которая затем диссоциирует на Н+ и НСО3-, увеличивая концентрацию Н+ и уменьшая показатель рН. При условии нормальной вентиляционной функции легких РаСО2 составляет 40 мм рт. ст. При вентиляционной дыхательной недостаточности ухудшается элиминация СО2, что приводит к понижению рН и развитию респираторного (вследствие нарушений респираторной функции легких) ацидоза; если СО2 выводится в количестве, превышающим его образование (гипервентиляция), то развивается респираторный алкалоз. Легкие в определенной степени могут компенсировать метаболические нарушения КОС: если возникает метаболический ацидоз, то вентиляция увеличивается за счет стимуляции Н+ дыхательного центра, и рН повышается, и наоборот, в случае метаболического алкалоза вентиляция уменьшается, накапливается СО2, и понижается рН.
В регуляции КОС важна роль почек, поскольку с мочой выводится избыток Н+ и поддерживается концентрация НСО3- на уровне 22—26 ммоль/л. Этот процесс взаимозависимый: Н+ выводится почками в составе NH4+, который замещается на НСО3- . При образовании избыточного количества оснований в почках уменьшается экскреция Н+ и реабсорбция НСО3-. Таковы механизмы нарушений КОС при почечной недостаточности.
Важную роль в поддержании нормального рН играет пищеварительная система, в первую очередь, за счет регуляции водно-электролитного баланса, так как К+, Na+ и Сl- в значительной степени влияют на показатель рН. Доказательством участия желудка и кишечника в регуляции рН является развитие метаболических нарушений в случае патологии этих органов. Так, при рецидивной рвоте (стеноз привратника) теряются кислотные валентности с последующим развитием метаболического алкалоза, а при диарее тяжелой степени, напротив, происходит потеря щелочных валентностей с развитием метаболического ацидоза.
Основные показатели, характеризующие КОС
рН — отрицательный десятичный логарифм концентрации Н+, или величина, обратная числу концентрации Н+, или степень растворения Н+ в растворе; это основной показатель, который определяет реакцию раствора (в норме — 7,35-7,45).
РСО2 — парциальное давление углекислого газа (норма в артериальной крови — 35—45 мм рт. ст.). Увеличение этого показателя сопровождается повышением концентрации угольной кислоты (Н2СО3) и, соответственно, уменьшением рН; наоборот — уменьшение РСО2 приводит к увеличению рН.
АВ — актуальный (истинный) гидрокарбонат, показатель фактической концентрации гидрокарбонатных ионов; в норме — 20—25 ммоль/л.
SB — стандартный бикарбонат, показатель концентрации гидрокарбонатных ионов в стандартных условиях: РСО2 — 40 мм рт. ст., температура тела — 38 "С, насыщение крови кислородом — полное; в норме — 25—28 ммоль/л.
ВВ — сумма оснований всех буферных систем крови (гидрокарбонатной, фосфатной, белковой и гемоглобиновой) при нормальных условиях: РСО2 — 40 мм рт. ст., температура тела — 38 °С, оксигенация крови — достаточная; в норме (NBB) — 46—52 ммоль/л.
BE — дефицит или избыток оснований (BE = ВВ - NBB). Если показатель BE выше нормы, то возникает избыток оснований; если BE меньше чем показатель NBB, то — дефицит оснований. BE уменьшается при метаболическом ацидозе и увеличивается при метаболическом алкалозе; в норме — ± 2,5 ммоль/л.
Показатели рН, РСО2 и BE взаимосвязаны. Так, увеличение или уменьшение РСО2 на 10 мм рт. ст. сопровождается, соответственно, уменьшением или увеличением рН крови на 0,08 при условии отсутствия изменений BE; повышение или понижение концентрации буферных оснований на 10 ммоль/л сопровождается, соответственно, повышением или понижением рН на 0,15 при условии отсутствия изменений РСО2.
ОТДЕЛЬНЫЕ ВИДЫ НАРУШЕНИЙ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ
Респираторный ацидоз
Респираторный ацидоз — уменьшение рН вследствие повышения РСО2. Компенсация рН обеспечивается увеличением экскреции Н+ и реабсорбции НСО3- в почках. Компенсация может достигаться в течение сравнительно продолжительного периода — 6—8 ч.
Этиология: все патологические состояния, которые приводят к развитию вентиляционной формы дыхательной недостаточности (см. соответствующий раздел).
Клинические признаки: нарушения сознания, вплоть до комы, судороги, отек мозга, теплая розовая кожа, тахикардия, артериальная гипертензия, которая в терминальном состоянии сменяется гипотензией.
Лабораторные показатели: рН < 7,35, РСО2 > 45 мм рт. ст., BE — в норме или более 2,5 ммоль/л (вследствие компенсации).
Лечение: терапия основного заболевания, которое обусловило развитие вентиляционной дыхательной недостаточности, в тяжелых случаях — ИВЛ.
Метаболический ацидоз
Метаболический ацидоз — уменьшение рН вследствие дефицита оснований в организме. Компенсация возможна за счет гипервентиляции легких и уменьшения РСО2.
Этиология: накопление органических кислот (лактат-ацидоз - при гипоксии, кетоацидоз — при сахарном диабете, алкоголизме, голодании), гиперхлоремия с соответствующим уменьшением концентрации НСО3-, значительная потеря НСО3- (диарея, фистула кишечника и поджелудочной железы), нарушение реабсорбции НСО3- в почках (почечная недостаточность), интоксикация салицилатами или многоатомными спиртами, применение ингибиторов карбоангидразы.
Клинические признаки: нарушение сознания, головная боль, периферическая вазодилатация, гипервентиляция (вплоть до дыхания Куссмауля), при продолжительном ацидозе — остеопороз с патологическими переломами костей. Если показатель рН < 7,2, то ухудшается функция миокарда и адренорецепторов сосудов, уменьшается СИ. При дальнейшем нарастании ацидоза развивается кома, артериальная гипотензия, угнетение дыхания.
Лабораторные показатели: рН < 7,35, РСО2 - в норме или понижено (вследствие компенсации), BE < -2,5 ммоль/л.
Лечение. Коррекция этиологического фактора, прежде всего, восстановление транспорта кислорода к тканям: коррекция гиповолемии, функции сердца, улучшение микроциркуляции, при необходимости - ИВЛ; восстановление функции почек, лечение диареи, коррекция ВБ.
При тяжелом метаболическом ацидозе (рН < 7, 1—7,2) вводят растворы, повышающие рН: натрия гидрокарбонат, натрия лактат, натрия ацетат, трисамин.
В последнее время показания к введению натрия гидрокарбоната (1 мл 4,2 % раствора содержит 0,5 ммоль гидрокарбоната) значительно уменьшились вследствие развития отрицательных эффектов при его применении. Это, прежде всего, гипернатриемия, гиперосмолярность плазмы крови, парадоксальное усиление внутриклеточного ацидоза, частая гиперкоррекция ацидоза с развитием алкалоза, который более тяжело переносится организмом. Таким образом, введение больному раствора натрия гидрокарбоната показано только при условии понижения рН до 7,1—7,2, если необходима профилактика почечной недостаточности при развитии миоглобинурии (рабдомиолиз), переливании несовместимой крови, а также при отравлении салицилатами и барбитуратами.
Дозу гидрокарбоната натрия рассчитывают по формуле:
Натрия гидрокарбонат (ммоль/л) = BE x M x 0,2,
где М — масса тела.
Необходимо отметить, что расчет необходимой дозы гидрокарбоната, согласно этой формуле, приблизительный, поэтому сначала вводят половину рассчитанной дозы, а затем проводят коррекцию метаболического ацидоза под контролем рН.
Растворы натрия лактата и ацетата более мягко влияют на показатель рН: в печени происходит их метаболическое превращение с образованием гидрокарбоната, но это не приводит к развитию гипернатриемии и гиперосмолярности плазмы крови. Натрия лактат и ацетат не применяют при лактат-ацидозе, поэтому их использование в клинической практике значительно ограничено.
Трис-буфер, или трисамин, является органическим акцептором Н+. В отличие от натрия гидрокарбоната трисамин корректирует внутриклеточный ацидоз, обладает осмодиуретическим действием, но его введение сопровождается побочными эффектами: угнетением, особенно при быстром введении, дыхания и сердечной деятельности, развитием гипокалиемии и внутриклеточной дегидратации. Трисамин противопоказан при снижении фильтрационной функции почек. Дозу трисамина рассчитывают по формуле:
Объем трисамина (мл, 3,66 % раствора) = BE x M,
где М - масса тела, кг.
Вводить трисамин необходимо медленно со скоростью не более 5 мл/кг/ч, только внутривенно (при попадании во вневенозное пространство развивается некроз околососудистой клетчатки).
Избыточные объемы натрия гидрохлорида или трис-буфера могут спровоцировать нежелательную реакцию превращения метаболического ацидоза в метаболический алкалоз.
|
|
|
 Скачать 370.5 Kb.
Скачать 370.5 Kb.
