Сборник материала по патофизиологии. Патфиз 1 кр. Нарушение периферического кровообращения. Венозная гиперемия. Причины, виды, механизмы развития, последствия
 Скачать 477.28 Kb. Скачать 477.28 Kb.
|
|
Часть пирогенов попадая в кровь,проходит гэб и дстигает термоцентра.В результате ИЛ-1 начинается образование простогландинов Е в кл термоцентра,повышается продукция ц.АМФ,в результате функциональной активность клетки повышается Существует 3 стадии развития лихорадки: I. Стадия повышения температуры II. Стадия стояния высокой температуры III. Стадия снижения температуры В основе этих стадий лежит перестройка процессов терморегуляции. В I стадии увеличиваются процессы теплопродукции и уменьшаются процессы теплоотдачи. Температура повышается. Характерным симптомом этой стадии является озноб. Во II стадии эти процессы выравниваются на более высоком уровне, чем в норме. Симптомом II стадии является жар. В III стадии снижаются процессы теплообразования и преобладают процессы теплоотдачи. Основным симптомом этой стадии является испарина, потоотделение. Снижение температуры на III стадии может быть медленным, литическим (несколько часов, дней) или быстрым, критическим вследствие резкого расширения сосудов, что может привести к развитию коллапса (острой сосудистой недостаточности). 21.Лихорадка как компонент РООФ. Классификация пирогенов. Механизм реализации эндопирогенов.Биологиеское значение лихорадки. Обычно РООФ начинается через 8-10 часов от начала повреждения и длится до окончания воспаления. Проявляется как :Головная боль, Мышечная боль, Недомогание, Слабость, Утрата аппетита, Бессонница, Лихорадка (связанно с тем, что большинство цитокинов являются эндопирогенами и снижают чувствительность центра терморегуляции к температурным сигналам) Классификация пирогенов. Эндо-выдел нейтрофилами и моноцитами,самый главный ИЛ-2 Свойства-Аг(белок,термостабил) Экзо-продукты жизнедеятельности микроорганизма(липополисахариды по природе),термлабильные,сами по себе не вызывают лихорадку Механизм реализации эндоперогенов: Микро в макро-активация иммуной системы-акт.лейкоциты синтезируют эндопирогенны (болле развёрнуто) Лихорадка вызывается особыми веществами - пирогенами. Они по происхождению делятся на: 1. Экзопирогены (из эндотоксинов микробов - бактериальные). 2. Эндопирогены (клеточные). Характеристика экзопирогенов: по химическому строению - это высокомолекулярные липополисахариды. Установлено, что: 1) экзопирогены вызывают лихорадку опосредованно через образование эндопирогенов, поэтому лихорадка развивается через 45-60 минут и максимум ее через 3-4 часа, 2) не токсичны, 3) термоустойчивы (для разрушения надо автоклавировать в течение 1-2 часов при температуре 200 градусов), 4) не аллергенны, 5) не антигенны, 6) но несут на себе антигенную химическую специфичность - т.е. являются гаптенами. Для приобретения антигенных свойств они должны соединиться с белками клеток и тканей, 7) при ежедневном введении 5-6 раз к экзопирогенам возникает толерантность и лихорадка не развивается, 8) экзопирогены вызывают ряд защитных эффектов. Эндогенные пирогены: их источником являются нейтрофилы, макрофаги и лимфоциты крови - это лейкоцитарные пирогены илиинтерлейкин-1. Свойства лейкопирогенов: 1) вырабатываются только живыми лейкоцитами, по строению - это белок типа альбумина, 2) неустойчивы к нагреванию - разрушаются при температуре, вызывающей коагуляцию белка (60-70 градусов), 3) температурная реакция на эндопироген развивается через 10-15 мин. Максимум подъема температуры после введения эндопирогена через 1-2 часа (экзопирогена 3-4). Характеристика интерлейкина-1: 1) он вырабатывается в микро- и макрофагах, не вызывает толерантности, нетоксичен, действует на все основные регулирующие системы организма и прежде всего те, которые определяют реактивность и резистентность - нервную и эндокринную, 2) действует на клетки гипоталамуса и усиливает выработку CRF, которые запускают стресс-реакцию, мобилизуют энергетические ресурсы, развиваются гипергликемия, липемия. Эндопирогены дают такой же биологический эффект, как и экзопирогены, повышая защитные свойства организма: 1) усиливают фагоцитоз, 2) усиливают выработку глюкокортикоидов, 3) усиливают регенерацию тканей, которая ведет к образованию нежных рубцов (применяется при повреждении ЦНС для предотвращения осложнений (эпилепсии, парезов, параличей), 4) усиливают дезинтоксикационную функцию печени, 5) улучшают процессы микроциркуляции - вот почему пирогены применяются при вялом течении заболеваний,при хронической язве желудка для ускорения заживления и рубцевания язв, при почечной гипертонии для улучшения процессов микроциркуляции в почках(в нефроне, клубочках) и уменьшения выработки ренина. Лейкопироген вырабатывается при раздражении лейкоцитов: 1) при воспалении, 2) действии токсинов, 3) под влиянием шероховатости стенки сосудов, при контакте лейкоцитов с микробами даже в кровеносном русле, 4) при изменении pH в кислую сторону (ацидоз). Характеристика лимфоцитарных и макрофагальных пирогенов. Макрофаги крови альвеол и брюшины в процессе фагоцитоза вырабатывают такое же вещество, как нейтрофилы - интерлейкин-1. Лимфоцитарный пироген вырабатывается сенсибилизированными лимфоцитами при аллергии при контакте с аллергеном. Биологическое значение Положительное: 38-субфибрильная нарушение жизнедеятельности для микроорганизмов Активирует антитоксические свойства печени и почек Активация фагацитоза и спец.иммунитета Понижает пролиферативне процессы Отрицательное: Опасна перегриванием Обезвоживание-коллапс В лечебных целях: аутоимунные зааболевания которые характиризуются пролиф.типом(красная волчанка) Половые инфекции (сифилис, гонорея) прим. При акт. Т-кл. иммунитета Воспаление вялотикущий процесс(пожилые) Защитно-приспособительное значение лихорадки подтверждается следующими наблюдениями: • при лихорадке усиливается иммунный ответ организма вследствие активации Т- и В-лимфоцитов, ускорения превращения последних в плазматические клетки, что стимулирует образование антител; повышается образование интерферона; • умеренная степень подъема температуры тела может активировать функцию фагоцитирующих клеток и NK-клеток (натуральные киллеры); • активируются ферменты, угнетающие репродукцию вирусов; • замедляется размножение многих бактерий и снижается устойчивость микроорганизмов к лекарственным препаратам; • возрастают барьерная и антитоксическая функции печени; • гепатоциты усиленно продуцируют так называемые белки острой фазы; некоторые из этих протеинов связывают бивалентные катионы, необходимые для размножения микроорганизмов; • кроме того, повышение температуры тела при лихорадке достаточно часто является первым и единственным признаком какого-либо заболевания, это сигнал тревоги.
Отрицательное воздействие лихорадки на организм выявляется главным образом при резко выраженном и длительном повышении температуры тела. Оно связано со стимуляцией функции сердца, которая может привести к развитию перегрузочной формы сердечной недостаточности, особенно у людей пожилого и старческого возраста, а также у пациентов, ранее уже имевших то или иное заболевание сердца. Представляет опасность возможность развития коллапса при критическом снижении температуры тела в заключительную стадию лихорадки. При лихорадке высокой степени может произойти подавление иммунных реакций. 22.Отличие лихорадки от экзогенного перегревания и других видов гипертермий. Для возникновения лихорадки главным этиологическим фактором является первичный пироген, а для развития перегревания - высокая температура окружающей среды (в условиях жаркого климата, производства). Механизм повышения температуры тела при лихорадке абсолютно не идентичен таковому при перегревании. При лихорадке происходит смещение «установочной точки» на более высокий уровень функционирования под влиянием пирогенов. Перестройка функции центра теплорегуляции при лихорадке направлена на активную задержку тепла в организме независимо от внешней температуры, при этом механизмы терморегуляции сохранены. При перегревании не происходит смещения «установочной точки» теплорегулирующего центра. При перегревании организм стремится освободиться от лишнего тепла путем максимального напряжения процессов теплоотдачи, чему препятствует повышенная температура окружающей среды. Таким образом, при перегревании механизмы терморегуляции нарушены: при высокой температуре воздуха, высокой влажности воздуха, отсутствии ветра теплоотдача существенно снижена. Как было сказано, повышение температуры тела при лихорадке связано со сдвигом «установочной точки» теплорегуляции на новый, более высокий уровень функционирования для активной задержки тепла в организме. В отличие от лихорадки повышение температуры тела при перегревании является не активным, а пассивным процессом, и деятельность теплорегулирующих центров направлена не на накопление в организме тепла, а на воспрепятствование изменению температурного гомеостаза.
При лихорадке процесс активного повышения температуры тела обычно останавливается, когда она достигает 41 °С (за счет системы эндогенного антипиреза). При перегревании такого ограничения нет: температура тела может повышаться вплоть до гибели организма. Человека лихорадит одинаково в широком диапазоне температур внешней среды (т.е. развитие лихорадки не зависит от внешней температуры). При перегревании же степень повышения температуры тела напрямую зависит от условий теплоотдачи во внешнюю среду (т.е. от температуры среды). Кроме этого, лихорадка и перегревание отличаются по последствиям их развития для организма. Лихорадка как типовой патологический процесс имеет двоякое значение для организма - положительное и отрицательное .Перегревание имеет отрицательное воздействие на организм ,если только не используется с лечебной целью 66) Иммунодефицитные состояния и аллергия как типовые иммунопатологические процессы. Взаимосвязь аллергии и воспаления, аллергии и иммунитета. Иммунопатология развивается в двух формах-избыточность иммунного ответа, гиперчувствительность, аллергия и недостаточность иммунного ответа- иммунодефицитные состояния. Иммунодефицитные состояния - врожденный или приобретенный дефект иммунной системы, выражающийся неспособностью организма осуществлять реакции клеточного и (или) гуморального иммунитета. Нарушение иммунологической реактивности может быть обусловлено патологией одного или нескольких механизмов иммунного ответа. Различают первичные и вторичные иммунодефицитные состояния: первичный иммунодефицит-врожденный дефект иммунной системы, вторичный иммунодефицит-следствие каких-либо патогенных воздействий окружающей среды-физических, химических или биологических факторов. Аллергия является типовой иммунопатологической реакцией повышенной чувствительности организма к веществам белковой и небелковой природы, в основе которой лежит иммунобиологическая реакция «антиген-антитело» или «антиген-сенсибилизированные Т-лимфоциты» с последующим повреждением клеток организма. Аллергия является одной из форм иммунологического реагирования (ИР) и вместе с другими формами ИР (иммунитет, толерантность, иммунологическая память) служит поддержанию постоянства внутренней среды в условиях постоянных соматических мутаций, старения клеток, внешней антигенной агрессии (генетическая чистота). Общность аллергии и иммунитета - единая основа иммунологического реагирования-образования комплекса АГ+АТ. Но при иммунитете следствием образования комплекса АГ+АТ будет нейтрализация АГ, быстрое его поглощение и разрушение фагоцитами и выведение из организма - защитная реакция. При аллергии, кроме обязательного образования комплекса АГ+АТ клеточного или гуморального типа, в реализации процесса принимает участие ансамбль неспецифических медиаторов - гиперэргическое воспаление с повреждением клеток и тканей организма. При иммунных же реакциях не происходит повреждения тканей. Аллергия и воспаление. Комплекс АГ-АТ является флогогенным агентом наряду с другими причинами воспаления. Когда АТ или клетки-киллеры реагируют непосредственно с АГ клеток организма, например при цитотоксических реакциях или аллергических реакциях замедленного типа, комплекс АГ-АТ выступает в роли фактора, вызывающего первичную альтерацию, с которой начинается воспаление. Если же образование комплекса АГ-АТ не приводит к прямому повреждению клетки, то и в этом случае стимулируется биохимическая стадия аллергических реакций, образуются те же биологически активные вещества, которые являются медиаторами воспаления и приводят ко вторичной альтерации. Комплекс АГ-АТ относится к числу факторов, которые могут при определенных условиях вызвать местную или генерализованную выработку биологически активных соединений-медиаторов воспаления и шока. В связи с этим аллергия является таким вариантом воспаления и шока, который в отличие от других воспалительных и шоковых состояний вызывается комплексом АГ-АТ, выступающим в качестве флогогенного агента. 68. Аллергия и иммунитет. Общность и различия. Классификация аллергических реакций. Аллергия является типовой иммунопатологической реакцией повышенной чувствительности организма к веществам белковой и небелковой природы, в основе которой лежит иммунобиологическая реакция «антиген-антитело» или «антиген-сенсибилизированные Т-лимфоциты» с последующим повреждением клеток организма. Аллергия является одной из форм иммунологического реагирования (ИР) и вместе с другими формами ИР (иммунитет, толерантность, иммунологическая память) служит поддержанию постоянства внутренней среды в условиях постоянных соматических мутаций, старения клеток, внешней антигенной агрессии (генетическая чистота). Общность аллергии и иммунитета - единая основа иммунологического реагирования-образования комплекса АГ+АТ. Но при иммунитете следствием образования комплекса АГ+АТ будет нейтрализация АГ, быстрое его поглощение и разрушение фагоцитами и выведение из организма - защитная реакция. При аллергии, кроме обязательного образования комплекса АГ+АТ клеточного или гуморального типа, в реализации процесса принимает участие ансамбль неспецифических медиаторов - гиперэргическое воспаление с повреждением клеток и тканей организма. При иммунных же реакциях не происходит повреждения тканей. Классификация аллергических реакций. 1. По скорости появления клинических признаков после повторного контакта с аллергеном различают: 1.1. ГНТ- гиперчувствительность немедленного типа - время начала клинических проявлений – от секунды до 1-2 часов. Время сенсибилизации-7-21 день Механизм-накопление специфических иммуноглобулинов разных типов - реакция гуморального вида. 1.2. ГЗТ - гиперчувствительность замедленного типа - клиника развивается через 24-72 часа. Время сенсибилизации-3-5 дней. Механизм - связан с образованием сенсибилизированных Т-лимфоцитов-эффекторов-реакция клеточного иммунитета. 2 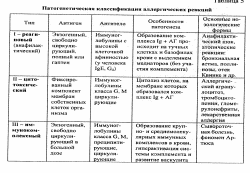 . По патогенезу выделяют 4 основных типа аллергических реакций: . По патогенезу выделяют 4 основных типа аллергических реакций: 69. Этиология аллергических заболеваний. Аллергены, их классификация. Аллергия является типовой иммунопатологической реакцией повышенной чувствительности организма к веществам белковой и небелковой природы, в основе которой лежит иммунобиологическая реакция «антиген-антитело» или «антиген-сенсибилизированные Т-лимфоциты» с последующим повреждением клеток организма. Причина аллергии заключается в аномальном взаимодействии иммунной системы с антигеном. Имеют значение вид антигена, путь его внедрения, срок персистирования в организме, доза и ритм введения при первом и повторном контакте, общее состояние иммунной системы и индивидуальная реакция на конкретный антиген. Аллергия всегда развивается на фоне какого-либо дефекта иммунитета (иммунодефицита) и складывается из усиленного и неадекватного иммунного ответа и последующего усиленного и плохо отрегулированного воспаления или нарушения регуляторных процессов. Любой аллерген является антигеном, но не каждый антиген вызывает аллергические реакции. Аллергены - это вещества с антигенными свойствами, полного или неполного (гаптены) характера, которые вызывают иммунный ответ гуморального или клеточного типа. Виды аллергенов: 1.Экзогенные: А) Инфекционные - микробы, вирусы, простейшие Б) Неинфекционные - пищевые, бытовые, промышленные, лекарственные, растительные. 2. Эндогенные: А) Первичные (истинные) - компоненты «забарьерных» тканей - мозга, хрусталика глаза, коллоида щитовидной железы и т.д. Б) Приобретенные (вторичные)- собственные, видоизмененные белки под влиянием инфекционного, токсического, лекарственного или других физических или химических воздействий. 70)Анафилаксия. Причины, механизмы развития. Сенсибилизация и десенсибилизация. Пассивная анафилаксия. Анафилактический шок. Все аллергические реакции протекают в три фазы: 1. Сенсибилизация 2. Разрешение, включающее 3 стадии- иммунологическая, патохимическая, патофизиологическая. 3.Десенсибилизация Анафилаксия - состояние приобретенной повышенной чувствительности организма к повторному парентеральному введению чужеродного белка. Анафилаксия может проявляться в виде местной (атопии) или общей реакции. Наиболее выраженную общую реакцию называют анафилактическим шоком. Анафилаксия не является разовым эпизодом болезни: она возникает как закономерное проявление хронического системного иммунопатологического процесса. Причины анафилактической реакции. 1.Лекарственные препараты (антибиотики, инсулин, экстракты аллергенов) 2.Продукты питания: орехи; яйца, морепродукты и др. 3.Белки. В эту группу обычно входят продукты крови при гемотрансфузии. 4.Яд животных. При первичном попадании аллергена иммунная система начинает вырабатывать из 2 видов лимфоцитов преимущественно Т-хелперы 2 типа, что приводит к усилению синтеза цитокинов (ИЛ-4, ИЛ-13). Цитокины сдвигают дифференцировку лимфоцитов в сторону Т-хелперов 2-го типа. Плазматические клетки начинают вырабатывать в аномально высоких концентрациях реагины ( IgE). IgE постоянно перемещаются из кровотока за пределы сосудистого русла, во внесосудистом пространстве они своими Fc-фрагментами связываются с Fc-рецепторами базофилов и тучных клеток. Реализация анафилактической реакции протекает в 3 фазы: 1.Иммунологическая - при повторном попадании в организм АГ происходит образование комплекса IgE + АГ на поверхности базофилов. Одна молекула АГ обязательно замыкает 2 молекулы IgE. 2. Патохимическая: А) Ранняя фаза: развивается в первый час после контакта с аллергеном. Обусловлена реагинзависимой дегрануляцией тучных клеток соединительной ткани, слизистых оболочек и базофилов. Первыми выбрасываются гистамин, гепарин, ферменты (триптаза и др.), ФНО-а. Повышается проницаемость стенок микрососудов, происходит сокращение гладкой мускулатуры бронхиального дерева или стенки кишки. Наблюдается активация эндотелия выработка провоспалительных цитокинов. Б) Поздняя фаза: возникает не ранее чем через 4 ч после введения аллергена. Ведущая роль принадлежит простагландинам, лейкотриенам, а также эозинофилам и мононуклеарам, инфильтрирующим очаг анафилактического воспаления. Простагландин F2 и тромбоксан А2 — короткоживущие констрикторы гладкой мускулатуры бронхов. Кроме того, простагландины усиливают активность слизистых желез и вязкость их секрета, вызывают быструю агрегацию тромбоцитов и активируют процессы коагуляции крови. 3.Патофизиологическая - в результате действия медиаторов местно и в кровотоке развиваются патологические процессы - спазм гладких мышц органов, вазодилатация, повышение проницаемости, отек, боль, зуд, увеличение секреции слизи, возбуждение ЦНС. Формируется симптомокомплекс общей анафилактической реакции. У человека развивается по типу сосудисто-дыхательной недостаточности. Сенсибилизация-совокупность последовательно развевающихся процессов – иммунологическое распознавание, клеточная кооперация, пролиферация и дифференцировка лимфоидных клеток в результате первичного попадания АГ в организм. Она заканчивается накоплением сенсибилизированных к данному АГ лимфоцитов (4 тип) или специфических антител- иммуноглобулинов- активная сенсибилизация. Возможна и пассивная сенсибилизация – введение в организм готовых специфических иммуноглобулинов или сенсибилизированных Т-лимфоцитов. Десенсибилизация - временное понижение чувствительности организма к данному АГ. Различают специфическую и неспецифическую десенсибилизацию. 1.Специфическая наиболее эффективна при реагиновом типе аллергии. При ГЗТ сенсибилизация неэффективна. Методы специфической десенсибилизации: -Дробное п/к в возрастающих дозах введение АГ, которое вызывает накопление Ig G, полных антител, «блокирующих» в кровотоке специфический АГ, не допуская его контакта с адсорбированными на клетках цитотропными IgE. -Введение разрешающей дозы под наркозом – происходит закрытие натриево-кальциевых каналов и прерывается переход патохимической фазы в патофизиологическую. - Профилактика и срочная десенсибилизация – метод Безредко-п/к введение малых доз сыворотки с получасовыми интервалами для связывания циркулирующих АТ с целью препятствования общей сывороточной анафилаксии. 2. Неспецифическая десенсибилизация - лекарственная коррекция. - воздействие на иммунную фазу – цитостатики, гормоны. Побочный эффект - снижение защитных сил организма. - воздействие на патохимичекую фазу – антигистаминные препараты – димедрол, пипольфен и др. активаторы внутриклеточного содержания цАМФ: простогландины группы Е, стимуляторы В-адренорецепторов, блокаторы альфа- адренорецепторов и т.д. Пассивная анафилаксия-анафилаксия, вызываемая после введения в организм аллергических антител от активно сенсибилизированного донора. У нормальных животных можно вызвать пассивную анафилаксию. Для этого у активно сенсибилизированной свинки берут кровь не ранее чем через 10-14 дней после сенсибилизации, получают сыворотку, которая уже содержит антитела к чужеродному белку и вводят ее интактной морской свинке. Через сутки вводят разрешающую дозу ( значительно большую). Развивается анафилактический шок. Наиболее опасным системным проявлением анафилаксии является анафилактический шок (развивается в случае генерализованной анафилаксии) Анафилактический шок — это острый системный аллергический процесс, развивающийся в сенсибилизированном организме в результате реакции антиген-антитело и проявляется острым периферическим сосудистым коллапсом. В основе патогенеза анафилактического шока лежит аллергическая реакция I типа, обусловленная IgE. Если человек оказался сенсибилизированным к определенному аллергену, то парентеральное введение этого аллергена может вызвать шок. Это бывает при ужаливании насекомыми (пчелы, осы, шмели), введении лекарств (пенициллин, антитоксические сыворотки и другие белковые препараты), нарушении техники специфической гипосенсибилизации, изредка как выражение пищевой аллергии. Проявления шока определяются его тяжестью. При тяжелых формах шока доминирует картина сосудистого коллапса, при менее тяжелых- снижение АД сочетается со спазмом гладкой мускулатуры и/ или отеками в связи с повышенной проницаемостью сосудов. 71.Атопии. Бронхиальная астма, сенная лихорадка. Причины, механизмы развития. Роль наследственности в развитии атопий. Атопии - это местные проявления аллергических реакций 1 го типа. К группе классических атопических болезней относят круглогодичный атопический ринит, поллиноз, атопическую форму бронхиальной астмы и атопический дерматит. Признаки, характеризующие атопию: естественное возникновение, наследственная предрасположенность, возможность повреждения любой системы организма в отличие от анафилаксии, при которой всегда имеется определенный шоковый орган. При реакциях обоих видов повреждение тканей вызывается аллергическими механизмами первого типа. Атопия отличается от анафилаксии еще одним признаком - в ее развитии большую роль играют неспецифические (неимунные) механизмы. Наследственная предрасположенность - важный признак атопии. В настоящее время обсуждается возможность участия в ее развитии около20 генов, для многих из них определены локализация и связь с тем или иным признаком атопии. Основу развития атопии составляет тот набор генов, который передается по наследству. Но эта наследственная предрасположенность не создает фенотипа атопии, а является лишь способствующим условием. Реализация этой предрасположенности в клинические проявления атопии происходит только при воздействии соответствующих факторов окружающей среды. Такими факторами для каждого индивидуума являются «свои» аллергены. Чаще всего аллергенами становятся: пищевые продукты, пыльца, домашняя пыль, шерсть животных и чистящие средства. В развитии атопии принимают участие группы механизмов: специфические (иммунные) и неспецифические (неиммунные). Особенность специфического механизма выражается в повышенной способности организма отвечать на аллергены образованием lgE-антител. При первичном попадании аллергена иммунная система начинает вырабатывать из 2 видов лимфоцитов преимущественно Т-хелперы 2 типа, что приводит к усилению синтеза цитокинов (ИЛ-4, ИЛ13). Эти медиаторы переключают в В-лимфоцитах синтез антител с В-класса на Е-класс. Плазматические клетки начинают вырабатывать в аномально высоких концентрациях реагины ( IgE). IgE постоянно перемещаются из кровотока за пределы сосудистого русла, во внесосудистом пространстве они своими Fc-фрагментами связываются с Fc-рецепторами базофилов и тучных клеток. Реализация реакции протекает в 3 фазы: 1.Иммунологическая - при повторном попадании в организм АГ происходит образование комплекса IgE + АГ на поверхности базофилов. Одна молекула АГ обязательно замыкает 2 молекулы IgE. 2. Патохимическая: А) Ранняя фаза: развивается в первый час после контакта с аллергеном. Обусловлена реагинзависимой дегрануляцией тучных клеток соединительной ткани, слизистых оболочек и базофилов. Первыми выбрасываются гистамин, гепарин, ферменты (триптаза и др.), ФНО-а. Повышается проницаемость стенок микрососудов, происходит сокращение гладкой мускулатуры бронхиального дерева или стенки кишки. Наблюдается активация эндотелия выработка провоспалительных цитокинов. Б) Поздняя фаза: возникает не ранее чем через 4 ч после введения аллергена. Ведущая роль принадлежит простагландинам, лейкотриенам, а также эозинофилам и мононуклеарам, инфильтрирующим очаг анафилактического воспаления. Простагландин F2 и тромбоксан А2 — короткоживущие констрикторы гладкой мускулатуры бронхов. Кроме того, простагландины усиливают активность слизистых желез и вязкость их секрета, вызывают быструю агрегацию тромбоцитов и активируют процессы коагуляции крови. 3. Патофизиологическая - в результате действия медиаторов местно и в кровотоке развиваются патологические процессы - спазм гладких мышц органов, вазодилатация, повышение проницаемости, отек, боль, зуд, увеличение секреции слизи. Неспецифические механизмы: 1) нарушения равновесия влияний симпатической и парасимпатической иннервации систем организма, менее выраженные при рините и наиболее резко -при атопическом дерматите. При всех трех классических атопических заболеваниях увеличена холинергическая реактивность, что проявляется более резким сужением зрачка на закапывание в глаза холиномиметиков по сравнению с таковым у здоровых лиц.. При атопической астме, кроме того, повышен холинергический тонус бронхов, что проявляется либо приступом астмы, либо повышением реактивности и чувствительности бронхов при проведении провокационных тестов с холиномиметиками. 2) повышенная способность тучных клеток и базофилов высвобождать медиаторы как спонтанно, так и в ответ на различные неиммунологические стимулы. Установлено, что базофилы больных атопическим ринитом и/или астмой, атопическим дерматитом более легко, чем лейкоциты здоровых людей, высвобождают гистамин в ответ на различные неиммунологические стимулы. Также у этих больных возможно спонтанное выделение гистамина базофилами. 72. Аллергические реакции II типа, этиология, патогенез. Защитное и патогенное значение цитотоксических реакций. Аллергические реакции II типа (цитотоксические аллергические реакции) опосредованы взаимодействием антител с антигенами, первично расположенными на поверхности клеток или вторично появившимися на мембране в процессе жизнедеятельности клетки. Аллергенами в данном типе становятся клетки своих тканей. Чтобы включился иммунный механизм, клетки должны приобрести аутоаллергенные свойства. Большую роль играет действие на клетки различных химических веществ, чаще лекарств. Изменение антигенной структуры клеточных мембран может происходить за счет: • конформационных изменений, присущих клетке антигенов; • повреждения мембраны и появления новых антигенов; • образования комплексных аллергенов с мембраной, в которой химическое вещество играет роль гаптена. Например, при лечении α-метилдофа по одному из указанных механизмов может развиваться аутоиммунная гемолитическая анемия, при введении прокаинамида возможно образование антинуклеарных антител и т.д. При паразитарных, бактериальных и вирусных инфекционных заболеваниях лизосомальные ферменты фагоцитирующих клеток, бактериальные энзимы, вирусы также могут влиять на антигенную структуру клеточных мембран. В результате образуются аутоантитела к различным клеткам тканей и развиваются гемолитическая анемия, тромбоцитопении и др. Для клиники особое значение имеют 4 вида АГ: -клетки крови-мембраны эритроцитов (гемолиз), тромбоцитов, лейкоцитов (лейкопения); -клетки тканей почек, печени и других органов; -лекарственные АГ, вторично фиксированные на мембранах; - неклеточные структурные белки, например – коллаген В ответ на появление измененных клеток образуются антитела (классы IgG и IgM). Антитела соединяются с соответствующими аутоаллергенами клеток. В результате возможно включение одного из двух цитотоксических механизмов: 1. Комплементарного механизма. При активации этого механизма образуются активные фрагменты комплемента, вызывающие повреждение клеток и даже их разрушение. 2. Механизма антителозависимой клеточно-опосредованной цитотоксичности. К антителам, фиксированным на поверхности клеток-мишеней, присоединяются так называемые К-клетки (вид лимфоцитов, активирующих в клетках-мишенях апоптоз). К-лимфоциты при контакте с клеткой-мишенью вызывают активацию гена (гена смерти), ответственного за продукцию эндонуклеаз. Эндонуклеазы вызывают фрагментацию ДНК. Кроме того, К-лимфоциты, как и макрофаги, эозинофилы и нейтрофилы, продуцируют супероксид, который повреждает клетку-мишень. Поврежденные клетки фагоцитируются макрофагами. Вид механизма зависит от характера антител (класс, подкласс) и их количества, фиксированного на поверхности клетки. К реакциям цитотоксического типа относятся такие проявления аутоаллергии, как лейкопения, тромбоцитопения, гемолитическая анемия, иммунный тиреоидит и др. Такие же реакции наблюдаются при попадании в организм аллогенных антигенов, например при переливании крови (в виде аллергических реакций на гемотрансфузию), и гемолитической болезни новорожденных. 1. Защитная роль реакций цитотоксического типа - когда реакция идет против микроорганизмов, простейших, опухолевых клеток, отработавших свой срок клеток организма. Такая цитотоксическая реакция встречается и в норме, т. е идет без повреждения здоровых клеток. 2. Патогенная роль реакций цитотоксического типа - реакция из иммунной переходит в аллергическую, повреждает и разрушает ткани, если направлена против клеток, которые стали аутоантигенными. 73. Болезни иммунных комплексов (сывороточная болезнь). Виды. Причины, механизмы развития, профилактика. Связывание антигенов антителами и доставка иммунных комплексов к мембранам собственных клеток, имеющих рецепторы к иммуноглобулинам - это один из главных механизмов удаления патогенов из внутренней среды организма. В норме иммунные комплексы при участии системы комплемента фиксируются на эритроцитах . В синусоидах селезенки и печени, где кровоток становится турбулентным, нагруженные иммунными комплексами эритроциты захватываются макрофагами и уничтожаются. |
