Пневмония и плеврит. Пневмонии и плевриты. Нетипируемая H. influenzae чаще вызывает вп у пациентов с сопутствующей хронической обструктивной болезнью легких (хобл)
 Скачать 1.57 Mb. Скачать 1.57 Mb.
|
|
Пневмонии Пневмонии – группа различных по этиологии, патогенезу, морфологической характеристике острых инфекционных (преимущественно бактериальных) заболеваний, характеризующихся очаговым поражением респираторных отделов легких с обязательным наличием внутриальвеолярной экссудации. Пневмонии четко обособлены от других очаговых воспалительных заболеваний легких неинфекционного происхождения, вызываемых физическими (например, лучевой пневмонит) или химическими факторами, имеющих аллергическое (например, эозинофильная пневмония) или сосудистое (например, инфаркт легкого) происхождение. Наиболее важный с клинической точки зрения принцип предусматривает подразделение пневмонии на внебольничную и нозокомиальную (НП). Внебольничной считают пневмонию, развившуюся вне стационара, либо диагностированную в первые 48 ч с момента госпитализации. Этиология Перечень потенциальных возбудителей ВП включает более 100 микроорганизмов (бактерии, вирусы, грибы, простейшие). Однако большинство случаев заболевания ассоциируется с относительно небольшим кругом патогенов, к которым относят Streptococcus pneumoniae, M. pneumoniae, C. pneumoniae, H. influenzae, респираторные вирусы, энтеробактерии, S. aureus и L. pneumophila. Streptococcus pneumoniae – самый частый возбудитель, на его долю приходится до 30-50% случаев ВП установленной этиологии. При нетяжелом течении ВП актуальными являются M. pneumoniae и C. pneumoniae - их доля в этиологической структуре суммарно достигает 20-30%. Нетипируемая H. influenzae чаще вызывает ВП у пациентов с сопутствующей хронической обструктивной болезнью легких (ХОБЛ); K. pneumoniae и E. coli (реже других представителей Enterobacterales) выявляют преимущественно у лиц с хроническими сопутствующими заболеваниями, такими как сахарный диабет (СД), хроническая сердечная недостаточность (ХСН), алкоголизм, цирроз печени и при ТВП. S. aureus чаще ассоциируется с развитием ВП у лиц пожилого возраста, в/в наркоманов, на фоне или после перенесенного гриппа; P. aeruginosa – с муковисцидозом, бронхоэктазами, применением системных глюкокортикостероидов (ГКС) в фармакодинамических дозах, предшествующей длительной АБТ. Удельный вес L. pneumophila, очевидно, является невысоким в общей популяции в РФ, однако значимость данного возбудителя существенно увеличивается при ТВП и наличии определенных факторов риска Вероятность инфицирования анаэробами может возрастать у лиц с доказанной или предполагаемой аспирацией, обусловленной эпизодами нарушения сознания при судорогах, некоторых неврологических заболеваниях (например, инсульт), дисфагии, алкоголизме. Частота встречаемости других бактериальных возбудителей - C. psittaci, S. pyogenes, B. pertussis и др. обычно не превышает 2-3%, а поражения легких, вызванные эндемичными микромицетами в России встречаются чрезвычайно редко. ВП помимо бактериальных возбудителей могут вызывать респираторные вирусы, наиболее часто вирусы гриппа, коронавирусы, риносинцитиальный вирус, метапневмовирус человека, бокавирус человека. Частота выявления респираторных вирусов у пациентов с ВП носит выраженный сезонный характер и возрастает в холодное время года. Различают первичную вирусную пневмонию (развивается в результате непосредственного вирусного поражения легких) и вторичную бактериальную пневмонию, которая может сочетаться с первичным вирусным поражением легких или быть самостоятельным поздним осложнением респираторной вирусной инфекции (в первую очередь гриппа). В большинстве случаев ВП, вызываемые респираторными вирусами, характеризуются нетяжелым течением, однако у лиц пожилого и старческого возраста, при наличии сопутствующих бронхолегочных, сердечно-сосудистых заболеваний или иммунодефицита они могут ассоциироваться с развитием тяжелых, угрожающих жизни осложнений. У 10-30% пациентов с ВП выявляется смешанная или ко-инфекция, которая может быть вызвана ассоциацией различных бактериальных возбудителей (например, Streptococcus pneumoniae с H. influenzae или M. pneumoniae), либо их сочетанием с респираторными вирусами. ВП, вызванная ассоциацией возбудителей, имеет тенденцию к более тяжелому течению и худшему прогнозу. Необходимо отметить тот факт, что, несмотря на расширение возможностей для микробиологической диагностики, примерно у половины пациентов с ВП этиологический диагноз остается неустановленным. Патогенез Известно четыре патогенетических механизма, которые могут обуславливать развитие ВП [1, 2]: аспирация секрета ротоглотки; вдыхание аэрозоля, содержащего микроорганизмы; гематогенное распространение микроорганизмов из внелегочного очага инфекции; непосредственное распространение инфекции из соседних пораженных органов или в результате инфицирования при проникающих ранениях грудной клетки. Аспирация секрета ротоглотки – основной путь инфицирования респираторных отделов легких и основной патогенетический механизм развития ВП. В нормальных условиях ряд микроорганизмов, например анаэробы, S. pneumoniae, H. influenzae могут колонизировать ротоглотку, но нижние отделы дыхательных путей остаются в большинстве случаев стерильными. Микроаспирация секрета ротоглотки – физиологический феномен, наблюдающийся у многих здоровых лиц, преимущественно во время сна. Однако кашлевой рефлекс, мукоцилиарный клиренс, антибактериальная активность альвеолярных макрофагов и секреторных иммуноглобулинов обеспечивают элиминацию инфицированного секрета из нижних отделов дыхательных путей и поддерживают их стерильность. При повреждении механизмов «самоочищения» трахеобронхиального дерева создаются благоприятные условия для развития пневмонии. В отдельных случаях самостоятельным патогенетическим фактором могут быть массивность дозы микроорганизмов или проникновение в респираторные отделы легких даже единичных высоковирулентных изолятов. С учетом особенностей патогенеза ВП очевидно, что ее этиология в подавляющем большинстве случаев связана с микрофлорой верхних отделов дыхательных путей, состав которой зависит от внешней среды, возраста пациента, сопутствующих заболеваний, предшествующей АБТ. Ингаляция микробного аэрозоля встречается реже, данный механизм играет основную роль при инфицировании нижних отделов дыхательных путей облигатными патогенами, например Legionella spp. Клиническая картина Клинические симптомы и признаки ВП широко варьируются, что обусловлено такими факторами, как различный объем и локализация поражения, вид возбудителя, выраженность “ответа” макроорганизма на инфекцию. Для ВП характерны острый кашель, одышка, отделение мокроты и/или боли в грудной клетке, связанные с дыханием, которые в большинстве случаев сопровождаются лихорадкой. Больные, переносящие пневмонию, часто жалуются на немотивированную слабость, утомляемость, ознобы, сильное потоотделение по ночам. Развитию ВП может предшествовать поражение верхних дыхательных путей или острый бронхит. У лиц пожилого и старческого возраста типичные жалобы могут отсутствовать, а на первый план в клинической картине заболевания выходит синдром интоксикации (сонливость или беспокойство, спутанность сознания, анорексия, тошнота, рвота) или декомпенсация хронических сопутствующих заболеваний (СД, ХСН и др.). Изменению классической картины заболевания способствует самолечение АБП. При тяжелой пневмонии клиническая картина заболевания может дополняться развитием септического шока, острой ДН и/или другой органной дисфункции. Несмотря на наличие определенных особенностей в клинической картине и течении ВП разной этиологии (например, для пневмококковой характерны острое начало, высокая лихорадка, боли в грудной клетке, для легионеллезной – диарея, неврологическая симптоматика, для микоплазменной - мышечные и головные боли, симптомы поражения верхних дыхательных путей), каких-либо закономерностей, позволяющих с высокой степенью надежности предсказать возбудителя заболевания без использования дополнительных методов исследования в настоящее время не существует. Диагностика Диагностические исследования при ВП направлены на верификацию диагноза, идентификацию возбудителя, оценку тяжести течения и прогноза заболевания, выявление осложнений. Критерии установления диагноза Диагноз ВП является определенным при наличии у пациента рентгенологически подтвержденной очаговой инфильтрации легочной ткани и, по крайней мере, двух клинических симптомов и признаков из числа следующих: остро возникшая лихорадка в начале заболевания (t > 38,0°С); кашель с мокротой; физические признаки (фокус крепитации/мелкопузырчатых хрипов, бронхиальное дыхание, укорочение перкуторного звука); лейкоцитоз > 10х109 /л и/или палочкоядерный сдвиг (> 10%). При этом необходимо учитывать и вероятность терапевтической альтернативы - известных синдромосходных заболеваний/патологических состояний. Жалобы и анамнез У всех пациентов с подозрением на ВП рекомендуется провести оценку жалоб, социального статуса и семейно-бытовых условий, собрать полный медицинский, эпидемиологический и профессиональный анамнез. Сбор анамнеза, оценка социального статуса и семейно-бытовых условий важны для уточнения факторов риска инфицирования определенными возбудителями ВП и дифференциальной диагностики пневмонии с другими заболеваниями. Ряд хронических сопутствующих заболеваний при ВП относится к независимым предикторам неблагоприятного прогноза Физическое обследование У всех пациентов с ВП рекомендуется провести общий осмотр, измерить показатели жизнедеятельности (ЧДД, ЧСС, АД, температура тела) и выполнить детальное обследование грудной клетки. Данные, получаемые при физическом обследовании, зависят от многих факторов, включая распространенность и локализацию пневмонической инфильтрации, степень тяжести ВП, возраст пациента, наличие сопутствующих заболеваний. Классическими объективными признаками являются отставание пораженной стороны грудной клетки при дыхании, усиление голосового дрожания, укорочение (притупление) перкуторного звука над пораженным участком легкого, появление бронхиального дыхания, наличие фокуса мелкопузырчатых хрипов или крепитации, усиление бронхофонии. Нужно иметь ввиду, что у части пациентов объективные признаки могут отличаться от типичных или вообще отсутствовать, что не исключает диагноза ВП. Лабораторная диагностика Всем пациентам с ВП рекомендуется выполнение общего (клиинческого) анализа крови с определением уровня эритроцитов, гематокрита, лейкоцитов, тромбоцитов, лейкоцитарной формулы. Данные общего анализа крови не являются специфичными и не позволяют высказаться о потенциальном возбудителе ВП. Однако лейкоцитоз >10-12*109/л с повышением уровня нейтрофилов и/или палочкоядерный сдвиг >10%, нейтрофильнолимфоцитарное соотношение > 20, указывают на высокую вероятность бактериальной инфекции; лейкопения <4 * 109 /л, тромбоцитопения <100*1012/л и гематокрит <30% являются неблагоприятными прогностическими признаками при ВП. Всем госпитализированным пациентам с ВП рекомендуется выполнить биохимический анализ крови (мочевина, креатинин, электролиты, печеночные ферменты, билирубин, глюкоза, альбумин). Биохимический анализ крови не дает какой-либо специфической информации при ВП, но обнаруживаемые отклонения могут указывать на наличие органной дисфункции, декомпенсацию сопутствующих заболеваний и развитие осложнений, имеют определенное прогностическое значение, оказывают влияние на выбор ЛС и/или режим их дозирования. Всем госпитализированным пациентам с ВП рекомендуется исследование уровня С-реактивного белка (СРБ) в сыворотке крови. Уровень СРБ коррелирует с тяжестью течения, распространенностью воспалительной инфильтрации и прогнозом при ВП [50-55]. Наиболее ценным с практической точки зрения является исследование уровня СРБ у лиц с неопределенным диагнозом ВП (отсутствие воспалительной инфильтрации у пациентов с характерным анамнезом, жалобами и локальными симптомами, свидетельствующими в пользу легочной консолидации); при концентрации >100 мг/л его специфичность в подтверждении диагноза превышает 90%. Напротив, при концентрации <20 мг/л диагноз пневмонии является маловероятным. Отсутствие значимого снижения уровня СРБ на фоне АБТ у госпитализированных пациентов с ВП является предиктором более высокой летальности. Всем госпитализированным пациентам с ВП, осложненной парапневмоническим плевритом, рекомендуется биохимическое (определение рН, активности лактатдегидрогеназы, содержания белка) и цитологическое исследование плевральной жидкости. Исследование проводится при наличии плеврального выпота и условий безопасного проведения плевральной пункции (визуализация на латерограмме свободно смещаемой жидкости с толщиной слоя > 1,0 см). Всем госпитализированным пациентам с ВП, осложненной ОДН (SрO2 < 90% по данным пульсоксиметрии) рекомендуется исследование газов артериальной крови с определением PaO2, PaCO2, pH, бикарбонатов, лактата. Всем пациентам с ТВП рекомендуется выполнение коагулограммы с определением протромбинового времени, международного нормализованного отношения и активированного частичного тромбопластинового времени. Лечение Лечение пациентов с ВП предполагает комплекс мероприятий, включающих назначение АБП, адекватную респираторную поддержку, применение по показаниям неантибактериальных ЛС и профилактику осложнений. Чрезвычайно важным является своевременное выявление и лечение декомпенсации/обострения сопутствующих заболеваний. 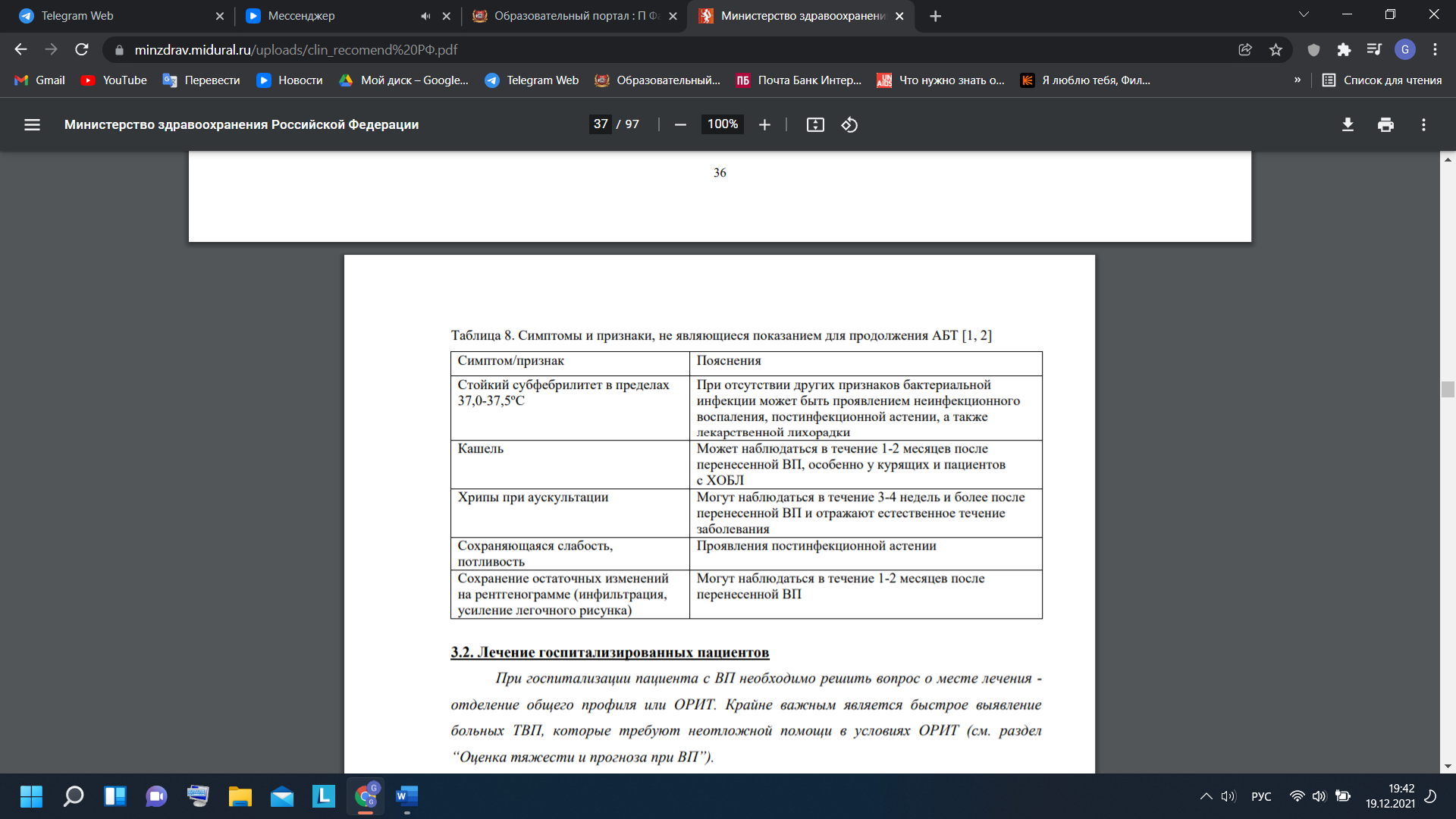 Антибактериальная терапия ВП у амбулаторных пациентов 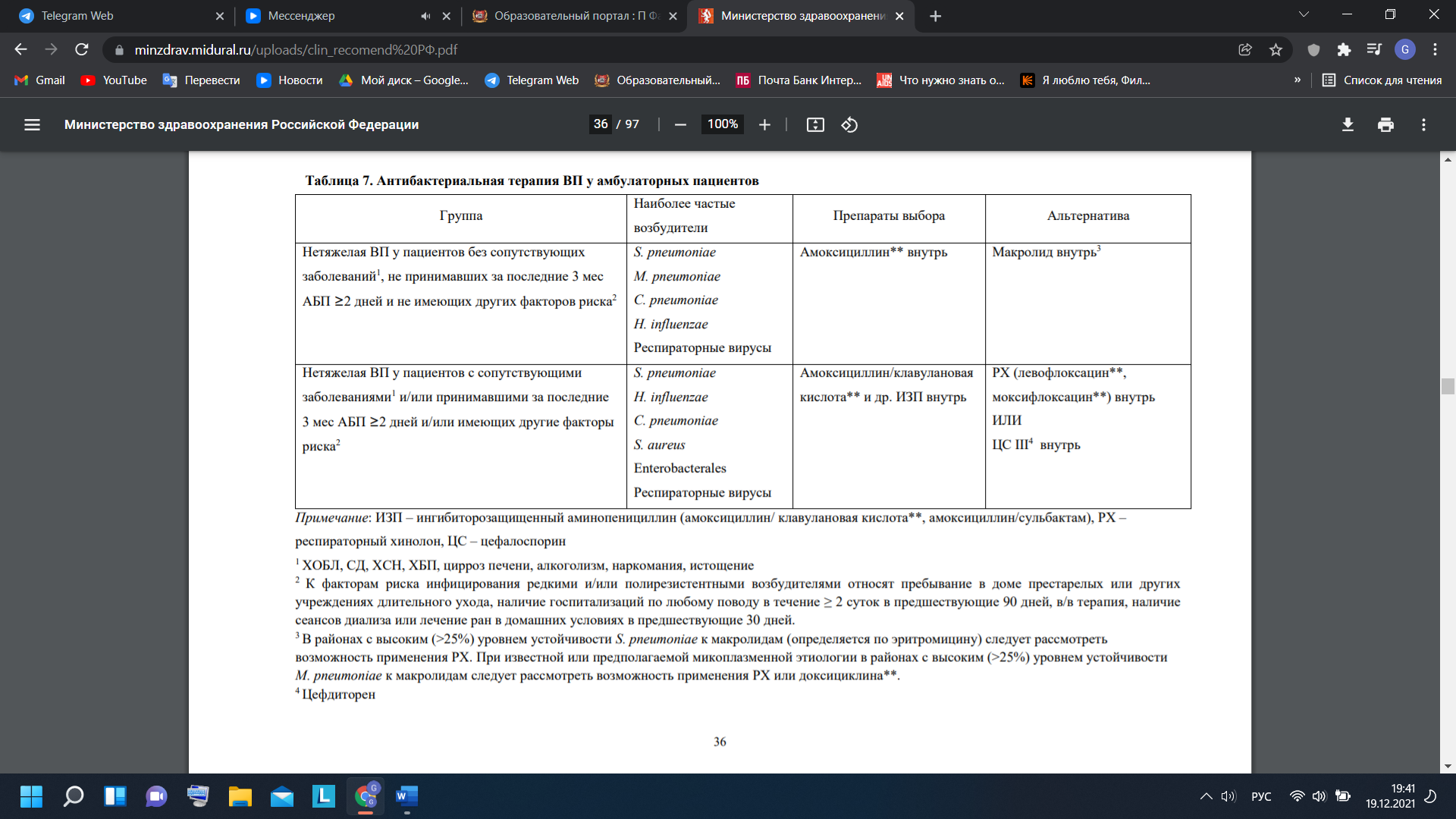 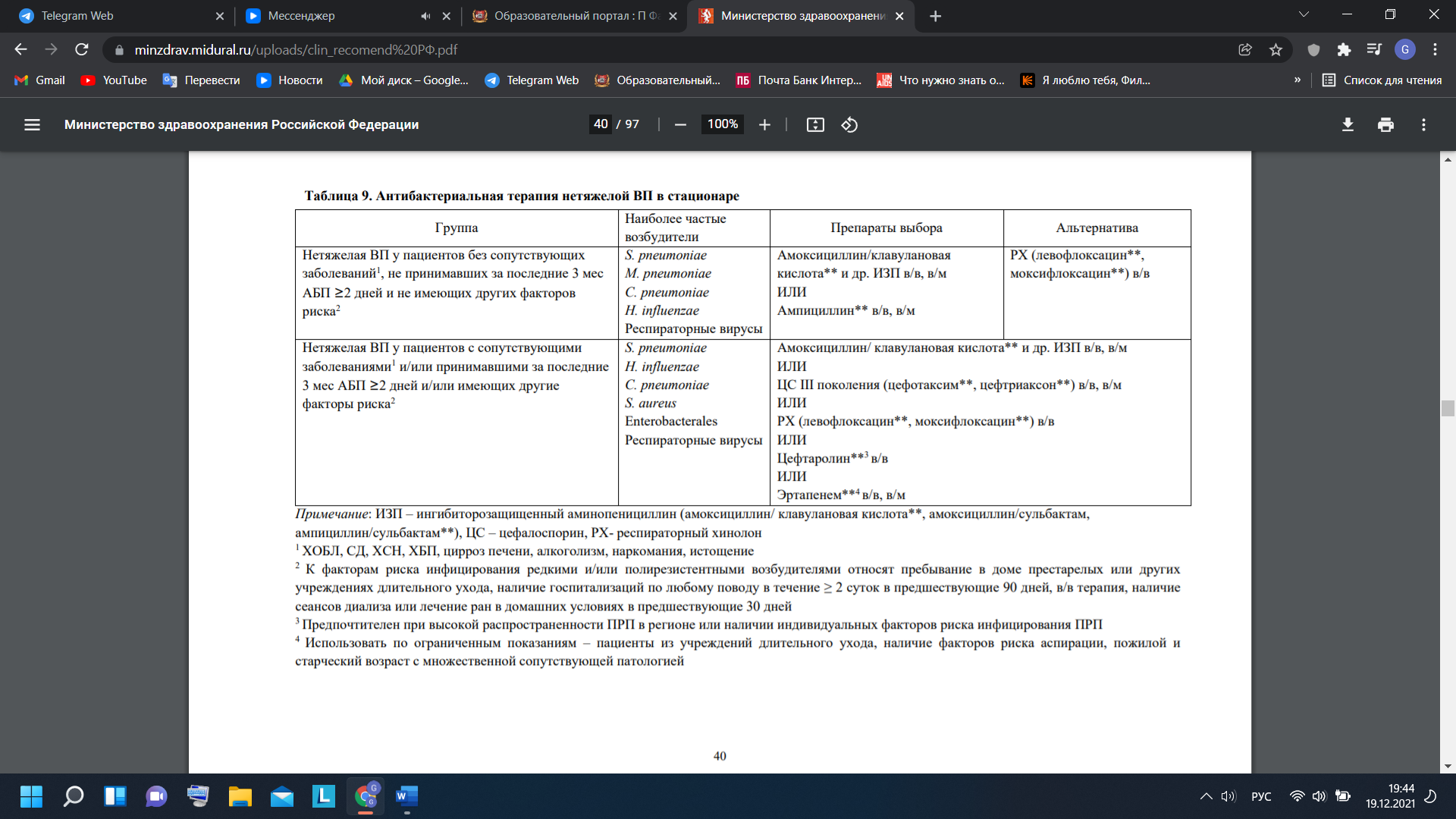 Всем госпитализированным пациентам с ВП рекомендуется перевод с парентерального на пероральный прием АБП при достижении критериев клинической стабильности (должны присутствовать все ниже перечисленные) [1, 12, 59, 110]: cнижение температуры тела до субфебрильных цифр (<37,8ºC) при двух измерениях с интервалом 8 ч; отсутствие нарушений сознания; частота дыхания < 24/мин; частота сердечных сокращений < 100/мин; систолическое АД > 90 мм рт ст; SpO2 > 90% или PaO2 > 60 мм рт ст (артериальная кровь) ; отсутствие нарушений всасывания в ЖКТ. Плеврит Плевральный выпот – это скопление жидкости в плевральной полости, обусловленное различными причинами. Плевральный выпот делится на транссудат и экссудат. Для выявления причины плеврального выпота выполняется пункция плевральной полости с последующим исследованием полученной жидкости. Диагноз ставится на основани данных объективного обследования и рентгенографии органов грудной клетки. При наличии бессимптомного транссудата лечение не требуется. Если транссудат сопровождается клинической симптоматикой или имеется экссудат, проводятся пункция и дренирование плевральной полости, плеврэктомия или комбинация этих методов. В норме в плевральной полости находится 10–20 мл жидкости, которая по составу сходна с плазмой крови, но имеет более низкое содержание белка (менее 1,5 г/дл [< 15 гр/л]). Жидкость распределена между висцеральным и париетальным листками плевры и обеспечивает их скольжение относительно друг друга. Жидкость поступает в плевральную полость из системных капилляров париетальной плевры и оттекает по устьям и лимфатическим сосудам париетальной плевры. В конечном итоге жидкость попадает в правое предсердие, поэтому клиренс отчасти зависит от давления справа. Накопление жидкости в плевральной полости происходит при избыточном поступлении или медленном выведении. Этиология плеврального выпота Плевральные выпоты обычно классифицируются как Транссудаты Экссудаты Классификация выпотов основана на лабораторных характеристиках жидкости. Независимо от того, является транссудат односторонним или двусторонним, его обычно можно лечить без проведения обширных обследований, в то время как причина его появления требует изучения. Есть множество причин. Транссудат образуется при увеличении гидростатического давления и уменьшении онкотического давления плазмы. Наиболее частой причиной появления транссудата является сердечная недостаточность, реже – цирроз печени с асцитом и гипоальбуминемия, обусловленная нефротическим синдромом. Экссудат образуется при наличии местных процессов, приводящих к увеличению проницаемости капилляров, в результате в плевральную полость попадает плазма крови, белок, форменные элементы и другие компоненты. Наиболее частыми причинами появления экссудата являются: пневмония, рак, тромбоэмболия легочной артерии, вирусная инфекция, туберкулез. Синдром жёлтых ногтей - это редкое расстройство, которое проявляется в хронических экссудативных плевральных выпотах, лимфедеме и дистрофических желтых ногтях - все эти симптомы считаются результатом нарушения лимфооттока. Хилезный выпот (хилоторакс) – это выпот молочно-белого цвета с высоким содержанием триглицеридов, в результате травматических или опухолевых (как правило, лимфомы) повреждений грудного лимфатического протока. Хилоторакс также наблюдается при синдроме верхней полой вены. Лимфоподобный (холестериновый или псевдохиллезный) выпот напоминает хилезный выпот, но имеет низкое содержание триглицеридов и высокое содержание холестерина. Считается, что лимфоподобный выпот появляется в результате высвобождения холестерина из лизированных эритроцитов и нейтрофилов при длительно существующем выпоте, когда отток жидкости из плевральной полости нарушается вследствие утолщения плевры. Гемоторакс – это скопление крови в плевральной полости (гематокрит плеврального выпота составляет > 50% гематокрита периферической крови), обусловленное травмой, реже – коагулопатией или разрывом крупного сосуда - аорты или легочной артерии. Эмпиема плевры – это скопление гноя в плевральной полости. Эмпиема плевры может быть осложнением пневмонии, торакотомии, абсцесса легкого, абсцесса печени, поддиафрагмального абсцесса, проникающей травмы (вторичная инфекция). Самопроизольное вскрытие эмпиемы приводит к проникновению гноя в мягкие ткани, инфицированию грудной стенки и наружному дренированию гнойного очага. Панцирное легкое – это легкое, покрытое фиброзной капсулой, появление которой обусловлено эмпиемой плевры или опухолью. Поскольку легкое не расправляется, давление в плевральной полости снижается, что приводит к транссудации плазмы крови из капилляров париетальной плевры. По содержанию различных компонентов плевральный выпот при панцирном легком представляет собой нечто среднее между транссудатом и экссудатом, т.е. увеличение биохимических показателей не превышает 15% согласно критериям Лайта. Ятрогенный плевральный выпот может быть вызван миграцией или смещением пищевого зонда в трахею или перфорацией верхней полой вены центральным венозным катетером, что приводит к попаданию пищи или растворов, вводимых внутривеннно, в плевральную полость. Плевральный выпот без видимой причины возникает при бессимптомной тромбоэмболии легочной артерии, туберкулезе или раке. В 15% случаев причину установить не удается даже после тщательного обследования. Во многих случаях появление плеврального выпота обусловлено вирусной инфекцией. Симптомы и признаки плеврального выпота В некоторых случаях плевральный выпот протекает бессимптомно и является случайной находкой при объективном обследовании или рентгенографии грудной клетки. К симптомам плеврального выпота относится одышка и/или плевритическая боль. Плевритическая боль, неопределенный дискомфорт или острая боль в грудной клетке, которая усиливается на вдохе, указывают на воспаление париетального листка плевры. Как правило, боль локализуется в зоне воспаления, но может наблюдаться иррадиация. Задняя и периферические части диафрагмальной плевры иннервируют 6 нижних межреберных нервов и их раздражение вызывает боль в нижних отделах грудной клетки или в брюшной полости. Раздражение центральной части диафрагмальной плевры, которую иннервируют диафрагмальные нервы, вызывает боль, иррадиирущую в шею и плечо. При объективном обследовании наблюдается отсутствие голосового дрожания, притупление перкуторного звука и ослабленное дыхание на стороне выпота. Указанные симптомы могут быть вызваны утолщением плевры. При большом объеме выпота дыхание частое и поверхностное. Классическим симптомом является шум трения плевры, хотя он встречается нечасто. Его выраженность варьирует от непостоянных звуков, напоминающих потрескивание, до интенсивного хруста на вдохе и выдохе. Шум трения рядом с сердцем (плевроперикардиальный шум) может варьироваться в зависимости от сердечного ритма и может быть спутан с шумом трения перикарда. Шум трения перикарда лучше всего прослушивается по левой границе грудины в 3-м и 4-м межреберном пространстве, имеет характерное пилящие звучание, синхронное с сердцебиением, и существенно не изменяется при дыхании. Чувствительность и специфичность объективного обследования для выявления выпота, вероятно, низкие. Диагностика плеврального выпота В некоторых случаях КТ-ангиография или другие методы исследования  Плевральный выпот следует заподозрить при наличии плевритической боли, необъяснимой одышки и других симптомов. Диагностические исследования назначаются с целью подтверждения наличия плеврального выпота и определения его причины. Для подтверждения наличия плеврального выпота, прежде всего, проводится рентгенография органов грудной клетки в положении стоя. При подозрении на плевральный выпот необходимо проанализировать снимок в боковой проекции. Затемнение в области заднего реберно-диафрагмального синуса свидетельствует о наличии 75 мл жидкости. При затемнении латерального реберно-диафрагмального синуса объем плеврального выпота составляет не менее 175 мл, но может достигать 500 мл. Большой плевральный выпот визуализируется как затемнение части легочного поля, может наблюдаться смещение средостения; если объем выпота > 4 л, может наблюдаться затемнение всего легочного поля и смещение средостения в противоположную сторону. Ограниченный выпот формируется при наличии плевральных спаек или располагается в междолевых щелях. Если природа затемнения не ясна или не удается определить, является ли выпот ограниченным или свободным, необходимо выполнить рентгенографию органов грудной клетки в боковой проекции в положении лежа, КТ органов грудной клетки или ультразвуковое исследование. Данные исследования более чувствительны, чем рентгенография в положении стоя, и позволяют обнаружить жидкость объемом менее 10 мл. Ограниченный выпот, особенно в горизонтальной или косой междолевых щелях, может быть ошибочно принят за солидное образование (ложная опухоль). Форма и размеры выпота меняются при изменении положения пациента и количества жидкости. КТ регулярно используется для оценки паренхимы легкого, закрытой выпотом, на предмет наличия инфильтратов или опухолей, для уточненя данных рентгенографии, для дифференциальной диагностики ограниченного выпота и солидных образований. Причина плеврального выпота Пункция плевральной полости проводится практически всем пациентам, у которых объем плеврального выпота по данным КТ, ультразвукового исследования или рентгенографии в боковой проекции в положении лежа составляет ≥ 10 мм, а также пациентам, у которых выпот выявлен впервые, или с выпотом неустановленной этиологии. В целом, при сердечной недостаточности с симметричным плевральным выпотом, отсутствии боли в груди или лихорадки пункция плевральной полости не нужна – таким пациентам показаны диуретики; пункция плевральной полости проводится только в том случае, если выпот сохраняется в течение ≥3 дней. Если плевральный выпот носит хронический характер, его причина установлена и он имеет бессимптомное течение, пункция плевральной полости не проводится. Здравый смысл и предостережения Рентгенография органов грудной клетки после пункции плевральной проводится тольков при появлении симптомов, позволяющих заподозрить пневмоторакс (одышка или боль в груди), или в том случае, если в плевральную полость мог попасть воздух. При возможности выполняют торакоцентез под ультрасонографическом контролем, что увеличивает выход жидкости и снижает риск осложнений, таких как пневмоторакс или прокол внутрибрюшинных органов. Исследование плеврального выпота выполняется с целью установления его причины. Сначала проводится визуальная оценка, которая позволяет: Дифференцировать геморрагический и хилезный (или лимфоподобный) выпот с другими видами выпота Установить наличие гнойного выпота, свидетельствующего об эмпиеме плевры Оценить вязкость выпота, поскольку выпот высокой вязкости характерен для некоторых мезотелиом В дальнейшем необходимо определить общий белок, лактатдегидрогеназу (ЛДГ), клеточный состав с подсчетом количества клеток, провести окрашивание по Граму и выполнить посев на аэробные и анаэробные питательные среды. В определенных клинических ситуациях проводят другие тесты: измерение уровня глюкозы, цитологическое исследование, тест на маркеры туберкулеза (аденозиндезаминаза или интерферон-гамма), измерение уровня амилазы, окрашивание и посев на микобактерии и грибы. Анализ жидкости позволяет дифференцировать транссудат от экссудата; существует большое количество критериев, которые позволяют дифференцировать 2 вида выпота, но ни один из них не является универсальным. При использовании критериев Лайта (см. таблицу Критерии экссудативного плеврального выпота) необходимо определить уровень ЛДГ и общего белка в сыворотке крови, а затем сравнить с показателями для плеврального выпота. Критерии Лайта позволяют почти всегда выявить экссудат, однако в 20% случаев ошибочно определяет транссудат как экссудат. При подозрении на транссудат (например, сердечная недостаточность или цирроз печени), в том случае когда увеличение биохимических показателей не превышает < 15% согласно критериям Лайта, используется разница содержания белка в сыворотке крови и плевральном выпоте. Если разница составляет > 3,1 г/дл (> 31 гр/л), следует думать о транссудате. Также может быть полезной визуализация. Если анализ плеврального выпота не позволяет поставить диагноз, выполняется КТ-ангиография. Она используется для выявления эмболов в легочной артерии, инфильтратов легких или поражения средостения. При наличии эмболов пациенту назначается длительная антикоагулянтная терапия, при наличии паренхиматозного инфильтрата проводится бронхоскопия, при поражениях средостения – трансторакальная аспирационная биопсия или медиастиноскопия. Однако при выполнении КТ-ангиографии пациент должен задержать дыхание как минимум на 24 секунды; не все пациенты могут это сделать. Если КТ-ангиография также не позволяет установить диагноз, при наличии симптомов, указывающих на рак или туберкулез (снижение массы тела, лихорадка и т.д.), проводится торакоскопия. Если не удается выполнить торакоскопию, проводится пункционная биопсия плевры. Если присутствуют плевральное утолщение или плевральные узелки, КТ или ультразвуковая биопсия будут полезными для диагностики. При подозрении на туберкулезный плеврит определяют уровень аденозин дезаминазы в плевральном выпоте. Уровень > 40 ед/л (667 нкат/л) имеет чувствительность 95% и специфичность для диагностики туберкулезного плеврита. Лечение плеврального выпота Проводится симптоматическое лечение и лечение основного заболевания При наличии симптомов некоторым пациентам проводится дренирование При парапневмоническом и злокачественном выпоте используются другие методы лечения При бессимптомном течении сам по себе выпот, как правило, не требует лечения, поскольку во многих случаях он разрешается спонтанно на фоне лечения основного заболевания, особенно при неосложненной пневмонии, тромбоэмболии легочной артерии или хирургических вмешательствах. Плевритическая боль купируется с помощью нестероидных противовоспалительных препаратов (НПВП) или других пероральных анальгетиков. Лишь в некоторых случаях требуется короткий курс пероральных опиоидов. При наличии симптомов проводится пункция плевральной полости; если выпот рецидивирует, пункция выполняется повторно. Не существует однозначных пределов относительно объема жидкости, который можно удалить (1). Эвакуация выпота проводится до тех пор, пока полученный у пациента выпот не приводит к появлнию сдавления в груди, боли в груди или сильного кашля. При хроническом, рецидивирующем выпоте, сопровождающимся клинической симптоматикой, проводят плевродез или устанавливают постоянный катетер. При парапневмоническом и злокачественном выпоте требуются дополнительные методы лечения. Парапневмонический выпот и эмпиема плевры При наличии неблагоприятных прогностических факторов (pH < 7,20, глюкоза < 60 мг/дл (< 3,33 ммоль/л), положительные результаты мазка с окраской по Граму или положительный результат посева, ограниченный выпот) необходимо полностью удалить выпот с помощью плевральной пункции или установки катетера. При невозможности полного дренирования используется внутриплевральное введения тромболитических (фибринолитических) средств (например, активатор тканевого плазминогена 10 мг) с ДНКазой (например, дорназа альфа 5 мг) на 100 мл физиологического раствора два раза в день в течение 3-х дней. При отсутствии эффекта выполняется торакоскопия, целью которой является удаление спаек и фиброзной капсулы, что обеспечивает расправление легкого. При отсутствии эффекта выполняется торакотомия и декортикация легкого (с удалением спаек, сгустков или фиброзной капсулы, окружающих легкое). Злокачественный плевральный выпот Если при злокачественном плевральном выпоте после пункции плевральной полости вновь появляется одышка и накапливается жидкость, в плевральную полость устанавливают катетер или проводят плевродез. Бессимптомный выпот и выпот, вызывающий одышку, которая не купируется после пункции плевральной полости, не требуют дополнительного лечения. Предпочтительным методом лечения для амбулаторных пациентов является установка постоянного катетера, поскольку для установки катетера госпитализация не требуется, а выпот непрерывно эвакуируется в вакуумные флаконы. Плевродез производится путем введения склерозирующего средства в плевральную полость с целью сращения висцерального и париетального листков плевры и облитерации плевральной полости. К наиболее эффективным склерозирующим средствам относится тальк, доксициклин и блеомицин; их вводят через катетер или во время торакоскопии. Плевродез противопоказан при смещении средостения в сторону выпота и при отсутствии расправления легкого после установки катетера. Шунтирование плеврального выпота в брюшную полость (плевроперитонеальный шунт) применяется при злокачественном выпоте при отсутствии эффекта от плевродеза и наличии панцирного легкого. |
