Ответы Физиология. Нормальная физиология как научная основа медицины, её связь с другими науками
 Скачать 1.62 Mb. Скачать 1.62 Mb.
|
Импульсы, возникшие в синусном узле, распространяются по мускулатуре предсердий. Дойдя до атриовентрикулярного узла, волна возбуждения распространяется по пучку Гиса, а затем по волокнам Пуркинье. Благодаря проводящей системе сердца наблюдается последовательное сокращение частей сердца: сначала сокращаются предсердия, затем желудочки (начиная с верхушки сердца волна сокращения распространяется к их основанию). Особенность атриовентрикулярного узла - проведение волны возбуждения только в одном направлении: от предсердий к желудочкам. Сократимость - это способность миокарда сокращаться. Оно основано на способности самих клеток миокарда отвечать на возбуждение сокращением. Это свойство сердечной мышцы определяет способность сердца выполнять механическую работу. Работа сердечной мышцы подчиняется закону "все или ничего".Суть этого закона состоит в следующем: если на сердечную мышцу наносить раздражающее действие различной силы, мышца отвечает каждый раз максимальным сокращением ("все"). Если сила раздражителя не достигает порогового значения, то сердечная мышца не отвечает сокращением ("ничего"). Закон сердца Старлинга: при увеличении кровенаполнения сердца в диастолу и, следовательно, при увеличении растяжения мышцы сердца сила сердечных сокращений возрастает. В условиях целостного организма действие закона Франка — Старлинга ограничено влиянием других механизмов регуляции деятельности сердца. Особенности потенциала действия кардиомиоцитов желудочков В состоянии покоя внутренняя поверхность мембран кардиомиоцитов заряжена отрицательно. Потенциал покоя определяется в основном трансмембранным градиентом концентрации ионов К+ и у большинства кардиомиоцитов (кроме синусового узла и АВ-узла) составляет от минус 80 до минус 90 мВ. При возбуждении в кардиомиоциты входят катионы, и возникает их временная деполяризация - потенциал действия. Ионные механизмы потенциала действия в рабочих кардиомиоцитах и в клетках синусового узла и АВ-узла разные, поэтому и форма потенциала действия также различается. У потенциала действия кардиомиоцитов системы Гиса-Пуркинье и рабочего миокарда желудочков выделяют пять фаз. Фаза быстрой деполяризации (фаза 0) обусловлена входом ионов Na+ по так называемым быстрым натриевым каналам . Затем, после кратковременной фазы ранней быстрой реполяризации (фаза 1), наступает фаза медленной деполяризации, или плато (фаза 2). Она обусловлена одновременным входом ионов Са2+ по медленным кальциевым каналам и выходом ионов К+. Фаза поздней быстрой реполяризации (фаза 3) обусловлена преобладающим выходом ионов К+. Наконец, фаза 4 - это потенциал покоя. 7.Потенциал действия кардиомиоцитов желудочков, его фазы, ионный механизм, графическое изображение. Потенциал действия кардиомиоцитажелудочка - это неспецифический эффект его возбуждения. | ||||||||||
| | |
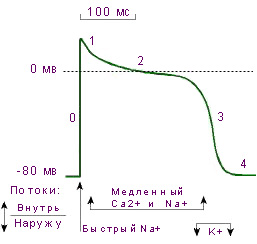
| Схема. Потенциал действия сократительного кардиомиоцита. В нижней части схемы показаны потоки различных ионов через сарколемму. См.: рис. управление сокращением и расслаблением кардиомиоцита. | |
 | |
| | |
Как и в любых возбудимыхклетках, возбуждение кардиомиоцитов начинается быстрой деполяризацией его мембраны до нулевого уровня, которая продолжается быстрой сменой знака полярности с отрицательной на положительную (реверсия потенциала), фаза 0 на схеме. Этим быстрым изменением полярности мембраны кардиомиоцита с уровня потенциала покоя (-80 мВ) до (+30 мВ) начинается потенциал действия кардиомиоцита. Длительность фазы деполяризации и реверсии знака потенциала мембраны составляет 1 ÷ 2 мс. За этой фазой следует фаза реполяризации.
В отличие от фазы реполяризации других возбудимых клеток фаза реполяризации кардиомиоцита имеет специфическую особенность. Сначала реполяризация осуществляется быстро (фаза 1 на схеме), затем медленно, так что на кривой записи потенциала действия кардиомиоцита видно плато (фаза 2 на схеме). Затем осуществляется плавный переход к быстрой реполяризации мембраны (фаза 3 на схеме) до потенциала покоя (фаза 4 на схеме). Длительность потенциала действия кардиомиоцитов составляет 200 ÷ 400 мс, что более чем в 100 раз превышает длительность потенциала действия клеток скелетных мышц и нервных волокон. Эта особенность неспецифического эффекта возбуждения кардиомиоцита обусловливает определенные особенности специфического эффекта возбуждения кардиомиоцита - его сокращение.
По современным представлениям ученых (ионные механизмы возбуждения) потенциал действия является следствием изменения проницаемости цитоплазматической мембраны для различных ионов. Это ведет к особым разнонаправленным потокамионов через сарколемму. Динамика потоков определяет электрические процессы на сарколемме и особенности потенциалов действия различных клеток сердца.
9. Миогенная регуляция сердечной деятельности. Гетеро- и гомеометрическая саморегуляция.
Внутриклеточные механизмы регуляции. Электронная микроскопия позволила установить, что миокард не является синцитием, а состоит из отдельных клеток — миоцитов, соединяющихся между собой вставочными дисками. В каждой клетке действуют механизмы регуляции синтеза белков, обеспечивающих сохранение ее структуры и функций. Скорость синтеза каждого из белков регулируется собственным ауторегуляторным механизмом, поддерживающим уровень воспроизводства данного белка в соответствии с интенсивностью его расходования.
При увеличении нагрузки на сердце (например, при регулярной мышечной деятельности) синтез сократительных белков миокарда и структур, обеспечивающих их деятельность, усиливается. Появляется так называемая рабочая (физиологическая) гипертрофия миокарда, наблюдающаяся у спортсменов.
Внутриклеточные механизмы регуляции обеспечивают и изменение интенсивности деятельности миокарда в соответствии с количеством притекающей к сердцу крови. Этот механизм получил название «закон сердца» (закон Франка—Старлинга): сила сокращения сердца (миокарда) пропорциональна степени его кровенаполнения в диастолу (степени растяжения), т. е. исходной длине его мышечных волокон. Более сильное растяжение миокарда в момент диастолы соответствует усиленному притоку крови к сердцу. При этом внутри каждой миофибриллы актиновые нити в большей степени выдвигаются из промежутков между миозиновыми иитями, а значит, растет количество резервных мостиков, т. е. тех актиновых точек, которые соединяют актиновые и миозиновые нити в момент сокращения. Следовательно, чем больше растянута каждая клетка миокарда во время диастолы, тем больше она сможет укоротиться во время систолы. По этой причине сердце перекачивает в артериальную систему то количество крови, которое притекает к нему из вен. Такой тип миогенной регуляции сократимости миокарда получил название гетерометрической (т. е. зависимой от переменной величины — исходной длины волокон миокарда) регуляции. Под гомеометрической регуляцией принято понимать изменения силы сокращений при неменяющейся исходной длине волокон миокарда. Это прежде всего ритмозависимые изменения силы сокращений. Если стимулировать полоску миокарда при равном растяжении с все увеличивающейся частотой, то можно наблюдать увеличение силы каждого последующего сокращения («лестница» Боудича). В качестве теста на гомеометрическую регуляцию используют также пробу Анрепа — резкое увеличение сопротивления выбросу крови из левого желудочка в аорту. Это приводит к увеличению в определенных границах силы сокращений миокарда. При проведении пробы выделяют две фазы. Вначале при увеличении сопротивления выбросу крови растет конечный диастолический объем и увеличение силы сокращений реализуется по гетерометрическому механизму. На втором этапе конечный диастолический объем стабилизируется и возрастание силы сокращений определяется гомеометрическим механизмом.
10.Нервная и гуморальная регуляция сердечной деятельности. Гемодинамические рефлексы.
Нервная экстракардиальная регуляция. Эта регуляция осуществляется импульсами, поступающими к сердцу из ЦНС по блуждающим и симпатическим нервам.
Подобно всем вегетативным нервам, сердечные нервы образованы двумя нейронами. Тела первых нейронов, отростки которых составляют блуждающие нервы (парасимпатический отдел автономной нервной системы), расположены в продолговатом мозге (рис. 7.11). Отростки этих нейронов заканчиваются в интрамуральных ганглиях сердца. Здесь находятся вторые нейроны, отростки которых идут к проводящей системе, миокарду и коронарным сосудам.
Влияние на сердце блуждающих нервов впервые изучили братья Вебер (1845). Они установили, что раздражение этих нервов тормозит работу сердца вплоть до полной его остановки в диастолу. Это был первый случай обнаружения в организме тормозящего влияния нервов.
При электрическом раздражении периферического отрезка перерезанного блуждающего нерва происходит урежение сердечных сокращений. Это явление называется отрицательным хронотропным эффектом. Одновременно отмечается уменьшение амплитуды сокращений — отрицательный инотропный эффект.
При сильном раздражении блуждающих нервов работа сердца на некоторое время прекращается. В этот период возбудимость мышцы сердца понижена. Понижение возбудимости мышцы сердца называется отрицательным батмотропным эффектом. Замедление проведения возбуждения в сердце называется отрицательным дромотропным эффектом. Нередко наблюдается полная блокада проведения возбуждения в предсердно-желудочковом узле.
Микроэлектродные отведения потенциалов от одиночных мышечных волокон предсердий показали увеличение мембранного потенциала — гиперполяризацию при сильном раздражении блуждающего нерва
При продолжительном раздражении блуждающего нерва прекратившиеся вначале сокращения сердца восстанавливаются, несмотря на продолжающееся раздражение. Это явление называют ускользанием сердца из-под влияния блуждающего нерва.
При раздражении симпатических нервов ускоряется спонтанная деполяризация клеток — водителей ритма в диастолу, что ведет к учащению сердечных сокращений.
Раздражение сердечных ветвей симпатического нерва улучшает проведение возбуждения в сердце (положительный дромотропный эффект) и повышает возбудимость сердца (положительный батмотропный эффект). Влияние раздражения симпатического нерва наблюдается после большого латентного периода (10 с и более) и продолжается еще долго после прекращения раздражения нерва.
Инотропный эффект «усиливающего» нерва хорошо виден при регистрации внутрижелудочкового давления электроманометром. Выраженное влияние «усиливающего» нерва на сократимость миокарда проявляется особенно при нарушениях сократимости. Одной из таких крайних форм нарушения сократимости является альтернация сердечных сокращений, когда одно «нормальное» сокращение миокарда (в желудочке развивается давление, превышающее давление в аорте и осуществляется выброс крови из желудочка в аорту) чередуется со «слабым» сокращением миокарда, при котором давление в желудочке в систолу не достигает давления в аорте и выброса крови не происходит. «Усиливающий» нерв не только усиливает обычные сокращения желудочков, но и устраняет альтернацию, восстанавливая неэффективные сокращения до обычных (рис. 7.13). По мнению И. П. Павлова, эти волокна являются специально трофическими, т. е. стимулирующими процессы обмена веществ.
Совокупность приведенных данных позволяет представить влияние нервной системы на ритм сердца как корригирующее, т. е. ритм сердца зарождается в его водителе ритма, а нервные влияния ускоряют или замедляют скорость спонтанной деполяризации клеток водителя ритма, ускоряя или замедляя таким образом частоту сердцебиений.
В последние годы стали известны факты, свидетельствующие о возможности не только корригирующих, но и пусковых влияний нервной системы на ритм сердца, когда сигналы, приходящие по нервам, инициируют сокращения сердца. Это можно наблюдать в опытах с раздражением блуждающего нерва в режиме, близком к естественной импульсации в нем, т. е. «залпами» («пачками») импульсов, а не непрерывным потоком, как это делалось традиционно. При раздражении блуждающего нерва «залпами» импульсов сердце сокращается в ритме этих «залпов» (каждому «залпу» соответствует одно сокращение сердца). Меняя частоту и характеристику «залпов», можно управлять ритмом сердца в широких пределах.
Воспроизведение сердцем центрального ритма резко изменяет электрофизиологические параметры деятельности синоатриального узла. При работе узла в режиме автоматии, а также при изменениях частоты под влиянием раздражения блуждающего нерва в традиционном режиме возбуждение возникает в одной точке узла, в случае воспроизведения центрального ритма в инициации возбуждения принимает участие одновременно множество клеток узла. На изохронной карте движения возбуждения в узле этот процесс отражается не в виде точки, а в виде большой площади, образованной одновременно возбуждающимися структурными элементами. Сигналы, обеспечивающие синхронное воспроизведение сердцем центрального ритма, отличаются по своей медиаторной природе от общетормозных влияний блуждающего нерва. По-видимому, выделяющиеся в этом случае наряду с ацетилхолином регуляторные пептиды отличаются по своему составу, т. е. реализация каждого типа эффектов блуждающего нерва обеспечивается своей смесью медиаторов («медиаторные коктейли»).
Гуморальная регуляция деятельности сердца
Изменения работы сердца наблюдаются при действии на него ряда биологически активных веществ, циркулирующих в крови.
Катехоламины (адреналин, норадреналин) увеличивают силу и учащают ритм сердечных сокращений, что имеет важное биологическое значение. При физических нагрузках или эмоциональном напряжении мозговой слой надпочечников выбрасывает в кровь большое количество адреналина, что приводит к усилению сердечной деятельности, крайне необходимому в данных условиях.
Указанный эффект возникает в результате стимуляции катехоламинами рецепторов миокарда, вызывающей активацию внутриклеточного фермента аденилатциклазы, которая ускоряет образование 3',5'-циклического аденозинмонофосфата (цАМФ). Он активирует фосфорилазу, вызывающую расщепление внутримышечного гликогена и образование глюкозы (источника энергии для сокращающегося миокарда). Кроме того, фосфорилаза необходима для активации ионов Са2+ — агента, реализующего сопряжение возбуждения и сокращения в миокарде (это также усиливает положительное инотропное действие катехоламинов). Помимо этого, катехоламины повышают проницаемость клеточных мембран для ионов Са2+, способствуя, с одной стороны, усилению поступления их из межклеточного пространства в клетку, а с другой — мобилизации ионов Са2+ из внутриклеточных депо.
Активация аденилатциклазы отмечается в миокарде и при действии глюкагона — гормона, выделяемого α-клетками панкреатических островков, что также вызывает положительный инотропный эффект.
Гормоны коры надпочечников, ангиотензин и серотонин также увеличивают силу сокращений миокарда, а тироксин учащает сердечный ритм. Гипоксемия, гиперкапния и ацидоз угнетают сократительную активность миокарда.
Рефлекторная регуляция деятельности сердца
Осуществляется при участии всех перечисленных отделов ЦНС. Рефлекторные реакции могут как тормозить (замедлять и ослаблять), так и возбуждать (ускорять и усиливать) сердечные сокращения.
Рефлекторные изменения работы сердца возникают при раздражении различных рецепторов. Особое значение в регуляции работы сердца имеют рецепторы, расположенные в некоторых участках сосудистой системы. Эти рецепторы возбуждаются при изменении давления крови в сосудах или при воздействии гуморальных (химических) раздражителей. Участки, где сосредоточены такие рецепторы, получили название сосудистых рефлексогенных зон. Наиболее значительна роль рефлексогенных зон, расположенных в дуге аорты и в области разветвления сонной артерии. Здесь находятся окончания центростремительных нервов, раздражение которых рефлекторно вызывает урежение сердечных сокращений. Эти нервные окончания представляют собой барорецепторы. Естественным их раздражителем служит растяжение сосудистой стенки при повышении давления в тех сосудах, где они расположены. Поток афферентных нервных импульсов от этих рецепторов повышает тонус ядер блуждающих нервов, что приводит к замедлению сердечных сокращений. Чем выше давление крови в сосудистой рефлексогенной зоне, тем чаще возникают афферентные импульсы.
Рефлекторные изменения сердечной деятельности можно вызвать раздражением рецепторов и других кровеносных сосудов. Например, при повышении давления в легочной артерии замедляется работа сердца. Можно изменить сердечную деятельность и путем раздражения рецепторов сосудов многих внутренних органов.
Обнаружены также рецепторы в самом сердце: эндокарде, миокарде и эпикарде; их раздражение рефлекторно изменяет и работу сердца, и тонус сосудов.
В правом предсердии и в устьях полых вен имеются механорецепторы, реагирующие на растяжение (при повышении давления в полости предсердия или в полых венах). Залпы афферентных импульсов от этих рецепторов проходят по центростремительным волокнам блуждающих нервов к группе нейронов ретикулярной формации ствола мозга, получивших название «сердечно-сосудистый центр». Афферентная стимуляция этих нейронов приводит к активации нейронов симпатического отдела автономной нервной системы и вызывает рефлекторное учащение сердечных сокращений. Импульсы, идущие в ЦНС от механорецепторов предсердий, влияют и на работу других органов.
Классический пример вагального рефлекса описал в 60-х годах прошлого века Гольц: легкое поколачивание по желудку и кишечнику лягушки вызывает остановку или замедление сокращений сердца (рис. 7.16). Остановка сердца при ударе по передней брюшной стенке наблюдалась также у человека. Центростремительные пути этого рефлекса идут от желудка и кишечника по чревному нерву в спинной мозг и достигают ядер блуждающих нервов в продолговатом мозге. Отсюда начинаются центробежные пути, образованные ветвями блуждающих нервов, идущими к сердцу. К числу вагальных рефлексов относится также глазосердечный рефлекс Ашнера (урежение сердцебиений на 10—20 в минуту при надавливании на глазные яблоки).
Рефлекторное учащение и усиление сердечной деятельности наблюдаются при болевых раздражениях и эмоциональных состояниях: ярости, гневе, радости, а также при мышечной работе. Изменения сердечной деятельности при этом вызываются импульсами, поступающими к сердцу по симпатическим нервам, а также ослаблением тонуса ядер блуждающих нервов.
11. Клеточные механизмы действия медиаторов сердечных нервов - ацетилхолина и норадреналина - на сократительные клетки миокарда и клетки проводящей системы.
При раздражении периферических отрезков блуждающих нервов в их окончаниях в сердце выделяется АХ, а при раздражении симпатических нервов — норадреналин. Эти вещества являются непосредственными агентами, вызывающими торможение или усиление деятельности сердца, и поэтому получили название медиаторов (передатчиков) нервных влияний. Существование медиаторов было показано Леви (1921). Он раздражал блуждающий или симпатический нерв изолированного сердца лягушки, а затем переносил жидкость из этого сердца в другое, тоже изолированное, но не подвергавшееся нервному влиянию — второе сердце давало такую же реакцию (рис. 7.14, 7.15). Следовательно, при раздражении нервов первого сердца в питающую его жидкость переходит соответствующий медиатор. На нижних кривых можно видеть эффекты, вызываемые перенесенным раствором Рингера, находившимся в сердце во время раздражения.
Получены данные, свидетельствующие о том, что при возбуждении наряду с основным медиаторным веществом в синаптическую щель поступают и другие биологически активные вещества, в частности пептиды. Последние обладают модулирующим действием, изменяя величину и направленность реакции сердца на основной медиатор. Так, опиоидные пептиды угнетают эффекты раздражения блуждающего нерва, а пептид дельта-сна усиливает вагусную брадикардию.
12.Объемная скорость кровотока как основной параметр системы кровообращения. Факторы, определяющие ее величину в покое и при физических нагрузках. Линейная скорость движения крови, скорость кругооборота.
Различают линейную и объемную скорость кровотока. Линейная скорость кровотока (V-лин) это расстояние, которое, проходит частица крови в единицу времени. Она зависит от суммарной площади перечного сечения всех сосудов, образующих участок сосудистого русла. Поэтому в кровеносной системе наиболее узким участком является аорта. Здесь наибольшая линейная скорость кровотока, составляющая 0,5-0,6 м/сек. В артериях среднего и мелкого калибра она снижается до 0,2-0,4 м/сек. Суммарный просвет капиллярного русла в 500-600 раз больше чем аорты, поэтому скорость кровотока в капиллярах уменьшается до 0,5 мм/сек. Замедление тока крови в капиллярах имеет большое физиологическое значение, так как в них происходит транскапиллярный обмен. В крупных венах линейная скорость кровотока вновь возрастает до 0,1-0.2 м/сек. Линейная скорость кровотока в артериях измеряется ультразвуковым методом. Он основан на эффекте Доплера. На сосуд помешают датчик с источником и приемником ультразвука. В движущейся среде - крови частота ультразвуковых колебаний изменяется. Чем больше скорость течения крови по сосуду, тем ниже частота отраженных ультразвуковых волн. Скорость кровотока в капиллярах измеряется под микроскопом с делениями в окуляре, путем наблюдения за движением определенного эритроцита. Объемная скорость кровотока (объём.) это количество крови проходящей через поперечное сечение сосуда за единицу времени. Она зависит от разности давлений в начале и конце сосуда и сопротивления току крови. Объёмная скорость кровотока в сердечно-сосудистой системе составляет 4—6 л/мин, она распределяется по регионам и органам в зависимости от интенсивности их метаболизма в состоянии функционального покоя и при деятельности (при активном состоянии тканей кровоток в них может возрастать в 2—20 раз).
Зная объемную скорость кровотока (количество крови, протекающее через поперечное сечение сосуда), измеряемую в миллилитрах в секунду, можно рассчитать линейную скорость кровотока, которая выражается в сантиметрах в секунду. Линейная скорость (V) отражает скорость продвижения частиц крови вдоль сосуда и равна объемной (Q), деленной на площадь сечения кровеносного сосуда: V=Q/πr2
Линейная скорость, вычисленная по этой формуле, есть средняя скорость. В действительности линейная скорость различна для частиц крови, продвигающихся в центре потока (вдоль продольной оси сосуда) и у сосудистой стенки. В центре сосуда линейная скорость максимальна, около стенки сосуда она минимальна в связи с тем, что здесь особенно велико трение частиц крови о стенку.
Объем крови, протекающей в 1 мин через аорту или полые вены и через легочную артерию или легочные вены, одинаков. Отток крови от сердца соответствует ее притоку. Из этого следует, что объем крови, протекший в 1 мин через всю артериальную и всю венозную систему большого и малого круга кровообращения, одинаков. При постоянном объеме крови, протекающей через любое общее сечение сосудистой системы, линейная скорость кровотока не может быть постоянной. Она зависит от общей ширины данного отдела сосудистого русла. Это следует из уравнения, выражающего соотношение линейной и объемной скорости: чем больше общая площадь сечения сосудов, тем меньше линейная скорость кровотока. В кровеносной системе самым узким местом является аорта. При разветвлении артерий, несмотря на то, что каждая ветвь сосуда уже той, от которой она произошла, наблюдается увеличение суммарного русла, так как сумма просветов артериальных ветвей больше просвета разветвившейся артерии. Наибольшее расширение русла отмечается в капиллярной сети: сумма просветов всех капилляров примерно в 500—600 раз больше просвета аорты. Соответственно этому кровь в капиллярах движется в 500—600 раз медленнее, чем в аорте.
В венах линейная скорость кровотока снова возрастает, так как при слиянии вен друг с другом суммарный просвет кровяного русла суживается. В полых венах линейная скорость кровотока достигает половины скорости в аорте.
Время кругооборота крови. Время полного кругооборота крови — это время, необходимое для того, чтобы она прошла через большой и малый круг кровообращения. Для измерения времени полного кругооборота крови применяют ряд способов, принцип которых заключается в том, что в вену вводят какое-либо вещество, не встречающееся обычно в организме, и определяют, через какой промежуток времени оно появляется в одноименной вене другой стороны. В последние годы скорость кругооборота (или только в малом, или только в большом круге) определяют при помощи радиоактивного изотопа натрия и счетчика электронов. Для этого несколько таких счетчиков помещают на разных частях тела вблизи крупных сосудов и в области сердца. После введения в локтевую вену радиоактивного изотопа натрия определяют время появления радиоактивного излучения в области сердца и исследуемых сосудов. Время полного кругооборота крови у человека составляет в среднем 27 систол сердца. При частоте сердечных сокращений 70—80 в минуту кругооборот крови происходит приблизительно за 20—23 с, однако скорость движения крови по оси сосуда больше, чем у его стенок. Поэтому не вся кровь совершает полный кругооборот так быстро и указанное время является минимальным. Исследования на собаках показали, что 1/5 времени полного кругооборота крови приходится на прохождение крови по малому кругу кровообращения и 4/5 — по большому.
13. Условия возникновения давления крови в сосудистой системе. Динамика изменения сопротивления и давления в сосудистой системе (график). Причины непрерывности тока крови по сосудам.
О сопротивлении в различных сосудах можно судить по разности давления крови в начале и в конце сосуда: чем выше сопротивление току крови, тем большая сила затрачивается на ее продвижение по сосуду и, следовательно, тем значительнее падение давления на протяжении данного сосуда. Как показывают прямые измерения давления крови в разных сосудах, давление на протяжении крупных и средних артерий падает всего на 10%, а в артериолах и капиллярах — на 85%. Это означает, что 10% энергии, затрачиваемой желудочками на изгнание крови, расходуется на продвижение крови в крупных и средних артериях, а 85% — на продвижение крови в артериолах и капиллярах.
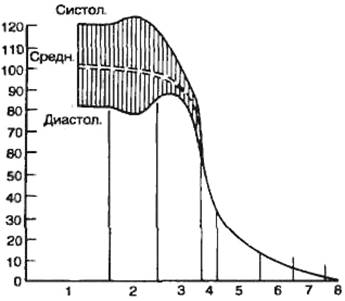 |
| Изменения давления в разных частях сосудистой системы. I — в аорте; 2 — в крупных артериях; 3 — в мелких артериях; 4 — в артериолах; 5 — в капиллярах; б — в венулах; 7 — в венах; 8 — в полой вене. Штриховкой обозначено колебание давления в систолу и диастолу, пунктиром — среднее давление. Среднее давление в аорте поддерживается на высоком уровне (примерно 100 мм рт. ст.), поскольку сердце непрестанно перекачивает кровь в аорту. С другой стороны, артериальное давление меняется от систолического уровня 120 мм рт. ст. до диастолического уровня 80 мм рт. ст., поскольку сердце перекачивает кровь в аорту периодически, только во время систолы. По мере продвижения крови в большом круге кровообращения среднее давление неуклонно снижается, и в месте впадения полых вен в правое предсердие оно составляет 0 мм рт. ст. Давление в капиллярах большого круга кровообращения снижается от 35 мм рт. ст. в артериальном конце капилляра до 10 мм рт. ст. в венозном конце капилляра. В среднем «функциональное» давление в большинстве капиллярных сетей составляет 17 мм рт. ст. Этого давления достаточно для перехода небольшого количества плазмы через мелкие поры в капиллярной стенке, в то время как питательные вещества легко диффундируют через эти поры к клеткам близлежащих тканей. Причины непрерывности тока крови по сосудам. Непрерывный ток крови по всей сосудистой системе обусловливают выраженные упругие свойства аорты и крупных артерий. В сердечно-сосудистой системе часть кинетической энергии, развиваемой сердцем во время систолы, затрачивается на растяжение аорты и отходящих от нее крупных артерий. Последние образуют эластическую, или компрессионную, камеру, в которую поступает значительный объем крови, растягивающий ее; при этом кинетическая энергия, развитая сердцем, переходит в энергию эластического напряжения артериальных стенок. Когда систола заканчивается, растянутые стенки артерий стремятся спасаться и проталкивают кровь в капилляры, поддерживая кровоток во время диастолы. |
14.Факторы, обеспечивающие возврат крови к сердцу. Центральное венозное давление.
Факторы, обеспечивающие возврат крови к сердцу
1. Разность давлений в начале и конце венозного русла.
2. Сокращения скелетных мышц при движении, в результате которых кровь выталкивается из периферических вен к правому предсердию.
3. Присасывающее действие грудной клетки. На вдохе давление в ней становится отрицательным, что способствует венозному кровотоку.
4. Присасывающее действие правого предсердия в период его диастолы. Расширение его полости приводит к появлению отрицательного давления в нем.
5. Сокращения гладких мышц вен.
Движение крови по венам к сердцу связано и с тем, что в них имеются выпячивания стенок, которые выполняют роль клапанов.
Под центральным венозным давлением обычно понимают величину давления в правом предсердии, которая в норме близка к 0 мм рт. ст. Однако в действительности центральному венозному давлению соответствует величина давления в устье полых вен. Между давлением в правом предсердии и в устье полых вен далеко не всегда существует соответствие, особенно в фазу переходных процессов в системе кровообращения, когда давление в правом предсердии нормализуется быстрее, чем центральное венозное давление. Уровень центрального венозного давления (ЦВД) оказывает существенное влияние на величину венозного возврата крови к сердцу. При понижении давления в правом предсердии от 0 до 4 мм рт. ст. приток венозной крови возрастает на 20—30 %, но когда давление в нем становится ниже — 4 мм рт. ст., дальнейшее снижение давления не вызывает уже увеличения притока венозной крови, что обусловлено спадением вен, впадающих в грудную клетку, вызванным резким падением давления крови в этих венах. Средняя величина ЦВД у здоровых людей составляет в состоянии мышечного покоя около 40 мм водн. ст. и в течение дня меняется, нарастая днем и особенно к вечеру на 10—30 мм водн. ст., что связано с ходьбой и мышечными движениями. Увеличение внутриплеврального давления, сопровождаемое сокращением мышц брюшной полости (кашель, натужива-ние), приводит к кратковременному резкому возрастанию ЦВД, а задержка дыхания на вдохе — к его временному падению.
При вдохе центральное венозное давление ( ЦВД ) уменьшается за счет падения плеврального давления, что вызывает дополнительное растяжение правого предсердия и более полное заполнение его кровью. При этом возрастает скорость венозного кровотока и увеличивается градиент давления в венах, что приводит к дополнительному падению ЦВД. Так как давление в венах, лежащих вблизи грудной полости (например, в яремных венах), в момент вдоха является отрицательным, их ранение опасно для жизни, поскольку при вдохе в этом случае возможно проникновение в вены воздуха, пузырьки которого, разносясь с кровью, могут закупорить кровеносное русло (развитие воздушной эмболии).
При выдохе центральное венозное давление ( ЦВД ) растет, а венозный возврат крови к сердцу уменьшается. Это является результатом повышения плеврального давления, увеличивающего венозное сопротивление вследствие спадения грудных вен и сдавливающего правое предсердие, что затрудняет его кровенаполнение.
15.Базальный тонус сосудов, его происхождение и регуляция.
Сосуды, лишенные нервных и гуморальных влияний, как оказалось, сохраняют (хотя и в меньшей мере) способность оказывать сопротивление кровотоку. Денервация сосудов скелетных мышц, например, увеличивает кровоток в них примерно в два раза, но последующее введение ацетилхо-лина в кровоток этой сосудистой области может вызвать дальнейшее десятикратное увеличение в ней кровотока, свидетельствующее о сохраняющейся в этом случае способности сосудов к вазодилатации. Для обозначения этой особенности денервированных сосудов оказывать сопротивление кровотоку введено понятие «базальный тонус сосудов».
Базальный тонус сосудов определяется структурными и миогенными факторами. Структурная часть его создается жесткой сосудистой «сумкой», образованной коллагеновыми волокнами, которая определяет сопротивление сосудов, если активность их гладких мышц полностью исключена. Миогенная часть базального тонуса обеспечивается напряжением гладких мышц сосудов в ответ на растягивающее усилие артериального давления.
Следовательно, изменения сопротивления сосудов под влиянием нервных или гуморальных факторов наслаиваются на базальный тонус, который для определенной сосудистой области более или менее постоянен. Если нервные и гуморальные влияния отсутствуют, а нейрогенный компонент сопротивления сосудов равен нулю, сопротивление их кровотоку определяется базальным тонусом.
16. Рефлекторная и гуморальная регуляция тонуса сосудов. Афферентные нервы (И.Ф. Цион, Э. Геринг), сосудодвигательный центр, сосудодвигательные нервы (К. Бернар). Особенности действия норадреналина и адреналина на сосуды различных органов.
Рефлекторная регуляция сосудистого тонуса
По классификации В. Н. Черниговского, рефлекторные изменения тонуса артерий — сосудистые рефлексы — могут быть разделены на две группы: собственные и сопряженные рефлексы.
Собственные сосудистые рефлексы. Вызываются сигналами от рецепторов самих сосудов. Особенно важное физиологическое значение имеют рецепторы, сосредоточенные в дуге аорты и в области разветвления сонной артерии на внутреннюю и наружную. Указанные участки сосудистой системы получили название сосудистых рефлексогенных зон.
Рецепторы, расположенные в дуге аорты, являются окончаниями центростремительных волокон, проходящих в составе аортального нерва. Ционом и Людвигом этот нерв функционально был обозначен как депрессор. Электрическое раздражение центрального конца нерва обусловливает падение АД вследствие рефлекторного повышения тонуса ядер блуждающих нервов и рефлекторного снижения тонуса сосудосуживающего центра. В результате сердечная деятельность тормозится, а сосуды внутренних органов расширяются. Если у подопытного животного, например у кролика, перерезаны блуждающие нервы, то раздражение аортального нерва вызывает только рефлекторное расширение сосудов без замедления сердечного ритма.
В рефлексогенной зоне сонного синуса (каротидный синус, sinus caroticus) расположены рецепторы, от которых идут центростремительные нервные волокна, образующие синокаротидный нерв, или нерв Геринга. Этот нерв вступает в мозг в составе языкоглоточного нерва. При введении в изолированный каротидный синус крови через канюлю под давлением можно наблюдать падение АД в сосудах тела (рис. 7.22). Понижение системного АД обусловлено тем, что растяжение стенки сонной артерии возбуждает рецепторы каротидного синуса, рефлекторно понижает тонус сосудосуживающего центра и повышает тонус ядер блуждающих нервов.
Рецепторы сосудистых рефлексогенных зон возбуждаются при повышении давления крови в сосудах, поэтому их называют прессорецепторами, или барорецепторами. Если перерезать синокаротидные и аортальные нервы с обеих сторон, возникает гипертензия, т. е. устойчивое повышение АД, достигающее в сонной артерии собаки 200—250 мм рт.ст. вместо 100—120 мм рт.ст. в норме.
Понижение АД вследствие, например, уменьшения объема крови в организме (при кровопотерях), ослабления деятельности сердца или при перераспределении крови и оттоке ее в избыточно расширившиеся кровеносные сосуды какого-нибудь крупного органа ведет к тому, что прессорецепторы дуги аорты и сонных артерий раздражаются менее интенсивно, чем при нормальном АД. Влияние аортальных и синокаротидных нервов на нейроны сердечно-сосудистого центра ослабляется, сосуды суживаются, работа сердца усиливается и АД нормализуется. Этот способ регуляции АД представляет собой регуляцию «на выходе» системы, работающую по принципу отрицательной обратной связи. При отклонении АД от заданной величины включаются компенсаторные реакции, восстанавливающие это давление до нормы. Это — регуляция «по рассогласованию».
Существует еще один, принципиально иной, механизм регуляции АД «на выходе» системы, «по возмущению». В данном случае компенсаторные реакции включаются еще до того, как АД изменится, предупреждая отклонение его от нормы. Необходимые для этого реакции запускаются сигналами, возникающими в рецепторах растяжения миокарда и коронарных сосудов, несущих информацию о степени наполнения кровью полостей сердца и артериальной системы. В этом случае регуляторные реакции реализуются через внутрисердечную нервную систему, а также через вегетативные центры ЦНС.
Сосудистые рефлексы можно вызвать, раздражая рецепторы не только дуги аорты или каротидного синуса, но и сосудов некоторых других областей тела. Так, при повышении давления в сосудах легкого, кишечника, селезенки наблюдаются рефлекторные изменения АД в других сосудистых областях.
Рефлекторная регуляция давления крови осуществляется при помощи не только механорецепторов, но и хеморецепторов, чувствительных к изменениям химического состава крови. Такие хеморецепторы сосредоточены в аортальном и сонном гломусе (glomus caroticum, каротидные тельца), т. е. в местах локализации хеморецепторов.
Хеморецепторы чувствительны к СО2 и недостатку кислорода в крови; они раздражаются также СО, цианидами, никотином. От этих рецепторов возбуждение по центростремительным нервным волокнам передается к сосудодвигательному центру и вызывает повышение его тонуса. В результате сосуды суживаются и давление повышается. Одновременно происходит возбуждение дыхательного центра.
Таким образом, возбуждение хеморецепторов аорты и сонной артерии вызывает сосудистые прессорные рефлексы, а раздражение механорецепторов — депрессорные рефлексы.
Хеморецепторы обнаружены также в сосудах селезенки, надпочечников, почек, костного мозга. Они чувствительны к различным химическим соединениям, циркулирующим в крови, например к ацетилхолину, адреналину и др. (В. Н. Черниговский).
Сопряженные сосудистые рефлексы. Это рефлексы, возникающие в других системах и органах, проявляются преимущественно повышением АД. Их можно вызвать, например, раздражением поверхности тела. Так, при болевых раздражениях рефлекторно суживаются сосуды, особенно органов брюшной полости, и АД повышается. Раздражение кожи холодом также вызывает рефлекторное сужение сосудов, главным образом кожных артериол.
Кортикальная регуляция сосудистого тонуса. Влияние коры большого мозга на сосуды было впервые доказано путем раздражения определенных участков коры.
Кортикальные сосудистые реакции у человека изучены методом условных рефлексов. В этих опытах о сужении или расширении сосудов судят по изменению объема руки при плетизмографии. Если сосуды суживаются, то кровенаполнение, а следовательно, и объем органа уменьшаются. При расширении сосудов, наоборот, кровенаполнение и объем органа увеличиваются.
Если многократно сочетать какое-либо раздражение, например согревание, охлаждение или болевое раздражение участка кожи с каким-нибудь индифферентным раздражителем (звуковым, световым и т. п.), то через некоторое число подобных сочетаний один индифферентный раздражитель может вызвать такую же сосудистую реакцию, как и безусловное раздражение.
Сосудистая реакция на ранее индифферентный раздражитель осуществляется условнорефлекторным путем, т. е. при участии коры большого мозга. У человека при этом часто возникает и соответствующее ощущение (холода, тепла или боли), хотя никакого раздражения кожи не было.
Влиянием коры большого мозга объясняется то, что у спортсменов перед началом упражнения или соревнования наблюдается повышение артериального давления, вызванное изменениями деятельности сердца и сосудистого тонуса.
Сосудодвигательный центр
В. Ф. Овсянниковым (1871) было установлено, что нервный центр, обеспечивающий определенную степень сужения артериального русла — сосудодвигательный центр — находится в продолговатом мозге. Локализация этого центра определена путем перерезки ствола мозга на разных уровнях. Если перерезка произведена у собаки или кошки выше четверохолмия, то АД не изменяется. Если перерезать мозг между продолговатым и спинным мозгом, то максимальное давление крови в сонной артерии понижается до 60—70 мм рт.ст. Отсюда следует, что сосудодвигательный центр локализован в продолговатом мозге и находится в состоянии тонической активности, т. е. длительного постоянного возбуждения. Устранение его влияния вызывает расширение сосудов и падение АД.
Более детальный анализ показал, что сосудодвигательный центр продолговатого мозга расположен на дне IV желудочка и состоит из двух отделов — прессорного и депрессорного. Раздражение прессорного отдела сосудодвигательного центра вызывает сужение артерий и подъем, а раздражение второго — расширение артерий и падение АД.
Считают, что депрессорный отдел сосудодвигательного центра вызывает расширение сосудов, понижая тонус прессорного отдела и снижая, таким образом, эффект сосудосуживающих нервов.
Влияния, идущие от сосудосуживающего центра продолговатого мозга, приходят к нервным центрам симпатической части вегетативной нервной системы, расположенным в боковых рогах грудных сегментов спинного мозга, регулирующих тонус сосудов отдельных участков тела. Спинномозговые центры способны через некоторое время после выключения сосудосуживающего центра продолговатого мозга немного повысить давление крови, снизившееся вследствие расширения артерий и артериол.
Гуморальные влияния на сосуды
Одни гуморальные агенты суживают, а другие расширяют просвет артериальных сосудов.
Сосудосуживающие вещества. К ним относятся гормоны мозгового вещества надпочечников — адреналин и норадреналин, а также задней доли гипофиза — вазопрессин.
Адреналин и норадреналин суживают артерии и артериолы кожи, органов брюшной полости и легких, а вазопрессин действует преимущественно на артериолы и капилляры.
Адреналин, норадреналин и вазопрессин оказывают влияние на сосуды в очень малых концентрациях. Так, сужение сосудов у теплокровных животных происходит при концентрации адреналина к крови 1*10 7 г/мл. Сосудосуживающий эффект этих веществ обусловливает резкое повышение АД
К числу гуморальных сосудосуживающих факторов относится серотонин (5-гидроокситриптамин), продуцируемый в слизистой оболочке кишечника и в некоторых участках головного мозга. Серотонин образуется также при распаде тромбоцитов. Физиологическое значение серотонина в данном случае состоит в том, что он суживает сосуды и препятствует кровотечению из пораженного сосуда. Во второй фазе свертывания крови, развивающейся после образования тромба, серотонин расширяет сосуды.
Особый сосудосуживающий фактор — ренин, образуется в почках, причем тем в большем количестве, чем ниже кровоснабжение почек. По этой причине после частичного сдавливания почечных артерий у животных возникает стойкое повышение артериального давления, обусловленное сужением артериол. Ренин представляет собой протеолитический фермент. Сам ренин не вызывает сужения сосудов, но, поступая в кровь, расщепляет α2-глобулин плазмы — ангиотензиноген и превращает его в относительно малоактивный дека-пептид — ангиотензин I. Последний под влиянием фермента дипептидкарбоксипептидазы превращается в очень активное сосудосуживающее вещество ангиотензин II. Ангиотензин II быстро разрушается в капиллярах ангиотензиназой.
Сосудорасширяющие вещества. В почках образуется также и сосудорасширяющее вещество, названное медуллином (вырабатывается в мозговом слое почки). Это вещество представляет собой липид.
В настоящее время известно образование во многих тканях тела ряда сосудорасширяющих веществ, получивших название простагландинов. Такое название дано потому, что впервые эти-вещества были найдены в семенной жидкости у мужчин и предполагалось, что их образует предстательная железа. Простагландины представляют собой производные ненасыщенных жирных кислот.
Из подчелюстной, поджелудочной желез, из легких и некоторых других органов получен активный сосудорасширяющий полипептид брадикинин. Он вызывает расслабление гладкой мускулатуры артериол и понижает уровень АД. Брадикинин появляется в коже при действии тепла и является одним из факторов, обусловливающих расширение сосудов при нагревании. Он образуется при расщеплении одного из глобулинов плазмы крови под влиянием находящегося в тканях фермента калликреина.
К сосудорасширяющим веществам относится ацетилхолин (АХ), который образуется в окончаниях парасимпатических нервов и симпатических вазодилататоров. Он быстро разрушается в крови, поэтому его действие на сосуды в физиологических условиях чисто местное.
Сосудорасширяющим веществом является также гистамин — вещество, образующееся в слизистой оболочке желудка и кишечника, а также во многих других органах, в частности в коже при ее раздражении и в скелетной мускулатуре во время работы. Гистамин расширяет артериолы и увеличивает кровенаполнение капилляров. При введении 1—2 мг гистамина в вену кошке, несмотря на то что сердце продолжает работать с прежней силой, уровень АД резко падает вследствие уменьшения притока крови к сердцу: очень большое количество крови животного оказывается сосредоточенным в капиллярах, главным образом брюшной полости. Снижение АД и нарушение кровообращения при этом подобны тем, какие возникают при большой кровопотере. Они сопровождаются нарушением деятельности ЦНС вследствие расстройства мозгового кровообращения. Совокупность перечисленных явлений объединяется понятием «шок». Тяжелые нарушения, возникающие в организме при введении больших доз гистамина, называют гистаминовым шоком.
17. Кровяное давление, его виды: систолическое, диастолическое, пульсовое, среднее, центральное (системное) и периферическое (органное); артериальное и венозное.
Кровяное давление - давление внутри кровеносных сосудов (внутри артерий - артериальное давление, внутри капилляров - капиллярное и внутри вен - венозное). Обеспечивает возможность продвижения крови по кровеносной системе и тем самым осуществление обменных процессов в тканях организма.
Артериальное давление — это давление крови в крупных артериях человека; это сила, с которой поток крови оказывает давление на стенки артерий. Различают два показателя артериального давления:
Систолическое (верхнее) артериальное давление — это уровень давления крови в момент максимального сокращения сердца.
Диастолическое (нижнее) артериальное давление — это уровень давления крови в момент максимального расслабления сердца.
Артериальное давление измеряется в миллиметрах ртутного столба, сокращенно мм рт. ст. Значение величины артериального давления 120/80 означает, что величина систолического (верхнего) давления равна 120 мм рт. ст., а величина диастолического (нижнего) артериального давления равна 80 мм рт. ст.
Разность между систолическим и диастолическим давлением, т. е. амплитуда колебаний давления, называется пульсовым давлением. Пульсовое давление при прочих равных условиях пропорционально количеству крови, выбрасываемой сердцем при каждой систоле.
Среднее артериальное давление представляет собой ту среднюю величину давления, при которой в отсутствие пульсовых колебаний наблюдается такой же гемодинамический эффект, как и при естественном пульсирующим давлении крови, т. е. среднее артериальное давление — это равнодействующая всех изменений давления в сосудах.
В клинической практике АД определяют обычно в плечевой артерии. У здоровых людей в возрасте 15—50 лет максимальное давление, измеренное способом Короткова, составляет 110—125 мм рт.ст. В возрасте старше 50 лет оно, как правило, повышается. У 60-летних максимальное давление равно в среднем 135—140 мм рт.ст. У новорожденных максимальное артериальное давление 50 мм рт.ст., но уже через несколько дней становится 70 мм рт.ст. и к концу 1-го месяца жизни — 80 мм рт.ст.
Минимальное артериальное давление у взрослых людей среднего возраста в плечевой артерии в среднем равно 60—80 мм рт.ст., пульсовое составляет 35—50 мм рт.ст., а среднее — 90—95 мм рт.ст.
Венозное давление - давление, которое кровь, находящаяся в просвете вены, оказывает на ее стенку: величина В. д. зависит от калибра вены, тонуса ее стенок, объемной скорости кровотока и величины внутригрудного давления.
18.Артериальное давление как одна из физиологических констант организма. Анализ периферических и центральных компонентов системы саморегуляции артериального давления.
Артериальное давление (АД) – это давление внутри кровеносных сосудов, благодаря которому осуществляется движение крови по ним.
Артериальное давление измеряют при оценке общего состояния организма, так как оно является одним из важнейших показателей состояния и функционирования сердечно-сосудистой системы. Измерение осуществляется различными способами, чаще всего с помощью специального медицинского прибора – тонометра, который определяет и верхнее, и нижнее давление, а также – некоторые модели – пульс.
Различают систолическое (верхнее) и диастолическое (нижнее) давления. У здорового человека АД составляет 120/80 мм рт. ст. с небольшими колебаниями (показатели различаются в зависимости от близости сосудов к сердцу – чем ближе к нему, тем выше). В норме давление человека характеризуется устойчивостью и регулируется организмом самостоятельно, в первую очередь, за этим следит вегетативная нервная система. При изменении внешних условий, которые также влияют на характер артериального давления, в организме срабатывает механизм саморегуляции давления – идет сигнал о необходимости возвращения уровня давления до физиологической нормы.
Высота артериального давления зависит от множества факторов:
от частоты сокращений сердца, которое гонит кровь по сосудам,
от качества стенок сосудов (их эластичность), которые оказывают крови сопротивление,
от объема циркулирующей крови и ее вязкости,
от психологического состояния человека,
от употребления некоторой пищи (например, кофе, колы), приема лекарственных препаратов.
от времени суток и др.
В некоторых ситуациях артериальное давление изменяется по физиологическим причинам: например, повышается в стрессовой ситуации или понижается во время сна. Кроме того, у некоторых людей оно может быть немного повышенным или пониженным от природы. Низкое давление в норме также отмечается у всех новорожденных, у многих подростков в период полового созревания. Однако часто подобные изменения носят патологический характер и являются признаками нарушений в организме и симптомами различных заболеваний, требующих профессиональной поддержки.
19.Общее количество капилляров. Количество функционирующих капилляров. Емкость капиллярного русла. Механизмы мерцания капилляров.
Капилляры представляют собой тончайшие сосуды, диаметром 5—7 мкм, длиной 0,5—1,1 мм. Эти сосуды пролегают в межклеточных пространствах, тесно соприкасаясь с клетками органов и тканей организма. Суммарная длина всех капилляров тела человека составляет около 100 000 км, т. е. нить, которой можно было бы 3 раза опоясать земной шар по экватору. Физиологическое значение капилляров состоит в том, что через их стенки осуществляется обмен веществ между кровью и тканями. Стенки капилляров образованы только одним слоем клеток эндотелия, снаружи которого находится тонкая соединительнотканная базальная мембрана.
Скорость кровотока в капиллярах невелика и составляет 0,5— 1 мм/с. Таким образом, каждая частица крови находится в капилляре примерно 1 с. Небольшая толщина слоя крови (7—8 мкм) и тесный контакт его с клетками органов и тканей, а также непрерывная смена крови в капиллярах обеспечивают возможность обмена веществ между кровью и тканевой (межклеточной) жидкостью.
В тканях, отличающихся интенсивным обменом веществ, число капилляров на 1 мм2 поперечного сечения больше, чем в тканях, в которых обмен веществ менее интенсивный. Так, в сердце на 1 мм2 сечения в 2 раза больше капилляров, чем в скелетной мышце. В сером веществе мозга, где много клеточных элементов, капиллярная сеть значительно более густая, чем в белом.
Различают два вида функционирующих капилляров. Одни из них образуют кратчайший путь между артериолами и венулами (магистральные капилляры). Другие представляют собой боковые ответвления от первых: они отходят от артериального конца магистральных капилляров и впадают в их венозный конец. Эти боковые ответвления образуют капиллярные сети. Объемная и линейная скорость кровотока в магистральных капиллярах больше, чем в боковых ответвлениях. Магистральные капилляры играют важную роль в распределении крови в капиллярных сетях и в других феноменах микроциркуляции.
Давление крови в капиллярах измеряют прямым способом: под контролем бинокулярного микроскопа в капилляр вводят тончайшую канюлю, соединенную с электроманометром. У человека давление на артериальном конце капилляра равно 32 мм рт.ст., а на венозном — 15 мм рт.ст., на вершине петли капилляра ногтевого ложа — 24 мм рт.ст. В капиллярах почечных клубочков давление достигает 65— 70 мм рт.ст., а в капиллярах, оплетающих почечные канальцы, — всего 14—18 мм рт.ст. Очень невелико давление в капиллярах легких — в среднем 6 мм рт.ст. Измерение капиллярного давления производят в положении тела, при котором капилляры исследуемой области находятся на одном уровне с сердцем. В случае расширения артериол давление в капиллярах повышается, а при сужении понижается.
Кровь течет лишь в «дежурных» капиллярах. Часть капилляров выключена из кровообращения. В период интенсивной деятельности органов (например, при сокращении мышц или секреторной активности желез), когда обмен веществ в них усиливается, количество функционирующих капилляров значительно возрастает.
Регулирование капиллярного кровообращения нервной системой, влияние на него физиологически активных веществ — гормонов и метаболитов — осуществляются при воздействии их на артерии и артериолы. Сужение или расширение артерий и артериол изменяет как количество функционирующих капилляров, распределение крови в ветвящейся капиллярной сети, так и состав крови, протекающей по капиллярам, т. е. соотношение эритроцитов и плазмы. При этом общий кровоток через метартериолы и капилляры определяется сокращением гладких мышечных клеток артериол, а степень сокращения прекапиллярных сфинктеров (гладких мышечных клеток, расположенных у устья капилляра при его отхождении от метаартериол) определяет, какая часть крови пройдет через истинные капилляры.
В некоторых участках тела, например в коже, легких и почках, имеются непосредственные соединения артериол и венул — артериовенозные анастомозы. Это наиболее короткий путь между артериолами и венулами. В обычных условиях анастомозы закрыты и кровь проходит через капиллярную сеть. Если анастомозы открываются, то часть крови может поступать в вены, минуя капилляры.
Артериовенозные анастомозы играют роль шунтов, регулирующих капиллярное кровообращение. Примером этого является изменение капиллярного кровообращения в коже при повышении (свыше 35°С) или понижении (ниже 15°С) температуры окружающей среды. Анастомозы в коже открываются и устанавливается ток крови из артериол непосредственно в вены, что играет большую роль в процессах терморегуляции.
Структурной и функциональной единицей кровотока в мелких сосудах является сосудистый модуль — относительно обособленный в гемодинамическом отношении комплекс микрососудов, снабжающий кровью определенную клеточную популяцию органа. При этом имеет место специфичность васкуляризации тканей различных органов, что проявляется в особенностях ветвления микрососудов, плотности капилляризации тканей и др. Наличие модулей позволяет регулировать локальный кровоток в отдельных микроучастках тканей.
Механизм активного расширения и сужения капилляров до сих пор еще представляет нерешенную проблему. Предполагается, что явление ритмического расширения и сжатия капилляров может быть обусловлено, во-первых, нервными импульсами, а во-вторых, они могут возникать под влиянием веществ, образующихся в тканях, окружающих капилляры, или, другими словами, в результате гуморальных воздействий.
Изучая расширение и сужение капилляров, исследователь прежде всего сталкивается с фактом, что никаких двигательных волокон, которые можно найти даже у самых мелких артериол, капилляры не получают. Вокруг капилляров в окружающей их соединительной ткани можно видеть очень богатую сеть нервных окончаний, развертывающихся между адвентипиальными клетками иногда даже в непосредственной близости к эндотелиальной стенке. Откуда идут эти волокна, пока не установлено; вероятнее всего, они чувствительной природы.
Раздражая электрическим током какое-либо окончание чувствительного нерва, можно наблюдать, что в соседних участках сейчас же произойдет расширение капилляров. Получается впечатление,что нервный импульс распространился с чувствительного волокна по сети нервных окончаний и вызвал это расширение. Такое распространение возбуждения называется антидромным, а все явления передачи импульса с периферии на соседние участки по конечным отросткам получили название аксонного рефлекса
20. Морфофункциональные особенности микроциркуляторного русла. Транскапиллярный обмен.
Микроциркуляторное русло включает в себя следующие компоненты:
артериолы;
прекапилляры;
капилляры;
посткапилляры;
венулы;
артериоло-венулярные анастомозы.
Функции микроциркуляторного русла состоят в следующем:
трофическая и дыхательная функции, так как обменная поверхность капилляров и венул составляет 1000 м2, или 1,5 м2 на 100 г ткани;
депонирующая функция, так как в сосудах микроциркуляторного русла в состоянии покоя депонируется значительная часть крови, которая во время физической работы включается в кровоток;
дренажная функция, так как микроциркуляторное русло собирает кровь из приносящих артерий и распределяет ее по органу;
регуляция кровотока в органе, эту функцию выполняют артериолы благодаря наличию в них сфинктеров;
транспортная функция, то есть транспорт крови.
В микроциркуляторном русле различают три звена:
артериальное (артериолы прекапилляры);
капиллярное;
венозное (посткапилляры, собирательные и мышечные венулы).
Артериолы имеют диаметр 50-100 мкм. В их строении сохраняются три оболочки, но они выражены слабее, чем в артериях. В области отхождения от артериолы капилляра находится гладкомышечный сфинктер, который регулирует кровоток. Этот участок называется прекапилляром.
Капилляры - это самые мелкие сосуды, они различаются по размерам на:
узкий тип 4-7 мкм;
обычный или соматический тип 7-11 мкм;
синусоидный тип 20-30 мкм;
лакунарный тип 50-70 мкм.
В их строении прослеживается слоистый принцип. Внутренний слой образован эндотелием. Эндотелиальный слой капилляра - аналог внутренней оболочки. Он лежит на базальной мембране, которая вначале расщепляется на два листка, а затем соединяется. В результате образуется полость, в которой лежат клетки перициты. На этих клетках на этих клетках заканчиваются вегетативные нервные окончания, под регулирующим действием которых клетки могут накапливать воду, увеличиваться в размере и закрывать просвет капилляра. При удалении из клеток воды они уменьшаются в размерах, и просвет капилляров открывается. Функции перицитов:
изменение просвета капилляров;
источник гладкомышечных клеток;
контроль пролиферации эндотелиальных клеток при регенерации капилляра;
синтез компонентов базальной мембраны;
фагоцитарная функция.
Для капилляров характерна органная специфичность, в связи с чем выделяют три типа капилляров:
капилляры соматического типа или непрерывные, они находятся в коже, мышцах, головном мозге, спинном мозге. Для них характерен непрерывный эндотелий и непрерывная базальная мембрана;
капилляры фенестрированного или висцерального типа (локализация - внутренние органы и эндокринные железы). Для них характерно наличие в эндотелии сужений - фенестр и непрерывной базальной мембраны;
капилляры прерывистого или синусоидного типа (красный костный мозг, селезенка, печень). В эндотелии этих капилляров имеются истинные отверстия, есть они и в базальной мембране, которая может вообще отсутствовать. Иногда к капиллярам относят лакуны - крупные сосуды со строением стенки как в капилляре (пещеристые тела полового члена).
Венулы делятся на:
посткапиллярные;
собирательные;
мышечные.
Посткапиллярные венулы образуются в результате слияния нескольких капилляров, имеют такое же строение, как и капилляр, но больший диаметр (12-30 мкм) и большое количество перицитов. В собирательных венулах (диаметр 30-50 мкм), которые образуются при слиянии нескольких посткапиллярных венул, уже имеются две выраженные оболочки: внутренняя (эндотелиальный и подэндотелиальный слои) и наружная - рыхлая волокнистая неоформленная соединительная ткань. Гладкие миоциты появляются только в крупных венулах, достигающих диаметра 50 мкм. Эти венулы называются мышечными и имеют диаметр до 100 мкм. Гладкие миоциты в них, однако, не имеют строгой ориентации и формируют один слой.
Артериоло-венулярные анастомозы или шунты - это вид сосудов микроциркуляторного русла, по которым кровь из артериол попадает в венулы, минуя капилляры. Это необходимо, например, в коже для терморегуляции. Все артериоло-венулярные анастомозы делятся на два типа:
истинные - простые и сложные;
атипичные анастомозы или полушунты.
В простых анастомозах отсутствуют сократительные элементы, и кровоток в них регулируется за счет сфинктера, расположенного в артериолах в месте отхождения анастомоза. В сложных анастомозах в стенке есть элементы, регулирующие их просвет и интенсивность кровотока через анастомоз. Сложные анастомозы делятся на анастомозы гломусного типа и анастомозы типа замыкающих артерий. В анастомозах типа замыкающих артерий во внутренней оболочке имеются скопления расположенных продольно гладких миоцитов. Их сокращение приводит к выпячиванию стенки в виде подушки в просвет анастомоза и закрытию его. В анастомозах типа гломуса (клубочек) в стенке есть скопление эпителиоидных Е-клеток (имеют вид эпителия), способных насасывать воду, увеличиваться в размерах и закрывать просвет анастомоза. При отдаче воды клетки уменьшаются в размерах, и просвет открывается.
В полушунтах в стенке отсутствуют сократительные элементы, ширина их просвета не регулируется. В них может забрасываться венозная кровь из венул, поэтому в полушунтах, в отличии от шунтов, течет смешанная кровь. Анастомозы выполняют функцию перераспределения крови, регуляции артериального давления.
Транскапиллярный обмен - обмен веществ между кровью капилляров и органами, тканями.
В капиллярах благоприятные условия:
медленное движение крови;
различное давление в артериальном и венозном отделах капиллярах;
проницаемость сосудистой стенки.
Транскапиллярный обмен осуществляется за счёт:
диффузии;
фильтрации;
активного транспорта;
пиноцитоза.
Диффузия - пассивный транспорт веществ через стенку по градиенту концентрации; ионы, минеральные вещества, вещества растворимые в воде. В капиллярах 2-х сторонняя диффузия. Облегчённая диффузия - образуется комплекс с молекулой-перносчиком и осуществляется диффузия по коэфициэнту концентрации этих комплексов. Диффузией обладает СО2 и О2. Они растворяются в липидах и затем диффундируют по всей поверхности стенок капилляров. Газовый состав крови, после прохождения через капилляры, меняется в 30-40 раз.
Фильтрация - пассивный транспорт, осуществляемый за счёт разности давлений. Таким образом, происходит движение воды и растворённых в ней веществ.
В процессе фильтрации участвуют 4 силы.
Гидростатическое давление крови - способствует фильтрации (Р г/кр).
Гидростатическое давление межтканевой жидкости - препятствует фильтрации. (Р г/межтк. ж).
Онкотическое давление крови - создаётся белками крови, которые удерживают жидкую часть крови в сосудах - препятствуют фильтрации. (Р омк/кр).
Онкотическое давление межтканевой жидкости. Р омк/межтк. Р онкотическое в капиллярах - Р онкотическое в межтканевой жидкости = сила, прерятствующая фильтрации.
Сила фильтрации = (Р г/кр - Р г/межтк. ж) - (Р онк/кр - Р межтк. ж.); Чем больше Р г/кр, тем больше сила фильтрации. Р г/кр легко меняется, остальные 3 величины - почти постоянные.
Фильтрация воды осуществляется через щели между эндотелиоцитами. Фильтрация жиров - по всей поверхности капилляров.
Активный транспорт - с помощью мелких переносчиков, с затратой энергии. Таким образом, транспортируются отдельные аминокислоты, углеводы и др. вещества. Активный транспорт часто связан с транспортом Na+. Т. е. вещество образует комплекс с молекулой переносчиком Na+.
Пиноцитоз - микровезикулярный транспорт. Внутри эндотелиоцитов есть везикулы, которые захватывают вещество у наружной поверхности клетки и транспортируют их к внутренней поверхности. В некоторых эндотелиоцитах микровезикулы выстраиваются, образуя микроканал, по которым осуществляется транспорт. Таким образом, транспортируются отдельные белки.
Факторы влияющие на транскапиллярный обмен.
Проницаемость стенки капилляра. (Р г/кр - Р г/межтк. жидк).
Разность концентрации различных веществ.
Наличие веществ-переносчиков.
