Пат физ устно экзамен. патфиз устно. Общая патофизиология патофізіологія як наука та навчальна дисципліна. Методи патофізіології
 Скачать 1.7 Mb. Скачать 1.7 Mb.
|
|
6. Захисні пристосувальні реакції. Адаптація, компенсація. Механізми негайної і довготривалої адаптації. Роль нервових і гуморальних чинників у їх реалізації. Адаптация - это приспособление организма и его структур к меняющимся условиям внешней среды. Адаптация обеспечивает сохранение гомеостаза и предупреждает повреждение в условиях действия факторов окружающей среды. Компенсация - это состояние, развивающееся как результат реализации компенсаторных реакций и процессов, направленных на восстановление нарушенного гомеостаза вследствие действия патогенных факторов. Компенсация ликвидирует последствия повреждения. Основу адаптации и компенсации составляют одни и те же механизмы, которые называют защитно-приспособительными, или защитно-компенсаторными. Отличие этих понятий заключается в том, что адаптация развивается при увеличении интенсивности действия обычных факторов внешней среды. Повреждения еще не произошло, а показатели гомеостаза находятся на крайний пределы нормы. Компенсация же развивается при воздействии патогенных факторов, когда происходит повреждение, а показатели гомеостаза уже вышли за пределы нормы. 4.6. Как происходит становление адаптации и компенсации? Различают два этапа развития этих состояний. I. Этап немедленной адаптации и компенсации. Происходит мобилизация существующих механизмов и резервов, в результате чего увеличивается нагрузка на единицу функционирующей системы, развивается ее гиперфункция, на этом этапе события разворачиваются по следующей схеме: действие патогенного фактора → нарушение гомеостаза → восприятие нарушений гомеостаза → регуляторные центры → немедленные защитные реакции (специфические и неспецифические) → гиперфункция соответствующих структур, поддерживающих гомеостаз. II . Этап долговременной адаптации и компенсации. Его основу составляет увеличение мощности систем, ответственных за адаптацию и компенсацию. Это достигается увеличением количества структур, обеспечивающих гиперфункции, то есть развивается гипертрофия. При этом нагрузка на единицу функционирующей системы уменьшается до нормы. На клеточном уровне развивается такая цепь событий: гиперфункция → нарушение внутриклеточного гомеостаза → активация генома → - увеличение синтеза соответствующих белков → гипертрофия клетки. Сравнительная характеристика немедленных и долгосрочных механизмов адаптации и компенсации:
4.7. Что такое причинно-следственные связи в патогенезе? Какие существуют варианты этих связей? Различные события, которые происходят в организме в процессе развития болезни, находятся между собой в определенных причинно-следственных связях, то есть одно и то же явление патогенеза одновременно является следствием одних событий и причиной других. Различают несколько типов таких связей. 1. "Прямая линия". События в патогенезе развиваются по прямой линии, когда одно явление является следствием предыдущего и причиной последующего (рис. 14). 2 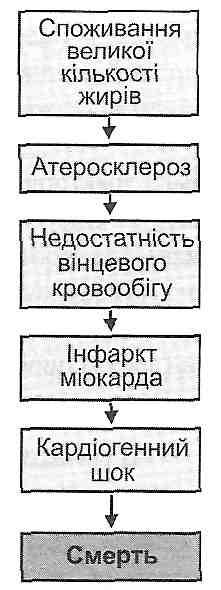 . Разветвленные типа. Таковы дивергенция и конвергенция. При дивергенции определенные события патогенеза имеют много последствий. Например, при сахарном диабете отсутствие инсулина как центральное звено патогенеза имеет своим следствием нарушения углеводного, жирового, белкового, водно-солевого обменов и кислотно-основного равновесия (рис. 15). . Разветвленные типа. Таковы дивергенция и конвергенция. При дивергенции определенные события патогенеза имеют много последствий. Например, при сахарном диабете отсутствие инсулина как центральное звено патогенеза имеет своим следствием нарушения углеводного, жирового, белкового, водно-солевого обменов и кислотно-основного равновесия (рис. 15).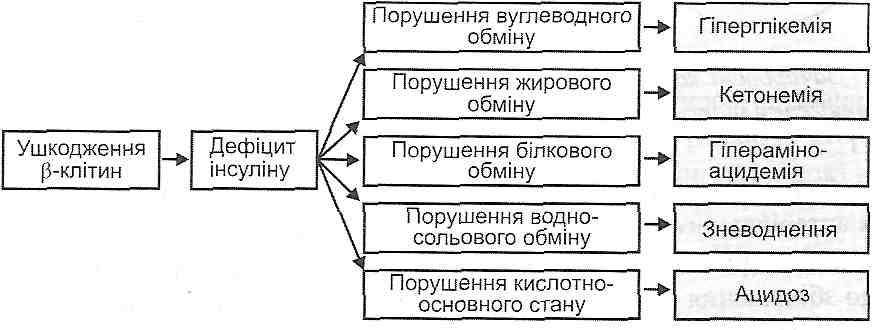 ¥ НЕ AS . Дивергенция в патогенезе сахарного диабета При конвергенции "различные события патогенеза ведут к одному и тому же результату. Например, при воспалении в различных клетках и в плазме крови образуются различные биологически активные вещества (гистамин, серотонин, простагландины, кинины). Все они вызывают расширение артериол (артериальную гиперемию) и повышают проницаемость сосудов (рис. 16). 3. "Заколдованный круг" (circulus vitiosus). Это такой тип причинно-следственных связей, когда определенные явления патогенеза через определенную последовательность событий приводят к усилению самих себя. Указанный вариант является наиболее опасным, так как он самопидтримуе патогенез болезни и ухудшает ее течение. 4.8. Приведите примеры развития патогенеза по типу "порочного круга". В патогенезе любого шока большое значение имеет снижение артериального давления. Артериальная гипотензия, возникает, является причиной кислородного голодания. гипоксия Р 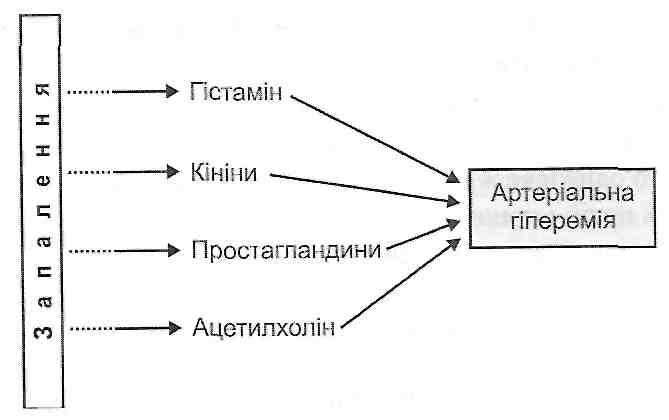 ис. 16. Конвергенция как тип причинно-следственных связей в патогенезе воспаления ис. 16. Конвергенция как тип причинно-следственных связей в патогенезе воспаленияголовного мозга приводит к угнетению сосудодвигательного центра и еще большего снижения артериального давления (круг замкнулся) (рис. 17). Рис. 17. "Заколдованный круг" в патогенезе шока В стадии декомпенсации при перегревании повышается температура тела. Это приводит к увеличению скорости всех биохимических реакций в организме, в том числе и окислительных. В результате этого возрастает теплопродукция и, как следствие, еще бы * льше повышается температура тела (рис. 18). 7. Закономірності розвитку механічної травми. Патогенна дія термічних факторів. Захисні, компенсаторні реакції та власне патологічні зміни при гіпертермії. Тепловий та сонячний удар. Опіки, опікова хвороба. Гіпотермія. Захисні, компенсаторні реакції і власне патологічні зміни. Механическая травма - это повреждение ткани твердым телом или ударной волной. Местно травма может проявлять себя разрывами, ушибами, переломами, раздавливания или их комбинациями. Часто механическая травма сочетается с кровопотерей, повреждением нервных стволов и кожных покровов. Наиболее тяжелыми общими проявлениями травмы является травматический шок и синдром длительного раздавливания (краш-синдром) (см. Разд. 12). 5.2. Патологические процессы могут развиваться при воздействии на организм термических факторов? При общей воздействия на организм высокой температуры может развиваться гипертермия (перегревание), при мисцевий- ожоги. Длительное пребывание организма в условиях низкой температуры может приводить к развитию гипотермии, местная же воздействие низкой температуры бывает причиной обморожения. В развитии гипер- и гипотермии выделяют две стадии: компенсации и декомпенсации. В первую стадию благодаря защитно-компенсаторным реакциям организма температура ядра тела не меняется, несмотря на действие термических факторов. Если указанные реакции будут недостаточны, то наступает стадия декомпенсации, основным признаком которой является выход температуры тела за пределы нормы. 5.3. Как меняется теплопродукция и теплоотдача в разные стадии гипо- и гипертермии?
5.4. Какие защитно-компенсаторные реакции развиваются при гипотермии? При гипотермии защитно-компенсаторные реакции развиваются в двух направлениях. I. Реакции, направленные на ограничение теплоотдачи: а) спазм периферических сосудов; б) уменьшение потоотделения; в) изменение позы и другие поведенческие реакции, уменьшают площадь открытых поверхностей тела г) повышение теплоизоляционных свойств шерсти у животных благодаря сокращению гладких мышц, поднимающих волосы (у человека сохранилась рудиментарная реакция - "гусиная кожа"). II. Реакции, направленные на повышение теплопродукции: а) увеличение сократительного термогенеза (повышения тонуса скелетных мышц, мышечная дрожь, непроизвольные движения) б) увеличение нескоротливого термогенеза (усиление окислительных процессов, разъединение окисления и фосфорилирования). 5.5. Которые собственно патологические изменения составляют суть стадии декомпенсации при гипотермии? Главным признаком этой стадии является снижение температуры ядра тела, закономерно приводит к уменьшению скорости всех биохимических реакций в организме, в том числе и процессов биологического окисления. При этом резко уменьшается потребление кислорода и образования АТФ в клетках. Дефицит энергии вызывается к угнетению жизненно важных функций организма: деятельности ЦНС, дыхания, кровообращения, в результате чего развивается кислородное голодание. Гипоксия, в свою очередь, увеличивает дефицит АТФ - замыкается "порочный круг", что ведет в конечном итоге к смерти. 5.6. Какие защитно-компенсаторные реакции развиваются при гипертермии? При гипертермии защитно-компенсаторные реакции направлены на увеличение теплоотдачи. Таковыми являются: 1) расширение периферических сосудов; 2) увеличение потоотделения; 3) реакции, направленные на увеличение площади открытой поверхности тела (изменение позы, поведенческие реакции) 4) тепловая одышка у животных. 5.7. Которые собственно патологические изменения характерны для стадии декомпенсации при гипертермии? Основным признаком второго периода перегревания - стадии декомпенсации - повышение температуры тела. Оно сопровождается резким возбуждением ЦНС, усилением дыхания, кровообращения и обмена веществ. Дальнейшее повышение температуры тела и перезбуджсння нервных центров могут закончиться их истощением, нарушением дыхания, функции сердца и снижением артериального давления. Развивается гипоксия. В результате интенсивного потоотделения возникает обезвоживание, нарушается электролитный обмен. Сгущение крови и повышение ее вязкости создают дополнительную нагрузку на аппарат кровообращения и являются одними из факторов развития недостаточности сердца. На фоне прогрессирования явлений кислородного голодания появляются судороги, наступает смерть. Острое перегрева с быстрым повышением температуры тела получило название теплового удара. 5.8. Какие общие изменения в организме могут возникать при ожогах? Комплекс общих изменений в организме, возникающих при больших и глубоких ожогах, называется ожоговой болезни. Различают следующие стадии ожоговой болезни: ожоговый шок, ожоговая токсемия, ожоговая инфекция, ожоговое истощение, завершение. В развитии ожогового шока главную роль играет болевой фактор. Именно этим объясняют довольно большую продолжительность эректильной фазы (фазы возбуждения) шока. Ожоговые токсины появляются в организме в результате нарушения обмена веществ, но больше всего их образуется в месте повреждения. С поврежденных тканей в общий кровоток поступают денатурированный белок и токсичные продукты его ферментативного гидролиза. Интоксикация организма усиливается инфекцией. ее источником является повреждены ткани и содержание кишок. Это осложнение связывают со снижением барьерных свойств организма и его структур, обусловленным некрозом кожи, нарушением функции системы мо-нонуклеарних фагоцитов, изменением защитных свойств слизистой оболочки кишечника. Большое значение в патогенезе ожоговой болезни имеют обезвоживание и нарушение электролитного обмена. Потеря белков и жидкости происходит главным образом на месте поражения как результат повышения проницаемости сосудистой стенки. Сгущение крови и повышение ее вязкости затрудняют кровообращение и работу сердца. Ожоговое истощение характеризуется постепенным развитием кахексии, отеками, анемией, дистрофическими изменениями во внутренних органах, осложнениями (пневмонией, гломерулонефритом), недостаточностью коры надпочечников. В процессе выздоровления происходит полное отторжение некротических тканей, заполнение дефекта грануляциями, рубцевание и эпителизация. 8. Патогенна дія променевої енергії. Види іонізуючого випромінювання. Радіочутливість тканин. Механізми прямого і непрямого променевого пошкодження біологічних структур. Радіоліз води. Радіотоксини. Прояви радіаційних уражень на молекулярному, клітинному, тканинному, органному і системному рівнях. Патогенез променевої хвороби, її основних форм та синдромів. Найближчі та віддалені наслідки великих і малих доз іонізуючого опромінення. Природні механізми протирадіаційного захисту. Патофізіологічні основи радіопротекції. Какие виды ионизирующего излучения могут оказывать патогенное действие на организм? Способность оказывать патогенное действие имеют все виды ионизирующего излучения: корпускулярные (а- и (3-частицы, нейтроны, протоны) и электромагнитные волны (рентгеновское, гамма-излучение). Механизмы действия ионизирующей радиации на клетки и последствия облучения организма представлено на рис. 19 . 5.10. От чего зависит чувствительность тканей к действию ионизирующей радиации? Основным фактором, определяющим чувствительность тканей к ионизирующей радиации, является способность клеток к делению и интенсивность этого процесса. Итак, самую высокую радиочувствительность имеют ткани, в которых процессы деления клеток происходят наиболее интенсивно. Это в первую очередь кроветворная и лимфоидная ткани, где восстановление клеток происходит постоянно. Далее идет эпителиальная ткань, особенно эпителий ЖКТ и половых желез, а также покровный эпителий кожи, затем - эндотелий сосудов; последние в этом ряду - хрящевая, мышечная и нервная ткани. 5.11. В чем сущность прямого патогенного действия ионизирующей радиации на клетки? Под прямым действием ионизирующей радиации понимают непосредственный ее влияние на макромолекулы и надмолекулярные структуры клеток (см. Рис. 19). Энергия ионизирующей радиации, превышающей энергию внутримолекулярных связей, вызывает ионизацию молекул, разрыв наименее прочных связей, образования свободных радикалов и т. Д. Структурными проявлениями прямого действия радиации разрыв хромосом, расщепление молекул ДНК, РНК, набухание органоидов клетки. Подсчитано, что прямое воздействие радиации обусловливает около 45% суммарного биологического ее эффекта. 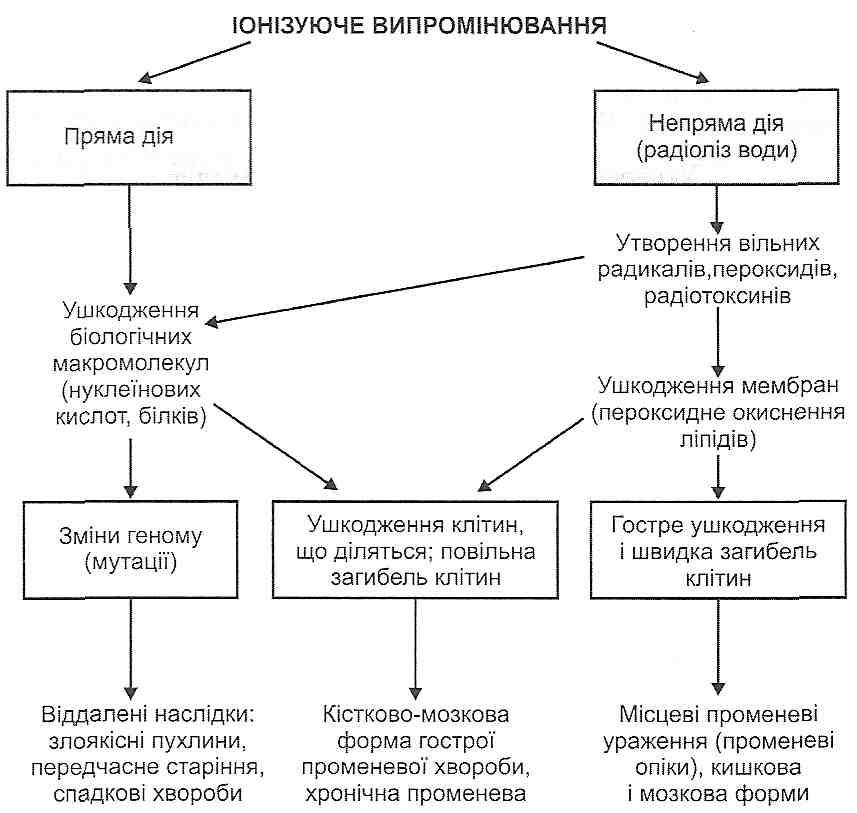 Рис. 19. Механизмы патогенного действия ионизирующего излучения 5.12. В чем сущность непрямого патогенного действия ионизирующей радиации на клетки? Что такое радиолиз воды? Косвенное воздействие ионизирующей радиации обусловлена образованием в клетках большого количества свободных радикалов. Основным их источником является молекулы воды. Процесс образования свободных радикалов водорода и гидроксила из воды под воздействием радиации получил название радиолиза воды. Радиолиз воды: Образование вторичных свободных радикалов: 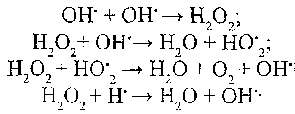 Образующиеся свободные радикалы взаимодействуют друг с другом, в результате чего образуются так называемые вторичные свободные радикалы и гидропероксиды. их накопление ведет к быстрой активации процессов свободнорадикального окисления азотистых оснований ДНК и РНК, белков-ферментов (особенно сульфгидрильных групп, что входят в состав активных центров), липидов, аминокислот. На долю непрямого действия приходится 55% суммарного биологического эффекта ионизирующей радиации. 5.13. Что такое радиотоксины? Радио токсин ее - это продукты свободнорадикального окисления, образующиеся в тканях под действием радиоактивного облучения. Наибольшее значение в патогенезе лучевых поражений имеют липидные радиотоксины (липидные гидропероксиды, эпоксиды, альдегиды, кетоны). Будучи промежуточными и конечными продуктами перекисного окисления липидов, они накапливаются в мембранах клеток и нарушают их барьерные свойства. Кроме того, в облученных клетках с некоторых аминокислот (тирозин, триптофан) образуются так называемые хиноны радиотоксины. Они являются химическими мутагенами, подавляют активность многих ферментов. Радиотоксины, попадая из поврежденных клеток в кровь, оказывают патогенное действие и на отдаленные от места их образования органы и ткани. Этим, в частности, объясняют общие нарушения в организме при местных лучевых поражениях. 5.14. Какие факторы способствуют и препятствующих развитию лучевых поражений? Развития лучевых поражений способствуют повышение температуры, увеличение напряжения кислорода и содержания воды в тканях. В этих условиях увеличивается скорость свободно-радикальных реакций, а следовательно, и косвенная патогенная действие ионизирующей радиации. И наоборот, снижение температуры, кислородное голодание и обезвоживание являются факторами, замедляющими развитие лучевых поражений. 5.15. Какие защитно-компенсаторные механизмы в клетках направлены на предупреждение и ликвидацию лучевого повреждения? Что такое Радиопротекторы? Для защиты клеток от лучевого поражения наибольшее значение имеют антиоксидантные системы и механизмы репарации ДНК (подробно см. Гл. 6 и 11). Радиопротектором называют вещества, введение которых предупреждает или уменьшает степень развития лучевых поражений. Наиболее изучены сегодня с этой точки зрения антиоксиданты и препараты, являющиеся донаторами сульфгидрильных групп. При использовании последних достигается эффект защиты собственных SH-групп, входящих в состав активных центров многих ферментов. 5.16. Назовите формы и стадии развития острой лучевой болезни. В зависимости от поглощенной дозы облучения выделяют три формы острой лучевой болезни: костно-мозговую (поглощенная доза - от 1 до 10 Гр), кишечную (от 10 до 20 Гр) , токсемическая (от 20 – 80 Гр) и мозговую (от 80 до 120 Гр). В клинике костно-мозговой формы различают 4 периода: 1) период первичных реакций (продолжительность - 1-2 суток); 2) период мнимого благополучия (несколько суток) 3) период выраженных клинических признаков; 4) завершение. Типичную форму острой лучевой болезни по тяжести поражения, определяемой поглощенной дозой излучения, подразделяют на четыре группы: I — легкой степени (1— 2 Гр); II — средней степени (2 — 4 Гр); III — тяжелой степени (4 — 6 Гр); IV — крайне тяжелой степени (свыше 6 Гр). В.ее течении выделяют четыре фазы: 1) первичной острой реакции; 2) мнимого клинического благополучия (скрытая фаза); 3) разгара болезни; 4) восстановления. Фаза первичной острой реакции организма человека возникает в зависимости от дозы в первые минуты или часы после облучения. В это время характерно некоторое возбуждение, головная боль, общая слабость. Затем наступают диспепсические расстройства (тошнота, рвота, потеря аппетита), со стороны крови — кратковременный нейтрофильный лейкоцитоз со сдвигом влево, абсолютная лимфопения. Клинические проявления болезни — это не только следствие прямого повреждающего действия ионизирующей радиации радиочувствительных систем, но и свидетельство ранних нарушений нервно-регуляторных и гуморальных взаимоотношений. Наблюдаются повышенная возбудимость нервной системы, связанная с ней лабильность (неустойчивость) вегетативных функций— колебания артериального давления, ритма сердца и т. д. Активация гипофиз-адреналовой системы приводит к усиленной секреции гормонов коры надпочечников, что в данной ситуации мажет иметь приспособительное значение. При дозах 8 — 10 Гр наблюдается развитие шокоподобного состояния с падением, артериального давления, кратковременной потерей сознания, повышением температуры тела, развитием поноса, нервнорефлекторными нарушениями. Продолжительность фазы первичной острой реакции 1-3 дня. Фаза мнимого клинического благополучия характеризуется включением в патологический процесс защитных механизмов организма. В связи с этим самочувствие больных становится удовлетворительным, проходят клинически видимые признаки болезни. Длительность скрытой фазы зависит от дозы облучения и колеблется от 10 — 15 дней до 4 — 5 нед. При сравнительно небольших дозах (до 1 Гр) начальные легкие функциональные реакции не переходят в развернутую клиническую картину и заболевание ограничивается затухающими явлениями начальных реакций. При очень тяжелых формах поражения (дозы более 10 Гр) скрытая фаза вообще отсутствует. Однако в это время нарастает поражение системы крови: в периферической крови прогрессирует лимфопения на фоне лейкопении, снижается содержание ретикулоцитов и тромбоцитов. В костном мозге развивается опустошение (аплазия). Могут наблюдаться атрофия гонад, подавление ранних стадий сперматогенеза, развитие изменений в тонком кишечнике и коже. Неврологическая симптоматика постепенно сглаживается. Фаза разгара болезни характеризуется тем, что самочувствие больных вновь резко ухудшается, нарастает слабость, повышается температура тела, появляются кровоточивость и кровоизлияния в кожу, слизистые оболочки, желудочно-кишечный тракт, мозг, сердце и легкие. В результате нарушения обмена веществ и диспепсических расстройств (потеря аппетита и поносы) резко снижается масса тела. На первый план выходит поражение системы крови. Развиваются глубокая лейкопения, тромбоцитопения, выраженная анемия; увеличивается скорость оседания эритроцитов (СОЭ); в костном мозге — картина опустошения с начальными признаками регенерации. Наблюдаются гипопротеинемия, гипоальбуминемия, повышение содержания остаточного азота и снижение уровня хлоридов. Угнетается иммунитет, в результате чего развиваются инфекционные осложнения, аутоинфекция и аутоинтоксикация. Продолжительность фазы выраженных клинических проявлений от нескольких дней до 2 — 3 нед. При облучении в дозе свыше 2,5 Гр без проведения лечебных мероприятий возможен смертельный исход. Фаза восстановления характеризуется постепенной нормализацией нарушенных функций, общее состояние больных заметно улучшается. Снижается до нормы температура телах исчезают геморрагические и диспепсические проявления, со 2 — 5-гo мес нормализуется функция потовых и сальных желез, возобновляется рост волос. Происходит постепенно восстановление показателей крови и обмена веществ. Период восстановления охватывает 3— 6 мес, в тяжелых случаях лучевого поражения может затягиваться на 1 — 3 года, при этом возможен переход болезни в хроническую форму. Кишечная форма острой лучевой болезни возникает при облучении лабораторных животных в дозах 10 — 20 Гр, вызывающих смерть на 3 — 5-е сут после облучения. При вскрытии животных всегда констатируют гибель основной массы кишечного эпителия, оголение ворсин, их уплощение и деструкцию. У человека при облучении в дозах 10— 20 Гр смерть чаще наступает на 7-10-е сут. Основными признаками болезни являются тошнота, рвота, кровавый понос, повышение температуры тела, могут наблюдаться полная паралитическая непроходимость кишечника и вздутие живота. Развиваются геморрагия и глубокая лейкопения с полным отсутствием лимфоцитов в периферической крови, а также картина сепсиса. Причиной смерти при кишечной форме острой лучевой болезни являются дегидратация организма, сопровождающаяся поте- рей электролитов и белка, развитие необратимого шока, связанного с действием токсических веществ микробного и тканевого происхождения. Токсемическая форма характеризуется выраженными гемодинамическими нарушениями главным образом в кишечнике и печени, парезом сосудов, тахикардией, кровоизлияниями, тяжелой интоксикацией и менингеальными симптомами (отек мозга). Наблюдается олигурия и гиперазотемия вследствие поражения почек. Смерть наступает на 4 — 7-е сут. Церебральная форма острой лучевой болезни возникает при облучении в дозах выше 80 Гр. Смерть при этом наступает через 1 — 3 дня после облучения, а при действии очень больших доз (150 — 200 Гр) смертельный исход может иметь место даже в ходе самого облучения (смерть под лучом) или через несколько минут — часов после воздействия, а также при локальном облучении головы в дозах 100 — 300 Гр. Эта форма лучевого поражения характеризуется развитием судорожно-паралитического синдрома, нарушением крово- и лимфообращения в центральной нервной системе, сосудистого тонуса и терморегуляции. Несколько позднее появляются функциональные нарушения пищеварительной и мочевыделительной систем, происходит прогрессивное снижение кровяного давления. Причиной смерти при церебральной форме острой лучевой болезни являются тяжелые и необратимые нарушения центральной нервной системы, характеризующиеся значительными структурными изменениями, гибелью клеток коры головного мозга и нейронов ядер гипоталамуса. В поражении нервной системы главную роль играют непосредственное повреждающее действие ионизирующей радиации на ткань, а также первичные радиотоксины в виде Н2О2 и других веществ, образующихся за счет окисления ненасыщенных жирных кислот и фенолов. Единичные наблюдения последствий облучения людей в дозах, превышающих 100 Гр, свидетельствуют о возникновении у них расстройств регуляции высшей нервной деятельности, кровообращения и дыхания. Хроническая лучевая болезнь возникает при длительном облучении организма в малых, но превышающих допустимые дозах. Выделяют два основных варианта болезни: обусловленной внешним общим или местным облучением, а также в результате поступления в организм равномерно и неравно- мерно распределяющихся радиоактивных нуклидов. Заболевание отличается постепенным развитием и длительным волнообразным течением, сроки возникновения и характер изменений при этом определяются интенсивностью и суммарной дозой облучения. Начальный период заболевания характеризуется развитием нестойкой лейкопении, признаками астенизации, вегетативно-сосудистой неустойчивостью и др. Развернутому периоду заболевания свойственна недостаточность физиологической регенерации наиболее радиочувствительных тканей в сочетании с функциональными изменениями в деятельности нервной и сердечно-сосудистой систем. Период восстановления характеризуется сглаживанием деструктивных и отчетливым преобладанием репаративных процессов в наиболее радиопоражаемых тканях. По тяжести хроническую лучевую болезнь, обусловленную общим облучением, подразделяют на три группы: легкой (I), средней (II) и тяжелой (Ш) степени. Хроническая лучевая болезнь I степени (легкая) характеризуется нерезко выраженными нервно-регуляторными нарушениями в деятельности различных органов и систем, умеренной нестойкой лейкопенией и тромбоцитопенией. При хронической лучевой болезни II степени (средней) тяжести присоединяются функциональные нарушения нервной, сердечно-сосудистой и пищеварительной систем. Прогрессируют лейкопения и лимфопения, количество тромбоцитов уменьшено; в костном мозге — явления гипоплазии кроветворения. При хронической лучевой болезни Ш степени (тяжелой) развиваются анемия, явления выраженной гипоплазии кроветворения, атрофические процессы в слизистой желудочно-кишечного тракта, присоединяются инфекционно-септические осложнения, гeморрагический синдром и нарушения кровообращения. Крайне тяжелые формы встречаются редко, при этом у больных развиваются поносы и кахексия. Клиническую картину хронической лучевой болезни, обусловленной внутренним облучением, формирует поражение одного или нескольких критических органов, в которых депонируются поступившие в организм радиоактивные нуклиды. 5.17. Какие синдромы наиболее характерные для периода выраженных клинических признаков острой лучевой болезни? Который их патогенез? 1. Гематологический синдром. Проявляет себя панцитопенией, то есть уменьшением содержания в крови всех форменных элементов. Прежде всего исчезают из крови лимфоциты. Лимфопению можно обнаружить уже в период мнимого благополучия. Затем уменьшается содержание гранулоцитов (нейтропения), затем - тромбоцитов (тромбоцитопения) и, наконец, эритроцитов (анемия). Развитие панцитопенией обусловлен поражением красного костного мозга и естественной гибелью зрелых форменных элементов, содержащихся в крови. Поскольку продолжительность жизни различных клеток крови неодинакова, то сначала уменьшается содержание короткоживущих форменных элементов - лимфоцитов, нейтрофилов, и значительно позже - эритроцитов. 2. Геморрагический синдром. Повышенная кровоточивость при острой лучевой болезни обусловлена следующими факторами: а) тромбоцитопенией; б) лучевым повреждением эндотелия сосудов; в) повышением проницаемости сосудистой стенки под действием биогенных аминов (гистамина, серотонина), высвобождающиеся тканевые базофилы в условиях облучения; г) нарушением свертывания крови в результате выделения тканевыми базофилами больших количеств гепарина. 3. Инфекционные осложнения. их развитие связано с нарушением внешних барьеров организма (повреждение покровного эпителия кожи, эпителия слизистой оболочки полости рта, глотки, кишечника) и лейкопения, результатом которой является нарушение иммунных реакций организма (иммунологическая недостаточность) и фагоцитоза. 4. Аутоиммунные реакции. Причиной их возникновения является появление аутоантигенов в облученных тканях. Радиационные аутоантигены представляют собой собственные тканевые белки, измененные под действием ионизирующего излучения. 5. Астенич ный синдром. Охватывает сложный комплекс клинических признаков, возникающих в результате функциональных нарушений центральной нервной системы (общая слабость, головокружение, обмороки, сонливость днем, бессонница ночью и др.). 6. Кишечный синдром. Проявляется нарушениями функции кишечника (понос, спастические боли). Развивается вследствие повреждения эпителия слизистой оболочки. 5. 18. Назовите наиболее важные отдаленные последствия воздействия на организм ионизирующей радиации. Такими последствиями являются мутации в половых и соматических клетках. Первые могут проявляться в следующих поколениях развитием наследственных болезней, вторые - возникновением злокачественных опухолей (лейкозы, рак) через много лет после облучения. 9. Патогенна дія променевої енергії інфрачервоного та ультрафіолетового спектрів. Фотосенсибілізація. Небезпека недостатньої інсоляції. Чем проявляется патогенное действие на организм инфракрасного и ультрафиолетового излучения? Инфракрасное излучение имеет тепловой эффект, поэтому при интенсивном воздействии на ткани может вызвать термические ожоги. Ультрафиолетовое излучение имеет тепловую, фотохимическое и слабую ионизирующее действие. При местной его действия может развиваться эритема (покраснение). Сначала она кратковременна, появляется через несколько минут и быстро проходит. Возникает рефлекторно и связана с тепловым воздействием ультрафиолетового излучения (первичная эритема). Через несколько часов появляется стойкое покраснение с явлениями отека, болью, общими изменениями (слабость, головная боль, интоксикация). Это вторичная эритема. Она обусловлена образованием и высвобождением в ткань биологически активных веществ (гистамина, серотонина, кининов, простагландинов), а также образованием токсичных продуктов при распаде тканевых белков, вызванном ультрафиолетовым излучением. Кроме того, длительное воздействие ультрафиолетового излучения может иметь генетические последствия: мутации, развитие злокачественных опухолей кожи и поверхностных тканей. 5.27. Что такое фотосенсибилизация? Фотосенсибилизация - это повышение чувствительности организма к действию ультрафиолетового излучения. Вещества, вызывающие эффект фотосенсибилизации, получили название фотосенсибилизаторов. Различают экзогенные (эозин, риванола, акридин, хинин, сульфаниламиды) и эндогенные фотосенсибилизаторы (желчные кислоты, Гематопорфирин, холестерол, билирубин). Считают, что под влиянием фотосенсибилизаторов ультрафиолетовые лучи начинают взаимодействовать с теми молекулами тканей, с которыми в отсутствие фотосенсибилизаторов они не взаимодействуют. Кроме того, есть основания полагать, что в этих условиях ускоряется прохождение энергии ультрафиолетовых лучей по углеродных скелетах биологических молекул. 10. Патогенна дія електричного струму. Фактори, які визначають характер уражень при цьому. От каких факторов зависит патогенное действие электрического тока? Патогенное действие электрического тока определяют такие факторы. 1. Физические параметры электрического тока: переменный или постоянный (при напряжении более 500 В опаснее постоянный ток), частота переменного тока (найнебез-печнишим есть ток городской сети- 50 Гц), напряжение и сила тока. Существует прямая зависимость между напряжением и силой тока, с одной стороны, и его патогенной действием, с другой. 2. Путь прохождения тока в организме. Наиболее опасным является прохождение электрического тока через сердце и головной мозг. В этих случаях может наступить смерть в результате фибрилляции сердца или центральной остановки дыхания. 3. Физиологическое состояние организма. Имеют значение: а) состояние кожных покровов (при увлажнении или повреждении кожи степень поражений электрическим током увеличивается) б) общее состояние (патогенная действие тока возрастает при перегревании, охлаждении, кровопотере и др.) в) адаптация к электрическому току (люди, работающие с током, менее чувствительны к его действия). 5.24. Какие местные изменения возникают в тканях при прохождении через них электрического тока? Электрический ток, проходя через ткани, оказывает электротермическую (ожоги), электрохимическую (электролиз),электромеханическую (разрыв тканей) действие. 5.25. Что может стать непосредственной причиной смерти при воздействии электрического тока на организм? 1. Фибрилляция сердца. При прохождении тока через сердце возникают частые асинхронные сокращения отдельных мышечных волокон миокарда желудочков, ведет к асистолии и остановки сердца. 2. Центральная остановка дыхания. Возникает при прохождении тока через структуры головного мозга, регулирующих внешнее дыхание. Смерть наступает в результате паралича дыхательного центра. 3. Периферическая остановка дыхания. Возникает в результате судом дыхательной мускулатуры, спазма голосовых связок. 11. Дія на організм високого та низького атмосферного тиску. Причинно-наслідкові відношення в патогенезі синдромів компресії та декомпресії. Вибухова декомпресія. 5.19. При каких обстоятельствах человек испытывает действия пониженного атмосферного давления? Какие патогенные факторы действуют на организм в этих условиях? Воздействия пониженного атмосферного давления человек испытывает при подъеме на высоту: в самолете, в горах. На организм человека при этих условиях действуют такие патогенные факторы. 1. Собственно уменьшение атмосферного давления. Этот фактор обусловливает развитие синдрома декомпрессии, что проявляется болью в ушах и лобных пазухах в конце воздуха, заполняет их полости; метеоризмом; кровотечениями из носа в результате разрыва мелких сосудов. 2. Уменьшение парциального давления кислорода в едихуваному воздухе является причиной развития кислородного голодания (гипоксии) (см. Разд. 19). 5.20. Когда человек испытывает действия повышенного атмосферного давления? Какие патогенные факторы действуют на организм в этих условиях? Влияния повышенного атмосферного давления человек испытывает при погружении на большую глубину в воду во время водолазных и кессонных работ. При этом на организм человека действуют следующие патогенные факторы. 1. Собственно повышение атмосферного давления (компрессия). Этот фактор вызывает вдавливания барабанных перепонок, в результате чего может появляться боль в ушах. При резком и быстром повышении атмосферного давления возможен разрыв легочных альвеол. В условиях компрессии в крови и тканях организма растворяется дополнительное количество газов (сатурация). 2. Азот оказывает патогенное действие при дыхании сжатым воздухом. При этом возникают нарушения деятельности центральной нервной системы: сначала легкое возбуждение, напоминающее эйфорию ( "глубинный экстаз"), далее - явления наркоза и интоксикации. Указанные нарушения объясняют тем, что в результате сатурации количество азота в организме возрастает в несколько раз, причем больше всего он накапливается в органах, богатых жировую ткань, в частности, в тканях головного мозга, содержащих большое количество липидов. Азот в высоких концентрациях оказывает наркотическое действие, напоминает действие оксида азота (I) ( "закись азота"). Чтобы избежать вредного воздействия азота, этот газ в дыхательной смеси заменяют гелием. Получают смесь - Гелиокс. 3. Кислород при повышении атмосферного давления обладает токсическим действием. Это связано в первую очередь с тем, что в условиях гипероксии активируются процессы свободнорадикального окисления, которые являются одним из механизмов повреждения клеток (подробно см. Гл. 11). Кроме того, как полагают, при гипероксии нарушается выведение из тканей углекислого газа, что приводит своеобразное их "удушения". 5.21. Что такое болезнь декомпрессии и взрывная декомпрессия? Болезнь декомпрессии возникает при быстром возвращении человека в условия нормального атмосферного давления после водолазных работ, работ в кессонах (кессонная болезнь). При этом растворенные в крови и тканях газы (азот, кислород) в большом количестве переходят в газообразное состояние, образуя огромное количество пузырьков, - происходит десатурация. Пузырьки газов, задерживаясь в крови и тканях, могут закупоривать кровеносные сосуды, оказывая давление на клетки, раздражая рецепторы (газовая эмболия). Клиническая картина такой болезни определяется локализацией газовых пузырьков. Чаще всего возникает боль в суставах, зуд кожи; в тяжелых случаях - нарушение зрения, паралич, потеря сознания. Чтобы избежать подобных нарушений, декомпрессию следует проводить медленно, чтобы скорость образования газов не превышала возможности легких по их вывода. Взрывная декомпрессия возникает в случае быстрого перепада атмосферного давления от нормального к пониженному, что бывает при разгерметизации высотных летательных аппаратов (самолетов, космических кораблей). В развитии этого синдрома имеет значение баротравма легких, сердца и крупных сосудов вследствие резкого повышения внутри- легочного давления. Разрыв альвеол и сосудов способствует проникновению газовых пузырьков в кровеносную систему (газовая эмболия). В крайних случаях наступает мгновенная смерть вследствие закипания крови и других жидкостей организма, а также в результате молниеносной формы гипоксии. 5.22. Какие патогенные факторы действуют на организм во время космического полета? 1. На динамической участке полета, то есть во время старта и приземления космического корабля, человек испытывает действия перегрузок, вибрации, шума. Перегрузка - это сила, действующая на организм во время движения с ускорением. В зависимости от характера движения различают прямолинейное и радиальное ускорение по отношению к продольной оси тела - поперечные и продольные перегрузки. Ведущим в механизме действия перегрузок является смещение органов и жидких сред в направлении, обратном движению. Если действие перегрузок совпадает с продольной осью тела, то резкий и опасный перераспределение крови происходит в системе мозгового кровообращения. В одних случаях это переполнение кровью сосудов головного мозга и кровоизлияния, в других - ишемия мозга. В космических полетах тело космонавта ориентировано относительно движения таким образом, чтобы действие перегрузок не совпадающее с продольной осью тела, а была направлена поперечно. 2. В орбитальном полете человек испытывает действия невесомости и гипокинезии. Периода адаптации к невесомости предшествует период острой реакции: нарушается чувствительность (дезориентация, иллюзорные ощущения, головокружение), точность, сила и координация движений; появляются вегетативные нарушения (тошнота, рвота, слюнотечение, неустойчивость пульса и артериального давления). Причина этих расстройств - в нарушении функции анализаторов вследствие искаженной афферентации с рецепторных зон вестибулярного аппарата, кожи, органов зрения, проприорецепторов. Наиболее выраженные адаптивные изменения происходят в системе кровообращения и опорно-двигательном аппарате. В результате выпадения гидростатической составляющей кровяного давления происходит перераспределение крови с увеличением кровенаполнения сосудов верхней половины туловища. Усиленное выведение натрия и воды почками ведет к уменьшению объема циркулирующей крови, уменьшается нагрузка на сердце. Невесомость и гипокинезия является причиной вывода из организма кальция и фосфора, в результате чего изменяется структура костей, развивается остеопороз. В то же время уменьшается масса скелетных мышц, снижается сила их сокращений, появляются признаки атрофии. 12. Хімічні патогенні чинники як проблема екології і медицини. Місцева та загальна дія хімічних факторів на організм. Поняття про токсичність, канцерогенність, тератогенність і алергогенність хімічних сполук. 13. Екзо- та ендоінтоксикації. Загальні закономірності дії токсинів, специфічні та неспецифічні механізми інтоксикації. Природні механізми захисту від дії токсинів. Патофізіологічні принципи дезінтоксикації. 14. Патофізіологічні аспекти алкоголізму, наркоманії, токсикоманії Наркомания - типовая форма психосоматической патологии, вызываемая средствами, включенными в официальный список наркотиков. Виды наркоманий. Каннабизм развивается в следствии применения препаратов каннабиса: марихуаны, анаши, гашиша. Эффекты: ощущение общей релаксации, эйфория, расстройство мышления, снижение сообразительности, поведенческие расстройства. Кокаинизм: улучшение настроения и самочувствия, увеличение ЧСС и АД, температуры тела. Опийная наркомания (морфин, кодеин) – снижение остроты болевых ощущений, седативный эффект, эйфория, угнетение дыхания, тошнота, рвота. Наркомания, вызванная галлюциногенами (ЛСД, мескалин и псилоцибин) – тахикардия, артериальная гипертензия, гипертермия, изменение настроения, галлюцинации. Полинаркомании. Токсикомания – типовая форма психосоматической патологии, формирующаяся при злоупотреблении веществами, не относящимися к наркотикам (в том числе – ЛС и алкоголем). Психотропные вещества (нейролептики – галоперидол, антидепрессанты – амитриптилин, транквилизаторы – диазепам. Диссоциативные анестетики (фенциклидин) – психомоторное возбуждение, аналгезия, дизартрия, нарушение координации движения, дезориентация мышления, психотическое состояние. Алкоголизм – вид токсикомании, характеризующийся патологическим влечением к употреблению спиртных напитков и формированием физической зависимости с развитием абстинентного синдрома в случае прекращения приема этанола. Общий патогенез. Патологическое влечение к повторному употреблению психоактивного вещества.Формирование психической зависимости (депрессия, тревога, глубокая тоска при прекращении поступления), физической зависимости (глубокой расстройство деятельности ЦНС, органов и тканей при прекращении поступления), синдром абстиненции. Развитие толерантности к психоактивному веществу (повторный прием наркотиков увеличивает вязкость мембран клеток, возрастает их ригидность, что увеличивает их устойчивость к действию психоактивных веществ). Исходы: Синдром физической зависимости, сниженной толерантности, полиорганной недостаточности, деградации личности. 15. Інфекційний процес, загальні закономірності розвитку. Класифікація інфекційних агентів. Захисні бар’єри від інфекції, умови їх подолання. Розповсюдження та дисемінація інфекційних агентів в організмі. Инфекционный процесс – сложный многокомпонентный процесс ди-намического взаимодействия инфекционных патогенных агентов с макроор-ганизмом, характеризующийся развитием комплекса типовых патологиче-ских реакций, системных функциональных сдвигов, расстройств гормональ-ного статуса, специфических иммунологических механизмов защиты и фак-торов неспецифической резистентности. Классификация. По биологическому фактору: 1) антропонозы – инфекционные болезни, встречающиеся только у человека; 2) антропозоонозы – инфекционные болезни как человека, так и животных; 3) биоценозы – это группа антропонозов и антропо-зоонозов, передающихся через укусы насекомых. По этиологическому признаку: 1) вирусные инфекции; 2) риккетсиозы; 3) бактериальные инфекции; 4) грибковые инфекции; 5) протозойные инфекции; 6) паразитарные инфекции. По механизму передачи: 1) кишечные инфекции; 2) инфекции дыхательных путей; 3) трансмиссивные или кровяные инфекции; 4) инфекции наружных покровов; 5) инфекции с различным механизмом передачи. По характеру клинико-анатомических проявлений различают инфекции с преимущественным поражением: 1) кожных покровов, клетчатки и мышц; 2) дыхательных путей; 3) пищеварительного тракта; 4) нервной системы; 5) сердечно-сосудистой системы; 6) кровеносной системы; 7) мочеполовых путей. По характеру течения различают острые, хронические, латентные (скрытые) и медленные инфекции. Любое острое заболевание характеризуется последовательной сменой разных периодов: инкубационный, продромальный, клинический (разгара болезни) и выздоровления (реконвалесценции). Каждому периоду свойственны свои особенности: продолжительность, локализация возбудителя в организме, его распространение и выделение в окружающую среду. Инкубационный период начинается с момента проникновения микроба до появления первых симптомов заболевания. Продолжительность инкубационного периода может составлять от нескольких часов до нескольких месяцев и даже лет при отдельных инфекциях и зависит от быстроты размножения микроба, особенностей токсических продуктов, реактивности организма и других факторов. После инкубационного периода наступает продромальный период, когда появляются первые симптомы заболевания, после которого наступает период развития основных клинических симптомов. Клинические проявления инфекционных болезней многообразны. Основными их признаками являются лихорадка, изменение картины крови, нарушение центральной и вегетативной нервной системы, функции органов дыхания, пищеварения и многих других синдромов и симптомов. В период реконвалесценции постепенно восстанавливаются физиологические функции макроорганизма. Этот период, как и все остальные стадии инфекционного процесса, неодинаков при различных заболеваниях и имеет различную продолжительность во времени. Исходы болезни: выздоровление (реконвалесценция), бактерионосительство, летальный исход. |
