Пат физ устно экзамен. патфиз устно. Общая патофизиология патофізіологія як наука та навчальна дисципліна. Методи патофізіології
 Скачать 1.7 Mb. Скачать 1.7 Mb.
|
|
27.26. Какие аритмии возникают в результате одновременного нарушения функций возбудимости и проводимости? 1. Трепетание предсердий (частота сокращений предсердий - 250-400 / мин.). 2. Мерцание предсердий (частота импульсов, возникающих в предсердиях, составляет 400-600 / мин.). Трепетание и мерцание предсердий имеют одинаковые причины развития и могут переходить друг в друга. Поэтому эти два вида нарушений ритма сердца объединяют одним понятием - мерцательная аритмия. 3. Трепетание желудочков (частота сокращений желудочков - 150-300 / мин.). 4. Мерцание (фибрилляция) желудочков (частота импульсов в шлуночках- 300-500 / мин, сердце не сокращается). 27.27. Какими признаками проявляется мерцательная аритмия? Какие механизмы ее развития? При наличии многочисленных эктопических очагов возбуждения и такого изменения проведения импульса, при которой нарушается скорость его проведения по различным участкам миокарда или происходит распространение импульса только в одном направлении, создаются условия для длительной циркуляции волны возбуждения в определенном отделе сердца, возникают расстройства ритма -миготлива аритмия,что может проявляться трепетанием [миганием предсердий (рис. 126). Рис. 126. Мерцательная аритмия При трепетании предсердий частота их сокращений достигает 250-400 / мин. При этом вследствие неспособности желудочков воспроизводить высокий ритм предсердий развивается относительная сердечная блокада желудочки отвечают сокращением на каждое второе, третье или четвертое сокращение предсердий, так как остальные волны возбуждения попадают в фазу рефрактерности. Сокращение желудочков могут возникать раньше, чем наступит достаточное наполнение их кровью - это вызывает тяжелые нарушения кровообращения. Если количество импульсов в предсердиях достигает 400-600 / мин, говорят о мигание, или фибрилляцией предсердий.При этом сокращаются лишь отдельные мышечные волокна, а все предсердия находится в состоянии неполного сокращения, его участие в перекачке крови прекращается. Импульсы, беспорядочно приходят к предсердий-но-желудочкового узла по отдельных мышечных волокнах предсердия, в основном способны вызвать его возбуждения, потому что застают узел в состоянии рефрактерности или не достигают критического уровня. Поэтому предсердно-желудочковый узел возбуждается нерегулярно, и сокращения желудочков носят случайный характер. Как правило, число сокращений желудочков в минуту превышает нормальное. Нередко сокращения желудочков происходят в их наполнение кровью и не сопровождаются пульсовой волной. Поэтому частота пульса становится меньше частоты сокращений сердца (дефицит пульса). Чаще всего причиной развития мерцательной аритмии являются (правило 03): а) стен оз левого атриовентрикулярного отверстия, б) тиреотоксик оз ; в) атеросклеротический кардиосклер оз . Сейчас наиболее признанной теорией, объясняющей механизмы развития мерцательной аритмии (и экстрасистолии!), Является теория повторного вхождения импульсов ( re - entry ) (Рис. 127). Согласно ей, трепетание и мерцание возникают как следствие нарушений проводимости, при которых распространение импульсов прекращается только в одном (антеградном) направлении и сохраняется в обратном (ретроградном). При этом создаются условия для постоянного движения импульсов по кругу в миокарде. В нормальных условиях волна возбуждения, возникнув в одном месте, распространяется в обе стороны сердечной камеры. Достигнув противоположной стенки, она угасает, встретившись с другой волной, оставила за собой зону рефрактерности. Если же вследствие возникновения временного блока или опоздание прихода возбуждения по некоторым волокнах миокарда возбуждения приходит на место, уже вышло из состояния рефрактерности, то создаются условия для тривалеи циркуляции импульса возник. 27.28. Что такое фибрилляция желудочков? Когда она возникает и чем проявляется? При некоторых патогенных воздействиях (прохождение электрического тока через сердце, наркоз хлороформом или циклопропаном, закупорка коронарных артерий или другие случаи резкой гипоксии, травма сердца, действие токсических доз наперстянки и кальция) возникает фибрилляция желудочков. При этом вследствие хаотичного сокращения отдельных мышечных волокон пропульсивная сила сокращений практически исчезает, кровообращение прекращается, быстро наступает потеря сознания и смерть. Фибрилляции способствуют уменьшению концентрации внутриклеточного калия, что ведет к снижению мембранного потенциала кардиомиоцитов и легкого возникновения в них деполяризации и возбуждения, а также изменение содержания нервных медиаторов, особенно катехоламинов. При лечении фибрилляции желудочков наиболее эффективным является пропускания через сердце короткого сильного единичного электрического разряда (дефибрилляция). При этом происходит одновременная деполяризация всех волокон миокарда и прекращаются асинхронные возбуждения мышечных волокон. В качестве меры, предупреждающей развитие фибрилляции, применяют коррекцию электролитного состава крови. 27.29. Чем может быть обусловлено развитие нарушений сократительной функции миокарда? В клетках рабочего миокарда происходит пять процессов, которые определяют сократительную функцию сердца. Все они могут нарушаться и составлять основу развития недостаточности сердца. Расстройства сократительной функции миокарда могут быть обусловлены нарушениями: 1) возбуждение кардиомиоцитов; 2) электромеханического сопряжения; 3) процессов собственно сокращения; 4) процессов расслабления; 5) энергообеспечения миокарда. 27.30. Какие факторы влияют на характер потенциала действия и возбудимость кардиомиоцитов? Какими электрофизиологическими признаками проявляют себя изменения их возбудимости? Основные характеристики потенциала действия (продолжительность, амплитуда, крутизна нарастания деполяризации) и возбудимость кардиомиоцитов зависят от таких факторов (рис. 128): 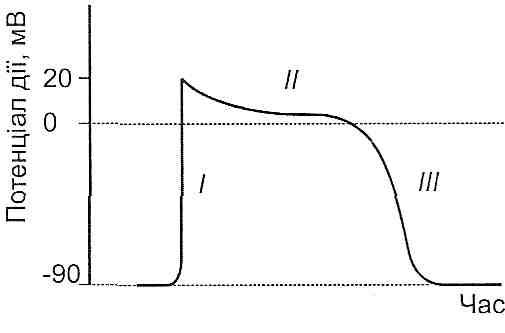 Рис. 128. Потенциал действия сократительных клеток миокарда I-фаза быстрой деполяризации; II - фаза повильноиреполяризации (фаза «плато») III - фаза быстрой реполяризации а) характера электрической импульсации, поступающей в кардиомиоцитов по проводниковой системе сердца. При аритмиях возможно нарушение основных параметров потенциала действия волокон рабочего миокарда и его возбудимости; б) состояния (свойств) сарколеммы кардиомиоцитов, и прежде всего ионных каналов. В настоящее время известны химические агенты, способные избирательно нарушать проводимость этих каналов. Это блокаторы Na-каналов, Са-каналов, К-каналов; в) концентрации внеклеточных ионов, участвующих в формировании электрических потенциалов на мембране кардиомиоцитов. В условиях in vivo наибольшее значение имеет внеклеточная концентрация ионов калия. Изменения возбудимости волокон миокарда могут проявлять себя: 1) изменениями продолжительности потенциалов действия, а следовательно, и силы сердечных сокращений. Уменьшение продолжительности потенциалов действия возникает при увеличении частоты стимуляции, увеличении внеклеточной концентрации ионов калия, при действии ацетилхолина. Увеличение продолжительности потенциала действия характерно для охлаждения; 2) изменениями продолжительности периодов абсолютной и относительной рефрактерности, а следовательно, способности воспринимать импульсацию (усваивать ритм). Продолжительность этих периодов зависит от длительности потенциалов действия. 27.31. Как влияют изменения внеклеточной концентрации ионов калия на возбудимость миокарда? Внеклеточная концентрация ионов калия влияет на возбудимость миокарда через уровень потенциала покоя кардиомиоцитов. Увеличение концентрации ионов калия - гиперкалиемия - вызывает деполяризацию мембраны мышечных волокон. При этом характер изменений возбудимости миокарда зависит от уровня гиперкалиемии. Выделяют следующие диапазоны концентраций ионов калия, для которых характерны определенные картины нарушений: 1) от 4 до 8 ммоль / л. Происходит незначительная деполяризация, мембранный потенциал падает от -90 мВ до -80 мВ. При этом состояние Na-каналов сарколеммы существенно не меняется. Вследствие того, что величина мембранного потенциала приближается к критическому уровню деполяризации, возбудимость мышечных волокон и скорость проведения импульсов растут; 2) от 8 до 35 ммоль / л. Мембранный потенциал падает от -80 мВ до -40 мВ. При таком уровне деполяризации значительно уменьшается проводимость быстрых потенциал-зависимых Na-каналов (период относительной рефрактерности). Следствием этого является уменьшение возбудимости и проводимости, а также изменения характера потенциалов действия (уменьшение продолжительности, амплитуды, крутизны) 3) более 3,5 ммоль / л. Мембранный потенциал становится меньше -40 мВ. При этом все быстрые потенциалзависимые Na-каналы находятся в состоянии инактивации (абсолютная рефрактерность) - происходит остановка сердца. Уменьшение внеклеточной концентрации ионов калия - гипокалиемия - вызывает ги-перполяризацию мембраны. Если гипокалиемия достигает уровня 2-3 ммоль / л, несколько увеличивается порог деполяризации, уменьшается возбудимость, увеличиваются продолжительность потенциалов действия и сила сокращений сердца. 27.32. Что такое Кардиоплегия? Которые используют подходы к ее осуществлению? Кардиоплегия - это искусственная остановка сердца, которую применяют во время операций на "сухом" сердце. Разработаны следующие подходы к осуществлению кардиоплегии: а) ишемическая Кардиоплегия. Пережимают аорту до отхождения венечных артерий. Поскольку через 30 мин. начинаются необратимые изменения в миокарде, этот подход можно использовать при кратковременных операциях (до 10-15 мин.); б) химическая Кардиоплегия. В венечные артерии вводят кардиоплегического растворы, в состав которых входят высокие концентрации ионов калия, ацетилхолин и некоторые другие препараты. Этот метод позволяет проводить операции на "сухом" сердце в течение 40-60 мин .; в) холодовая Кардиоплегия. ее достигают орошением сердца охлажденным до + 4 ° С ... - 5 ° С физиологическим раствором. Продолжительность операций на сердце при этом может составлять 60 мин. 27.33. Какие факторы влияют на характер электромеханического сопряжения в миокарде? 1. Продолжительность потенциала действия. 2. Частота потенциалов действия. 3. Концентрация ионов кальция во внеклеточной жидкости. 4. Состояние Са-каналов сарколеммы кардиомиоцитов. 5. Состояние систем удаления ионов кальция из цитоплазмы мышечных волокон. 27.34. Как изменения продолжительности и частоты потенциалов действия влияют на силу сердечных сокращений? Изменения продолжительности потенциалов действия в кардиомиоцитах происходят за счет укорочения или удлинения фазы "плато", во время которой ионы Са 2+ через потенциалзалеж-ни Са-каналы сарколеммы поступают в саркоплазму. С учетом того, что концентрация ионов Са 2+ в цитоплазме мышечных волокон определяет количество актомиозинових образующихся, а следовательно, и силу сокращений, можно сделать такой вывод. При уменьшении продолжительности потенциала действия уменьшается поступление ионов Са 2+ в саркоплазму и, как следствие, уменьшается сила сокращения мышечного волокна. При увеличении продолжительности потенциала действия - все наоборот. Продолжительность потенциала действия кардиомиоцитов уменьшается при гиперкалиемии, при воздействии на мышечные волокна ацетилхолина. Увеличение продолжительности потенциала действия характерно для гипокалиемии, охлаждение сердца. При увеличении частоты потенциалов действия, несмотря на то, что продолжительность каждого отдельного потенциала, а следовательно, и фазы "плато" уменьшается, суммарная продолжительность указанной фазы за единицу времени увеличивается. Это означает, что в кардиомиоцитах создаются более высокие концентрации Са 2+ и, как следствие, увеличивается сила сокращения мышечных волокон. Этим, в частности, объясняется хроноинотропний механизм немедленной компенсации сердца (см. Запрос. 27.10). При уменьшении частоты потенциалов действия (например, при брадикардии) суммарная продолжительность фазы "плато" в единицу времени уменьшается, что ведет к уменьшению концентрации Са 2+ в саркоплазме и уменьшение силы сокращений сердца. 27.35. Как влияет внеклеточная концентрация ионов кальция в силу сокращений сердца? Что такое "кальциевый парадокс"? В начале XX в. Рингер было показано, что в растворе, лишенном ионов кальция, изолированное сердце быстро останавливается. Сейчас известно, что причиной этого является полное разъединение возбуждения и сокращения. В условиях нормы ионы кальция, поступающие во время фазы "плато" потенциала действия из внеклеточной среды в саркоплазму кардиомиоцитов, "запускают" высвобождение Са 2+ из саркоплазматического ретикулума и пополняют его запасы в этих структурах мышечных волокон. При уменьшении внеклеточной концентрации Са 2+ его запасы в саркоплазматического ретикулуме быстро истощаются, концентрация Са 2+ в саркоплазме падает и, следовательно, уменьшается сила сердечных сокращений. "Кальциевый парадокс" - это экспериментальный феномен, развивается после того, как в безкальциевая раствор, которым осуществляли перфузию сердца в течение нескольких минут, вносят ионы кальция. При этом развивается необратимое повреждение миокарда уменьшается содержание АТФ и креатинфосфата, из кардиомиоцитов выходят белки, в том числе ферменты (миоглобин, креатинкиназы), разрушается саркоплазму-тический ретикулум. "Кальциевый парадокс" объясняют тем, что в безкальциевая растворе происходит расслоение гликокаликса кардиомиоцитов (внешний слой гликокаликса отделяется от внутреннего), в результате чего значительно возрастает проницаемость сарколеммы к ионам кальция. При последующем внесении в среду ионов Са 2+ происходит их массивное поступление в клетки, резко возрастает его концентрация в саркоплазме, что "запускает" кальциевые механизмы повреждения (см. Разд. 11). 27.36. Какие факторы влияют на состояние кальциевых каналов сарколеммы кардиомиоцитов? Чем могут быть обусловлены их активация и блокада? В сарколеммой кардиомиоцитов является потенциолзалежни медленные Са-каналы. Это белковые молекулы, встроенные в плазматическую мембрану и способны пропускать через себя ионы кальция в том случае, когда они открыты. Открытие Са-каналов происходит при деполяризации мембраны. Открываться способны не все имеющиеся каналы, а только фосфо-мерованы (активированные). Под активацией Са-каиалив понимают их фосфорилирования, в результате чего увеличивается количество Са-каналов, способных открываться при возникновении потенциала действия. В основе фосфорилирования Са-каналов лежит увеличение концентрации цАМФ в саркоплазме мышечных волокон. Все факторы, вызывающие образование цАМФ, ведут к активации Са-каналов. К таким, в частности, относятся: а) катехоламины и фармакологические агенты, активирующие fi адренорецепторы; б) ингибиторы фосфодиэстеразы (метилкеантины: теофиллин, кофеин и др.). Указанные агенты увеличивают содержание цАМФ или через активацию аденилатциклазы (через 0-адренорецепторы), или из-за подавления разрушения цАМФ (ингибиторы фосфодиэстеразы). С активацией Са-каналов связан положительный инотропный эффект катехол-минив / Q основе его такая последовательность событий: катехоламины → активация р-адрено-рецепторов → активация аденилатциклазы → образование цАМФ → активация проте-инкиназ → фосфорилирования Са-каналов сарколеммы → увеличение поступления са 2+ в саркоплазму во время потенциалов действия → увеличение концентрации Са 2+ в саркоплазме → увеличение силы сокращений сердца. В условиях блокады Са-капала уменьшается поступление ионов Са в саркоплазму кардиомиоцитов и, следовательно, уменьшается сила сердечных сокращений. Блокаду Са-каналов вызывают: а) эндогенные факторы - дефицит АТФ, дефицит цАМФ, ионы водорода (ацидоз) б) экзогенные факторы - двухвалентные ионы (Ni 2+ , Со 2+ , Мп 2+ ), некоторые трехвалентные ионы (La 3+ ), органические соединения, применяемые в практической медицине (верапамил, нифедипин и др.). 27.37. Какие факторы влияют на состояние систем удаления ионов кальция из кардиомиоцитов и, как следствие, на силу сердечных сокращений? К таким факторам относят: а) сердечные гликозиды - фармакологические препараты растительного происхождения, повышающие силу сокращений сердца (препараты наперстянки, строфантин и др.) б) эндогенные дигиталисоподибни и строфантиноподибни факторы. Считают, что сердечные гликозиды, которые издавна используют в медицине, имитирующие действие этих, относительно недавно открытых, эндогенных природных факторов. Физиологическое значение последних сегодня еще не установлено. Механизм действия сердечных гликозидов и подобных эндогенных факторов связан с угнетением активности Na - K -АТФазыкардиомиоцитов. Следствием этого является нарушение работы Na-K-насосов сарколеммы, уменьшение градиента концентраций ионов Na + по обе стороны плазматической мембраны мышечных волокон. Это приводит к нарушению Na - Ca обменных механизмав кардиомиоцитах, в результате чего уменьшается удаления Са 2+ с саркоплазмы во внеклеточную среду и увеличивается внутриклеточная концентрация Са 2+ . Последнее и обусловливает увеличение силы сердечных сокращений. |
