Пептид если от 10 до 40 аминокислот полипептид
 Скачать 7.45 Mb. Скачать 7.45 Mb.
|
37 вопросИнгибиторы матричных синтезов (ингибиторырепликации и транскрипции. Роль антибиотиков.Вирусы, токсины, система интерферона. А. Ингибиторы репликации - противоопухолевые препараты Антибиотики, взаимодействующие с ДНК, нарушают её матричную функцию и вызывают подавление процессов репликации и транскрипции. Их используют для лечения злокачественных новообразований и называют противоопухолевыми препаратами (см. раздел 15). Дауномицин, доксорубицин и некоторые другие взаимодействуют с молекулой ДНК таким образом, что циклическая структура этих антибиотиков встраивается ("интеркалирует") между парами оснований G≡C, а углеводный компонент занимает малую бороздку ДНК. Это ведёт к локальному изменению структуры ДНК и ингибированию репликации и транскрипции.Избирательность действия противоопухолевых антибиотиков обеспечивается более высокой по сравнению с нормальными клетками скоростью синтеза ДНК и РНК, а также повышенной проницаемостью клеточных мембран опухолевых клеток. В то же время эти соединения токсичны для быстроделящихся нормальных клеток организма, таких как стволовые клетки кроветворной системы, клетки слизистой оболочки желудка и кишечника, фолликулов волос. К препаратам, останавливающим репликацию, относят алкилирующие агенты и ингибиторы ДНК-топоизомеразы II (одной из изоформ топоизомераз). Последние называют ингибиторами гираз, поскольку ДНК-гиразы - ферменты прокариотических клеток, ответственные за суперспира-лизацию ДНК; у эукариотов аналогичную функцию выполняют ДНК-топоизомеразы.. Соединения, вмешивающиеся в работу ДНК-гираз, могут ингибировать или активировать синтез РНК. К ингибиторам гираз принадлежат налидиксовая кислота, новобиоцин и номермицин. Б. Ингибиторы транскрипции и трансляции - антибактериальные препараты К ингибиторам матричных синтезов, оказывающим противобактериальное действие, относят вещества, блокирующие синтез РНК или белка. В эту группу входит широко применяемый в клинике рифампицин, получаемый на основе природного антибиотика рифамицина. Антибиотики из семейства рифамицинов ингибируют только бактериальную ДНК-зависимую РНК-полимеразу,связываясь с β-субъединицей фермента и препятствуя инициации транскрипции. Их применяют для лечения туберкулёза, так как эти препараты не влияют на работу ядерных РНК-полимераз эукариотических клеток. Однако они могут ингибировать синтез митохондриальных РНК, хотя дозы препарата, при которых блокируется образование митохондриальных РНК, выше тех, что используют в лечении инфекционного заболевания. Вирусы Генетический материал вирусов представлен молекулой ДНК или РНК. Он, как правило, невелик и содержит информацию лишь о некоторых специфических белках и ферментах, необходимых для репродукции вируса (например, вирусов оспы, гриппа, полиомиелита, гепатита). Вскоре после заражения с высокой скоростью начинается синтез вирусных ДНК, РНК и белков с использованием ферментов и белков, субстратов и источников энергии клетки хозяина. При этом в инфицированных клетках прекращается синтез нуклеиновых кислот и белков, свойственных организму хозяина. Репродукция вирусных частиц идёт вплоть до гибели заражённой клетки. Токсины Причиной гибели людей при отравлении бледной поганкой является токсин - α-аманитин,который содержится в теле гриба и вызывает необратимую дисфункцию печени и почек. Высокая токсичность этого соединения для человека связана с тем, что оно ингибирует эукариотические РНК-полиме-разы. Наибольшую чувствительность к яду обнаруживает РНК-полимераза II, катализирующая синтез мРНК. Для α-аманитина LD50 (доза per os,при которой погибает 50% лиц, получивших токсин) составляет 0,1 мг/кг массы тела. Чрезвычайно токсичен белок рицин,выделенный из клещевины обыкновенной. Он представляет собой N-гликозилазу, которая удаляет один остаток аденина из 28S рРНК большой субъединицы рибосомы и ингибирует синтез белка у эукариотов. Рицин - белковый компонент касторового масла, иногда используемого в качестве слабительного средства. Из-за высокой токсичности рицина лечение касторовым маслом проводят короткими курсами, так как длительное употребление может вызвать непрекращающийся понос, нарушение работы кишечника и даже гибель больного. 38 вопросПереваривание белков в желудке. Образование и роль соляной кислоты в переваривании белков. Механизм активации пепсина. Нарушения переваривания белков в желудке. Всасывание продуктов переваривания белков в кишечнике. Активация панкреатических ферментов. Специфичность действия протеаз. Защита клеток от действия протеаз. Механизм всасывания аминокислот в кишечнике. Возрастная характеристика процессов переваривания и всасывания белков. Нарушения переваривания белков и транспорта аминокислот. В пищевых продуктах содержание свободных аминокислот очень мало. Подавляющее их количество входит в состав белков, которые гидролизуются в ЖКТ под действием ферментов протеаз. Гидролиз заключается в разрыве пептидных связей —СО—NH— белковой молекулы. Желудочный сок - продукт нескольких типов клеток. Обкладочные (париетальные) клетки стенок желудка образуют соляную кислоту, главные клетки секретируют пепсиноген. Добавочные и другие клетки эпителия желудка выделяют муцинсодержащую слизь. Париетальные клетки секретируют в полость желудка также гликопротеин, который называют "внутренним фактором" (фактором Касла). Этот белок связывает "внешний фактор" - витамин В12, предотвращает его разрушение и способствует всасыванию. Образование и роль соляной кислоты НСI образуется в обкладочных клетках желудочных желёз. 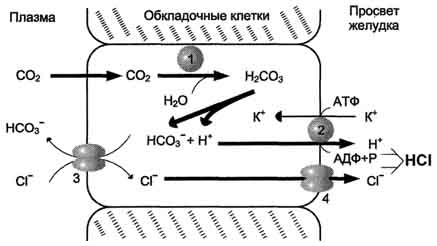 Источником Н+ является Н2СО3, которая образуется в обкладочных клетках желудка из СО2, диффундирующего из крови, и Н2О под действием фермента карбоангидразы (карбонатдегидра-тазы): Н2О + СО2 → Н2СО3 → НСО3- + H+ Диссоциация Н2СО3 приводит к образованию бикарбоната, который с участием специальных белков выделяется в плазму в обмен на С1-, и ионов Н+, которые поступают в просвет желудка путём активного транспорта, катализируемого мембранной Н+/К+-АТФ-азой. При этом концентрация протонов в просвете желудка увеличивается в 106 раз. Ионы С1- поступают в просвет желудка через хлоридный канал. Концентрация НСl в желудочном соке может достигать 0,16 М, за счёт чего значение рН снижается до 1,0-2,0. Приём белковой пищи часто сопровождается выделением щелочной мочи за счёт секреции большого количества бикарбоната в процессе образования НСl. Под действием НСl происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей для протеаз. НСl обладает бактерицидным действием и препятствует попаданию патогенных бактерий в кишечник. Кроме того, соляная кислота активирует пепсиноген и создаёт оптимум рН для действия пепсина. Механизм активации пепсина Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена - неактивной формы пепсина. Под действием НСl он превращается в активный пепсин. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене. Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра. Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее - образованные лейцином и дикарбоновыми аминокислотами. Пепсин - эндопептидаза, поэтому в результате его действия в желудке образуются более короткие пептиды, но не свободные аминокислоты. Нарушения переваривания белков в желудке При различных заболеваниях ЖКТ в желудке нарушается выделение НСl и пепсиногена, при этом переваривание белков заметно снижается. Наиболее часто встречаются патологические изменения кислотности желудочного сока. Нарушение образования пепсина отмечают реже и выявляют при более значительных поражениях желудка. Определение кислотности желудочного сока используют для диагностики различных заболеваний желудка. Повышенная кислотностьжелудочного сока обычно сопровождается изжогой, диареей и может быть симптомом язвы желудка и двенадцатиперстной кишки, а также гиперацидного гастрита. Пониженная кислотностьбывает при некоторых видах гастритов. Полное отсутствие НСl и пепсина (желудочная ахилия) наблюдается при атрофических гастритах и часто сопровождается пернициозной анемией вследствие недостаточности выработки фактора Касла и нарушения всасывания-витамина В12. Анацидность(рН желудочного сока >6,0) свидетельствует о значительной потере слизистой оболочкой желудка обкладочных клеток, секретирующих соляную кислоту, что часто вызывает рак желудка. Молочная кислота в норме в желудочном соке отсутствует. Она образуется при уменьшении содержания или отсутствии свободной соляной кислоты в результате размножения молочнокислых бактерий или при злокачественных опухолях желудка, в клетках которых глюкоза окисляется анаэробным путём. При диагностике заболеваний желудка, кроме биохимических анализов, обязательно проводят рентгенологические и эндоскопические исследования, а также биопсию. Переваривание белков в кишечнике Желудочное содержимое (химус) в процессе переваривания поступает в двенадцатиперстную кишку. Низкое значение рН химуса вызывает в кишечнике выделение белкового гормона секретина, поступающего в кровь. Этот гормон в свою очередь стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСО3-, что приводит к нейтрализации НСl желудочного сока и ингибированию пепсина. В результате рН резко возрастает от 1,5-2,0 до ∼7,0. Поступление пептидов в тонкий кишечник вызывает секрецию другого белкового гормона – холецистокинина, который стимулирует выделение панкреатических ферментов с оптимумом рН 7,5-8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков. Активация панкреатических ферментов Протеолитические ферменты пищеварительного тракта, а также поджелудочной железы синтезируются в неактивной форме – в виде проферментов (зимогенов). Регуляция в этих случаях сводится к превращению проферментов в активные ферменты под влиянием специфических агентов или других ферментов – протеиназ. Так, трипсин в поджелудочной железе синтезируется в форме неактивного трипсиногена. Поступив в кишечник, он превращается в активный трипсин под действием протеиназ. Превращение неактивного пепсиногена в активный пепсин происходит в результате специфического ограниченного протеолиза в присутствии соляной кислоты. Эти превращения зимогенов в активные ферменты связаны с конформационными изменениями молекулы фермента и формированием активного центра или его раскрытием (демаскирование). Соляной кислоте принадлежит значительная роль в желудочном пищеварении, так как она не только активирует ферменты, но и способствует перевариванию белков. Соляная кислота желудочного сока вызывает денатурацию и набухание белков, подготавливая их к последующему расщеплению пепсинами; активирует пепсиногены; создает кислую среду, необходимую для расщепления пищевых белков пепсинами. Специфичность действия протеаз Трипсин преимущественно гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина. Химотрипсины наиболее активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (Фен, Тир, Три). Карбоксипептидазы А и В - цинксодержащие ферменты, отщепляют С-концевые остатки аминокислот. Причём карбоксипептидаза А отщепляет преимущественно аминокислоты, содержащие ароматические или гидрофобные радикалы, а карбоксипептидаза В - остатки аргинина и лизина. Последний этап переваривания - гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
В результате последовательного действия всех пищеварительных протеаз большинство пищевых белков расщепляется до свободных аминокислот. Защита клеток от действия протеаз Клетки поджелудочной железы защищены от действия пищеварительных ферментов тем, что:
В полости желудка и кишечника протеазы не контактируют с белками клеток, поскольку слизистая оболочка покрыта слоем слизи, а каждая клетка содержит на наружной поверхности плазматической мембраны полисахариды, которые не расщепляются протеазами и тем самым защищают клетку от их действия. Разрушение клеточных белков протеазами происходит при язвенной болезни желудка или двенадцатиперстной кишки. Однако начальные механизмы возникновения язвы ещё мало изучены. Всасывание. Аминокислоты, образовавшиеся при переваривании белков, быстро всасываются в кишечнике. Транспорт их осуществляется двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной лимфатический проток. Механизм всасывания аминокислот в кишечнике. L-аминокислота поступает в энтероцит путём симпорта с ионом Na+. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично-активного транспорта с помощью Nа+,К+-АТФ-азы. Различная скорость проникновения аминокислот через мембраны клеток указывает на наличие транспортных систем, обеспечивающих перенос аминокислот как через внешнюю плазматическую мембрану, так и через внутриклеточные мембраны. В настоящее время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот:
Возрастные особенности переваривания белков в желудке У детей грудного возраста в желудке находится фермент реннин(химозин) , вызывающий свёртывание молока. Основной белок молока - казеин, представляющий смесь нескольких белков, различающихся по аминокислотному составу и электрофоретической подвижности. Реннин катализирует отщепление от казеина гликопептида, в результате чего образуется параказеин. Параказеин присоединяет ионы Са2+, образуя нерастворимый сгусток, чем предотвращает быстрый выход молока из желудка. Белки успевают расщепиться под действием пепсина. В желудке взрослых людей реннина нет, молоко у них створаживается под действием НСl и пепсина. В слизистой оболочке желудка человека найдена ещё одна протеаза - гастриксин.Все 3 фермента (пепсин, реннин и гастриксин) сходны по первичной структуре, что указывает на их происхождение от общего гена-предшественника. Нарушение переваривания белков и транспорта аминокислот Небольшую долю продуктов переваривания белка составляют негидролизованные короткие пептиды. У некоторых людей возникает иммунная реакция на приём белка, что, очевидно, связано со способностью к всасыванию таких пептидов. Продукты полностью переваренного белка (аминокислоты) лишены антигенных свойств и иммунных реакций не вызывают. У новорождённых проницаемость слизистой оболочки кишечника выше, чем у взрослых, поэтому в кровь могут поступать антитела молозива (секрет молочных желёз, выделяющийся в первые дни после родов, обогащённый антителами и антитоксинами). Это усугубляется наличием в молозиве белка - ингибитора трипсина. Протеолитические ферменты в пищеварительных секретах новорождённых обладают низкой активностью. Всё это способствует всасыванию в кишечнике небольшого количества нативных белков, достаточного для обеспечения иммунной реакции. Очевидно, подобное усиление всасывающей способности кишечника является причиной наблюдаемой иногда непереносимости белков пищи (например, молока и яиц) у взрослых людей. Всё больше подтверждений получает гипотеза, согласно которой при заболевании целиакии (нетропической спру)происходит нарушение клеток слизистой оболочки кишечника, где всасываются небольшие негидролизованные пептиды. Целиакия характеризуется повышенной чувствительностью к глютену - белку клейковины зёрен злаков, употребляемых с пищей человеком. Этот белок оказывает токсическое действие на слизистую оболочку тонкой кишки, что приводит к её патологическим изменениям и нарушению всасывания. Патогенез заболевания недостаточно ясен. Такие заболевания, как цистинурия,болезнь Хартнапаи некоторые другие, возникают вследствие дефекта переносчиков нейтральных аминокислот в кишечнике и почках. Описана врождённая патология, связанная с дефектом фермента 5-оксопролиназы. При этом с мочой выделяется оксопролин. У этих больных нарушены транспорт аминокислот в ткани и их метаболизм в клетках. |
